Новая лазерная система с автоматизированным контролем глубины коагуляции: к вопросу о сопоставимости яркости и глубины лазерных коагулятов
Автор: Суетов А.А., Бойко Э.В., Измайлов А.С., Докторова Т.А., Иванов А.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4S1 т.19, 2024 года.
Бесплатный доступ
Обоснование. Разработка лазерных систем с автоматизированным контролем глубины коагуляции сетчатки позволит при проведении лечения получать воспроизводимые лазерные ожоги заданной яркости. Тем не менее, остается малоизученным вопрос соответствия яркости формируемого коагулята, фиксируемого при видеозахвате, глубине формируемого коагулята в толще сетчатки.Цель. Изучить соответствие между фиксируемой при видеозахвате яркостью формируемых ожогов и глубиной коагуляции сетчатки при проведении дозируемой лазерной коагуляции с помощью автоматизированной лазерной системы, работающей по принципу обратной связи.Материалы и методы. Прототип автоматизированной системы лазерной коагуляции сетчатки, состоящий из диодного лазера 0,81 мкм и блока видеозахвата, интегрированных в оптическую систему щелевой лампы, а также программного обеспечения, осуществляющего контроль лазерного воздействия по принципу обратной связи. Исследования проводили на глазах кроликов (n = 20). При диаметре пятна 200 мкм, мощности 100, 140, 180, 220, 260 и 300 мВт и планируемых уровнях коагуляции 5, 10, 20, 30, 40, 50 и 70% изучали фактическую яркость полученных коагулятов (%), соответствие планируемой и фактической яркости коагулята. При ОКТ изучали глубину коагуляции (% от толщины нейроретины) и ее корреляцию с фактической яркостью коагулятов.Результаты. При планируемой яркости 5-10% (1 степень по L’Esperance) фактическая яркость ожогов была значимо выше, глубина коагуляции при ОКТ составила от 20 до 30% толщины сетчатки. При планируемой яркости 20-40% и 5-70% (2 и 3 степень по L’Esperance) фактическая яркость коагулятов значимо не отличалась во всем диапазоне мощности, глубина коагуляции по ОКТ составила 35-50% и 80-120% соответственно. Коэффициент вариации фактической яркости и глубины коагуляции не превышал 15% для всего диапазона планируемой яркости и использованной мощности, кроме случаев планируемой яркости 5-10% и мощности 220 мВт и более. Между фактической яркостью и глубиной коагуляции выявлена значимая корреляция (R = 0,96, p = 0,001).Заключение. При проведении лазерной коагуляции сетчатки с использованием новой автоматизированной лазерной системы, работающей на принципе обратной связи, в автоматическом режиме формируются однородные лазерные коагуляты, при этом между глубиной коагуляции нейроретины и яркостью фиксируемых при видеозахвате ожогов существует значимая корреляция.
Сетчатка, лазерная коагуляция, автоматизированная лазерная система, обратная связь
Короткий адрес: https://sciup.org/140307437
IDR: 140307437 | DOI: 10.25881/20728255_2024_19_4_S1_110
A new laser system with automated control of coagulation depth: towards the question of comparability of brightness and depth of laser burns
Background. The development of laser systems with automated control of retinal coagulation depth will make it possible to obtain reproducible laser burns of a given brightness on the ocular fundus during treatment. Nevertheless, the problem of correspondence of the brightness of the formed coagulates fixed by video capture to the depth of the formed coagulates in the retinal thickness remains poorly studied.Objective. To study the correspondence between the brightness of the formed burns recorded by video capture and the depth of retinal coagulation during dose-dependent laser photocoagulation using an automated laser system based on the feedback principle.Materials and methods. A prototype of an automated system for laser photocoagulation of the retina, consisting of a 0.81 µm diode laser and a video capture module integrated into the optical system of the slit lamp, as well as software that controls laser exposure using the feedback principle. Studies were performed on rabbit eyes (n=20). At spot diameter 200 µm, power 100, 140, 180, 220, 260 and 300 mW and planned coagulation levels 5, 10, 20, 30, 40, 50 and 70%, the actual brightness of the obtained coagulates (%), the correspondence between planned and actual coagulate brightness were studied. The depth of coagulation (% of neuroretina thickness) and its correlation with the actual brightness of coagulates were studied at OCT.Results. With a planned brightness of 5-10% (grade 1 according to L’Esperance), the actual brightness of the burns was significantly higher, the depth of coagulation on OCT was 20 to 30% of the retinal thickness. At the planned brightness of 20-40% and 5-70% (grade 2 and 3 according to L’Esperance), the actual burns brightness was not significantly different throughout the power range, and the depth of coagulation by OCT was 35-50% and 80-120%, respectively. The coefficient of variation of actual brightness and coagulation depth did not exceed 15% for the whole range of planned brightness and used power, except for cases of planned brightness of 5-10% and power of 220 mW and more. A significant correlation was found between actual brightness and coagulation depth (R=0.96, p=0.001).Conclusion. During laser coagulation of the retina using a new automated laser system based on the feedback principle, homogeneous laser coagulates are automatically formed, and there is a significant correlation between the depth of neuroretinal coagulation and the brightness of burns recorded by video capture.
Текст научной статьи Новая лазерная система с автоматизированным контролем глубины коагуляции: к вопросу о сопоставимости яркости и глубины лазерных коагулятов
Актуальность
При таких заболеваниях, как пролиферативная ретинопатия различного генеза (постокклюзионная, диа- бетическая и другие), периферические разрывы сетчатки, экстрафовеолярная хориоидальная неоваскуляризация, внутриглазные опухоли или центральная серозная рети-

нопатия с идентифицированной точкой просачивания важную роль в лечении играют различные варианты надпороговых лазерных воздействий [1; 2]. В клинической практике при этом имеет значение не только расположение и плотность лазерных ожогов, но и их яркость, характеризующая глубину коагуляции нейроретины, при этом для характеристики ожогов наиболее часто используется градация L’Esperance [3]. Для проведения эффективного лечения требуется получение однородных по яркости и, соответственно, по глубине коагуляции лазерных ожогов, а отклонение от необходимых параметров может приводить не только к более низким результатам лечения, но и повышать риски побочных эффектов. При недостаточной прозрачности оптических сред, слабой или неравномерной пигментации глазного дна возможность получения однородных по глубине лазерных коагулятов значительно усложняется. Несмотря на разработку и внедрение в клиническую практику роботизированных лазерных систем, управление параметрами проводимого лазерного лечения остается ручным, при этом в случаях использования паттернов не учитываются возможные различия в глубине коагуляции тканей в разных участках глазного дна.
Ранее был предложен ряд способов автоматизированного контроля степени коагуляции сетчатки, например, посредством использования интегрированных в оптическую систему щелевой лампы рефлектометра или видеокамеры с компьютерным управлением отключения лазерного воздействия [4; 5], а также при использовании оптоакустического феномена [6; 7]. Тем не менее, предложенные прототипы не позволяли дозировать глубину коагуляции и из-за конструктивной сложности и малой эффективности не получили дальнейшего развития.
Разработанная нами новая автоматизированная лазерная система [8] призвана обеспечить получение лазерных ожогов требуемой яркости без контроля оператора, то есть полностью в автоматическом режиме дозируя лазерное воздействие в выбранной точке глазного дна. Первые экспериментальные исследования показали, что заложенный в систему принцип обратной связи вполне реализуется и позволяет получать хорошо воспроизводимые лазерные ожоги заданной яркости, при этом в зависимости от требуемой яркости ожога возможна корректировка мощности лазерного излучения для более быстрого формирования ожогов с их более низкой вариабельностью [9]. Тем не менее, остается малоизученным вопрос соответствия яркости формируемого коагулята, фиксируемого при видеозахвате и анализируемого управляющей программой лазерной системы, глубине формируемого лазерного ожога в толще сетчатки.
Цель
Изучить соответствие между фиксируемой при видеозахвате яркостью формируемых ожогов и глубиной коагуляции сетчатки при проведении дозируемой лазерной коагуляции с помощью автоматизированной лазерной системы, работающей по принципу обратной связи.
Материалы и методы
Исследование проведено на прототипе лазерной системы, в которой в оптическую систему щелевой лампы посредством лазерной приставки ПКФ-01 были интегрированы лазерный модуль АЛОД-01 (длина волны 0,81 мкм, Алком Медика, Россия) и видеокамера Toupc-amMicro U3CMOS03100KPA (Touptek, КНР). Лазерный модуль и видеокамеру подключили к персональному компьютеру, на котором с помощью программного обеспечения происходило автоматизированное управление процессом лазерного воздействия.
При работе лазерной системы в управляющей программе проводится покадровый анализ видеопотока. При этом в каждом кадре программа анализирует среднюю яркость пикселей в участке изображения, соответствующем пятну планируемой коагуляции, и сравнивает с яркостью пикселей окружающей области (фон). При достижении заданного уровня яркости пикселей в пятне коагуляции (относительно фоновых показателей) программа отключает лазерный модуль. Настройки программы позволяют выбирать диаметр пятна, соответствующего области коагуляции (зона лазерного воздействия), и диаметр зоны, служащей для сравнения (фон). В программе происходит отслеживание метки пилотного лазера (длина волны 0,65 мкм), при этом к ней автоматически перемещаются зона лазерного воздействия и фон. Во время лазерного воздействия пилотный лазер отключается, исключая влияние на анализ видеопотока.
Лазерный модуль работает в режиме непрерывной генерации лазерного излучения, при этом длительность воздействия в выбранном участке зависит от задаваемых оператором мощности лазерного излучения и планируемой яркости коагулята, определяемой как превышение яркости формируемого ожога над уровнем яркости фона (%).
Эксперименты были выполнены на 10 кроликах (20 глаз) породы шиншилла (самцы массой 2,5–3 кг) с умеренной пигментацией глазного дна. Работа была проведена в соответствии с международными правилами работы с животными (European Communities Council Directive, 86/609/EEC).
Лазерное воздействие проводили в условиях в условиях наркоза (ксилазин 5 мг/кг и кетамина гидрохлорид 35 мг/кг внутримышечно за 15 мин. до манипуляций), мидриаза (циклопентолат 1%) и местной анестезии (оксибупрокаина гидрохлорид 0,4%). Для доставки лазерного излучения использовали линзу Майнстера (Mainster central, увеличение лазерного пятна 1,0, увеличение изображения 1,0, Ocular inc, США) с контактным гелем (Визитил, Россия). При проведении воздействия использовали диаметр пятна лазерного излучения на поверхности сетчатки 200 мкм, мощность в диапазоне от 100 до 300 мВт с интервалом 40 мВт. Во всех глазах наносили по 30 лазерных ожогов с уровнем коагуляции 5, 10, 20, 30, 40, 50 и 70%. При тестируемых уровнях мощности изучали соответствие планируемой и фактической

яркости коагулята, вариабельность яркости получаемых коагулятов, фиксируемых при видеозахвате.
Непосредственно после проведения лазерного воздействия выполняли оптическую когерентную томографию (ОКТ) сетчатки с использованием томографа Solix (Optovue, США) в режиме структурных линейных сканов через центр сформированных коагулятов. Поскольку акцептором лазерного излучения служит меланин в клетках пигментного эпителия, то ожог в ткани сетчатки распространялся в глубину в направлении от наружных к внутренним ее слоям. Глубину коагуляции нейроретины определяли с помощью программы Image J (NIH, США, ver.1.8.0_172), измеряя на структурных сканах соотношение высоты гиперрефлективных областей, соответствующих ожогу, к толщине нейроретины (в %). В использованных диапазонах уровней коагуляции и мощности лазерного излучения, помимо средних значений глубины коагуляции, изучали вариабельность глубины коагуляции, по данным ОКТ, а также взаимосвязь с фактической яркостью ожогов, регистрируемой при видеозахвате и анализе управляющей программой лазерной системы.
Статистический анализ результатов производили в пакете программ Statistica 10.0 Statistica 12.0 (StatSoft Inc., США). Результаты представлены в виде M±m, коэффициента вариации V (%). Анализ различия значений показателей с помощью t-критерия Стьюдента. Для оценки взаимосвязи показателей использовали корреляционный анализ. Статистически значимыми считали результаты с уровнем значимости p<0,05.
Результаты
При проведении лазерной коагуляции сетчатки у кроликов с применением новой автоматизированной лазерной системы лазерное воздействие во всех случаях прекращалось автоматически по достижении заданного уровня яркости коагулятов (Рис. 1). При этом длительность лазерного воздействия в выбранной точке сетчатки варьировала от 120 мс до 1,2 с в зависимости от требуемой яркости ожога и мощности лазерного излучения.
Анализ фактической яркости коагулятов показал, что при планируемой яркости 5–10% (соответствует
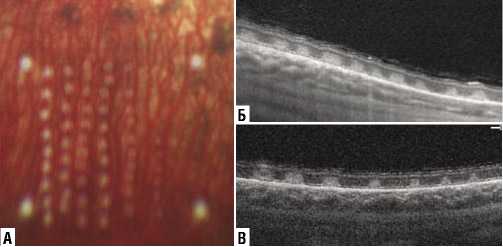
Рис. 1. Формируемые лазерные коагуляты на глазном дне кролика (а) при мощности лазерного излучения 180 мВт и структурные ОКТсканы через коагуляты с одинаковой яркостью коагуляции 40% (б) и с различной яркостью коагулятов: слева направо ожоги 70, 50, 40, 30, 20, 10 и 5% (в).
ожогам 1 степени по F.A. L’Esperance) значения фактической яркости оказывались больше, при этом превышение значений было более выраженным при мощности лазерного излучения 220–300 мВт (Табл. 1). При планируемой яркости 20–40% и 50–70% (соответствует ожогам 2 и 3 степени по F.A. L’Esperance) значения фактической яркости были близки к планируемым при всех использованных значениях мощности лазерного излучения, при этом наименьшее отклонение фактической яркости от запланированной в диапазоне 10–70% яркости наблюдали при использовании мощности 180 мВт.
Коэффициент вариации фактической яркости коагулятов не превышал 15% для планируемой яркости коагулятов от 20 до 70% во всем диапазоне использованной мощности лазерного излучения (Табл. 1). Для коагулятов с планируемой яркостью 5–10%, то есть при воздействии, близкому к пороговому, коэффициент вариации фактической яркости возрастал до 28,6–38,6% при увеличении мощности лазерного излучения до 180–300 мВт.
При анализе структурных ОКТ-сканов через центр получаемых коагулятов на сканах наблюдали гиперрефлективные зоны, распространяющиеся от наружных слоев сетчатки к внутренним (Рис. 1). При этом было выявлено, что при формировании коагулятов с планируемой яркостью 20–40%, соответствующих ожогам 2 степени по F.A. L’Esperance, глубина коагуляции ткани
Табл. 1. Фактическая яркость (M±m, %) и коэффициент вариации (V, %) получаемых коагулятов при использовании различной планируемой яркости коагулятов и выходной мощности лазерного излучения, по данным видеозахвата в управляющей программе
|
P, мВт |
Градация коагулятов по F.A. L'Esperance |
||||||
|
1 |
2 |
3 |
|||||
|
Планируемая яркость коагулятов, % |
|||||||
|
5 |
10 |
20 |
30 |
40 |
50 |
70 |
|
|
100 |
12,6±2,2 (17,5) |
15,8±2,6 (16,2) |
24,4±3,5 (14,3) |
35,0±3,9 (11,2) |
45,1±3,7 (8,3) |
51,3±3,9 (7,6) |
70,6±4,0 (5,6) |
|
140 |
16,8±2,6 (15,4) |
16,1±2,9 (18,1) |
25,4±3,2 (12,6) |
31,6±3,2 (10,2) |
44,8±4,1 (9,2) |
51,8±3,3 (6,3) |
70,0±5,8 (8,3) |
|
180 |
15,4±4,4 (28,6) |
15,8±2,3 (14,8) |
22,9±2,4 (10,6) |
34,2±2,8 (8,3) |
39,7±2,6 (6,5) |
50,5±3,1 (6,1) |
70,0±4,5 (6,4) |
|
220 |
23,6±8,1 (34,2) |
20,5±4,3 (20,8) |
22,8±3,0 (13,0) |
39,5±4,1 (10,5) |
44,2±4,6 (10,5) |
50,1±4,1 (8,2) |
70,0±3,7 (5,3) |
|
260 |
32,9±10,8 (32,8) |
26,6±7,3 (27,6) |
25,3±4,0 (15,8) |
36,4±3,5 (9,5) |
42,5±5,4 (12,7) |
50,5±3,2 (6,3) |
70,0±5,5 (7,8) |
|
300 |
27,3±10,5 (38,6) |
24,5±7,3 (29,6) |
27,4±4,1 (14,9) |
37,0±3,7 (10,0) |
42,0±3,2 (7,6) |
51,0±2,9 (5,7) |
70,1±3,9 (5,6) |

Табл. 2. Глубина получаемых коагулятов (M±m, %) и коэффициент вариации (V, %), при использовании различной планируемой яркости коагулятов и выходной мощности лазерного излучения, по данным структурной ОКТ
P, мВт Градация коагулятов по F.A. L' Esperance
|
1 \ |
2 1 |
3 |
|
Планируемая яркость коагулятов, % |
||
|
5 1 |
10 1 |
20 |
30 1 |
40 |
50 1 |
70 |
|
|
Глубина коагуляции, % от общей толщины сетчатки |
|||||||
|
100 |
22,8±3,3 (14,5) |
25,6±3,9 (15,2) |
35,2±3,4 (9,7) |
42,4±3,6 (8,5) |
48,9±4,8 (9,8) |
82,9±5,4 (6,5) |
114,3±6,9 (6,0) |
|
140 |
20,9±3,0 (14,4) |
26,5±3,7 (13,9) |
37,7±3,8 (10,1) |
40,3±3,5 (8,7) |
51,3±4,3 (8,4) |
84,2±6,1 (7,2) |
117,1±8,2 (7,0) |
|
180 |
23,1±3,4 (14,7) |
28,3±4,0 (14,1) |
36,9±3,5 (9,5) |
40,5±3,9 (9,6) |
50,7±4,0 (7,9) |
83,9±6,0 (7,1) |
111,6±7,4 (6,6) |
|
220 |
29,9±6,7а (22,4) |
30,5±5,3a (17,4) |
36,4±3,9 (10,7) |
41,4±4,0 (9,7) |
51,0±4,5 (8,8) |
85,2±6,8 (7,9) |
116,5±6,7 (5,8) |
|
260 |
36,8±8,9b (24,2) |
32,8±5,1a (15,5) |
36,0±3,6 (10,0) |
39,7±3,7 (9,3) |
52,1±3,9 (7,5) |
85,5±5,7 (6,7) |
120,0±7,9 (6,6) |
|
300 |
37,5±12,6b (33,6) |
34,2±7,9b (23,1) |
37,7±3,7 (9,8) |
40,9±4,0 (9,8) |
50,8±3,7 (7,3) |
84,9±5,8 (6,8) |
118,4±7,3 (6,2) |
Примечание : а – p<0,01; b – <0,001 по сравнению со значениями меньшей мощности.
нейроретины составляет от 35 до 50% толщины нейроретины, а изменение мощности не приводило к получению значимо отличающихся по глубине ожогов (Табл. 2). При получении коагулятов с планируемой яркостью 50–70%, соответствующих ожогам 3 степени по F.A. L’Esperance, глубина коагуляции на ОКТ сканах составляла от 82,9 до 118,4% на фоне развития отека сетчатки, при этом глубина коагуляции значимо не отличалась при использовании разного уровня мощности лазерного излучения.
При анализе вариации значений глубины коагуляции сетчатки наблюдали сходные показатели с полученными для фактической яркости коагулятов при видеозахвате: для уровней планируемой яркости 20–70% коэффициент вариации составлял менее 10%, но для планируемой яркости 5–10% увеличивался до 22,4–33,6% при повышении мощности лазерного излучения до 220–300 мВт (Табл. 2). То есть использование более высокой мощности для получения близких к пороговым ожогов сетчатки приводило к формированию более глубоких и менее однородных коагулятов.
При проведении корреляционного анализа выявлено наличие значимой сильной прямой связи между фиксируемой при видеозахвате управляющей программой яркостью коагулятов и глубиной коагуляции ткани сетчатки при проведении структурной ОКТ сразу после лазерного воздействия (R = 0,96, p = 0,001; Рис. 2). Анализ в группах с разной мощностью, а также в группах с разной планируемой яркостью также показал сходные результаты: коэффициент корреляции варьировал от R = 0,91 до R = 0,98, p<0,01.
Таким образом, регистрируемые значения яркости формируемых коагулятов в высокой степени согласуются с глубиной лазерного повреждения сетчатки, то есть разработанная система позволяет проводить дозируемое по глубине лазерное воздействие в автоматическом режиме и получать воспроизводимые и однородные лазерные коагуляты с необходимыми оператору характеристиками. Тем не менее, технические характеристики прототипа автоматизированной лазерной системы, работающей на принципе обратной связи, обеспечивают наиболее точное
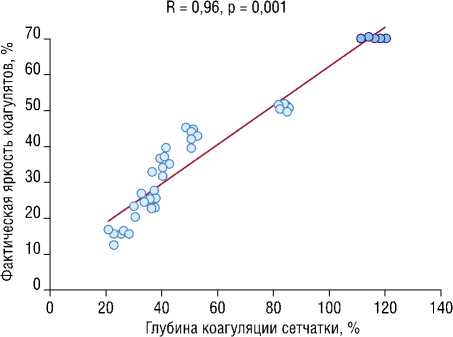
Рис. 2. Диаграмма рассеивания для пары фактическая яркость формируемых коагулятов, по данным видеозахвата управляющей программой, и глубины коагуляции сетчатки, по данным структурной ОКТ.
воздействие с наименьшим отклонением от требуемых параметров в случаях, когда необходимо получение лазерных ожогов 2–3 степени по L’Esperance (планируемая яркость ожогов 20–70%). Последующее улучшение технических характеристик позволит улучшить работу лазерной системы при формировании менее интенсивных коагулятов.
Заключение
При проведении воздействия с помощью новой автоматизированной лазерной системы, работающей на принципе обратной связи, в автоматическом режиме формируются однородные лазерные коагуляты, при этом между глубиной коагуляции нейроретины и яркостью фиксируемых при видеозахвате ожогов существует значимая корреляция.
Источник финансирования : исследовательская работа проведена на личные средства авторского коллектива.

Список литературы Новая лазерная система с автоматизированным контролем глубины коагуляции: к вопросу о сопоставимости яркости и глубины лазерных коагулятов
- Бойко Э.В. Лазеры в офтальмохирургии: теоретические и практические основы. СПб: ВМедА им.С.М.Кирова; 2003.
- Фёдоров СН. Лазерные методы лечения заболеваний глаз. Москва: Медицина; 1990.
- L'Esperance FA. Ophthalmic Lasers. Photocoagulation, Photoradiation and Surgery. St. Louis: Mosby; 1989.
- Inderfurth JHC, Ferguson RD, Frish MB, Birngruber R. Dynamic reflectometer for control of laser photocoagulation on the retina. Lasers Surg Med 1994;15:54-61. DOI: 10.1002/lsm.1900150108
- Jerath MR, Chundru R, Barrett SF, Rylander HG, Welch AJ. Reflectance Feedback Control of Photocoagulation in Vivo. Arch Ophthalmol 1993;111: 531-4. DOI: 10.1001/archopht.1993.01090040123045
- Schlott K, Koinzer S, Ptaszynski L, Bever M, Baade A, Roider J, et al. Automatic temperature controlled retinal photocoagulation. J Biomed Opt 2012;17:061223. DOI: 10.1117/1.JBO.17.6.061223
- Серебряков В.А., Бойко Э.В., Ян А.В. Оптико-акустический мониторинг температуры сетчатки при лазерной терапии в режиме реального времени. Оптический журнал. 2014;81(6):14-16. DOI: 10.1364/JOT.81.000312 EDN: TQQKIP
- Бойко Э.В., Суетов А.А., Докторова Т.А., Измайлов А.С., Иванов А.А., Пищелин А.В. Новая автоматизированная система лазерной коагуляции сетчатки с обратной связью. Офтальмохирургия. 2023;3S: С.64-71. DOI: 10.25276/0235-4160-2023-3S-64-71 EDN: FSJRVR
- Бойко Э.В., Суетов А.А., Измайлов А.С., Докторова Т.А., Иванов А.А., Пищелин А.В. Подбор оптимальных энергетических параметров для проведения дозируемой в автоматическом режиме лазерной коагуляции сетчатки (экспериментальное исследование). Вестник Волгоградского государственного медицинского университета. 2024;21(1):35-40. DOI: 10.19163/1994-9480-2024-21-1-35-40 EDN: OTOECT


