Новые 1-бензил и 1,3-дибензилпроизводные 5-(фениламино)урацила: синтез и противовирусная активность
Автор: Луганченко А.И., Новиков М.С., Озеров А.А.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Обзорные статьи
Статья в выпуске: 4 (64), 2019 года.
Бесплатный доступ
Осуществлен синтез новых потенциальных антивирусных агентов ненуклеозидной природы, содержащих бензильные фрагменты в положениях N1 и N3 5-(фениламино)урацила. 1-(3-Бензоилбензил)-5-(фениламино)урацил эффективно подавляет репликацию различных штаммов цитомегаловируса человека и варицелла-зостер вируса в клеточной культуре HEL с величиной ингибиторной концентрации от 1,64 до 11,14 мкг/мл.
5-(фениламино)урацил, цитомегаловирус человека, варицелла-зостер вирус
Короткий адрес: https://sciup.org/142224357
IDR: 142224357 | УДК: 547.854
Novel 1-benzyl and 1,3-dibenzyl 5-(phenylamino)uracil derivatives: synthesis and antiviral activity
Synthesis of new potential antiviral agents as non-nucleoside inhibitors of virus-specific enzymes of pyrimidine nature, containing benzyl fragments at N1 and N3 position of the 5-(phenylamino)uracil was carried out. 1-(3-Benzoylbenzyl)-5-(phenylamino)uracil effectively suppresses the replication of various strains of human cytomegalovirus and varicella-zoster virus in HEL cell culture with the value of inhibitory concentration in the range from 1,64 to 11,14 pg/ml.
Текст научной статьи Новые 1-бензил и 1,3-дибензилпроизводные 5-(фениламино)урацила: синтез и противовирусная активность
N-Замещенные производные пиримидиновых оснований проявляют разнообразную фармакологическую активность, в том числе противовирусную, противоопухолевую [2] и антибактериальную [3]. Ранее нами среди N-бензил-производных 5-(фениламино)урацила был выявлен ряд соединений, эффективно подавляющих репликацию ВИЧ-1 и герпесвирусов [4]. В продолжение этих исследований нами осуществлен синтез новых N1-моно- и N1,N3-дибензил-производных 5-(фениламино)урацила, содержащих замещенные бензильные фрагменты в составе боковой цепи, что обеспечивает, как нами было показано ранее [5], эффективное ингибирование вирусспецифических ферментов.
ЦЕЛЬ РАБОТЫ
Синтез различных N-бензилпроизводных 5-(фениламино)урацила и исследование их противовирусной активности in vitro в отношении различных ДНК- и РНК-содержащих вирусов.
МЕТОДИКА ИССЛЕДОВАНИЯ
Спектры ЯМР 1Н и 13С регистрировали на спектрометре «Bruker Avance 400» (400 МГц для 1H и 100 МГц для 13С) в ДМСО-D6, внутренний стандарт тетраметилсилан. Тонкослойную хроматографию выполняли на пластинах TLC Silica gel 60 F254, используя в качестве элюента смесь 1,2-дихлорэтан – этилацетат (1:1). Пла- стины проявляли с помощью УФ-лампы VL-6.LC (Франция). Температуры плавления измерены в стеклянных капиллярах на приборе «Mel-Temp 3.0» (Laboratory Devices Inc., США).
1-(3-Бензоилбензил)-5-(фениламино)ура-цил (2). К кипящему раствору 5,0 г (25,5 ммоль) 3-бензоилтолуола в 50 мл безводного тетрахлор-метана при интенсивном освещении светом видимого диапазона добавляют в течение 30 мин раствор 4,5 г (28,2 ммоль) брома в 25 мл тетрах-лорметана, кипятят с защитой от влаги воздуха 4 ч, растворитель отгоняют в вакууме водоструйного насоса на кипящей водяной бане и получают продукты бромирования в виде вязкого янтарного масла. Смесь 5,0 г (24,6 ммоль) 5-(фениламино)урацила (1), 50 мл гексаметилдисилазана и 0,05 г хлорида аммония кипятят с защитой от влаги воздуха в течение 1 ч до образования прозрачного раствора, избыток гексаметилдисилазана удаляют в вакууме, остаток растворяют в 50 мл безводного 1,2-дихлорэтана, добавляют раствор продуктов бромирования в 50 мл 1,2-дихлорэтана и кипятят в течение 20 ч. Охлаждают, добавляют 10 мл воды и 2 мл концентрированного гидроксида аммония, перемешивают, выдерживают при температуре 0–5 оС в течение суток, образовавшийся осадок отфильтровывают, промывают 25 мл холодного 1,2-дихлорэтана, водой, сушат на воздухе, дважды кристаллизуют из 95%-го этилового спирта и получают 4,35 г золотистого игольчатого кристаллического вещества, выход 46 %, Т. пл. 179–181,5 оС.
Спектр ЯМР 1Н, δ, м. д.: 5,00 с (2Н, СН 2 ); 6,65–7,76 м (14 Н, арил, NH); 7,81 с (1Н, H6); 11,63 с (1Н, NH).
Спектр ЯМР 13С, δ, м. д.: 53,40; 117,81; 120,22; 121,54; 131,96; 132,00; 132,24; 132,37; 132,45; 133,05; 135,28; 136,19; 138,07; 140,18; 140,59; 141,06; 149,01; 153,35; 165,18; 198,86.
1-(4-Бензоилбензил)-5-(фениламино) урацил ( 3 ) получают аналогично из 4-бензоил-толуола. Золотистое пластинчатое кристаллическое вещество, выход 51 %, Т. пл. 196,5– 198,5 оС.
Спектр ЯМР 1Н, δ, м. д.: 5,03 с (2Н, СН 2 ); 6,66–7,76 м (14 Н, арил, NH); 7,74 с (1Н, H6); 11,59 с (1Н, NH).
Спектр ЯМР 13С, δ, м. д.: 53,53; 118,03; 120,43; 121,67; 130,81; 131,94; 132,23; 132,95; 133,41; 136,05; 137,58; 139,67; 140,40; 145,29; 148,90; 153,32; 165,17; 198,73.
1-(3-Бензоилбензил)-3-бензил-5-(фенила-мино)урацил (4). Смесь 1,0 г (2,52 ммоль) 1-(3-бензоилбензил)-5-(фениламино) урацила (2) и 1,0 г (7,24 ммоль) тонко измельченного безводного карбоната калия в 25 мл безводного диме-тилформамида перемешивают при температуре 80–85 оС в течение 30 мин, добавляют 0,35 мл (3,04 ммоль) бензилхлорида и перемешивают при той же температуре в течение 2 ч. Охлаждают, фильтруют, фильтрат упаривают в вакууме, остаток растирают с 10 мл воды, выдерживают при температуре 0–5 оС в течение суток, образовавшийся осадок отфильтровывают, промывают водой, сушат на воздухе, кристаллизуют из метилового спирта и получают 0,85 г лимонно-желтого кристаллического вещества, выход 69 %, Т. пл. 122–124,5 оС.
Спектр ЯМР 1Н, δ, м. д.: 5,04 с (2Н, СН 2 ); 5,08 с (2Н, СН 2 ); 6,65–7,76 м (20Н, арил, NH); 7,94 с (1Н, H6).
Спектр ЯМР 13С, δ, м. д.: 47,59; 54,67; 117,90; 119,63; 121,69; 130,57; 130,85; 131,71; 131,96; 131,98; 132,28; 132,39; 132,47; 133,04; 135,30; 136,22; 137,22; 140,14; 140,39; 140,62; 140,82; 148,96; 153,47; 163,24; 198,83.
1-(4-Бензоилбензил)-3-бензил-5-(фенила-мино)урацил ( 5 ) получают аналогично из 1-(4-бензоилбензил)-5-(фениламино)урацила ( 3 ).
Светло-желтое кристаллическое вещество, выход 74 %, Т. пл. 135–137,5 оС.
Спектр ЯМР 1Н, δ, м. д.: 5,07 с (2Н, СН 2 ); 5,11 с (2Н, СН 2 ); 6,68–7,76 м (20Н, арил, NH); 7,88 с (1Н, H6).
Спектр ЯМР 13С, δ, м. д.: 47,67; 54,81; 118,15; 119,89; 121,84; 130,58; 130,83; 130,99; 131,71; 131,94; 132,28; 132,95; 133,41; 136,07; 136,62; 139,73; 140,38; 140,42; 145,05; 148,82; 153,48; 164,27; 198,71.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Синтез N1-моно- и N1,N3-дибензил-заме-щенных производных 5-(фениламино)-урацила ( 1 ) был основан на разработанном нами методе N-алкилирования триметилсилилпроизводных пиримидиновых оснований алкилгалогенидами с невысокой реакционной способностью [1] (схема).
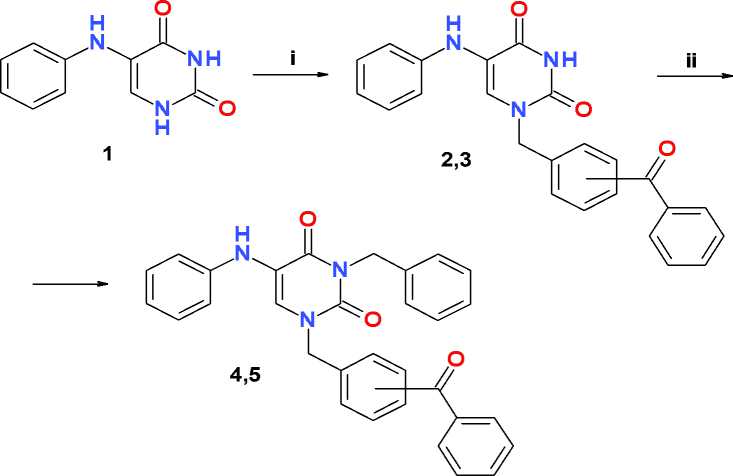
Схема. Синтез N-бензилпроизводных 5-(фениламино)урацила. Условия и реагенты: I) ГМДС, NH 4 Cl, кипячение, 1 ч; бензоилбензилбромид, 1,2-дихлорэтан, кипячение, 20 ч; II) бензилхлорид, К 2 СО 3 , ДМФА, 80–85 оС, 2 ч
Кипячение исходного 5-(фениламино)-урацила ( 1 ) в избытке гексаметилдисилазана в присутствии каталитического количества аммония хлорида в течение 1 ч приводит к образованию прозрачного раствора, упаривание которого в вакууме с количественным выходом дает триметилсилилпроизводное 5-(фениламино)-урацила. Однако, в отличие от триметилси-лилпроизводных урацила, тимина или 6-метил-урацила, производное 5-(фениламино)урацила быстро и полностью кристаллизуется при охлаждении, что свидетельствует о его более высокой полярности. Методом спектроскопии ЯМР было установлено, что экзоциклическая аминогруппа 5-(фениламино)урацила ( 1 ) не подвергается силилированию, и полученный продукт представляет собой 2,4-ди(триметилсилило-кси)-5-фениламинопиримидин. Тем не менее триме-тилсилилпроизводное 5-(фениламино)урацила легко растворяется в малополярном 1,2-дихлорэтане, что способствует успешному селективному N1-алкилированию этого соединения.
Взаимодействие триметилсилилпроизводно-го 5-(фениламино)урацила с бензоилзамещен-ными бензилбромидами протекает в течение 20 ч при кипячении их раствора в 1,2-дихлорэтане с защитой от влаги воздуха. Выход целевых 1-(бензоилбензил)производных 5-(фениламино) урацила (2, 3), составляющий 46–51 %, можно считать достаточно высоким, поскольку алкилирующие агенты не выделялись в индивидуальном состоянии и не подвергались очистке. Заключительное N3-бензилирование соединений 2 и 3 бензилхлоридом, приводящее к дибензилпроиз-водным 5-(фениламино)урацила (4, 5), протекает в «классических» условиях – при нагревании в среде безводного диметилформамида в присутствии карбоната калия, что обеспечивает удовлетворительный (69–74 %) выход конечных продуктов. Противовирусная активность новых соединений 2–5 in vitro была изучена в Рега институте медицинских исследований (Католический университет, Лёвен, Бельгия). Обнаружено, что 1-(3-бензоилбензил)-5-(фениламино)урацил (2) проявляет умеренную активность в клеточной культуре HEL в отношении различных герпесвирусов: цитомегаловируса человека (герпесвирус человека типа 5) и вируса ветряной оспы / опоясывающего лишая (варицелла-зостер вирус, герпесвирус человека типа 3) при невысокой цитотоксичности (см. табл.). Интересно отметить, что активность этого соединения в отношении штамма вируса варицелла-зостер, не кодирующего тимидинкиназу (TK- VZV, штамм 07-1), была значительно выше, чем в отношении вируса, кодирующего этот фермент (TK+ VZV, штамм OKA), в то время как для других противогерпетических агентов, в частности ацикловира, обычно наблюдается обратная закономерность. Это позволяет сделать предположение о том, что соединение 2 является ненуклеозидным ингибитором репликации вируса варицелла-зостер. Остальные соединения 3–5 не продемонстрировали заметной противовирусной активности в отношении указанных герпесвирусов. Активности в отношении других ДНК- и РНК-содержащих вирусов: вируса герпеса простого типа 1 и типа 2, вируса оспы, аденовируса, коронавируса, вируса везикулярного стоматита, Коксаки вируса, респираторно-синцитиального вируса, вируса парагриппа, реовируса, вирусов Синдбис, Пунта Торо и желтой лихорадки, вирусов гриппа A/H1N1, A/H3N2 и B обнаружено не было.
Противовирусная активность синтезированных соединений
|
Соединение |
Противовирусная активность, EC 50 , µM |
Цитоток-сичность, СС 50 , µM |
|||
|
VZV |
HCMV |
||||
|
OKA |
07-1 |
AD-169 |
Davis |
||
|
2 |
11,14 |
1,92 |
1,64 |
1,64 |
91,72 |
|
3 |
> 20 |
5,52 |
> 20 |
> 4 |
> 100 |
|
4 |
> 100 |
> 100 |
> 100 |
> 20 |
> 100 |
|
5 |
> 100 |
> 100 |
> 100 |
> 20 |
> 100 |
|
Ганцикловир |
- |
- |
0,58 |
0,16 |
> 100 |
|
Ацикловир |
0,16 |
1,59 |
- |
- |
> 100 |
ЗАКЛЮЧЕНИЕ
Таким образом, нами получен ряд новых производных 5-(фениламино)урацила, содержащих замещенные и незамещенные бензильные фрагменты в положениях N1 и N3 пиримидиновой системы. Целесообразен дальнейший поиск высокоселективных ингибиторов вирусной репродукции для лечения заболеваний, вызываемых цитомегаловирусом человека и вирусом ветряной оспы / опоясывающего лишая на основе соединений этого ряда.
Список литературы Новые 1-бензил и 1,3-дибензилпроизводные 5-(фениламино)урацила: синтез и противовирусная активность
- Новиков, М. С. Хим. гетероциклич. соед. / М. С. Новиков, A. A. Озеров, Ю. А. Орлова [и др.]. - 2005. - № 6. - С. 887-892.
- Engel, D. [et al.] // J. Med. Chem. - 2008. -Vol. 51. - № 2. - P. 314-323.
- Kawatkar, S. P. [et al.] // J. Med. Chem. - 2014. -Vol. 57. - № 11. - P. 4584-4597.
- Novikov, M. S. [et al.] // Bioorganic & Medicinal Chemistry. - 2010. - Vol. 18. - № 23. - P. 8310-8314.
- Novikov, M. S. [et al.] // Bioorg. Med. Chem. -2011. - Vol. 19. - № 19. - P. 5794-5902.


