Новые ионные комплексы платины(IV): [Ph3PCH3][PtBr5(dmso)] и [C(CH2OH)3NH3][K][Pt(SCN)6]
Автор: Зыкова Ална Романовна, Жеребцов Дмитрий Анатольевич, Ельцов Олег Станиславович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Неорганическая химия
Статья в выпуске: 1 т.14, 2022 года.
Бесплатный доступ
Первые сообщения о диметилсульфоксидных комплексах появились в начале 60-х годов прошлого века. Большой вклад в развитие этой темы внесла группа ученых под руководством Ю.Н. Кукушкина, исследовавших свойства комплексов платиновых металлов(II). Ионные диметилсульфоксидные комплексы платины(IV) в настоящее время изучены в меньшей степени. (Диметилсульфоксидо)пентабромоплатинат метилтрифенилфосфония [Ph3PCH3][PtBr5(dmso)] (1) получен путем растворения гексабромоплатината метилтрифенилфосфония в диметилсульфоксиде c выходом 85 %. Комплексы платины с гексакис (тиоцианато-S)платинатными анионами практически не изучены. По сведениям из Кембриджской базы структурных данных CSD, синтезировано и структурно охарактеризовано только пять гексакис (тиоцианато- S )платинатных комплексов, большинство из которых получены в период с 1978 по 1999 год. Гексакис (тиоцианато- S )платинатный комплекс [C(CH2OH)3NH3][K][Pt(SCN)6] (2) с двумя различными катионами (калия и органиламмония) синтезирован из хлорида трис (2-гидроксиметил)метиламмония и гексатиоцианатоплатината калия в водном растворе ацетона с выходом 58 %. Строение комплексов доказано с помощью ИК-, 1H-, 13C ЯМР-спектроскопии и ренгенофлуоресцентного анализа. ИК-спектры соединений 1 и 2 записывали на ИК-спектрометре Shimadzu IRAffinity-1S в таблетках KBr в области 4000-400 см-1. Спектры ЯМР 1H и 13C регистрировали на спектрометре Bruker AVANCE 500 (500 МГц). Химические сдвиги измерены от внутреннего стандарта ТМС для ядер 1H, от сигнала растворителя для ядер 13C (d C 39,5 м. д.). Элементный состав полученных образцов был исследован на сканирующем электронном микроскопе Jeol JSM 7001F, оборудованном энергодисперсионным рентгенофлуоресцентным спектрометром Oxford INCA X-max 80.
Гексабромоплатинат, гексакис(тиоцианато-s)платинат, диметилсульфоксид, ацетонитрил, ик, ямр-спектроскопия, элементный анализ
Короткий адрес: https://sciup.org/147236626
IDR: 147236626 | УДК: 546.185 | DOI: 10.14529/chem220108
New ionic complexes of platinum(IV): [Ph3PCH3][PtBr5(dmso)] and [C(CH2OH)3NH3][K][Pt(SCN)6]
The first reports on dimethyl sulfoxide complexes appeared in the early 60s of the previous century. A large contribution into development of this field was made by a group of scientists led by Yu.N. Kukushkin, who studied the properties of complexes of platinum metals (II). Ionic dimethyl sulfoxide complexes of platinum (IV) are currently studied to a lesser extent. Methyltriphenylphosphonium (dimethylsulfoxide) pentabromoplatinate [Ph3PCH3][PtBr5(dmso)] (1) was obtained by dissolution of methyltriphenylphosphonium hexabromoplatinate in dimethyl sulfoxide with the 85% yield. Complexes of platinum with hexa kis (thiocyanato-S)platinum anions have hardly been studied. According to the data from the Cambridge Structural Database CSD, only five hexa kis (thiocyanato-S)platinum complexes were synthesized and structurally characterized, most of which had been obtained in the period from 1978 to 1999. Hexa kis (thiocyanato-S)platinum complex of platinum [C(CH2OH)3NH3(K)][Pt(SCN)6] (2) with two different cations (potassium and organylammonium) was synthesized from tris (2-hydroxymethyl)methylammonium chloride and potassium hexathiocyanatoplatinate in an aqueous solution of acetone with the 58% yield. The structure of the synthesized compounds was proven by IR, NMR spectroscopy and X-ray fluorescence analysis. The IR spectra of compounds 1 and 2 were recorded on a Shimadzu IRAffinity-1S IR spectrometer in KBr pellets in the range 4000-400 cm-1. The 1H and 13C NMR spectra were recorded on a Bruker AVANCE 500 spectrometer (500 MHz). Chemical shifts were measured from the internal TMS standard for 1H nuclei, from the solvent signal for 13C nuclei (dC 39.5 ppm). The elemental composition of the obtained samples was studied on a Jeol JSM 7001F scanning electron microscope equipped with an Oxford INCA X-max 80 X-ray energy-dispersive spectrometer.
Текст научной статьи Новые ионные комплексы платины(IV): [Ph3PCH3][PtBr5(dmso)] и [C(CH2OH)3NH3][K][Pt(SCN)6]
Диалкилсульфоксиды используются в качестве модельных соединений для изучения реакционной способности комплексов переходных металлов.
Синтез и структурные параметры свободных и металл-координированных сульфоксидов (Ru, Os, Rh, Ir) рассмотрены в нескольких обзорах [1–3]. Возрастающий интерес к диалкилсульфокси-дам вызван их способностью образовывать прочные комплексы с соединениями платины, поскольку они обладают свободными π* орбиталями, которые могут принимать электронную плотность от металлического центра. Молекула диметилсульфоксида (dmso) координируется атомом платины через атом серы, если между лигандами нет серьезных стерических препятствий, таких как наличие двух S-связанных и двух О-связанных лигандов диметилсульфоксида. Координация через атом серы более затруднена стерически, чем через атом кислорода [4–6].
Монозамещенные комплексы K[Pt(R 2 SO)Cl 3 ] синтезируют по реакции K 2 [PtCl 4 ] с сульфоксидом в мольном соотношении 1:1. Эти соединения являются важным исходным материалом для синтеза комплексов платины, содержащих смешанные сульфоксидные лиганды Pt(R 2 SO)(L)Cl 2 [4], которые нашли применение в химиотерапии из-за цитотоксических свойств в отношении устойчивых раковых клеток [7] и в процессах гидросилилирования благодаря своим каталитическим свойствам [8]. Комплексы платины с несимметричными сульфоксидами применяются в ка-
Неорганическая химия честве хиральных меток для изучения реакций лигандного обмена с помощью оптических измерений [9].
В комплексах с гексагалогеноплатинатными(IV) анионами возможна реакция лигандного замещения в координационной сфере платины. Замещение галогена на молекулу диметилсульфоксида происходит при взаимодействии галогенида тетраорганилфосфония, -аммония или -стибония с гексагалогеноплатиноводородной кислотой или ее солью непосредственно в растворе диметилсульфоксида либо при перекристаллизации гексагалогеноплатинатов(IV) из диметилсульфоксида [10–13].
Взаимодействием тетрахлороплатината(II) калия с бромидом калия и диэтилсульфоксидом в растворе смеси нитрометана и толуола с последующим медленным охлаждением был получен и структурно охарактеризован первый бромосодержащий сульфоксидный комплекс платины(II) – K[PtBr3(deso- S )] [14].
Мало изученными являются комплексы с гексакис (тиоцианато- S )платинатными анионами, хотя тиоцианатные лиганды представляют интерес, поскольку могут координироваться как атомом азота, так и атомом серы [15]. Из пяти структурно охарактеризованных комплексов, три комплекса: (H-thiamine)[Pt(SCN) 6 ]·H 2 O, (C 12 H 9 N 2 ) 2 [Pt(SCN) 6 ] и (Py 2 CH 2 )[Pt(SCN) 6 ] содержат катионы производных тиамина, фенантролина и пиридина [16–18]. Синтез комплексов осуществляли взаимодействием хлорида платины(IV) либо калиевой или натриевой соли гексахлороплатиноводородной кислоты с тиоцианатом калия или натрия с добавлением гетероциклического соединения. Остальные два комплекса представлены катионами сложного строения, содержащими Pt и V [15, 19]. О синтезе и строении гексакис (тиоцианато- S )платинатных комплексов, содержащих катионы аммония, ранее не сообщалось. Нами впервые был получен комплекс [(C 2 H 5 ) 4 N][K][Pt(SCN) 6 ] взаимодействием водно-ацетонитрильных растворов хлоридов органилам-мония и гексакис (тиоцианато- S )платината калия [20]. По данным РСА, в состав данного комплекса входят катионы калия, тетраэтиламмония и гексакис (тиоцианато- S )платинатные анионы, связанные в единое целое посредством мостиковых изоцианатных лигандов и катионов калия. Полученная структура представляет собой трехмерную сетку, в ячейках которой расположены катионы тетра-этиламмония. Посредством мостиковых тиоцианатных лигандов образуется трехмерный координационный полимер. Поэтому получение таких соединений вызывает несомненный интерес.
В настоящей работе описан синтез ионных комплексов платины(IV) и их состав.
Экспериментальная часть
[Ph 3 PCH 3 ][PtBr 5 (dmso)] ( 1 ). 0,035 г (0,028 ммоль) гексабромоплатината метилтрифенилфосфония растворяли в 2 мл диметилсульфоксида. После испарения растворителя наблюдали образование кристаллов. Выход комплекса 0,023 г (85 %), красно-коричневые кристаллы, т. разл. 226 °С.
ИК-спектр, ν, см–1: 3055, 2970, 2904, 1585, 1481, 1443, 1400, 1318, 1287, 1192, 1157, 1113, 1052, 995, 934, 896, 782, 747, 718, 688, 515, 499, 422. Найдено, %: С 26,91; Н 2,62. C 21 H 24 OSPPtBr 5 . Вычислено, %: С 26,95; Н 2,57.
[C(CH 2 OH) 3 NH 3 ][K][Pt(SCN) 6 ] (2) . Раствор 0,025 г (0,16 ммоль) хлорида трис (2-гидроксиметил)метиламмония в 6 мл смеси вода-ацетонитрил (1:1) приливали к раствору 0,05 г (0,08 ммоль) гексатиоцианатоплатината калия в 6 мл водно-ацетонитрильной смеси. Раствор концентрировали, образовавшиеся кристаллы фильтровали и сушили. Выход комплекса 0,046 г (58 %), красно-коричневые кристаллы, т. разл. 173 °С.
ИК-спектр, ν, см–1: 3348, 3310, 3267, 2989, 2898, 2170, 2116, 1500, 1462, 1405, 1359, 1315, 1234, 1202, 1095, 1031, 1006, 918, 785, 608, 532, 424. Найдено, %: С 18,43; H 1,89. C 10 H 12 O 3 N 7 KS 6 Pt. Вычислено, %: С 18,46, H 1,85.
ИК-спектры соединений 1 и 2 записывали на ИК-спектрометре Shimadzu IRAffinity-1S в таблетках KBr в области 4000–400 см–1.
Спектры ЯМР 1H и 13C регистрировали на спектрометре Bruker AVANCE 500 (500 МГц). Химические сдвиги измерены от внутреннего стандарта ТМС для ядер 1H, от сигнала растворителя для ядер 13C ( δ C 39,5 м. д.). В качестве растворителя использовали ДМСО.
Элементный состав полученных образцов был исследован на С, Н на анализаторе Carlo Erba CHNS-O EA1108 CHNS-O, а также на более тяжелые элементы (P, S, K, Br, Pt) на сканирующем электронном микроскопе Jeol JSM 7001F, оборудованном энергодисперсионным рентгенофлуоресцентным спектрометром Oxford INCA X-max 80.
Обсуждение результатов
Ранее взаимодействием бромида метилтрифенилфосфония с гексабромоплатинатом калия (2:1 мольн. соотношение) в ацетонитриле был получен комплекс [Ph3PCH3]2[PtBr6] [21]. Нами показано, что растворение последнего в диметилсульфоксиде приводит к встраиванию молекулы растворителя в координационную сферу платины, при этом образуются красно-коричневые кристаллы комплекса [Ph 3 PCH 3 ][PtBr 5 (dmso)] 1 с выходом 85 %:
dmso
[Ph 3 PCH 3 ] 2 [PtBr 6 ] → [Ph 3 PCH 3 ][PtBr 5 (dmso)] + [Ph 3 PCH 3 ]Br
Найдено, что взаимодействие гексатиоцианатоплатината калия с хлоридом трис (2-гидроксиэтил)метиламмония в мольном соотношении 1:2 сопровождалось изменением цвета реакционной смеси на красно-коричневый. Медленное испарение растворителя приводит к образованию оранжево-красных кристаллов 2 (58 %):
CH 3 CN
K 2 [Pt(SCN) 6 ] + [C(CH 2 OH) 3 NH 3 ]Cl → [C(CH 2 OH) 3 NH 3 ][K][Pt(SCN) 6 ] + KCl
В табл. 1 приведен элементный состав синтезированного комплекса 1 . Нормировка результатов показала, что соотношение элементов Pt:Br:S:P=1:4,95:0,98:0,95 хорошо согласуется с ожидаемым 1:5:1:1, что подтверждает предполагаемое строение комплекса [Ph 3 PCH 3 ][PtBr 5 (dmso)].
Из табл. 2 следует, что соотношение элементов в комплексе 2 Pt:K:S:N=1:1,54:5,01:7,33 удовлетворительно соответствует ожидаемому 1:1:6:7.
Таблица 1
Результаты элементного анализа комплекса 1
|
Элементный состав, ат. % |
|||
|
Pt |
Br |
S |
P |
|
1,76 |
8,72 |
1,73 |
1,67 |
Таблица 2
Результаты элементного анализа комплекса 2
|
Элементный состав, ат. % |
|||
|
Pt |
K |
S |
N |
|
2,37 |
3,65 |
11,87 |
17,38 |
Для рентгенофлуоресцентного энергодисперсионного анализа характерно систематическое завышение содержания легких элементов, поэтому содержание С, О и H не представлено в таблицах.
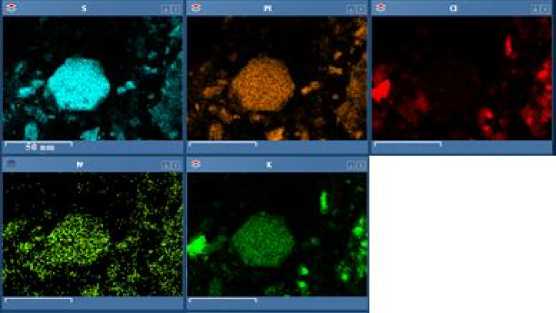
Образцы кристаллов комплексов 1 и 2 исследовали с помощью сканирующего электронного микроскопа, оснащенного приставкой для микрорентгеноспектрального анализа. На рис. 1а представлена морфология поверхности кристаллов комплекса 2 , которые представляют множество осколков кристаллов и правильный кристалл в форме шестигранной призмы. Также на картах распределения элементов видны следы побочного продукта – хлорида калия (рис. 1б).

а)
б)
Рис. 1. Микрофотография кристаллов комплекса 2 (а), карта распределения элементов (б)
Неорганическая химия
На основе данных элементного анализа можно предположить, что в комплексе 1 молекула диметилсульфоксида действительно встраивается в координационную сферу платины, замещая один бромид-ион, а присутствие К подтверждает предполагаемое строение комплекса 2 (рис. 2).
Br
Ph
I Br
Pt CH
I S3
Ph P CH 3
Ph
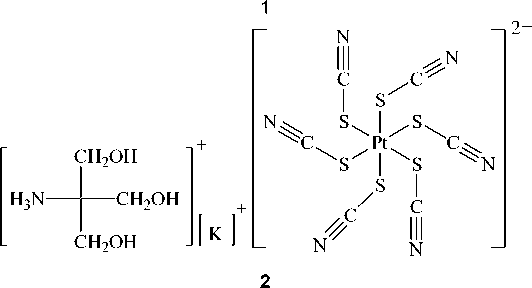
Рис. 2. Предполагаемое строение комплексов
Br II CH3
O
ИК-спектр комплекса 1 содержит полосы поглощения при 1443 см–1, характерные для колебаний связей фосфор-углерод. Присутствуют полосы средней интенсивности, соответствующие валентным колебаниям CAr–H в области 3080 - 3030 см–1. В ИК-спектре 1 , помимо вышеперечисленных полос, наблюдается интенсивная полоса поглощения S=O групп при 1113 см–1. Данные значения совпадают со справочными и указывают на связывание сульфоксида через атом серы [22, 23]. В ИК-спектре комплекса 2 при 2989 см–1 наблюдаются валентные колебания связи N– H (RNH 3 +). ИК-спектр также содержит характерные полосы OH-группы (3267 см–1) и колебания связи С–OH (1234, 1315, 1359 см–1). Кроме того, в ИК-спектре присутствует интенсивная полоса поглощения при 2116 см–1, характеризующая валентные колебания C≡N. Наблюдаются и слабые полосы в области 415–458 см–1, относящиеся к деформационным колебания NCS фрагмента [18, 19]. Анализ ИК-спектров указывает на S -координацию атома платины с тиоцианатным лигандом и согласуется с найденными полосами поглощения в аналогичных фрагментах.
Комплексы 1 и 2 исследовали методами 1H, 13C, 195Pt ЯМР спектроскопии. Для проведения анализа 1H ЯМР в качестве растворителя использовался диметилсульфоксид с сигналом при 2,50 м. д. ТМС использовали в качестве стандарта, химический сдвиг которого принят за 0 м. д.
В 1H ЯМР спектре 1 в области слабого поля (7,75 - 7,91 м. д.) наблюдаются сигналы протонов фенильных колец. Протоны, находящиеся в орто - и мета -положении фенильных лигандов, эквиваленты и дают мультиплетный сигнал в области 7,75 - 7,78 м. д. Протоны, находящиеся в пара положении фенильных колец, эквиваленты и дают мультиплетный сигнал в области 7,89 - 7,91 м. д. Сигнал от протонов CH 3 - группы наблюдается в виде дуплета в области 3,16 м. д. Спектр содержит сигнал диметилсульфоксидного лиганда в виде синглета в области 2,54 м. д.
Спектр 1H ЯМР комплекса 2 содержит синглетный сигнал протона гидроксильной группы -OH при 5,19 м. д. Сигналы эквивалентных протонов -СH 2 - наблюдаются в области 3,48 м. д., протонов при атоме азота при 7,71 м. д.
Спектр 13C ЯМР комплексов 1 и 2 регистрировали в ДМСО, сигнал растворителя наблюдали в области 39,82 и 40,90 м. д. Спектр 13С ЯМР комплекса 1 содержит сигналы атомов ароматического кольца при 120,39 м. д. С ip so , 130,54 м. д. С о , 133,69 м. д. С м , 135,31 м. д. С p . Сигнал атома углерода – CH 3 группы наблюдается при 7,75 м. д. В спектре комплекса 2 содержатся три неэквивалетных углеродных атома: сигнал атома углерода фрагмента -CH 2 - обнаруживается при 59,59 м. д., сигнал узлового атома углерода при 61,62 м. д., сигнал атома углерода фрагмента -SCN при 113,44 м. д.
В 195Pt ЯМР спектре комплекса 1 сигнал атома платины c диметилсульфоксидным лигандом в координационной сфере наблюдается при -2323 м. д. Полученные значения согласуются с литературными данными [24, 25].
Выводы
Таким образом, взаимодействие гексабромоплатината метилтрифенилфосфония с диметилсульфоксидом приводит к замещению хлорид-иона на молекулу растворителя в координационной сфере платины с образованием [Ph 3 PCH 3 ][PtBr 5 (dmso)] 1 . Реакция хлорида трис (гидрокси-метил)метиламмония с гексатиоцианатоплатинатом калия приводит к образованию [C(CH 2 OH) 3 NH 3 ][K][Pt(SCN) 6 ] 2 . Строение полученных соединений установлено ИК- и 1H-, 13C ЯМР-спектроскопией и ренгенофлуоресцентным анализом.
Список литературы Новые ионные комплексы платины(IV): [Ph3PCH3][PtBr5(dmso)] и [C(CH2OH)3NH3][K][Pt(SCN)6]
- Calligaris, M. Structure and Bonding in Metal Sulfoxide Complexes / M. Calligaris, O. Carugo // Coord. Chem. Rev. – 1996. – V. 153. – P. 83–154. DOI: 10.1016/0010-8545(95)01193-5.
- Calligaris, M. Structure and Bonding in Metal Sulfoxide Complexes: an Update / M. Calligaris // Coord. Chem. Rev. – 2004. – V. 248. – P. 351–375. DOI: 10.1016/j.ccr.2004.02.005.
- Alessio, E. Synthesis and Reactivity of Ru-, Os-, Rh-, and Ir-halide−sulfoxide Complexes / E. Alessio // Chem. Rev. – 2004. – V. 104. – P. 4203−4242. DOI: 10.1021/cr0307291.
- Rochon, F.D. Pt(II) Compounds with Sulfoxide Ligands and Crystal Structures of Complexes of the Types I(R2SO)Pt(ϻ-I)2Pt(R2SO)I and Trans-Pt(R2SO)(L)X2 (L = Amine, Pyridine and Pyrimidine) / F.D. Rochon, Ch. Tessier // Inorg. Chimica Acta. – 2008. – V. 361. – P. 2591–2600. DOI: 10.1016/j.ica.2007.10.041.
- Meek, D.W. Transition Metal Complexes of Dimethyl Sulfoxide / D.W. Meek, D.K. Straub, R.S. Drago // J. Am. Chem. Soc. – 1960. – V. 82. – P. 6013–6016. DOI: 10.1021/ja01508a012.
- Кукушкин, Ю.Н. Вклад исследований диметилсульфоксидных комплексов в теории координационной химии / Ю.Н. Кукушкин // Коорд. химия. – 1997. – Т. 23, № 3. – С. 163–174.
- Chiral and Achiral Platinum(II) Complexes for Potential Use as Chemotherapeutic Agents: Crystal and Molecular Structures of Cis-[Pt(L1)2] and [Pt(L1)Cl(MPSO)] [HL1 = N,N-diethyl-N′-benzoylthiourea] / Ch. Sacht, M.S. Datt, S. Otto et al. // J. Chem. Soc., Dalton Trans. – 2000. – P. 727–733. DOI: 10.1039/a908985c.
- Vekki, D.A. Hydrosilylation of Low-molecular Siloxanes in the Presence of Photoactivated Al-kene and Sulfoxide Platinum(II) Complexes / D.A. Vekki, N.K. Skvortsov // Russ. J. Gen. Chem. – 2006. – V. 76, № 1. – P. 116. DOI: 10.1134/S107036320601021X.
- Synthesis, Crystal Structures and Optical Activity of Cis- and Trans-(−)-dichloro[(S)-methylp-tolylsulfoxide]pyridylplatinum(II) Complexes / A.N. Skvortsov, D.A. de Vekki, A.I. Stash et al. // Tetra-hedron: Asymmetry. – 2002. – V. 13. – P. 1663–1671. DOI: 10.1016/S0957-4166(02)00420-2.
- Синтез и строение комплексов платины [Ph4P]+[PtCl3(dmso)]– и [Ph4P]+[PtCl5(dmso)]– / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Журн. неорг. химии. – 2013. – Т. 58, № 1. – С. 36–40. DOI: 10.1134/S0036023613010191.
- Шарутин, В.В. Синтез и строение комплекса платины [Ph4Sb(dmso)]+[PtCl5(dmso)]– / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина // Бутлеровские сообщения. – 2011. – Т. 28, № 20. – С. 35–39.
- Кукушкин, В.Ю. Дезоксигенирование диметилсульфоксида в комплексах платины / В.Ю. Кукушкин, Е.Ю. Панькова // Журн. общей хим. – 1987. – Т. 57, № 10. – С. 2391–2392.
- Окислительно-восстановительное превращение комплексов Pt(IV) с координационными молекулами диметилсульфоксида. Кристаллическая и молекулярная структуры трифенилбензил-фосфоний трихлоро(диметилсульфоксид)-платината(II) / С.С. Сотман, В.С. Фундаменский, В.Ю. Кукушкин и др. // Журн. общ. химии. – 1988. – Т. 58, № 10. – С. 2297–2304.
- Belsky, V.K. Structure of Potassium Tribromo(diethylsulfoxide)platinate(II) / V.K. Belsky, V.E. Konovalov, V.Yu. Kukushkin // Acta Cryst. – 1993. – C49. – P. 751–752. DOI: 10.1107/S0108270192008308.
- Кембриджская база структурных данных (CSD, Version 1.19) https://www.ccdc.cam.ac.uk
- Interactions Between Thiamine and Large Anions. Crystal Structures of (H-thiamine)[PtII(SCN)4]·3H2O and (H-thiamine)[PtIV(SCN)6]·H2O / K. Aoki, N.-H. Hu, T.Tokuno et al. // Inorg. Chimica Acta. – 1999. – V. 290. – P. 145–152. DOI: 10.1016/S0020-1693(99)00116-4.
- Ha, K. Crystal Structure of Bis(1,10-phenanthrolinium) Hexakis(thiocyanato-S)platinate(IV), (C12H9N2)2[Pt(SCN)6] / K. Ha // Z. Kristallogr. NCS. – 2010. – V. 225. – P. 699–700. DOI: 10.1524/ncrs.2010.0307.
- Seemann, J. Schwingungsspektren und Normalkoordinatenanalyse von Hexathiocyanatoplati-nat(IV), Kristallstruktur von [Py2CH2][Pt(SCN)6] / J. Seemann, W. Preetz // Z. Naturforsch. B: Chem. Sci. – 1998. – V. 53. – P. 13–16. DOI: 10.1515/znb-1998-0105.
- Spectral Properties and Crystal Structure of Bis(p-thiocyanato-iV,S)bis-(thiocyanato-N)tetrakis(5,7-dimethyl[1,2,4]triazolo[1,5-a]pyrimidine-N3)-dicopper(II) and of Tetrakis(5,7-dimethyl[1,2,4]triazolo[1,5-a]pyrimidine-N3)-platinum(II) Hexa(thiocyanatoS)platinate(IV) / M. Cingi, A. Lanfredi, A. Tiripicchio et al. // Inorg. Chimica Acta. – 1983. – V. 72. – P. 81–88. DOI: 10.1016/S0020-1693(00)81699-0.
- Шарутин, В.В. Синтез и строение гексатиоцианатоплатината(IV) калийтетраэтиламмония / В.В. Шарутин, О.К. Шарутина, А.Р. Ткачѐва // Изв. высш. уч. завед. Серия: Химия и хим. технология. – 2018. – Т. 61, № 12. – С. 6367. DOI: 10.6060/ivkkt.20206305.6115.
- Зыкова, А.Р. Новые гексабромоплатинаты органилтрифенилфосфония [Ph3PR]2[PtBr6], R = CH3, CH=CH2, CH2CH=CH2 / А.Р. Зыкова, В.В. Шарутин, О.К. Шарутина // Журн. неорг. хи-мии. – 2021. – Т. 66, № 1. – С. 63–68. DOI: 10.1134/S0036023621010149.
- Тарасевич, Б.Н. ИК-спектры основных классов органических соединений: справочные материалы / Б.Н. Тарасевич. – М.: МГУ имени М.В. Ломоносова, 2012. – 55 с.
- Palladium(II) and Platinum(II) Alkyl Sulfoxide Complexes of Sulfur-Bonded, Mixed Sulfur- and Oxygen-Bonded, and Totally Oxygen-Bonded Complexes / J.H. Price, A.N. Williamson, R.F. Schramm et al. // Inorg. Chem. – 1972. – V. 11, № 6. – P. 1280–1284. DOI: 10.1021/IC50112A025.
- Новиков, В.В. Анализ спектров ЯМР высокого разрешения / В.В. Новиков. – М.: Учебно-научный центр им. А.Н. Несмеянова, 2009. – 16 с.
- Three New Asymmetric Trans-amine(azole)dichloridoplatinum Complexes that Overcome Cis-platin Resistance and Their Reactions with 50 -GMP / E. Pantoja, A. Gallipoli, S. van Zutphen et al. // J. of Inorg. Biochem. – 2006. – V. 100. – P. 1955–1964. DOI: 10.1016/j.jinorgbio.2006.09.015.

![Новые ионные комплексы платины(IV): [Ph3PCH3][PtBr5(dmso)] и [C(CH2OH)3NH3][K][Pt(SCN)6] Новые ионные комплексы платины(IV): [Ph3PCH3][PtBr5(dmso)] и [C(CH2OH)3NH3][K][Pt(SCN)6]](/file/cover/147236626/novye-ionnye-kompleksy-platiny-ivph3pch3-ptbr5-dmso-i-c-ch2oh-3nh3-k-pt-scn.png)
