Новые маркеры для исследования пролиферации Т-лимфоцитов человека
Автор: Марченко Дарья Максимовна, Сайдакова Евгения Владимировна
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Иммунология
Статья в выпуске: 4, 2021 года.
Бесплатный доступ
Стандартная методика изучения пролиферации Т-лимфоцитов предполагает применение метода проточной цитометрии с использованием внутриклеточного маркера Ki67. Однако данный анализ требует предварительной фиксации и пермеабилизации клеток, что ограничивает возможность проведения дополнительных исследований. Цель настоящей работы - оценить потенциал использования поверхностной молекулы CD71 в качестве альтернативного маркера пролиферации Т-лимфоцитов. Методом проточной цитометрии определяли долю и уровень экспрессии CD71 и Кi67 в нестимулированных и стимулированных фитогемагглютинином Т-клетках периферической крови человека; выявляли взаимосвязь показателей экспрессии двух маркеров. Установлено, что стимуляция увеличивает долю и уровень экспрессии как Ki67, так и CD71 в CD4+ и CD8+ Т-лимфоцитах. Обнаружена сильная положительная корреляция между экспрессией двух молекул на Т-клетках различной субпопуляционной принадлежности. Вместе с тем выявлено, что все Ki67-положительные лимфоциты экспрессируют молекулу CD71, но большая часть CD71-позитивных клеток не экспрессирует молекулу Ki67. Исходя из полученных данных, можно заключить, что молекула CD71 не является полным аналогом Ki67, но может быть использована для исследований активированных/делящихся Т-лимфоцитов.
Cd4+ т-лимфоциты, cd8+ т-лимфоциты, пролиферация, проточная цитометрия, маркер ki67, маркер cd71
Короткий адрес: https://sciup.org/147236790
IDR: 147236790 | УДК: 571.27 | DOI: 10.17072/1994-9952-2021-4-316-323
Novel human T-cell proliferation markers
The standard method to study T-cell proliferation is flow cytometric evaluation of the intracellular Ki67 expression. However, this analysis requires preliminary cell fixation and permeabilization that limits further research. The aim of the present work was to evaluate the possibility of using the surface molecule CD71 as an alternative marker for T-cell proliferation. Frequencies of CD71+ and Ki67+ T-lymphocytes and candidate proliferation markers’ expression levels were studied in unstimulated and phytohemagglutinin-stimulated human peripheral blood cells using flow cytometry. We found that stimulation increases the frequency and level of Ki67 and CD71 expression in CD4+ and CD8+ T-cells. We revealed a strong positive correlation between the two molecules in different T-cell subsets. It should be noted that all Ki67+ T-cells expressed CD71, while the majority of CD71+ cells did not express Ki67. Based on the data obtained, one can conclude that CD71 is not a complete analog of Ki67, but it can be used for investigations of activated/cycling T-lymphocytes.
Текст научной статьи Новые маркеры для исследования пролиферации Т-лимфоцитов человека
Т-лимфоциты играют важную роль в формировании иммунного ответа [Zhu, Paul, 2008]. Благодаря пролиферации в периферических лимфоидных органах они быстро увеличивают свою численность для эффективной борьбы с патогенами [Liao et al., 2016]. Нарушение в процессе деления Т-клеток приводит к возникновению различных патологий, в т.ч. опухолевых, хронических инфекционных [Chou, Effros, 2013] и аутоиммунных заболеваний [Moulton, Tsokos, 2011]. Наиболее широко используемым методом исследования пролиферации лимфоцитов является проточная цитометрия с оценкой экспрессии маркера Ki67 [Scholzen, Gerdes, 2000]. Следует отметить, что внутриклеточная локализация этой молекулы обусловливает необходимость фиксации и пермеабилизации клеточных мембран [Jamur, Oliver, 2010], что исключает возможность дальнейшей оценки функционального состояния делящихся лимфоцитов. В связи с этим отказ от фиксации/пермеабилизации клеток и поиск поверхностных молекул-аналогов Ki67 представляется актуальным. Перспективным кандидатом на роль такой молекулы является рецептор трансферрина 1 (CD71).
Цель настоящей работы – исследование возможности использования CD71 в качестве альтернативного маркера пролиферации Т-лимфоцитов.
Материалы и методы исследований
Получение биологического материала
План работы был одобрен локальным этическим комитетом (рег. № комитета IRB00008964); каждый обследованный подписал форму информированного согласия. В исследование были приглашены 10 относительно здоровых добровольных доноров крови. Большинство участников (80%) составили женщины. Средний возраст обследованных составил 25 лет.
Забор крови осуществляли из кубитальной вены в пробирки, обработанные антикоагулянтом. Моно-нуклеарные клетки получали путем центрифугирования (400 g, 40 мин) крови в градиенте плотности диаколла ρ = 1.077 (Диаэм; Россия). Полученные образцы подвергали контролируемому замораживанию до –80ºС в течение суток в среде, содержащей 90% инактивированной теплом эмбриональной телячьей сыворотки (ЭТС; Gibco; США) и 10% диметилсульфоксида (MP Biochemicals; США), после чего переносили в жидкий азот для длительного хранения.
Постановка культур
Мононуклеарные клетки периферической крови размораживали и использовали для постановки культур. Лейкоциты культивировали в полной питательной среде (10% ЭТС, 100 Ед./мл пенициллина и 100 мкг/мл стрептомицина (Sigma, США) в RPMI-1640 (Sigma, США)) в концентрации 2×106/мл. Образцы стимулировали фитогемагглютинином (ФГА; Serva, Германия) в конечной концентрации 15 мкг/мл. В качестве контроля использовали клетки без добавления митогена. Полученные лейкоциты инкубировали в пробирках типа эппендорф объемом 2 мл при +37ºС в течение 42 ч.
Цитометрический анализ
Субпопуляционную принадлежность клеток периферической крови определяли с помощью коммерческих флуоресцентных красителей и антител: Zombie UV, CD3 PerCP, CD4 Brilliant Violet 605 (BioLegend, США); CD8 FITC (Dako, Дания); CD45R0 APCe-Fluor780 (eBioscience, США); CD71 Alexa Fluor 700 (Invitrogen, США); Ki67 PE (BD Pharmingen, США).
Цитометрический анализ проводили на приборе CytoFLEX S (Beckman Coulter, США). Для визуализации результатов использовали программу CytExpert (Beckman Coulter, США).
Гейтирование клеток осуществляли с помощью программы FlowJo v10 (FlowJo LLC, США). Из пула анализируемых клеток последовательно выделяли одиночные и жизнеспособные элементы. Т-клетки идентифицировали как CD3-позитивные лимфоциты, которые делили на CD8+ и CD4+ Т-клетки. Степень дифференцировки каждой субпопуляции анализировали по экспрессии CD45R0: CD45R0+ элементы оценивали как Т-лимфоциты памяти, CD45R0– – как наивные Т-клетки. Следует отметить, что среди CD8+CD45R0– Т-лимфоцитов присутствовали как наивные, так и терминально дифференцированные клетки [Akbar et al., 1988].
Статистическая обработка данных
Анализ данных выполнялся методами непараметрической статистики. Рассчитывали медиану и интерквартильный размах (25–75%). Статистическую значимость различий между группами устанавливали на основе U-критерия Манна-Уитни. Корреляционный анализ выполняли по методу Спирмена. Вычис- ления и построение графиков проводили с использованием пакета Microsoft Office и программы GraphPad Prism 8 (GraphPad Software, США).
Результаты и их обсуждение
Экспрессия Ki67
Стимуляция мононуклеарных лейкоцитов ФГА в течение 42 ч. привела к увеличению доли Т-лимфоцитов, экспрессирующих Ki67. Это наблюдалось в общем пуле Т-клеток (рис. 1А) и в пулах CD4-позитивных (рис. 1Б) и CD8-позитивных (рис. 1В) Т-лимфоцитов.
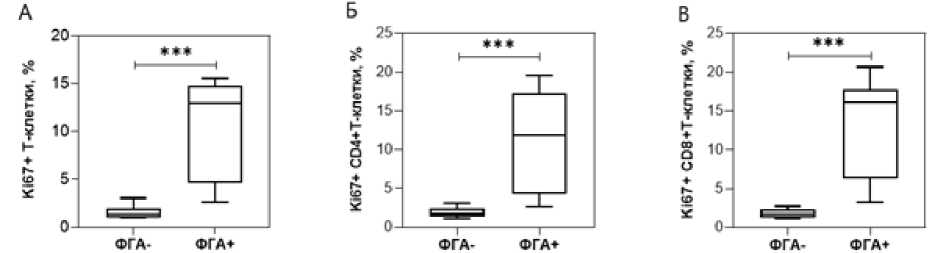
Рис. 1 . Процентное содержание Ki67-позитивных клеток среди нестимулированных и стимулированных Т-лимфоцитов.
ФГА+ – клетки, стимулированные фитогемагглютинином; ФГА– – нестимулированные клетки. Различия между группами устанавливали с использованием U-критерия Манна-Уитни (*** – P < 0.001). А – все Т-лимфоциты; Б – CD4+ Т-лимфоциты; В – CD8+ Т-лимфоциты
[Percentage of Ki 67-positive cells among unstimulated and stimulated T-lymphocytes.
PHA+ - cells stimulated by phytohemagglutinin; PHA- - unstimulated cells. The differences between the groups were established using the Mann-Whitney U-test (*** - P < 0.001). A – all T-lymphocytes; B - CD4+ T-lymphocytes; C -
CD8+ T-lymphocytes]
Помимо этого, в стимулированных Т-клетках по сравнению с нестимулированными лимфоцитами повысился средний уровень экспрессии молекулы Ki67. Отмеченное изменение не зависело от субпопуляционной принадлежности Т-лимфоцитов и наблюдалось в их общем пуле (рис. 2А) и пулах CD4+ (рис. 2Б) и CD8+ (рис. 2В) Т-клеток.
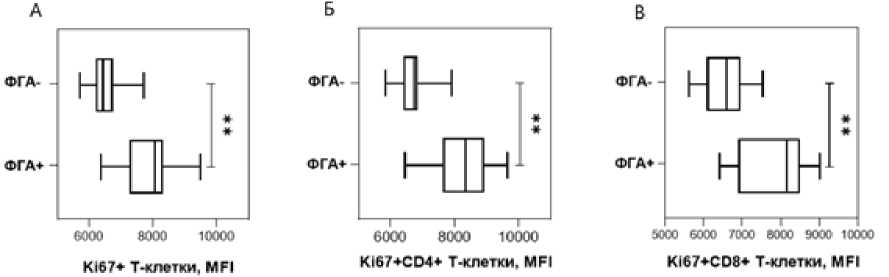
Рис. 2 . Уровень внутриклеточной экспрессии Ki67 в нестимулированных и стимулированных Т-лимфоцитах.
ФГА+ – клетки, стимулированные фитогемагглютинином; ФГА– – нестимулированные клетки. MFI – медиана интенсивности флуоресценции (median fluorescence intensity). Различия между группами устанавливали с использованием U-критерия Манна-Уитни (** – P < 0.001). А – все Т-лимфоциты; Б – CD4+ Т-лимфоциты; В –
CD8+ Т-лимфоциты
[The level of intracellular expression of Ki67 in unstimulated and stimulated T-lymphocytes.
PHA+ – cells stimulated by phytohemagglutinin; PHA- – unstimulated cells. MFI is the median fluorescence intensity. The differences between the groups were established using the Mann-Whitney U-test (** – P < 0.001). A – all T-lymphocytes; B – CD4+ T-lymphocytes; C – CD8+ T-lymphocytes]
Аналогичные результаты были получены в субпопуляциях различной степени зрелости, в т.ч. наивных Т-клетках и Т-лимфоцитах памяти (табл. 1): после стимуляции среди них выросли доля Ki67-положительных клеток и уровень экспрессии молекулы.
Таблица 1
Отличия экспрессии Ki67 в нестимулированных и стимулированных Т-лимфоцитах различной степени зрелости
[Differences in Ki67 expression in unstimulated and stimulated T-lymphocytes of varying degrees of maturity]
|
Показатели |
CD4+ Т-клетки |
CD8+ Т-клетки |
|||
|
ФГА – |
ФГА + |
ФГА – |
ФГА + |
||
|
CD45R0–Ki67+ Т-клетки |
(%) |
1,4 (1,0-2,0) P<0,001 |
11,6 (4,8-16,6) |
1,4 (1,3-2,2) P<0,001 |
15,4 (5,1-19,8) |
|
CD45R0+Ki67+ Т-клетки |
(%) |
2,0 (1,8-3,1) P<0,001 |
9,2 (5,4-13,4) |
1,7 (1,6-2,1) P<0,001 |
10,6 (6,4-15,7) |
|
CD45R0–Ki67+ Т-клетки |
(MFI) |
6270 (5983-6439) P<0,001 |
8002 (7686-8090) |
6583 (6112-6783) P<0,01 |
8228 (7198-8683) |
|
CD45R0+Ki67+ Т-клетки |
(MFI) |
7209 (7098-7300) P<0,01 |
8573 (8072-9326) |
6621 (6234-6868) P<0,05 |
7899 (7463-8355) |
Примечание. Указаны медианы и интерквартильные размахи. ФГА+ – клетки, стимулированные фитогемагглютинином; ФГА– – нестимулированные клетки. MFI – медиана интенсивности флуоресценции (median fluorescence intensity). Статистический анализ – U-критерий Манна-Уитни.
Экспрессия CD71
Анализ экспрессии молекулы CD71 на поверхности нестимулированных и стимулированных Т-лимфоцитов показал следующее. Было обнаружено, что содержание CD71-позитивных Т-клеток повысилось в стимулированных образцах относительно нестимулированных проб. Рост был характерен для общего пула Т-лимфоцитов (рис. 3А) и пулов CD4+ (рис. 3Б) и CD8+ (рис. 3В) Т-клеток.
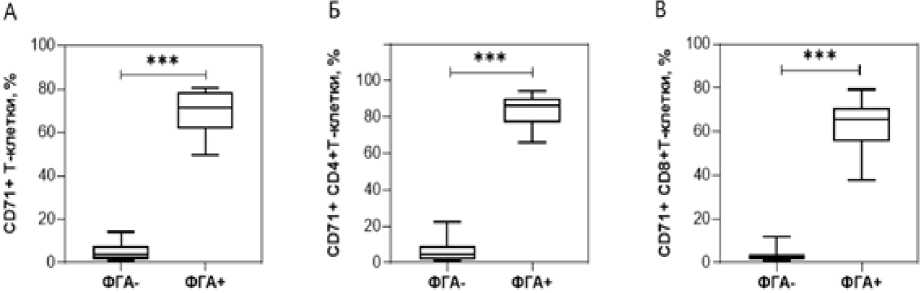
Рис. 3 . Процентное содержание CD71-позитивных клеток среди нестимулированных и стимулированных Т-лимфоцитов.
ФГА+ – клетки, стимулированные фитогемагглютинином; ФГА– – нестимулированные клетки. Различия между группами устанавливали с использованием U-критерия Манна-Уитни (*** – P < 0.001). А – все Т-лимфоциты; Б – CD4+ Т-лимфоциты; В – CD8+ Т-лимфоциты
[Percentage of CD71-positive cells among unstimulated and stimulated T-lymphocytes.
PHA+ – cells stimulated by phytohemagglutinin; PHA- – unstimulated cells. The differences between the groups were established using the Mann-Whitney U-test (***– P < 0.001). A – all T-lymphocytes; B – CD4+ T-lymphocytes; C – CD8+ T-lymphocytes]
Также после стимуляции увеличился средний уровень экспрессии молекулы CD71, что было отмечено в общем пуле Т-клеток (рис. 4А) и среди CD4-позитивных (рис. 4Б) и CD8-позитивных (рис. 4В) Т-лимфоцитов.
Сходное увеличение доли CD71+ элементов и уровня экспрессии молекулы было зафиксировано в субпопуляциях различной степени зрелости, в т.ч. наивных Т-клетках и Т-лимфоцитах памяти (табл. 2).
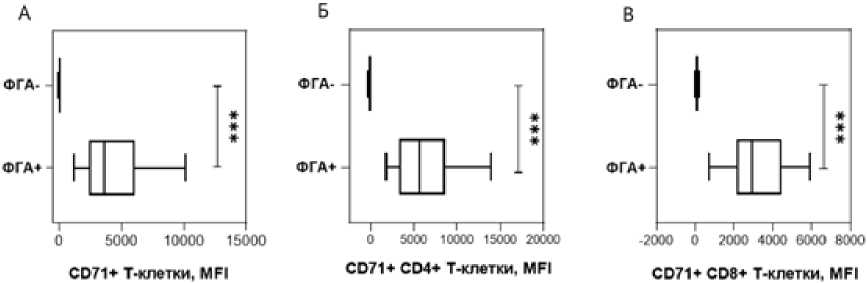
Рис. 4 . Уровень поверхностной экспрессии CD71 на нестимулированных и стимулированных Т-лимфоцитах.
ФГА+ – клетки, стимулированные фитогемагглютинином; ФГА– – нестимулированные клетки. MFI – медиана интенсивности флуоресценции (median fluorescence intensity). Различия между группами устанавливали с использованием U-критерия Манна-Уитни (*** – P < 0.001). А – все Т-лимфоциты; Б – CD4+ Т-лимфоциты; В –
CD8+ Т-лимфоциты
[The level of CD71 surface expression on unstimulated and stimulated T-lymphocytes.
PHA+ – cells stimulated by phytohemagglutinin; PHA- – unstimulated cells. MFI is the median fluorescence intensity. The differences between the groups were established using the Mann-Whitney U-test (*** – P < 0.001). A – all T-lymphocytes; B – CD4+ T-lymphocytes; C – CD8+ T-lymphocytes]
Таблица 2
Отличия экспрессии CD71 на нестимулированных и стимулированных Т-лимфоцитах различной степени зрелости
[Differences in CD71 expression on unstimulated and stimulated T-lymphocytes of varying degrees of maturity]
|
Показатели |
CD4+ Т-клетки |
CD8+ Т-клетки |
||
|
ФГА – |
ФГА + |
ФГА – |
ФГА + |
|
|
CD45R0–CD71+ Т-клетки (%) |
6,0 (3,8-8,5) P<0,001 |
94,1 (88,1-95,8) |
5,3 (2,8-7,0) P<0,001 |
70,1 (63,8-77,5) |
|
CD45R0+CD71+ Т-клетки (%) |
5,5 (2,6-5,9) P<0,001 |
79,6 (73,7-85,9) |
2,3 (1,8-3,8) P<0,001 |
61,2 (44,0-63,7) |
|
CD45R0–CD71+ Т-клетки (MFI) |
-191 (-237… -149) P<0,001 |
7827 (3626-10392) |
96,3 (26,2-135,3) P<0,001 |
4456 (2922-5484) |
|
CD45R0+CD71+ Т-клетки (MFI) |
9,8 (-26,8…56,7) P<0,001 |
4436 (3152-4937) |
220 (181-297) P<0,001 |
2184 (1497-3461) |
Примечание. Указаны медианы и интерквартильные размахи. ФГА+ – клетки, стимулированные фитогемагглютинином; ФГА– – нестимулированные клетки. MFI – медиана интенсивности флуоресценции (median fluorescence intensity). Статистический анализ – U-критерий Манна-Уитни.
Взаимосвязь экспрессии Ki67 и CD71
Оценка взаимосвязи экспрессии Ki67 и CD71 показала наличие сильной положительной корреляции, которая наблюдалась в следующих субпопуляциях: CD4+ Т-клетки, наивные CD4+ Т-лимфоциты, CD4+ Т-клетки памяти, CD8+ Т-лимфоциты, CD8+CD45R0- Т-клетки, CD8+ Т-лимфоциты памяти (табл. 3).
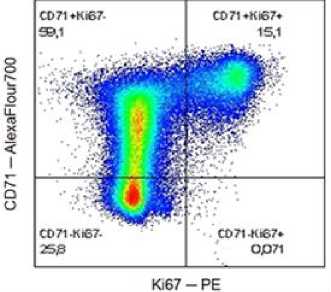
Примечательно, что среди Т-лимфоцитов все Ki67-позитивные клетки экспрессировали CD71, но при этом в культуре присутствовала субпопуляция CD71-монопозитивных лимфоцитов (рис. 5).
Анализ численности CD71+Ki67– Т-лимфоцитов показал, что содержание этих клеток в стимулированных и нестимулирован-
Рис. 5. Показательная точечная диаграмма экспрессии CD71 и Ki67 в стимулированных Т-лимфоцитах [Indicative dot diagram of CD71 and Ki67 expression in stimulated T-lymphocytes]
ных образцах значительно превышало количество CD71+Ki67+ Т-лимфоцитов. Данное явление наблюдалась в их общем пуле (рис. 6А) и пулах CD4+ (рис. 6Б) и CD8+ (рис. 6В) Т-клеток.
Таблица 3
Связь между экспрессией CD71 и Ki67 в субпопуляциях T-лимфоцитов различной степени зрелости [The relationship between CD71 and Ki67 expression in subpopulations of T-lymphocytes of varying degrees of maturity]
|
Корреляционная связь |
R |
P |
|
Т-клетки (%) |
0,793 |
<0,001 |
|
CD4+ Т-клетки (%) |
0,830 |
<0,001 |
|
Наивные CD4+ Т-клетки (%) |
0,854 |
<0,001 |
|
CD4+ Т-клетки памяти (%) |
0,823 |
<0,001 |
|
CD8+ Т-клетки (%) |
0,847 |
<0,001 |
|
CD8+CD45R0- Т-клетки (%) |
0,842 |
<0,001 |
|
CD8+ Т-клетки памяти (%) |
0,827 |
<0,001 |
Примечание. При проведении анализа использован метод ранговых корреляций Спирмена.
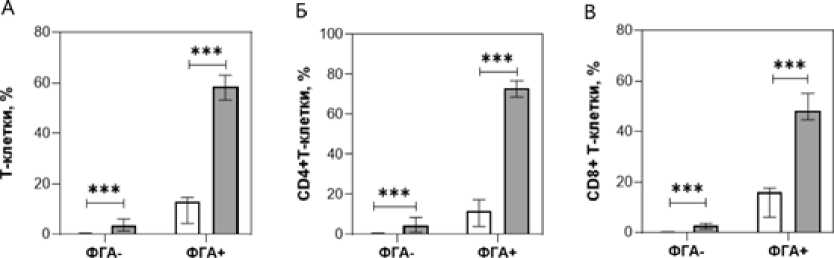
□ CD71+Ki67* клетки □ CD71+Ki67- клетки
Рис. 6 . Процентное содержание CD71+Ki67+ и CD71+Ki67– клеток среди нестимулированных и стимулированных Т-лимфоцитов.
ФГА+ – клетки, стимулированные фитогемагглютинином; ФГА– – нестимулированные клетки. Различия между группами устанавливали с использованием U-критерия Манна-Уитни (*** – P < 0.001). А – все Т-лимфоциты; Б – CD4+ Т-лимфоциты; В – CD8+ Т-лимфоциты
[Percentage of CD71+Ki67+ and CD71+Ki67 cells among unstimulated and stimulated T-lymphocytes.
PHA+ - cells stimulated by phytohemagglutinin; PHA- – unstimulated cells. The differences between the groups were established using the Mann-Whitney U-test (***– P < 0.001). A – all T-lymphocytes; B - CD4+ T-lymphocytes;
C – CD8+ T-lymphocytes]
Сходное отличие долей CD71+Ki67+ и CD71+Ki67– клеток было установлено в субпопуляциях различной степени зрелости, в т.ч. наивных Т-лимфоцитах и Т-клетках памяти (табл. 4).
Таблица 4
Отличие относительного количества CD71+Ki67+ и CD71+Ki67– клеток среди нестимулированных и стимулированных Т-лимфоцитов различной степени зрелости
[The difference in the relative number of CD71+Ki67+ and CD71+Ki67‒ cells among unstimulated and stimulated T-lymphocytes of varying degrees of maturity]
|
Показатели |
ФГА– |
ФГА+ |
||
|
CD71+Ki67+ |
CD71+Ki67– |
CD71+Ki67+ |
CD71+Ki67– |
|
|
Наивные CD4+ Т-клетки (%) |
0,17 (0,11-0,44) P 1-2 <0,001 |
5,76 (3,71-8,15) |
11,51 (4,77-16,57) P 3-4 <0,001 |
80,42 (74,14-84,04) |
|
CD4+ Т-клетки памяти(%) |
0,59 (0,39-1,01) P 1-2 <0,001 |
4,91 (2,04-9,12) |
9,15 (5,14-13,40) P 3-4 <0,001 |
69,30 (65,25-73,42) |
|
CD8+ СD45R0-Т-клетки (%) |
0,21 (0,13-0,38) P 1-2 <0,001 |
5,07 (2,70-6,40) |
15,30 (4,96-19,44) P 3-4 <0,001 |
51,33 (48,76-54,76) |
|
CD8+ Т-клетки памяти (%) |
0,23 (0,20-0,33) P 1-2 <0,001 |
2,10 (1,60-3,50) |
10,47 (6,12-15,51) P 3-4 <0,001 |
44,98 (34,25-53,42) |
Примечание. Указаны медианы и интерквартильные размахи. ФГА+ – клетки, стимулированные фитогемагглютинином; ФГА– – нестимулированные клетки. Статистический анализ – U-критерий Манна-Уитни.
Известно, что функция рецептора трансферрина 1 состоит в поставке железа внутрь клетки [Gammella et al., 2017]. Активированным Т-лимфоцитам требуется больше этого микроэлемента, чем покоящимся клеткам. Так, железо необходимо для интенсификации биохимических процессов, связанных с последующим делением, в т.ч. активации циклин-зависимых киназ, синтеза дезоксирибонуклеотидов [Testa, Pelosi, Peschle, 1993] и железосерных кластеров митохондрий [Napier, Ponka, Richardson, 2005]. Также известно, что истощение запасов железа вызывает остановку клеточного цикла в G1/S и апоптоз лимфоцитов [Yu, Kovacevic, Richardson, 2007]. Однако наши данные свидетельствуют, что CD71-позитивные Т-клетки отражают субпопуляцию не только делящихся, но и активированных лимфоцитов.
Отсутствие экспрессии Ki67 в части CD71-позивтивных Т-клеток вызывает много вопросов. Поступившие внутрь лимфоцита атомы железа могут не только вовлекаться в процесс деления клетки, но и связываться с белком ферритином для хранения [Dörner et al., 1980]. Однако известно, что экспрессия рецептора трансферрина 1 и ферритина являются взаимоисключающими процессами в Т-лимфоцитах. Трансляция этих белков регулируется системой, включающей железочувствительный элемент мРНК (IRE) и его регуляторный белок (IRP) [Testa et al., 1991]. При активации Т-лимфоцита свободный от железа IRP присоединяется к мРНК рецептора трансферрина и усиливает трансляцию CD71, чем увеличивает поток железа в клетку. В это же время к мРНК ферритина присоединяется блокирующий его трансляцию IRP. Следовательно, усиление притока железа через обильно экспрессирующийся на активированных Т-лимфоцитах рецептор CD71 не может рассматриваться как механизм увеличения запасов микроэлемента, но свидетельствует о подготовке клеток к делению. Поэтому судьба CD71+Ki67– Т-лимфоцитов остается не до конца понятной.
Заключение
Таким образом, в стимулированной ФГА культуре мононуклеарных лейкоцитов по сравнению с не-стимулированными клетками растут доли Ki67+ и CD71+ Т-лимфоцитов, а также уровни экспрессии данных маркеров, что говорит о вступлении клеток в пролиферативный цикл. Ввиду того, что молекула CD71 экспрессируется как на делящихся, так и на активированных Т-лимфоцитах, этот маркер не является полным аналогом Ki67 и не может использоваться как точный индикатор пролиферации Т-клеток. Вместе с тем молекула CD71 может применяться при исследовании активации/пролиферации Т-лимфоцитов.
Список литературы Новые маркеры для исследования пролиферации Т-лимфоцитов человека
- Akbar A.N. et al. Loss of CD45R and gain of UCHL1 reactivity is a feature of primed T cells // J. Immunol. 1988. Vol. 140. P. 2171-2178.
- Chou J.P., Effros R.B. T Cell Replicative Senescence in Human Aging // Curr. Pharm. Des. 2013. Vol. 19. P. 1680-1698.
- Dorner M.H. et al. Ferritin synthesis by human T lymphocytes // Science. 1980. Vol. 209, № 4460. P. 1019-1021.
- Gammella E. et al. The transferrin receptor: the cellular iron gate // Metallomics. 2017. Vol. 9, № 10. Р. 1367-1375.
- Jamur M.C., Oliver C. Permeabilization of cell membranes // Methods Mol Biol. 2010. Vol. 588. P. 63-66.
- Liao F. et al. T cell proliferation and adaptive immune responses are critically regulated by protein // Cell Cycle. 2016. Vol. 15, № 8. P. 1073-1083.
- Moulton V.R., Tsokos G.C. Abnormalities of T cell signaling in systemic lupus erythematosus // Arthritis. Res. Ther. 2011. Vol. 13. P. 207.
- Napier I., Ponka P., Richardson D.R. Iron trafficking in the mitochondrion: novel pathways revealed by disease // Blood. 2005. Vol. 105, № 5. P. 1867-1874.
- Scholzen T., Gerdes J. The Ki-67 protein: from the known and the unknown // J. Cell. Physiol. 2000. Vol. 182, № 3. P. 311-322.
- Testa U. et al. Differential regulation of iron regulatory element-binding protein(s) in cell extracts of activated lymphocytes versus monocytes-macrophages // J. Biol. Chem. 1991. Vol. 266, № 21. P. 13925-13930.
- Testa U., Pelosi E., Peschle C. The transferrin receptor // Critical Reviews in Oncogenesis. 1993. Vol. 4, № 3. P. 241-276.
- Yu Y., Kovacevic Z., Richardson D.R. Tuning cell cycle regulation with an iron key // Cell Cycle. 2007. Vol. 6, № 16. P. 1982-1994.
- Zhu J., Paul W.E. CD4 T cells: fates, functions, and faults // Blood. 2008. Vol. 112, № 5. P. 1557-1569.


