Новые твердые электролиты для электрохимических сенсоров контроля серы и индия в различных средах
Автор: Леушина А.П., Мамонтова Е.В., Зяблицев В.Е., Ашихмина Т.Я.
Журнал: Известия Коми научного центра УрО РАН @izvestia-komisc
Рубрика: Химические науки
Статья в выпуске: 4 (20), 2014 года.
Бесплатный доступ
Для создания электрохимического сенсора, селективного по отношению к сере и индию, впервые получены индийпроводящий твёрдый электролит (In2S3)1-х (InCl3)х и индийсодержащие твёрдоэлектролитные мембраны (InCl3)1-х(MCl2)х. Исследованы их транспортные характеристики: электропроводность, среднеионные числа переноса, определен тип ионной проводимости. Показана возможность их применения для получения измерительного электрода In2±δ S3 с контролируемым составом и свойствами для электрохимического сенсора на сера- и индийсодержащие среды
Твёрдый электролит, электрохимические сенсоры, транспортные характеристики, полупроводниковые соединения, контролируемый состав, кулонометрическое титрование
Короткий адрес: https://sciup.org/14992711
IDR: 14992711 | УДК: 546.681
New solid electrolytes for electrochemical sensors of sulphur and indium in various media
To create an electrochemical sensor, selective with respect to sulfur and indium the indium-conductive solid electrolyte (In2S3)1-х(InCl3)х and indium-containing solid electrolyte membranes (InCl3)1-х(MgCl2)х were obtained for the first time. Their structure and transport properties: electrical conductivity, secondary ion transport numbers were studied, the type of ionic conductivity was defined. According to the obtained x-ray pictures, the region of existence of solid solutions based on indium sulfide extends to 7.0 mol.% InCl3. Presumably the dissolution of indium chloride in indium sulfide occurs by the vacancy mechanism of defect formation. The formation of vacancies in the indium sublattice can be a source of cationic ion transport In3 + in this system.The activation energy of electroconductivity of compositions that lie within the area of solid solutions, changes from 1.81 to 1.95 eV for the system (InCl3)1- х(MgCl2)х and from 2.15 to 4.85 eV for the system (In2S3)1-х(InCl3)х. With increase of temperature from 373 to 503 K the electroconductivity increases in the system (InCl3)1-х(MgCl2)х from 10-7 to 10-5 Sm/cm, in the system (In2S3)1-х(InCl3)х from 10 -9 to 10-6 Sm/cm.For solid solutions of indium chloride, in indium sulfide the ion transport numbers are close to unity, so the system (In2S3)1-х(InCl3)х in the range of optimal temperatures and compositions can be used as a solid electrolyte with presumable ion conductivity In3+. The experimental results obtained by Tubandta method confirmed almost unipolar indium cation conductivity (III).The picture of coulometric titration curve indicates the existence of bilateral field homogeneity on the basis of In2S3, and the areas with excess and lack of indium are symmetrical, that is indium sulfide is described by In2±δS3. The width of the homogeneity region is 0.43%, which indicates the deviation from stoichiometry δ = 2,2 · 10-3 of atomic fractions of indium.
Текст научной статьи Новые твердые электролиты для электрохимических сенсоров контроля серы и индия в различных средах
Нарастающая антропогенная нагрузка приводит к необходимости повышения контроля в окружающей среде экологически опасных веществ как ши- роко распространённых (например, сера и её соединения), так и редко встречающихся (например, индий и его соединения). Наиболее широкое применение в аналитическом контроле получили методы потенциометрии и хроматографии, чувствитель- ным элементом которых являются датчики, обратимые относительно анализируемого компонента. Однако существующие промышленные датчики не обеспечивают достаточную точность в области концентраций, близких к ПДК, и характеризуются не высоким быстродействием [1].
Этих недостатков лишены электрохимические сенсоры с нестехиометрическими полупроводниковыми измерительными электродами, позволяющими определять содержание токсичных веществ в области их концентраций до 10-6 % при величине быстродействия 3 – 5 сек. [2, 3]. Для получения нестехиометрического сульфида индия, используемого в качестве измерительного электрода в составе электрохимического сенсора на серо- и индийсодержащие соединения высокоточным методом кулонометрического титрования (КТ), необходимы твёрдые электролиты (ТЭ) с проводимостью по ионам индия (III). В настоящей работе рассматривается возможность получения твёрдых электролитов на базе индийсодержащих соединений In 2 S 3 и InCl 3 , исследование их транспортных характеристик и типа ионной проводимости, а также возможность применения полученных ТЭ для электрохимического регулирования состава нестехиометрического сульфида индия. Актуальность работы подчеркивается отсутствием в литературе сведений об индийпроводящих ТЭ.
Создание ТЭ с проводимостью по катионам индия затруднено, так как многозарядные ионы сильно связаны в кристалле за счёт большого электростатического взаимодействия [4]. Поэтому для получения индийпроводящего ТЭ представляют интерес материалы с ионной проводимостью на основе квазибинарных солевых систем (КБСС) [5].
Объектом исследования выбраны КБСС (In 2 S 3 ) 1-х (InCl 3 ) х и ( InCl 3 ) 1-х (MCl 2 ) х (М = Cd, Mg, Mn, Sn, Zn) , в которых возможен вакансионный механизм ионного переноса в случае образования твёрдых растворов на основе In 2 S 3 и InCl 3 .
Диаграммы плавкости систем (InCl 3 ) 1-х (MCl 2 ) х содержат ограниченные твёрдые растворы эвтектического типа на основе InCl 3 [6]. Электролитические свойства этих квазибинарных солевых систем исследовали в области составов твёрдых растворов, которую определяли по диаграммам состояния [6]. Для системы (In 2 S 3 ) 1-х (InCl 3 ) х в литературе данные о диаграмме состояния отсутствуют. В настоящей работе система (In 2 S 3 ) 1-х (InCl 3 ) х синтезирована и исследована впервые.
Методика эксперимента
Для получения образцов предполагаемых индийсодержащих ТЭ рассчитанные навески безводных солей базисного соединения и легирующей добавки взвешивали, растирали в агатовой ступке 20–30 мин. до получения однородной смеси и таблетировали при давлении 15 МПа/см2. Таблетки толщиной 1 – 2 мм отжигали 15 – 20 час. (в зависимости от состава) при температуре 523 К в непрерывном токе аргона (марка А, ГОСТ 10157-79), очищенного от воды и кислорода по методике Гнау- ка [7]. Для более полной гомогенизации состава таблетки в тех же условиях повторно растирали в агатовой ступке, таблетировали и отжигали в течение 8–10 час. Готовые таблетки полировали до получения гладкой поверхности и исследовали под микроскопом МБС-2 (80-кратное увеличение); на поверхности таблеток не было обнаружено пор и других дефектов.
Отожжённые образцы системы (In 2 S 3 ) 1-х (InCl 3 ) х с содержанием 1,0–14,0 мол.% хлорида индия исследовали до и после измерения транспортных свойств рентгенофазовым анализом (РФА) на дифрактометре ДРОН-4-07 (Си К -излучение, 2 0 = 10 -80 ° , шаг 0,2 ° , время экспозиции 1 с.). Для обработки рентгенограмм использовали программный пакет WinXPower, причём учитывали дифракционные линии с интенсивностью более 2%.
Измерение электропроводности проводили методом кондуктометрии с блокирующими графитовыми электродами. Для обеспечения хорошего контакта с электродами таблетки полировали на графите. Кондуктометрические вычисления выполняли с помощью моста переменного тока Р-577 (частота 1кГц). Электропроводность измеряли при температурах от 350 до 525 К, максимальная относительная погрешность измерений составляла 5%. На основании полученных данных о величине сопротивления рассчитывали значение общей электропроводности.
Среднеионные числа переноса определяли компенсационным методом измерения электродвижущей силы (ЭДС) в ячейке:
С / InSb, Sb / TЭ, In3+/ In 2 Se 3 , Se / С . (1)
Для электрохимического введения индия в сульфид индия использовали электролиз с ТЭ (In 2 S 3 ) 1-х (InCl 3 ) х в присутствии мембраны ( InCl 3 ) 1-х (MCl 2 ) х . Кулонометрическое титрование проводили в гальваностатическом режиме при температуре 553±2 К с использованием электрохимической ячейки:
(-) С / In 2±δ S 3 , X / (In 2 S 3 ) 0,95 (InCl 3 ) 0,05 ¦¦
(InCl 3 ) 0,985 (CdCl 2 ) 0,015 / InSb, In /С(+). (2)
Сигнал ЭДС измеряли универсальным вольтметром В7-16А с использованием усилителя У5-9. Исследовали зависимость ЭДС от температуры в интервале 373 – 553 К. Истинной (равновесной) считали ЭДС, значения которой не изменялись в течение 0,5–1,0 час. и совпадали для параллельных экспериментов.
Результаты эксперимента
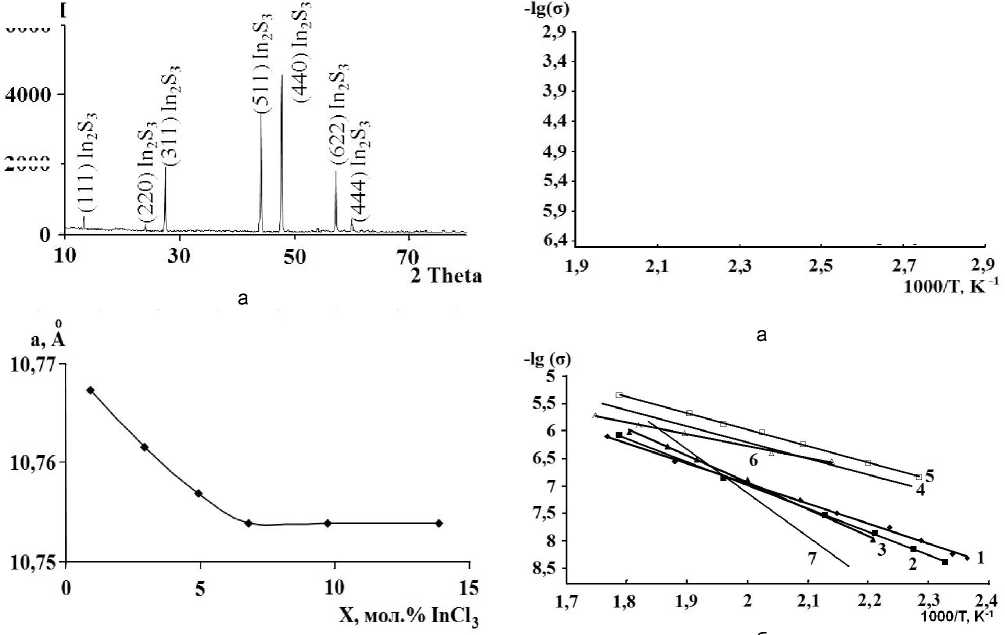
Рентгенограммы образцов, содержащих 1,0– 7,0 мол.% InCl 3 , имеют рефлексы только базисного соединения, которое кристаллизуется в кубической решётке. Об этом же свидетельствует зависимость параметра а от содержания легирующей добавки, который линейно убывает до 7,0 мол.% InCl 3 , а затем остается постоянным (рис. 1). Таким образом, определяемая экспериментально область существования твёрдых растворов на основе сульфида индия простирается до 7,0 мол.% InCl 3 .
Предположительно понижение параметра а при введении легирующей добавки может быть свя-
6000-
2000 4
б
Рис. 1. Рентгенограмма образца системы (In 2 S 3 ) 0,99 (InCl 3 ) 0,01 (а); зависимость параметра а кристаллической решетки базисного соединения In2S3 от состава системы (In 2 S 3 ) 1-х (InCl 3 ) х (б).
зано с вакансионным механизмом дефектообразо-вания. Растворение хлорида индия в сульфиде индия можно записать следующим квазихимическим уравнением:
InCl 3 ( ^ In 2 S 3 ) ^ Inx xn + 3 C1 S + V / . (3)
Образование вакансий в подрешетке индия может служить источником катионного переноса ионов In3+ в этой системе. Однако это предположение требует дальнейшей проверки.
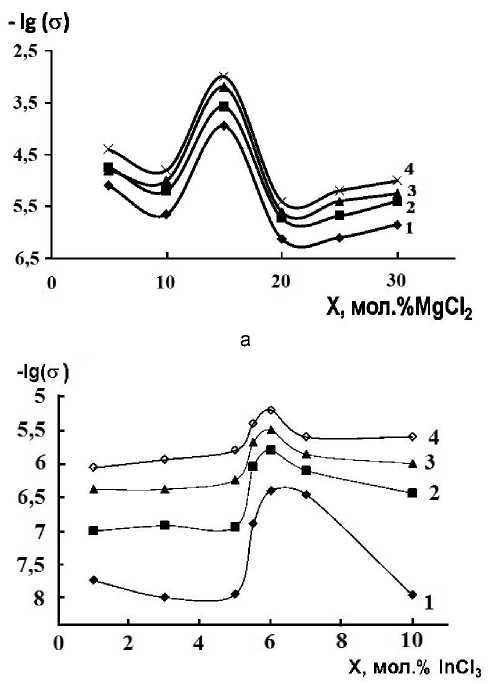
Результаты измерения температурной электропроводности методом кондуктометрии для образцов системы (In 2 S 3 ) 1-х (InCl 3 ) х и одной из систем ( InCl 3 ) 1-х (MCl 2 ) х представлены на рис. 2.
Энергия активации электропроводности составов, лежащих внутри области твёрдых растворов, меняется с 1,81 до 1,95 эВ для системы (InCl 3 ) 1-х (MgCl 2 ) х и от 2,15 до 4,85 эВ – для системы (In 2 S 3 ) 1-х (InCl 3 ) x . Для образцов, находящихся за пределами области гомогенности, энергия активации возрастает в три–четыре раза, что можно связать с увеличением межзеренного сопротивления в двухфазной области. С повышением температуры от 373 до 503 К электропроводность увеличивается в системе (InCl 3 ) 1-х (MgCl 2 ) х от 10-7 до 10-5 Cм/см, в системе (In 2 S 3 ) 1-х (InCl 3 ) x – от 10-9 до 10-6 Cм/см.

Рис. 2. Температурные зависимости электропроводности систем:
-
а) (InCl 3 ) 1-х (MgCl 2 ) х при содержании MgCl 2 : 1 – 5,0 мол.%; 2 – 10,0 мол.%; 3 – 15,0 мол.%; 4 – 20,0 мол.%; 5 – 25,0 мол.%; 6 – 30,0 мол.%;
-
б) (In 2 S 3 ) 1-х (InCl 3 ) х при содержании InCl 3 : 1 – 1,0 мол.%; 2 – 3,0 мол.%; 3 – 5,0 мол.%; 4 – 5,5 мол.%; 5 – 6,0 мол.%; 6 – 7,0 мол.%; 7 – 10,0 мол.%
На изотермических зависимостях электропроводности от состава (рис. 3) чётко выражены несколько участков. Незначительное снижение электропроводности при введении малых порций легирующего компонента типично для твёрдых растворов полупроводниковых соединений [5], которыми являются базисные соединения, и связано, по-видимому, с уменьшением электронной составляющей проводимости. При дальнейшем увеличении содержания легирующей добавки проводимость в основном обусловливается ионами в соответствии с квазихимической реакцией (3) и растёт с увеличением количества добавки.
При достижении 6,0 мол.% InCl 3 в (In 2 S 3 ) 1-х (InCl 3 ) х и 15,0 мол.% MgCl 2 в (InCl 3 ) 1-х (MgCl 2 ) х , очевидно, начинается ассоциация дефектов, что приводит к уменьшению электропроводности. В системе (In 2 S 3 ) 1-х (InCl 3 ) х для образцов, содержащих выше 7,0 мол.% InCl 3 , электропроводность слабо зависит от состава, что характерно для двухфазных областей [5]. Результаты кондуктометрии подтверждают данные РФА о протяжённости области твёрдых растворов в In 2 S 3 до 7,0 мол.% InCl 3 .
б
Рис. 3. Изотермы электропроводности систем.
а) (InCl 3 ) 1-х (MgCl 2 ) х при температурах: 1 – 400 К; 2 – 435 К; 3 – 450 К; 4 – 475 К;
б) (In 2 S 3 ) 1-х (InCl 3 ) х при температурах: 1 – 455 К; 2 – 500 К; 3 – 526 К; 4 – 553 К.
Среднеионные числа переноса для всех исследованных систем определены при помощи ЭДС гальванической ячейки (1), измеренной в интервале температур 373–503 К (табл. 1).
Таблица 1
Как видно из табл.1, образцы систем (InCl 3 ) 1-х (MCl 2 ) х , где M – Zn, Sn и Mn являются ионными проводниками с низкими ионными числами переноса и малоперспективны как твёрдые электролиты. Легирование хлорида индия хлоридами кадмия и магния приводит к увеличению доли ионной проводимости (t i = 0,8 - 1,0), однако в соответствии с ква-зихимической реакцией:
MCl 2 ( ^ InCl 3 ) ^ M In + 2 Cl X + V CCl ,
механизм дефектообразования в этих системах связан с образованием вакансий хлора. В этом случае можно ожидать проводимость по хлорид-ионам.
Для твёрдых растворов хлорида индия в сульфиде индия числа переноса ионов близки к единице, поэтому систему (In 2 S 3 ) 1-х (InCl 3 ) х в области оптимальных температур и составов можно использовать в качестве твёрдого электролита с предположительной проводимостью по ионам In3+ .
С целью проверки типа ионной проводимости для ТЭ, (In 2 S 3 ) 0,95 (InCl 3 ) 0,05 был выполнен эксперимент по методу Тубандта в электрохимической ячейке (5):
(-) С / InSb, Sb | ТЭ, In3+ | ТЭ, In3+ | ТЭ, In3+ | InSb,
Sb / С (+), (5) где InSb, Sb – электроды; ТЭ, In3+ – твёрдый электролит (In 2 S 3 ) 1-х (InCl 3 ) х .
Результаты эксперимента, приведённые в табл. 2, подтвердили практически униполярную проводимость по катионам индия (III).
Таблица 2
Значение чисел переноса катионов по методу Тубандта
|
Количество электричества, А•ч |
Изменение массы катода теоретическое, г |
Изменение массы практическое, г |
Числа переноса катионов (t + ±0,005) |
||
|
анода и анолита |
катода и католита |
средней таблетки |
|||
|
2 • 10-3 |
0,00200 |
-0,00192 |
+0,00191 |
0 |
0,960 |
|
1 • 10-3 |
0,00100 |
-0,00096 |
+0,00095 |
0 |
0,955 |
Характеристики индийсодержащих твёрдых электролитов
|
Базисное соединение |
Легирующая добавка |
Содержание легирующей добавки, мол.% |
Интервал температур, К |
Электропроводность, См/см |
Значение чисел переноса ионов (t i ±0,1) |
|
InCl 3 |
ZnCl 2 |
16,0 – 18,0 |
423 – 503 |
1 • 10-6 – 4 • 10-6 |
0,5 - 1,0 |
|
SnCl 2 |
3,0 – 6,0 |
473 – 503 |
1 • 10-5 – 2 • 10-4 |
0,6 - 07 |
|
|
MnCl 2 |
2,0 – 3,0 |
373– 503 |
2 • 10-6 – 5 • 10-6 |
0,5 - 0,9 |
|
|
CdCl 2 |
1,0 - 2,0 |
473 – 503 |
4 • 10-6 – 5 • 10-5 |
0,8 - 1,0 |
|
|
MgCl 2 |
10,0 - 18,0 |
373 – 503 |
3 • 10-4 – 1 • 10-3 |
0,9 - 1,0 |
|
|
In 2 S 3 |
InCl 3 |
5,0 – 7,0 |
423 – 503 |
2 • 10-6 – 6 • 10-6 |
0,9 - 1,0 |
Твёрдые электролиты (InCl 3 ) 0,85 (MgCl 2 ) 0,15 , (InCl 3 ) 0,985 (CdCl 2 ) 0,015 , (In 2 S 3 ) 0,95 (InCl 3 ) 0,05 были использованы для определения стандартной энергии Гиббса (ΔG0 T ) образования полупроводниковых соединений типа In n X m , где X – S, Se, Te, P, Sb. Значения ΔG0 T (In n X m ) рассчитывали с учетом ЭДС гальванической ячейки (6):
С /InSb, Sb / TЭ, In3+ / In n X m , X/ С, (6) где InSb, Sb – электроды; ТЭ, In3+ – твердый электролит с проводимостью по индию; In n X m , X – исследуемое полупроводниковое соединение.
В ячейке (6) при проведении эксперимента с твёрдым электролитом (In 2 S 3 ) 1-х (InCl 3 ) х наблюдалась самодиффузия серы, приводящая к искажению результатов. Во избежание этого процесса в качестве ТЭ, In3+ был использован сдвоенный твёрдый электролит (In 2 S 3 ) 1-х (InCl 3 ) х | (InCl 3 ) 1-х (MCl 2 ) х
(М = Cd, Mg), где система (InCl 3 ) 1-х (MCl 2 ) х выполняла роль мембраны, селективной в отношении ионов индия. Результаты эксперимента приведены в табл. 3.
Таблица 3
Стандартная энергия Гиббса образования полупроводниковых соединений
|
Показатели |
Полупроводниковое соединение |
||||
|
In 2 S 3 |
In 2 Se 3 |
In 2 Te 3 |
InP |
InSb |
|
|
E 503К , мВ |
713 |
568 |
312 |
255 |
52 |
|
ΔG 503 (по методу ЭДС), кДж/моль |
- 413 |
- 329 |
-181 |
-74 |
-15 |
|
ΔG0 T (по методу ЭДС), кДж/моль |
-444 |
-335 |
-195 |
-79 |
-21 |
|
ΔG0 T (по термохимическим данным), кДж/моль |
-462 |
-350 |
-206 |
-77 |
-22 |
Токообразующая реакция в этих ячейках протекает с участием иона индия и возможна только в случае катионного переноса в электролите. Этот эксперимент позволил повторно определить числа переноса ионов по уравнению:
A G 0
t =---- Тэкс- , (7)
i A G 0
T теор .
где A G T эксп - экспериментальное значение стандартной энергии Гиббса, кДж/моль; A G T теор - теоретическое значение стандартной энергии Гиббса, кДж/моль.
Числа переноса ионов меняются от 0,95 до 0,98. Этот эксперимент подтверждает данные метода Тубандта о практически униполярной проводимости ТЭ по ионам индия (III).
Возможность применения индийпроводящего ТЭ (In 2 S 3 ) 1-х (InCl 3 ) х и ионселективной мембраны (InCl 3 ) 1-х (MCl 2 ) х (М = Cd, Mg) в составе электрохимической ячейки (8) для кулонометрического титрования и контролируемого изменения состава нестехиометрического сульфида индия исследовали при температуре 553 К (при более высоких температурах происходит выплавление индия из электродов, при более низких – уменьшается электропроводность ТЭ).
С | In 2±δ S 3 | ТЭ, In3+ | InSb, Sb | С, (8) где In 2±δ S 3 – легируемое полупроводниковое соединение; InSb, Sb – электрод – донор индия.
На рис. 4 представлены кривые кулонометрического титрования в ячейке (8). При введении индия в In 2±δ S 3 ЭДС гальванической ячейки (4) снижается за счет увеличения содержания индия в сульфиде индия. Снижение ЭДС тем значительнее, чем больше масса введённого металла (Δm).
Вид интегральной кривой кулонометрического титрования позволяет судить о существовании двухсторонней области гомогенности в нестехиометрическом сульфиде индия (III). Приведенная дифференциальная кривая показывает существование двухсторонней области гомогенности на основе In 2 S 3 , причем области с избытком и недостатком индия симметричны, т.е. сульфид индия описы-
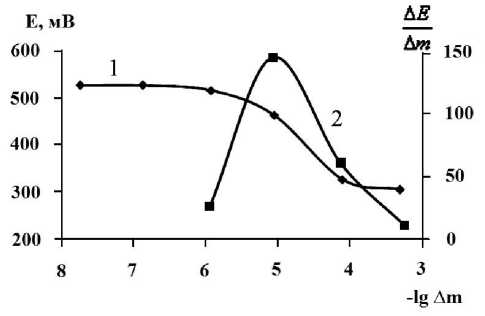
Рис. 4. Интегральная (1) и дифференциальная (2)
кривые кулонометрического титрования в электрохимической ячейке (-) С/ InSb, Sb / ТЭ, In3+ / In 2± δ S 3 , S / C (+).
вается формулой In 2±δ S 3 . Ширина области гомогенности 0,43%, что свидетельствует об отклонении от стехиометрии δ = 2,2·10-3 атомных долей индия.
Имеющиеся в литературе данные о диаграмме состояния In– S противоречивы. Согласно работе [9], существует фаза, отвечающая формуле In 2,001 S 3 , а согласно [10], при температуре ниже 350° С существует двухсторонняя область гомогенности, и формулу сульфида индия можно описать как In 2±δ S 3 . Результат эксперимента подтверждает данные [10] и уточняет ширину области гомогенности сульфида индия.
Кроме того, результаты эксперимента доказывают необходимость получения методом КТ полупроводникового измерительного электрода сульфида индия, состав которого отвечает In 2±(0,0005-0,002) S 3 . Это связано с тем, что в соответствии с исследованиями [2, 3], наибольшая точность и селективность присуща измерительным электродам, которые способны значительно изменять свойства при незначительном изменении состава.
Таким образом, выполненный эксперимент показал возможность практического применения индийпроводящего ТЭ (In 2 S 3 ) 1-х (InCl 3 ) х для осуществления контроля состава и свойств нестехиометрического сульфида индия, используемого в качестве измерительного электрода электрохимического сенсора на сера- и индийсодержащие среды.
Выводы
-
1. Разработаны условия получения квазибинар-ной солевой системы (In 2 S 3 ) 1-х (InCl 3 ) х , определена протяжённость области гомогенности (до х = 0,07).
-
2. Установлены температурные интервалы 373 – 673 К и области оптимальных составов твёрдых растворов индийсодержащих квазибинарных солевых систем с наибольшей ионной проводимостью.
-
3. Определены среднеионные числа переноса (0,8 – 1,0) твёрдых электролитов (In 2 S 3 ) 1-х (InCl 3 ) х и (InCl 3 ) 1-х (MCl 2 ) х (М = Cd, Mg). Впервые в ТЭ (In 2 S 3 ) 0,95 (InCl 3 ) 0 , 05 обнаружена преимущественная ионная проводимость по катионам индия (III) ( t In = 0,955).
-
4. Исследована возможность применения впервые синтезированного индийпроводящего твердого электролита в квазибинарной солевой системе (In 2 S 3 ) 1-х (InCl 3 ) х в составе электрохимической ячейки для кулонометрического титрования сульфида индия (In 2±δ S 3 ), а также для изучения термодинамических характеристик индийсодержащих полупроводниковых соединений (In 2 S 3 , In 2 Se 3 , In 2 Te 3 , InP, InSb) .
-
5. С помощью индийпроводящего твёрдого электролита (In 2 S 3 ) 1-х (InCl 3 ) х определены ширина и симметрия области нестехиометрии сульфида индия.
-
6. Для использования в качестве измерительного электрода электрохимического сенсора, позволяющего осуществлять контроль содержания серы, индия и их соединений в различных средах, рекомендован In 2±(0,0005-0,002) S 3 .
Список литературы Новые твердые электролиты для электрохимических сенсоров контроля серы и индия в различных средах
- Каганцов С.М., Самойлов А.Г. Импульсный датчик газового контроля//Датчики и системы. 2002. №10. С. 31-33.
- Малышев В.В., Писляков А.В. Чувствительность полупроводниковых оксидов металлов (SnO2, WO3, ZnO) к сероводороду в сухой и влажной газовых средах//Журнал аналитической химии. 2014. Т. 69. №2. С. 135-148.
- Леушина А.П., Маханова Е.В., Оржаева О.П., Зломанов В.П. Разработка методов получения электродов нестехиометрического состава для твердоэлектролитных сенсоров с прогнозируемой чувствительностью//Электрохимия. 2005. Т.41. №6. С. 728-734.
- Чеботин В.Н., Перфильев М.В. Электрохимия твёрдых электролитов. М.: Химия, 1978. 312 с.
- Леушина А.П. О контролируемом влиянии на тип и концентрацию дефектов в квазибинарных солевых твёрдоэлектролитных системах//Химическая и биохимическая технология, технология переработки эластомеров, физическая химия и электрохимия: Сб. науч. тр. ВятГУ. Киров, 1999. Вып. 1 (10). С. 150-155.
- Посыпайко В.И. Диаграммы плавкости солевых систем. М.: Металлургия, 1977. Ч. 1. 416 с.
- Мюллер Г., Гнаук Г. Газы высокой чистоты/Пер. с нем. М.: Мир, 1968. 236 с.
- Иванов-Шиц А.К., Мурин И.В. Ионика твёрдого тела. СПб.: СПбГУ, 2010. Т. 2. 1000 с.
- Duffin W.J., Hogg J.H. Crystalline phase in the system In-In2S3//Acta crystallogr. 1966. Vol. 20. P.566 -569.
- Косяков А.В., Завтражнов А.Ю., Наумов А.В., Сергеева А.В. Уточнение фазовой диаграммы системы In -S по данным спектрофотометрических исследований равновесия между сульфидами индия и водородом//Вестник ВГУ. Серия химия, биология, фармация. 2009. №2. С. 28-39.


