Нозокомиальные инфекции, вызванные бактериями семейства Enterobacteriacae, в онкологической клинике
Автор: Дмитриева Наталья Владимировна, Агинова Виктория Викторовна, Петухова Ирина Николаевна, Григорьевская Злата Валерьевна, Дмитриева Анна Игоревна, Багирова Наталья Сергеевна, Терещенко Инна Васильевна, Хмаладзе Елена Николаевна
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 1 т.18, 2019 года.
Бесплатный доступ
Цель исследования - проанализировать частоту выделения мультирезистентных (MDR) возбудителей госпитальных инфекций - Escherichia coli и Klebsiella pneumoniae. материал и методы. Проанализи-ровано 862 штамма E. coli и 1 461 штамм K. pneumoniae, выделенных в 2014-16 гг. из раневого отде-ляемого, крови, мочи и других патологических материалов от онкологических больных, находившихся в НМИЦ онкологии им. Н.Н. Блохина МЗ РФ. Результаты. За 3 года отмечено значимое (p≤0,0001) увеличение числа E. coli, устойчивых к пиперациллину-тазобактаму (с 8,1 до 25 %), цефтриаксону (с 15,7 до 100 %), эртапенему (c 8,1 до 97,7 %), амикацину (c 4,5 до 14,6 %). Количество E. coli, про-дуцирующих карбапенемазы, увеличилось с 5,8 до 20,8 % (p≤0,0001). Среди K. pneumoniae отмечено значимое (p≤0,0001) увеличение числа штаммов, устойчивых к пиперациллину-тазобактаму (с 59,7 до 89,7 %), цефтазидиму (с 62,8 до 82,8 %), цефтриаксону (с 62,8 до 100 %), цефепиму (с 63,1 до 83,8 %), эртапенему (c 62,1 до 100 %), имипенему (c 30,0 до 81,0 %), меропенему (c 53,9 до 86,8 %). заключение. Оценка частоты выделения MDR-микроорганизмов в динамике является важнейшим элементом эпидемиологического надзора и необходима для правильного лечения пациентов с ин-фекционными осложнениями.
Энтеробактерии, мультирезистентные микроорганизмы, онкологические больные, внутрибольничные инфекции, антибактериальные препараты, лекарственная устойчивость
Короткий адрес: https://sciup.org/140254239
IDR: 140254239 | УДК: 616-006-06:616.9-022 | DOI: 10.21294/1814-4861-2019-18-1-36-42
Nosocomial infections caused by bacteria of Enterobacteriacae family in cancer clinic
The purpose of the study was to analyze the prevalence of multidrug-resistant (MDR) pathogens ( Escherichia coli and Klebsiella pneumonia) isolated from cancer patients. material and methods. 862 strains of E. coli and 1 461 strains of K. pneumoniae isolated from wound, blood, urine and other pathological materials from cancer patients treated at N.N. Blokhin National Medical Research Center of Oncology (Moscow) between 2014 and 2016 were analyzed. results. Over the last 3 years, there has been a significant increase in the number of E.coli resistant to piperacillin-tazobactam (from 8.1 to 25 %), ceftriaxone (from 15.7 to 100 %), ertapenem (from 8.1 to 97.7 %), and amikacin (c 4.5 to 14.6 %). The number of E. coli producing carbapenemases has increased from 5.8 to 20.8 % (p≤0.0001). Among K. pneumoniae, a significant increase in the number of strains resistant to piperacillin-tazobactam (from 59.7 to 89.7 %), ceftazidime (from 62.8 to 82.8 %), ceftriaxone (from 62.8 to 100 %), cefepime (from 63.1 to 83.8 %), ertapenem (from 62.1 to 100 % ), imipenem (from 30.0 to 81.0 %), and meropenem (from 53.9 to 86.8% ) is observed. conclusion. Evaluation of the frequency of isolation of MDR microorganisms over time is an essential element of epidemiological surveillance and is necessary for the correct treatment of patients with infectious complications.
Текст научной статьи Нозокомиальные инфекции, вызванные бактериями семейства Enterobacteriacae, в онкологической клинике
Нозокомиальные инфекции (НИ) представляют серьезную проблему для клиник, особенно он‑ кологических. Нозокомиальные инфекции – это группа различных инфекций, объединенных по признаку общего эпидемиологического характера инфицирования, возникающих в стационаре спустя 24–72 ч после госпитализации больного. Онколо‑ гические больные являются группой риска в от‑ ношении развития НИ [1]. Частота инфекционных осложнений в различных группах онкологических больных составляет от 12 до 50 %, а среди больных лейкозами достигает 75 % [2]. В последние годы отмечается значительное увеличение интереса к проблеме нозокомиальных инфекций в связи с вы‑ соким уровнем заболеваемости и связанным с этим серьезным социально‑экономическим ущербом. По данным ЦНИИ эпидемиологии МЗ РФ, ежегодное количество госпитальных инфекций составляет не менее 2–2,5 млн случаев в год, а ежегодный эконо‑ мический ущерб – более 5 млрд руб. [3].
Спектр возбудителей инфекционных ослож‑ нений у онкологических больных широк и раз‑ нообразен. Он включает аэробные и анаэробные бактерии, патогенные грибы, вирусы, простейшие, однако ведущими возбудителями являются грам‑ отрицательные неферментирующие бактерии ( Acinetobacter baumannii, Pseudomonas aeruginosa ), характеризующиеся множественной лекарствен‑ ной устойчивостью.
Пациенты с инфекциями, вызванными рези‑ стентными бактериями, имеют повышенный риск отрицательных клинических результатов и леталь‑ ного исхода, а также потребляют больше медицин‑ ских ресурсов, чем пациенты, инфицированные чувствительными к антибиотикам штаммами тех же возбудителей [4]. Например, устойчивость Klebsiella pneumoniae – распространенной кишеч‑ ной бактерии, которая может вызывать угрожающие жизни инфекции и резистентной к карбапенемам, препаратам, используемым в качестве «последней лечебной возможности», – распространилась на все регионы мира [5]. K. pneumoniae часто становится причиной внутрибольничных инфекций, таких как пневмонии, инфекции кровотока, а также инфекции новорожденных и пациентов отделений интенсив‑ ной терапии. В некоторых странах из‑за развившей‑ ся устойчивости K. pneumoniae к карбапенемам они оказываются неэффективны при лечении более чем половины пациентов с этой инфекцией [6, 7].
Широкое распространение получила устой‑ чивость E. coli к фторхинолонам, антибиотикам, наиболее часто применяемым при лечении ин‑ фекций мочевыводящих путей. Теперь во многих странах и на разных континентах терапия фтор‑ хинолонами неэффективна более чем в половине случаев. Количество карбапенем‑резистентных вариантов несколько меньше, чем у клебсиелл, и обычно не превышает 30 % [8]. Согласно данным по Европейскому региону, НИ приводят к значи‑ тельному увеличению нагрузки на экономику и здравоохранение европейских стран: число паци‑ ентов, погибших в результате внутрибольничных инфекций, вызванных резистентными бактериями, ежегодно превышает 25 тысяч человек [9]. По‑ мимо роста уровня заболеваемости и смертности, среди пациентов, следует принимать во внимание и такие факторы, как увеличение сопутствующих расходов на здравоохранение, которые ежегодно составляют более 1,5 млрд евро [10]. В последние годы к проблеме антимикробной резистентности (АМР) усилено внимание со стороны не только врачей, но и политиков, экономистов, так как АМР преодолела межгосударственные границы и получила повсеместное распространение [11]. В Российской Федерации также предпринята попытка разработки стратегии предупреждения распространения антимикробной резистентности на период до 2030 г. [12].
Материал и методы
Работа выполнена в ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России. Проана‑ лизирована таксономическая структура микро‑ организмов (без учета грибковой микрофлоры), выделенных в 2014–2016 гг. из 24 357 патологиче‑ ских биоматериалов от онкологических больных, проходивших лечение в клинике. Пристальное внимание было уделено наиболее часто выделяе‑ мым микроорганизмам, общее количество которых составило 6 218 (52,1 %). Данные микроорганизмы являются клинически значимыми и были устойчи‑ вы к большинству антибактериальных препаратов. Все изоляты были идентифицированы до вида колориметрическим методом на анализаторах «Microscan WalkAway – 40 SI» (Siemens Healthcare Diagnostics, США) и «Vitek 2» (BioMerieux, Фран‑ ция), а также методом матрично‑ассоциированной лазерной десорбции/ионизации – времяпролетной масс‑спектрометрии (MALDI‑TOF) и программ‑ ного обеспечения MALDI Biotyper v.3.0 (Bruker Daltonics, Германия).
Результаты
Исследованию подвергались такие биома‑ териалы, как отделяемое нижних дыхательных путей (ОНДП), полученное при бронхоскопии, бронхоальвеолярном лаваже, посеве мокроты, а также отделяемое по дренажам (ОД) и раневое отделяемое (РО), моча, кровь, прочие патологи‑ ческие материалы (кал, ликвор, аспират суставной жидкости, мазки и т. д.) (табл. 1).
Причиной инфекционных осложнений нижних дыхательных путей в 21,0 % случаев являлась K. рneumoniaе. Число выделенных из ОНДП штам‑ мов было больше, чем из мочи (18,7 %) (p>0,05), однако разница была недостоверна, в то время как из мочи (18,7 %) и ОД + РО (15,9 %) K. рneumoniaе выделялись достоверно чаще, чем из крови (3,9 %) (р<0,0001).
E. coli становилась причиной инфекций моче‑ выводящих путей в 67,9 % случаев, что достоверно выше частоты ее выделения при инфекциях нижних дыхательных путей (5,9 %), инфекциях кровотока (6,6 %) и частоты выделения данного микроорга‑ низма в отделяемом из дренажей и ран (13,6 %). Разница статистически достоверна (р<0,0001). Причем число выделенных штаммов из ОД + РО больше, чем из ОНДП и крови (р<0,0001).
В ходе исследований также был проведен ана‑ лиз выявления резистентных штаммов E. coli и K. pneumoniae из патологических материалов от больных. В период исследований отмечена тенден‑ ция к увеличению устойчивости кишечной палочки к ингибитор‑защищенным пенициллинам (табл. 2). Установлена достоверная разница в увеличении количества резистентных штаммов к пиперацил‑ лину/тазобактаму с 8,1 % в 2014 г. до 15,8 % в 2015 г. (p<0,05) и до 25,1 % в 2016 г. (p≤0,0001). По отношению к ампициллину/сульбактаму число устойчивых штаммов в 2014 г. составило 58,6 %, таблица 1
Частота выделения проблемных грамотрицательных микроорганизмов из патологических материалов, 2014–16 гг.
Динамика выявления устойчивых к антибиотикам штаммов E. coli
|
Препараты |
Годы/количество штаммов E.coli 2014 г. (n=223) 2015 г. (n=227) 2016 г. (n=403) |
|
Ампициллин/сульбактам Пиперациллин/тазобактам Цефтазидим Цефтриаксон Цефепим Имипенем Меропенем Эртапенем Амикацин Ципрофлоксацин Триметоприм/сульфаметок‑ сазол |
130 (58,6 %) 121(53,3 %) 253 (62,8 %) 18 (8,1 %) 36 (15,8 %) 101 (25,1 %) 41 (18,3 %) 42 (18,5 %) 120 (29,8 %) 35 (15,7 %) 47 (20,7 %) 403 (100,0 %) 33 (14,7 %) 40 (17,6 %) 106 (26,3 %) 7 (3,1 %) 11 (4,8 %) 68 (16,9 %) 13 (5,8 %) 15 (6,6 %) 84 (20,8 %) 18 (8,1 %) 27(11,8 %) 394 (97,7%) 10 (4,5 %) 18 (7,9 %) 59 (14,6 %) 77 (34,5 %) 106 (46,7 %) 193 (47,8 %) 100 (44,8 %) 102 (44,9 %) 209 (51,8 %) |
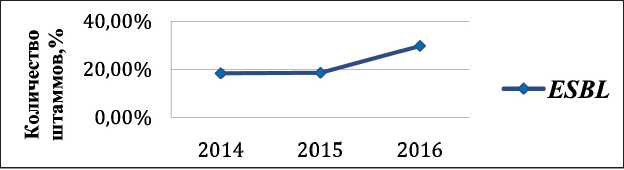
Рис. 1. Динамика частоты выделения E. coli, продуцирующих бета-лактамазы расширенного спектра действия ( ESBL – бета-лактамазы расширенного спектра действия)
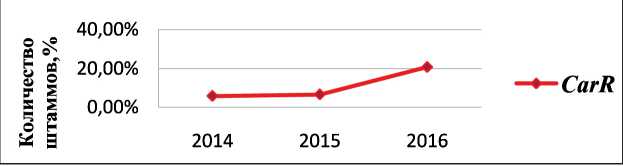
Рис. 2. Динамика частоты выделения карбапенем-резистентных ( CarR- карбапенем-резистентный штамм ) E. coli
в 2015 г. незначительно снизилось – до 53,3 %, а в 2016 г. возросло до 62,8 %, однако достоверной разницы обнаружено не было (p>0,05).
По отношению к цефалоспоринам число устойчивых штаммов увеличилось. Причем, если к цефтазидину и цефепиму наблюдался постепен‑ ный достоверный рост числа устойчивых штаммов (18,3–29,8 % и 14,7–26,3 % соответственно), то количество штаммов, устойчивых к цефтриаксо‑ ну, в 2016 г. составило 100,0 % против 15,7 % в 2014 г. Разница достоверна (p≤0,0001).
В 2016 г. существенно увеличилось выделение карбапенем‑резистентных кишечных палочек. Так, число штаммов, резистентных к эртапенему, возросло с 8,1 % в 2014 г. до 97,7 % в 2016 г. По отношению к имипенему и меропенему общий процент устойчивых штаммов был невелик (не‑ много более 20 %), однако наблюдалась тенденция к увеличению количества таких штаммов с 3,1 % до 16,9 % для имипенема и от 5,8 % до 20,8 % для меропенема (p≤0,0001).
При анализе устойчивости кишечной палочки к аминогликозидам (амикацин) была обнаружена достоверная разница в увеличении количества устойчивых штаммов с 4,5 % в 2014 г. до 14,6 % в 2016 г. (p≤0,0001), однако общее количество таких штаммов незначительно. По отношению к фторхинолонам (ципрофлоксацин) резистентных штаммов за период исследований было выделено менее 50 %, при этом достоверного увеличения (34,5–47,8 %) в динамике не отмечалось. Коли‑ чество устойчивых штаммов к триметоприму/ сульфаметоксазолу в период 2014–15 гг. не из‑ менилось и составило 44,8–44,9 %, а в 2016 г. их число увеличилось до 51,8 % (p>0,05). Разница недостоверна (p>0,05).
Динамика частоты выделения продуцентов бета‑лактамаз расширенного спектра действия (англ. – ESBL) и карбапенем‑резистентных ( СarR) штаммов E. coli за период 2014–16 гг. представлена на рис. 1 и 2. В период 2014–2016 гг. произошло увеличение частоты выделения ESBL- продуцентов с 18,3 % до 29,8 % (p<0,05) и СarR штаммов E. coli с 5,8 % до 20,8 % (p≤0,0001). В табл. 3 показана динамика устойчивости K.pneumoniaе к антибак‑ териальным препаратам.
Анализ данных показал, что K. pneumoniae ха‑ рактеризуются высоким процентом резистентных штаммов к большому количеству антибиотиков. На протяжении 2014–2016 гг. происходило нарас‑ тание числа устойчивых штаммов K. pneumoniae практически ко всем применяемым антибиотикам. Отмечено увеличение количества устойчивых штаммов к «защищенным» антибиотикам пени‑ циллинового ряда. Так, число резистентных к ампициллину/сульбактаму штаммов увеличилось за период 2014–2015 гг. незначительно – с 77,7 до 78,8 % (p>0,05), а в 2016 г. – до 89,8 %. Раз‑ ница за период 2014–16 гг. достоверна (p≤0,0001). Число устойчивых штаммов к пиперациллину/ тазобактаму увеличилось с 59,7 % в 2014 г. до 87,9 % в 2016 г. (p≤0,0001). Произошло дальнейшее таблица 3
Динамика выявления устойчивых к антибиотикам штаммов K. pneumoniae
|
Препараты |
2014 г. (n=293) |
Годы/количество штаммов 2015 г. (n=402) |
2016 г. (n=766) |
|
Ампициллин/сульбактам |
213 (77,7 %) |
317 (78,8 %) |
688 (89,8 %) |
|
Пиперациллин/тазобактам |
175 (59,7 %) |
277 (68,9 %) |
667 (87,1 %) |
|
Цефтазидим |
184 (62,7 %) |
261 (64,9 %) |
635 (82,8 %) |
|
Цефтриаксон |
184 (62,8 %) |
289 (71,9 %) |
766 (100,0 %) |
|
Цефепим |
185 (63,1 %) |
265 (65,9 %) |
642 (83,8 %) |
|
Имипенем |
88 (30,0 %) |
147 (36,7%) |
621 (81,0 %) |
|
Меропенем |
158 (53,9 %) |
248 (61,9 %) |
665 (86,8 %) |
|
Эртапенем |
182 (62,1 %) |
284 (70,6 %) |
766 (100,0 %) |
|
Амикацин |
41 (13,9 %) |
127 (31,7 %) |
168 (21,9 %) |
|
Ципрофлоксацин |
187 (63,8 %) |
275 (68,4 %) |
668 (87,2 %) |
|
Триметоприм/сульфаметок‑ сазол |
186 (63,4 %) |
260 (64,7 %) |
664 (86,6 %) |
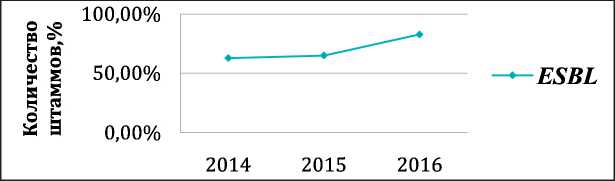
Рис. 3. Частота выделения ESBL- продуцирующих штаммов K. pneumoniae за период 2014–16 гг.
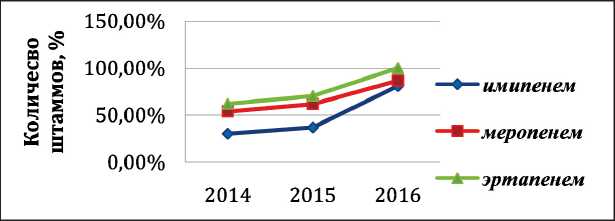
Рис. 4. Частота выделений ÑarR штаммов K. pneumoniaå за период 2014–16 гг.
увеличение количества резистентных штаммов к цефалоспоринам. Так, к препаратам III поколения устойчивость возросла с 62,7 до 82,8 % для цефта‑ зидима (p≤0,0001) и с 62,8 до 100,0 % (p≤0,0001) для цефтриаксона. Также достоверно увеличи‑ лось число устойчивых штаммов по отношению к цефепиму (IV поколение цефалоспоринов) – с 63,1 % в 2014 г. до 83,8 % в 2016 г. (p≤0,0001). Аналогично выросло и количество CarR штаммов. Значимо повысилась устойчивость к имипенему – с 30,0 % в 2014 г. до 81,0 % в 2016 г. (p≤0,0001) и к меропенему – с 53,9 % в 2014 г. до 61,9 % в 2015 г. (p<0,05) и до 86,8 % в 2016 г. (p≤0,0001). Устойчи‑ вость к эртапенему в 2016 г. увеличилась до 100,0 против 62,1 % в 2014 г. (p≤0,0001). Количество резистентных к аминогликозидам (амикацину) штаммов было достаточно невелико (21,9 %), тем не менее отмечен достоверный рост резистентно‑ сти. В 2014 г. было выделено 13,1 % устойчивых штаммов, в 2015 г. – 31,7 % (p≤0,0001), в 2016 г. – 21,9 % (p<0,002). Значимо возросла устойчивость к фторхинолонам (ципрофлоксацину) – с 63,8 % в 2014 г. до 87,2 % в 2016 г. (p≤0,0001). Количество штаммов, нечувствительных к бисептолу (триме‑ топриму/сульфаметоксазолу), в период 2014–15 гг. было примерно на одном уровне (63,4–64,7 %), а в 2016 г. увеличилось до 86,6 % (p≤0,0001).
Динамика частоты выделения ESBL- продуцен‑ тов и СarR штаммов K. pneumoniaе за период 2014–16 гг. представлена на рис. 3 и 4. Отмечено достоверное нарастание числа ESBL- продуцентов (62,7–82,8%) и СarR (53,9–86,8 %) штаммов K. pneumoniaе (p≤0,0001).
Список литературы Нозокомиальные инфекции, вызванные бактериями семейства Enterobacteriacae, в онкологической клинике
- Maschmeyer G., Haas A. The epidemiology and treatment of infections in cancer patients. Int J Antimicrob Agents. 2008; 31: 193-7.
- Дмитриева Н.В., Петухова И.Н., Смолянская А.З. Инфекционные осложнения в онкологической клинике. Практическая онкология. 2001; 1 (5): 18-20. [Dmitrieva N.V., Petukhova I.N., Smolyanskaya A.Z. Infectious complications in the oncological clinic. Practical Oncology. 2001; 1 (5): 18-20. (in Russian)].
- Козлов Р.С. Нозокомиальные инфекции: эпидемиология, патогенез, профилактика, контроль. Клиническая микробиология и антимикробная химиотерапия. 2000; 2 (1): 16-30. [Kozlov R.S. Nosocomial infections: epidemiology, pathogenesis, prevention, control. Clinical microbiology and antimicrobial chemotherapy. 2000; 2 (1): 16-30. (in Russian)].
- Григорьевская З.В., Петухова И.Н., Багирова Н.С., Шильникова И.И., Терещенко И.В., Григорьевский Е.Д., Дмитриева Н.В. Нозокомиальные инфекции у онкологических больных: проблема нарастающей резистентности грамотрицательных микроорганизмов. Сибирский онкологический журнал. 2017; 16 (1): 91-97. [Grigorievskaya Z.V., Petukhova I.N., Bagirova N.S., Shilnikova I.I., Tereshchenko I.V., Grigorievsky E.D., Dmitrieva N.V. Nasocomial infectoions in cancer patients: problem of gram-negative bacterial resistance. Siberian Journal of Oncology. 2017; 16 (1): 91-97. (in Russian)]. DOI: 10.21294/1814-4861-2017-16-1-91-97
- Kallen A., Guh A. United States centers for disease control and prevention issue updated guidance for tackling carbapenem-resistant Enterobacteriaceae. Euro Surveill. 2012 Jun 28; 17 (26). pii: 20207.


