О дегидрирующих свойствах 2,2'-(антрацен-9,10-диилиден)бис(4,5-дифенил-2Н-имидазола)
Автор: Живечкова Лариса Александровна, Самсонкин Александр Александрович, Мурюмин Евгений Евгеньевич, Пряничникова Маргарита Константиновна, Коновалова Евгения Петровна, Танасейчук Борис Сергеевич
Журнал: Инженерные технологии и системы @vestnik-mrsu
Рубрика: Химия
Статья в выпуске: 1-2, 2014 года.
Бесплатный доступ
В статье представлены результаты изучения дегидрирующих свойств 2,2'-(антрацен-9,10-диилиден)бис(4,5-дифенил-2Н-имидазола), а также кинетики взаимодействия фенотиазина с 2,2'-(антрацен-9,10-диилиден)бис(4,5-дифенил-2Н-имидазолом); высказывается предположение о строении продукта присоединения фенотиазина к 2,2'-(антрацен-9,10-диилиден)бис(4,5-дифенил-2Н-имидазолу).
Бисимидазол, фенотиазин, кинетика, скорость реакции, дегидрирование, строение, свойства
Короткий адрес: https://sciup.org/14720069
IDR: 14720069 | УДК: 547.569
On the dehidrating properties of 2,2'-(anthracene-9,10-diylidene)bis(4,5-diphenyl-2H-imidazole)
Has been studied dehydrating properties 2,2'-(antracene-9,10-diylidene)bis(4,5-diphe-nyl-2H-imidazole). It was found that in the reaction with diphenylamine, hidroqinone, diphenylpicrylhidrazine, acetic acid is formed by source bisimidazole. It was found that in the reaction with phenotiazine - product attaching phenotiazine with 2,2'-(antracene-9,10-diylidene)bis(4,5-diphenyl-2H-imidazole). Was the reaction kinetics of phenotiazine with 2,2'-(antracene-9,10-diylidene)bis(4,5-diphenyl-2H-imidazole). Found that the rate of this reaction is described by the eguation of the second order (the first for each of the participating in the reaction components). Suggested the structure of product attaching of phenotiazine to 2,2'-(antracene-9,10-diylidene)bis(4,5-diphenyl-2H-imidazole).
Текст научной статьи О дегидрирующих свойствах 2,2'-(антрацен-9,10-диилиден)бис(4,5-дифенил-2Н-имидазола)
Ди- и полирадикалы представляют интерес в качестве строительных блоков для создания органических магнитов [3]. Радикалы триарилимидазолильного ряда в этом отношении являются весьма перспективными, поскольку устойчивы на воздухе и не реагируют с кислородом.
Простейшими системами, способными при окислении образовывать бирадикал, могли бы быть 1,4-бис(4,5-дифенилимидазолил-2)бензолы (I а–b). Однако при их окислении образуются хиноны (III а–b) [6]. Существование бирадикального состояния (II б) наблюдается только в случае X=F, что
подтверждается образованием соответствующего димера (схема 1). Роль атомов фтора в стабилизации бирадикального состояния объясняется влиянием, как их электронных, так и стерических эффектов [4]. На схеме 1 представлены возможные превращения структур (I), где в качестве заместителей в бензольном кольце могут быть атомы H и F.
Схема 1
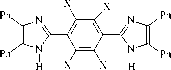
I a,b где а – Н; b – F. Нам представилось, что аналогичное равновесие должно существовать и в том случае, когда два имидазолильных остатка связаны через фрагмент, создающий определенные пространственные затруднения к образованию хиноидной системы.
В качестве такого затрудняющего фрагмента был использован антрацен, и осуществлен синтез (2,2′-антрацен-9,10-диил)бис(4,5-дифенил-2Н-имидазола) (IV), который при окислении гексацианоферратом (III) калия в щелочной среде образует хиноидное соединение 2,2′-(антрацен-9,10-диилиден)бис(4,5-дифенил-2Н-имидазол) (V) [1].
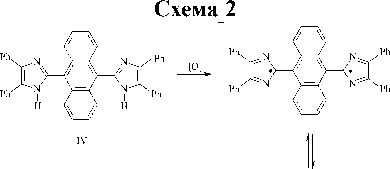
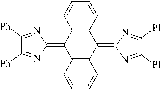
Хинон (V) представляет собой черные с красноватым блеском кристаллы, растворы которого в органических растворителях имеют ярко-красную окраску, но не дают сигнала ЭПР. Соединение (V) обладает дегидрирующими свойствами, его растворы обесцвечиваются при добавлении дифениламина, уксусной кислоты и гидрохинона. При этом в реакционной смеси был обнаружен исходный бисимидазол (IV).
Дегидрирующие свойства хинона (V) достаточно слабы. Так, если хинон (III b) способен дегидрировать спирт, то у хинона (V) эта способность практически отсутствует. Дегидрирующая способность хинона (V) ниже и по сравнению с аналогичной способностью 2,4,5-трифенилими-дазола. Это подтверждается отсутствием обесцвечивания (V) в реакции хинона (V) с 2,4,5-трифенилимидазолом.
Низкие дегидрирующие свойства хинона (V) связаны с тем, что в бисмидазоле (IV) оба имидазольных цикла «вывернуты» из плоскости сопряжения с антраценовым циклом на ~82о, а в хиноидной системе (V) имидазольные кольца сопряжены с антраценовым фрагментом. Квантовохимический расчет, выполненный неэмпирическим методом Хартри-Фока в базисе 6–31 G из пакета прикладных программ GAMESS [5] показал, что более стабильной системой является бисимидазол (IV). Относительная стабильность (IV) составляет -9427,52 ккал/моль, а хинона (V) – -9261,92 ккал/моль. Разность энергий этих соединений равна 165,6 ккал/моль, что составляет ~2 % от относительной стабильности (IV) и (V).
Очень интересным является то, что хинон (V) реагирует с ДФПГ∙Н (VI) с образованием в результате ДФПГ (VII) и бисимидазола (IV). Реакция является обратимой, и при взаимодействии бисимидазола (IV) с ДФПГ (VII) образуются соответственно хинон (V) и ДФПГ∙Н (VI) (схема 3). Однако, протекание обратной реакции с образованием соединений (V) и (VI) происходит несколько труднее, что подтверждается квантово-химическими расчетами.
Серия «Естественные и технические науки»
Схема 3
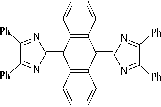
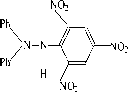
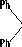
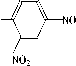
VII
ВЕСТНИК Мордовского университета | 2014 | № 1-2
В случае реакции хинона (V) с фенотиазином (VIII) красная окраска первого постепенно ослабевает, и через некоторое время раствор становится зеленым. В реакционной смеси по данным ТСХ (элюент хлороформ) нет бисимидазола (IV), но присутствует новое соединение (XI), которое, скорее всего, является продуктом взаимодействия фено-тиазинильного радикала (X) c хиноном (V).
При ЭПР исследованиях зеленого раствора не было обнаружено сигнала, т. е. образующийся продукт (XI) не имеет радикальной формы, а также не может являться комплексом с переносом заряда, поскольку обладающий более сильными электронодонорными свойствами N-метилфенотиазин с хиноном (V) не реагирует. Об этом свидетельствует отсутствие изменения окраски реакционной смеси.
Взаимодействие хинона (V) с фенотиазином (VIII) протекает достаточно медленно, что позволило изучить кинетику данной реакции.
Для этого на спектрофотометре «Specord UV VIS» были предварительно сняты электронные спектры поглощения хинона (V) и фенотиазина (VIII) в дихлорметане в видимой области. Фенотиазин (VIII) в данном растворителе не имеет максимумов поглощения, а для хинона (V) зафиксированы два: при длине волны 400–410 нм и – очень интенсивный – в области 513–518 нм. Изучение электронных спектров поглощения хинона (V) в дихлорметане (рис. 1) и бензоле при разных концентрациях показало подчинение оптической плотности растворов закону Бугера-Ламберта-Бера.
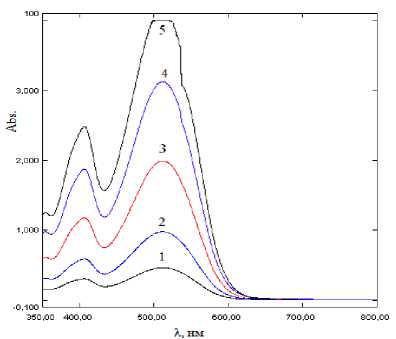
Р и с . 1. Электронные спектры поглощения растворов хинона (V) различной концентрации в дихлорметане (1 – 1•10-5М, 2 – 2•10-5М, 3 – 4•10-5М, 4 – 6•10-5М, 5 – 8•10-5М)
Изучение кинетики реакции хинона (V) с фенотиазином (VIII) проводилось в дихлорметане на максимуме поглощения хинона (V) (513 нм) и соотношении компонентов 1:1 при исходных концентрациях реагентов 1∙10-4 моль/л. Спектрофотометрические измерения проводили на спектрометре «UV-1800» в режиме спектрофотометрических и кинетических исследований. При этом интенсивность максимума поглощения при длине волны 513 нм с течением времени уменьшалась и появлялся новый максимум в области 650–660 нм (рис. 2).
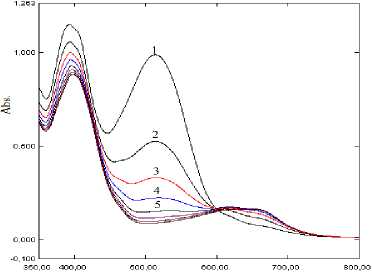
Р и с . 2. Изменение электронных спектров поглощения системы хинон (V) + фенотиазин (1:1) в дихлорметане во времени (1 – начало реакции; 2–5 мин; 3–10 мин;
4–15 мин; 5–20 мин и т. д. через 5 мин)
Полученные экспериментальные данные были использованы для определения порядка реакции графическим способом. Наличие линейной зависимости в координатах 1/С = f(t) в пределах превращения хинона (V) до 70–75 % свидетельствует об общем втором порядке реакции (первом по каждому из реагентов). Расчет экспериментальных данных с помощью программы Microcoft Office Excel представлен уравнением:
y = 35,7х + 2,33∙104; R = 0,9978.
Коэффициент корреляции подтверждает наличие линейной зависимости. Константа скорости реакции равна 35,7 л/моль∙с. Отложенный на оси ординат отрезок, равный 2,33∙104, соответствует величине 1/Со.
При попытке изучения кинетики данной реакции в менее полярном растворителе (бензоле) при тех же концентрациях, что и в дихлорметане, было обнаружено, что она протекает очень медленно. В связи с этим исходную концентрацию хинона (V) мы оставили прежней, а фенотиазина (VIII) – увеличили в 10 раз и реакционную смесь готовили в соотношении компонентов хинон
-
(V) : фенотиазин (VIII) = 1:20. Использование такого соотношения привело к тому, что реакция стала реакцией псевдопервого порядка по отношению к хинону (V).
Проведенные кинетические исследования при длине волны 513 нм показали, что реакция протекает на 90 % за 35 мин. Построение графиков в координатах ln C о /C = f(t) и расчет с помощью программы Excel указывает на наличие линейной зависимости, проходящей через начало координат, что соответствует реакции первого порядка.
y = 0,0015х; R = 0,9959
Константа скорости реакции при данных условиях равна 1,5∙10-3 с-1.
Методом наименьших квадратов были рассчитаны среднее значение константы и доверительный интервал:
К ср =(1,55±0,16) х 10-3с-1.
Полученные кинетические данные позволяют предложить возможный механизм реакции (схема 4).
Серия «Естественные и технические науки»
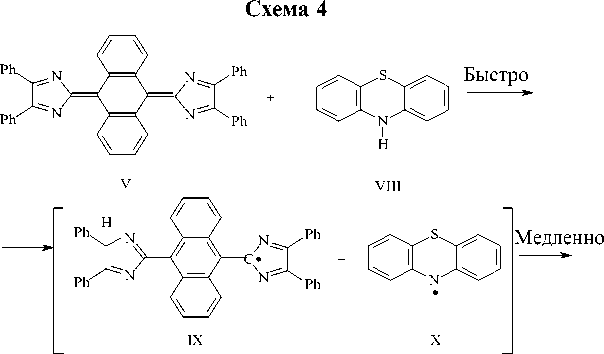
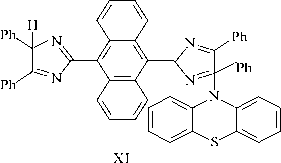
На медленной первой стадии происходит отрыв атома водорода из положения 10 (N–H-связи) фенотиазина (VIII) с промежуточной стадией образования двух радикалов (IX–X), которые затем быстро реагируют друг с другом. При этом из-за стерических затруднений, создаваемых антраценовым кольцом, присоединение атома водорода и фено-тиазинильного радикала (Х) происходит по положениям 4(5) имидазольного цикла.
Экспериментальная часть
Анализ продуктов проводили методом ТСХ на пластинках Silufol UV-254 (элюент – хлороформ), проявляли при УФ-облучении.
Синтез 2,2′-(антрацен-9,10-диилиден)-бис (4,5-дифенил-2Н-имидазола) (IV) был осуществлен согласно литературной методике [2].
Электронные спектры поглощения в видимой области в бензоле и дихлормета-не регистрировались на приборах «Specord UV VIS» и «UV-1800» при толщине поглощающего слоя 10 мм. За скоростью реакции хинона (V) с фенотиазином (VIII) следили по изменению оптической плотности раствора с течением времени при длине волны 513 нм. Исходные концентрации реагентов варьировали в пределах 10-4– 10-3 моль/л. Константы скорости реакции рассчитывали графически, используя зависимость 1/С = f(t), где С – текущая концентрация хинона (V), и с помощью программы «Microcoft Office Excel». Порядок реакции определяли в соответствии с [1].
Квантово-химический расчет был выполнен неэмпирическим методом Хартри-Фока в базисе 6–31 G из пакета прикладных программ GAMESS [5].
ВЕСТНИК Мордовского университета | 2014 | № 1-2
Список литературы О дегидрирующих свойствах 2,2'-(антрацен-9,10-диилиден)бис(4,5-дифенил-2Н-имидазола)
- Основы физической химии: Теория и задачи: учебное пособие для вузов/В. В. Еремин [и др.]. -Москва: Изд-во Экзамен, 2005. -480 с.
- Редокс-индуцированная обратимая трансформация системы хинон -дианион на основе 2,2'-ан-трацент-9,10-диилиденбис(4,5-дифенил-2Н-имидазола)/Б. С. Танасейчук [и др.]//Журнал органической химии. -2013. -Т. 4. -№ 5. -С. 756-759.
- Allinson, G. Organic molecular magnets -the search for stable building blocks/G. Allinson, R. J. Bushby, J.-L. Paillaud//Journal Materials Sciense: Materials in Electronics. -1994. -Vol. 5. -Р. 67-74.
- Kikuchi, A. Definitive evidence for the contribution of biradical character in a-closed-shell molecule, derivative of 1,4-bis-(4,5-diphenylimidazol-2-ylidene)cyclohexa-2,5-diene/A. Kikushi, F. Iwahori, J. Abe//Journal American Chemical Society. -2004. -Vol. 126. -Р. 6526-6527.
- General atomic and molecular electronic structure system/M.W. Schmidt [et al.]//J. Comput. Chem. -1993. -Vol. 14. -P. 1347-1363.
- Structures and chromotropic properties of 1,4-bis-(4,5-diphenylimidazol-2-yl)benzene derivatives/Y. Sakaino [et al.]//Journal American Chemical Society. -1979. -Vol. 5. -№ 8. -Р. 1241-1244.
- Veciana, J. Organic Magnets/J. Veciana, H. Ivamura//MRS Bulletin. -2000. -P. 41-15.


