Об электронной структуре мономеров катионной полимеризации 4, 6-диметилиндена и 5, 7-диметилиндена
Автор: Бабкин Владимир Александрович, Андреев Дмитрий Сергеевич, Петров Владислав Владимирович, Стоянов Олег Владиславович
Журнал: НБИ технологии @nbi-technologies
Рубрика: Технико-технологические инновации
Статья в выпуске: 2 (21), 2016 года.
Бесплатный доступ
В настоящей статье представлены квантово-химические расчеты молекул 4,6-диметилиндена и 5,7-диметилиндена методом PM3 с оптимизацией геометрии по всем параметрам градиентным методом. Получено оптимизированное геометрическое и электронное строение этих соединений. Теоретически оценена их кислотная сила ( р Ка = 23). Установлено, что молекулы 4,6-диметилиндена и 5,7-диметилиндена относятся к классу очень слабых кислот ( p Ka > 14).
Квантово-химический расчет, метод pm3, 6-диметилинден, 7-диметилинден, кислотная сила
Короткий адрес: https://sciup.org/14968426
IDR: 14968426 | УДК: 547.64:544.183.26 | DOI: 10.15688/jvolsu10.2016.2.5
On electron structure of monomers of cation polymerization of 4, 6-dimethylindene and 5, 7-dimethylindene
The first studies on cationic polymerization of monomers 4,6-dimethylindene and 5,7-dimethylindene were carried out in the early 1970s. The highest viscosity had the products obtained by BF8 * ОМе2. In the presence of BF8 * OR2 temperature does not affect the inherent viscosity. Relatively high molecular weight characterizes the products obtained in the presence of TiCl4. With this Lewis acid, the greatest value of Mn (molecular weight of the polymer) 20 000 at -30 °C and 120,000 at -72 °C. The enthalpy of polymerization was 18,5 ± 0,9 kcal/mol. However, geometric and electronic structure of monomers of the cationic polymerization of 4,6-dimethylindene and 5,7-dimethylindene are better to study by quantum-chemical PM3 method specifically parameterized for the calculation of multivalent atoms and cyclic compounds, which the investigated monomers belong to. In this regard, the aim of the present work is quantum-chemical calculation study of the monomer 4,6-dimethylindene and 5,7- dimethylindene РМ3с optimization of geometry on all parameters gradient descent method embedded in the program, which is partly based on the source code GAMESS (US), in the approximation of isolated molecules in the gas phase and theoretical evaluation of their acid strength. For a visual representation of the model molecule we used the program MacMolPlt. In the present work we first performed quantum-chemical calculation of molecules of 4,6-dimethylindene and 5,7-dimethylindene based on quantum-chemical method PM3. We determined the optimized geometrical and electronic structure of these compounds and evaluated theoretically their acid strength (pKa = 23). Furthermore, it is shown that the studied monomers 4,6-dimethylindene and 5,7-dimethylindene belong to the class of very weak H-acids (because pKa > 14).
Текст научной статьи Об электронной структуре мономеров катионной полимеризации 4, 6-диметилиндена и 5, 7-диметилиндена
DOI:
Первые исследования по катионной полимеризации мономеров 4,6-диметилиндена и 5,7-диметилиндена были выполнены еще в начале 70-х гг. XX столетия. Например, в работах [10; 11] изучали влияние различных кислот Льюиса (TiCl4, BF8, OR2 и SbCl4, AlBr8, SbCl4) и H2SO4 в металенхлориде при -20 и -72 °С на выход и характеристическую вязкость поли-4,6-диметилиндена. Наибольшую вязкость имели продукты, полученные с BF8 * ОМе2. В присутствии BF8 * OR2 температура не сильно влияет на характеристическую вязкость. Также относительно высокомолекулярные продукты получены и в присутствии TiCl4. С этой кислотой Льюиса наибольшее значение Mn (молекулярная масса полимера) 20 000 при -30 °С и 120 000 при -72 °С. Энтальпия полимеризации составляла 18,5 ± 0,9 ккал/моль. Эти же авторы (Марешаль и сотрудники) [8] первыми синтезировали мономер 5,7-диметилиндена и изучили его катионную полимеризацию. Авторы использовали различные кислоты Льюиса, например TiCl4, SnCl4, AlBr8 и SbCl4, в 1,2-дихлорэтане или метиленхлориде при -30 и -72 °С. В присутствии этих инициаторов были получены продукты сравнительно низкого молекулярного веса, и полимеризация совсем не проходила в присутствии BF8 * ОМе2 и BF8 * OEt2. При -30 °С в присутствии TiCl4 этот мономер сополимеризуется с инденом, константы сополимеризации имеют следующие значения: r5,7-диM... = 3,80 ± 0,04, rln = 0,10 ± 0,05. Очевидно, по отношению к катиону индена 5,7-диметилинден гораздо активнее, чем сам инден. Это весьма неожиданный и трудно объяснимый результат. В публикации [10] Марешаль привел данные по исследованию влияния различных условий на выход и среднечисловой молекулярный вес поли-5,7-диметилиндена. Среди использованных активных инициаторов, например TiCl4, SnCl4, AlBr3, SbCl5..., и H2SO4, продукт с относительно высокой характеристической вязкостью при 100 %-м выходе был получен в присутствии AlBr3 в метиленхло-риде при -30 °С и при -72 °С [4; 8; 10; 11]. Другая информация по полимеризации этих мономеров практически отсутствует. И осо- бенно это касается механизмов элементарных актов этих процессов, и в частности, механизмов инициирования, роста и обрыва материальной цепи на электронном уровне. Первым шагом в решении этого комплекса задач является изучение геометрического и электронного строения этих мономеров, что в дальнейших исследованиях, очевидно, позволит выработать стратегию изучения механизмов элементарных актов. Теоретическими и, в частности, методом квантовой химии MNDO уже предприняты первые попытки изучения геометрического и электронного строения этих соединений [1; 2].
Однако геометрическое и электронное строение мономеров катионной полимеризации 4,6-диметилиндена и 5,7-диметилиндена лучше изучать квантово-химическим методом PM3, специально параметризованным для расчета многовалентных атомов и циклических соединений [6], к которым и относятся исследуемые мономеры.
В связи с этим, целью настоящей работы является квантово-химический расчет изучаемых мономеров 4,6-диметилиндена и 5,7-диметилиндена PM3 с оптимизацией геометрии по всем параметрам градиентным методом, встроенным в программу Firefly [7], который частично основан на исходном коде GAMESS (US) [12], в приближении изолированной молекулы в газовой фазе и теоретической оценки их кислотной силы. Для визуального представления модели молекулы использовалась программа MacMolPlt [9].
Результаты расчетов
Оптимизированное геометрическое и электронное строение и квантово-химические характеристики молекул 4,6-диметилин-дена и 5,7-диметилиндена, полученные методом PM3, показаны на рисунках 1–2 и в таблицах 1–3. Используя формулу р Ка = 42,936 – 165,11 q max H+ , полученную авторами по методике [5] ( q max H+ = +0,12 – максимальный заряд на атомах водорода данных молекул; р Ка – универсальный показатель кислотности, см. табл. 1–3), находим значение кислотной силы, равное р Ка = 23.
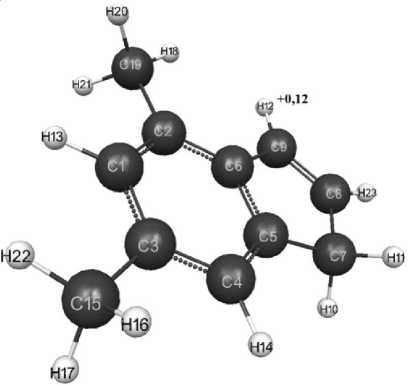
Рис. 1. Геометрическое и электронное строение молекулы 4,6-диметилиндена (метод PM3) ( Е 0 = -143 547 кДж/моль)
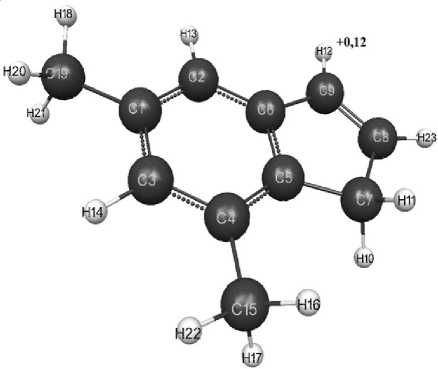
Рис. 2. Геометрическое и электронное строение молекулы 5,7-диметилиндена (метод PM3) ( Е 0 = -143 548 кДж/моль)
Таблица 1
Оптимизированные длины связей, валентные углы и заряды на атомах молекулы 4,6-диметилиндена (метод PM3)
|
Длины связей |
R , Å |
Валентные углы |
Град |
Атом |
Заряды на атомах молекулы |
|
C(2)-C(1) |
1,40 |
С(2)-С(1)-С(3) |
122 |
C(1) |
-0,11 |
|
C(2)-C(19) |
1,48 |
С(1)-С(3)-С(4) |
120 |
C(2) |
-0,04 |
|
C(3)-C(1) |
1,39 |
С(3)-С(4)-С(5) |
118 |
C(3) |
-0,07 |
|
C(3)-C(15) |
1,49 |
С(2)-С(6)-С(5) |
121 |
C(4) |
-0,09 |
|
C(4)-C(3) |
1,40 |
С(1)-С(2)-С(6) |
118 |
C(5) |
-0,08 |
|
C(5)-C(4) |
1,38 |
С(4)-С(5)-С(6) |
121 |
C(6) |
-0,07 |
|
C(6)-C(2) |
1,39 |
С(4)-С(5)-С(7) |
130 |
C(7) |
-0,02 |
|
C(6)-C(5) |
1,42 |
С(6)-С(5)-С(7) |
109 |
C(8) |
-0,16 |
|
C(7)-C(5) |
1,50 |
С(5)-С(7)-С(8) |
103 |
C(9) |
-0,09 |
|
C(8)-C(7) |
1,51 |
С(6)-С(9)-С(8) |
109 |
H(10) |
+0,08 |
|
C(9)-C(8) |
1,35 |
С(2)-С(6)-С(9) |
131 |
H(11) |
+0,08 |
|
C(9)-C(6) |
1,46 |
С(5)-С(6)-С(9) |
108 |
H(12) |
+0,12 |
|
H(10)-C(7) |
1,11 |
С(7)-С(8)-С(9) |
111 |
H(13) |
+0,11 |
|
H(11)-C(7) |
1,11 |
С(5)-С(7)-Н(10) |
112 |
H(14) |
+0,11 |
|
H(12)-C(9) |
1,09 |
С(8)-С(7)-Н(10) |
112 |
C(15) |
-0,07 |
|
H(13)-C(1) |
1,10 |
С(5)-С(7)-Н(11) |
112 |
H(16) |
+0,05 |
|
H(14)-C(4) |
1,09 |
С(8)-С(7)-Н(11) |
112 |
H(17) |
+0,05 |
|
H(16)-C(15) |
1,10 |
Н(10)-С(7)-Н(11) |
107 |
H(18) |
+0,05 |
|
H(17)-C(15) |
1,10 |
С(6)-С(9)-Н(12) |
123 |
C(19) |
-0,06 |
|
H(18)-C(19) |
1,10 |
С(8)-С(9)-Н(12) |
127 |
H(20) |
+0,05 |
|
H(20)-C(19) |
1,10 |
С(2)-С(1)-Н(13) |
119 |
H(21) |
+0,05 |
|
H(21)-C(19) |
1,10 |
С(3)-С(1)-Н(13) |
120 |
H(22) |
+0,04 |
|
H(22)-C(15) |
1,10 |
С(3)-С(4)-Н(14) |
121 |
H(23) |
+0,11 |
|
H(23)-C(8) |
1,09 |
С(5)-С(4)-Н(14) |
121 |
||
|
С(1)-С(3)-С(15) |
120 |
||||
|
С(4)-С(3)-С(15) |
119 |
||||
|
С(3)-С(15)-Н(16) |
111 |
||||
|
С(3)-С(15)-Н(17) |
111 |
||||
|
Н(16)-С(15)-Н(17) |
107 |
||||
|
С(2)-С(19)-Н(18) |
112 |
Окончание таблицы 1
|
Длины связей |
R , Å |
Валентные углы |
Град |
Атом |
Заряды на атомах молекулы |
|
С(1)-С(2)-С(19) |
120 |
||||
|
С(6)-С(2)-С(19) |
122 |
||||
|
С(2)-С(19)-Н(20) |
111 |
||||
|
Н(18)-С(19)-Н(20) |
108 |
||||
|
С(2)-С(19)-Н(21) |
111 |
||||
|
Н(20)-С(19)-Н(21) |
108 |
||||
|
Н(18)-С(19)-(21) |
108 |
||||
|
С(3)-С(15)-Н(22) |
112 |
||||
|
Н(17)-С(15)-Н(22) |
108 |
||||
|
Н(16)-С(15)-Н(22) |
108 |
||||
|
С(7)-С(8)-Н(23) |
122 |
||||
|
С(9)-С(8)-Н(23) |
127 |
Таблица 2
Оптимизированные длины связей, валентные углы и заряды на атомах молекулы 5,7-диметилиндена (метод PM3)
|
Длины связей |
R , Å |
Валентные углы |
Град |
Атом |
Заряды на атомах молекулы |
|
C(1)-C(19) |
1,49 |
С(2)-С(1)-С(3) |
121 |
C(1) |
-0,08 |
|
C(2)-C(1) |
1,40 |
С(1)-С(3)-С(4) |
121 |
C(2) |
-0,08 |
|
C(3)-C(1) |
1,40 |
С(3)-С(4)-С(5) |
118 |
C(3) |
-0,11 |
|
C(4)-C(3) |
1,40 |
С(2)-С(6)-С(5) |
121 |
C(4) |
-0,05 |
|
C(4)-C(15) |
1,48 |
С(1)-С(2)-С(6) |
118 |
C(5) |
-0,10 |
|
C(5)-C(4) |
1,39 |
С(4)-С(5)-С(6) |
121 |
C(6) |
-0,05 |
|
C(6)-C(2) |
1,38 |
С(4)-С(5)-С(7) |
130 |
C(7) |
-0,02 |
|
C(6)-C(5) |
1,41 |
С(6)-С(5)-С(7) |
109 |
C(8) |
-0,15 |
|
C(7)-C(5) |
1,50 |
С(5)-С(7)-С(8) |
103 |
C(9) |
-0,10 |
|
C(8)-C(7) |
1,51 |
С(6)-С(9)-С(8) |
109 |
H(10) |
+0,08 |
|
C(9)-C(8) |
1,35 |
С(2)-С(6)-С(9) |
131 |
H(11) |
+0,08 |
|
C(9)-C(6) |
1,46 |
С(5)-С(6)-С(9) |
108 |
H(12) |
+0,12 |
|
H(10)-C(7) |
1,11 |
С(7)-С(8)-С(9) |
111 |
H(13) |
+0,11 |
|
H(11)-C(7) |
1,11 |
С(5)-С(7)-Н(10) |
112 |
H(14) |
+0,11 |
|
H(12)-C(9) |
1,09 |
С(8)-С(7)-Н(10) |
112 |
C(15) |
-0,06 |
|
H(13)-C(2) |
1,09 |
С(5)-С(7)-Н(11) |
112 |
H(16) |
+0,04 |
|
H(14)-C(3) |
1,10 |
С(8)-С(7)-Н(11) |
112 |
H(17) |
+0,05 |
|
H(16)-C(15) |
1,10 |
Н(10)-С(7)-Н(11) |
107 |
H(18) |
+0,04 |
|
H(17)-C(15) |
1,10 |
С(6)-С(9)-Н(12) |
123 |
C(19) |
-0,06 |
|
H(18)-C(19) |
1,10 |
С(8)-С(9)-Н(12) |
128 |
H(20) |
+0,04 |
|
H(20)-C(19) |
1,10 |
С(1)-С(2)-Н(13) |
121 |
H(21) |
+0,05 |
|
H(21)-C(19) |
1,10 |
С(6)-С(2)-Н(13) |
121 |
H(22) |
+0,04 |
|
H(22)-C(15) |
1,10 |
С(1)-С(3)-Н(14) |
119 |
H(23) |
+0,11 |
|
H(23)-C(8) |
1,09 |
С(4)-С(3)-Н(14) |
119 |
||
|
С(3)-С(4)-С(15) |
121 |
||||
|
С(5)-С(4)-С(15) |
121 |
||||
|
С(4)-С(15)-(16) |
111 |
||||
|
С(4)-С(15)-Н(17) |
111 |
||||
|
Н(16)-С(15)-(17) |
107 |
||||
|
С(1)-С(19)-Н(18) |
112 |
||||
|
С(2)-С(1)-С(19) |
120 |
||||
|
С(3)-С(1)-С(19) |
120 |
||||
|
С(1)-С(19)-Н(20) |
112 |
||||
|
Н(18)-С(19)-Н(20) |
108 |
||||
|
С(1)-С(19)-Н(21) |
110 |
Окончание таблицы 2
|
Длины связей |
R , Å |
Валентные углы |
Град |
Атом |
Заряды на атомах молекулы |
|
Н(20)-С(19)-Н(21) |
108 |
||||
|
Н(18)-С(19)-Н(21) |
108 |
||||
|
С(4)-С(15)-Н(22) |
112 |
||||
|
Н(17)-С(15)-Н(22) |
108 |
||||
|
Н(16)-С(15)-Н(22) |
108 |
||||
|
С(7)-С(8)-Н(23) |
122 |
||||
|
С(9)-С(8)-Н(23) |
127 |
Таблица 3
Общая энергия (Е0, кДж/моль), максимальный заряд на атоме водорода (qmaxH+) и универсальный показатель кислотности (рКа) мономеров
(метод PM3)
|
№ п/п |
Мономер |
Е 0 |
H+ q max |
р Ка |
|
1 |
4,6-диметилиндена |
-143 547 |
+0,12 |
23 |
|
2 |
5,7-диметилиндена |
-143 548 |
+0,12 |
23 |
Заключение
В настоящей работе впервые был выполнен квантово-химический расчет молекул 4,6-диметилиндена и 5,7-диметилиндена квантово-химическим методом PM3. Определено оптимизированное геометрическое и электронное строение этих соединений. Теоретически оценена их кислотная сила ( р Ка = 23). Эти данные качественно находятся в хорошем соответствии с данными, представленными в работе [3], что свидетельствует о более корректном выборе метода PM3 для оценки кислотной силы изучаемых инденов, чем, например, в работах [1–2]. Кроме того, показано, что изучаемые мономеры 4,6-диметилинде-на и 5,7-диметилиндена относятся к классу очень слабых Н-кислот (так как p Ka > 14).
Список литературы Об электронной структуре мономеров катионной полимеризации 4, 6-диметилиндена и 5, 7-диметилиндена
- Бабкин, В. А. Квантово-химический расчет молекулы 4,6-диметилиндена/В. А. Бабкин, К. Н. Садыков//Квантово-химический расчет уникальных молекулярных систем: сб. ст. каф. Ми-ЕНД СФ ВолгГАСУ. -Волгоград: Изд-во ВолГУ, 2010. -Т. 3. -С. 189-192.
- Бабкин, В. А. Квантово-химический расчет молекулы 5,7-диметилиндена/В. А. Бабкин, К. Н. Садыков//Квантово-химический расчет уникальных молекулярных систем: сб. ст. каф. Ми-ЕНД СФ ВолгГАСУ. -Волгоград: Изд-во ВолГУ, 2010. -Т. 3. -С. 184-186.
- Белл, Р. Протон в химии/Р. Белл. -М.: Мир, 1977. -381 с.
- Кеннеди, Дж. Катионная полимеризация олефинов/Дж. Кеннеди. -М., 1978. -431 с.
- О корреляционной зависимости универсального показателя кислотности с максимальным зарядом на атоме водорода Н-кислот. Метод АМ1/В. А. Бабкин, Д. С. Андреев, В. Т. Фомичев, Г. Е. Заиков, Э. Р. Мухамедзянова//Вестник Казанского технологического университет а. -2012. -№ 10. -С. 15-18.
- Цирельсон, В. Г. Квантовая химия. Молекулы, молекулярные системы и твердые тела/В. Г. Цирельсон. -М.: Бином, 2010. -422 с.
- Alex, A. Granovsky, Firefly version 8/A. Alex. -Electronic text data. -Mode of access: http://classic.chem.msu.su/gran/firefly/index.html. -Title from screen.
- Anton, A. Confidence intervals for copolymerization reactivity ratios determined/A. Anton, J. Zwegers, E. Marechal//Bull. Soc. Chim. France. -1970. -Р. 1466.
- Bode, B. M. MacMolPlt: A Graphical User Interface for GAMESS/B. M. Bode, M. S. Gordon//J. Molec. Graphics. -1998. -№ 16. -Р. 133-138.
- Marechal, E. Polymeric Dyes-Synthesis, Properties and Uses/E. Marechal//J. Polymer Sci. -1970. -Vol. A-1. -№ 8. -Р. 2867.
- Marechal, E. Sigwalt Synth esis of Poly(indene-g-isobutylene) by Cationic Techniques/E. Marechal, P. Evard, P.//Bull. Soc. Chim. France. -1981. -Р. 2247-2250.
- Shmidt, M. W. General Atomic and Molecular Electronic Structure System/M. W. Shmidt, K. K. Baldrosge, J. A. Elbert //J. Comput. Chem. -1993. -Vol. 14. -Р. 1347-1363.


