Образования титана никеля в мелкодисперсной системе оксидов TiO2 (анатаз) -NiO
Автор: Сериков Александр Сергеевич, Гладков Владимир Евгеньевич, Жеребцов Дмитрий Анатольевич, Колмогорцев Алексей Михайлович, Викторов Валерий Викторович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия конденсированного состояния
Статья в выпуске: 31 (207), 2010 года.
Бесплатный доступ
Физико-химическими методами (РСА, ДТА, масс-спектрометрия, маг-нетохимический анализ) исследован фазовый переход анатаз- рутил в мелкодисперсных порошках ТiO2, отличающихся способом получения. Установлено, что температура фазового перехода зависит от предыстории получения анатаза. При прокаливании эквимолярной смеси TiO2 (анатаз) -Ni(N03)2 и ТiO2 (анатаз)-(NiOH)2CO3 образуется только титанат никеля, других оксидных соединений с Ti (IV) и Ni (II) не обнаружено. Установлено, что фазовый переход анатаз-рутил препятствует образованию титаната никеля в интервале температур 700-850 °С.
Диоксид титана, анатаз, рутил, фазовый переход, титанат никеля
Короткий адрес: https://sciup.org/147160180
IDR: 147160180 | УДК: 548.3
Formation of nickel titanate in the system of smallsized oxide of ТiO2 (anatese) and NiO
Transition from anatase to rutile in smallsized ТiO2 was characterized by physical-chemistry methods (XRD, DTA, MS methods). It was investigated that the temperature of phase translation depended on ways of preparation of Ti02. Only nickel titanate was formed during calcinations of equimolar mixture of TiO2(anatase)-Ni(N03)2 and TiO2(anatese)-((NiOH)2CO3). Another oxide of Ti (TV) and Ni (II) was no found. It was investigated that transition from anatase to rutile in temperature rang 700-850 °C was hindered formation of NiTiO3.
Текст обзорной статьи Образования титана никеля в мелкодисперсной системе оксидов TiO2 (анатаз) -NiO
Титанат никеля NiTiO3 широко применяется в качестве полупроводников, оптических материалов, катализаторов, пигментов и др. [1-5]. Известно, что NiTiO3 имеет структуру ильменита, где атомы Ni и Ti находятся в октаэдрической координации. Установлено [6], что это соединение имеет антиферромагнитную структуру с температурой Нееля -250 °C. Измерения, проводившиеся в интервале температур -269.. .30 °C, показали, что титанат никеля обладает слабой магнитной анизотропией при низких температурах. Синтез титаната никеля осуществляется множеством способов с использованием органических производных титана, например, его оксалатных комплексов или тетрабутоксититана (IV) [7-10]. Синтез NiTiO3 твердофазным взаимодействием осложняется тем, что при низких температурах (Т <1000 °C) наряду с образующимся титанатом в системе остается TiO2 рутильной и анатазной модификации и NiO. Высокие температуры приводят к неконтролируемому увеличению размера частиц с различной морфологией. Вместе с тем, влияние фазового перехода анатаз -» рутил на особенности синтеза NiTiO3 при взаимодействии в мелкодисперсной системе TiO2-NiO изучено недостаточно.
Цель работы - изучение влияния фазового перехода анатаза в рутил на особенности образования титаната никеля в мелкодисперсной системе TiO2-NiO.
Экспериментальная часть
Исходные реакционные смеси готовили тщательным смешением оксидов титана и солей никеля квалификации «х.ч.» или «ос.ч.» в агатовой ступке до получения порошков однородного цвета.
Оксид титана (IV) анатазной и рутильной модификации получали прокаливанием гидролизного диоксида титана (ГДТ) при 600 °C и 1200 °C, соответственно, в течение 1,5-2 ч и термолизом TiCl4. ГДТ получали способом, детально описанным в [11].
Исходные механические смеси готовили по следующим вариантам: смесь I - ТЮ2 (анатаз из ГДТ)-Ni(NO3)2-6H2O; смесь II - TiO2 (анатаз из TiCl4)-Ni(NO3)2-6H2O; смесь III - ТЮ2 (анатаз из ГДТ) - (NiOH)2CO3; смесь IV - ТЮ2 (анатаз из TiCl4) - (NiOH)2CO3; смесь V - ТЮ2 (рутил из ГДТ) -Ni(NO3)2-6H2O и смесь VI - TiO2 (рутил из ГДТ) - (NiOH)2CO3 путем смешения в спирте эквимолярных отношений (в пересчете на NiO). Оксиды титана и смеси I-VI прокаливали при температурах 700-1200 °C с интервалом 50 °C.
Химическую чистоту образцов контролировали спектральными методами на приборе PGS-2. Прокаленные смеси исследовали рентгенографически на дифрактометре ДРОН-ЗМ с К„-излуче-нием меди. Спектры дифференциально-термического и масс-спектрометрического анализов получали на приборе Netzch Jupiter. Анализ проводили со скоростью нагрева 20 °C в минуту, в кисло-родно-аргоновой смеси от комнатной температуры до 1100 °C.
Химия конденсированного состояния
Количественный рентгеновский анализ рутила и анатаза, а также титаната никеля проводили по калибровочному графику, полученному из рентгеновских данных механических смесей.
Магнетохимический анализ смесей после прокаливания проводили методом Фарадея при комнатной температуре.
Результаты и обсуждение
Размер частиц исходного анатаза, оцененный по ширине рентгеновских дифракционных максимумов, составлял величину ~20 нм. В зависимости от температуры прокаливания смеси I-VI имели различную окраску от темно-коричневой до ярко-желтой.
РСА полученных образцов показал, что температура и скорость фазового перехода анатаз-рутил для Т1О2 (ГДТ) и TiO2 (Т1С14) различна. Методом ДТА (рис. 1, а) установили, что для Т1О2 (ГДТ) при температурах 700-710 °C идет активная десульфатизация, достигающая максимума при температуре 780 °C. Масс-спектрометрические исследования показали, что при 780 °C наблюдали максимум выделения оксидов серы (m/е = 64 и т/е = 48). Слабый экзоэффект при температуре =850 °C относится к фазовому переходу ТЮ2 (анатаз) -» ТЮ2 (рутил) (АН перехода = = 1,8 кДж/моль).
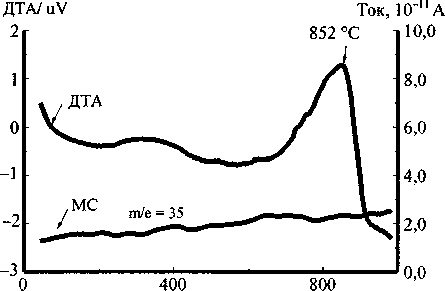
Отметим, что кривые ДТА TiO2 (TiCl4) не содержат эффектов, связанных с десорбцией каких-либо соединений. При этом потерь массы этим образцом при нагревании не обнаружили. Экзоэффект в области 852 °C связан с фазовым переходом анатаз-рутил. Выделения хлора при этом не обнаружили (рис. 1, б).
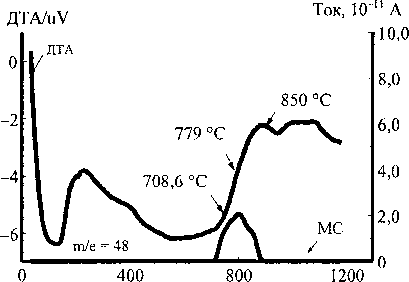
Рис. 1. Дифференциально-термический и масс-спектрометрический анализ: а - анатаз из ГДТ; б - анатаз из TiCI4
На рис. 2 представлены зависимости концентрации рутила от времени и температуры изотермической выдержки. При этом полный переход в рутил для Т1О2 (ГДТ) при 950 и 900 °C в течение 1 и 3 ч соответственно, тогда как фазовый переход анатаз-рутил TiO2(TiCl4) заканчивается при температуре на 100 °C выше.
На основании рутильной модификации ТЮ2 при прокаливании смесей V и VI в интервале температур 700-850 °C титаната никеля не обнаружили. Тогда как в прокаленных смесях I-IV с анатазом в этом температурном интервале образуется титанат никеля, количество которого зависит от времени изотермической выдержки и температуры прокаливания смесей.
Степень превращения Т1О2 в титанат никеля представлена на рис. 3. При этом реакция заканчивается фактически в течение 1 ч. Увеличение концентрации титаната никеля при изменении времени прокаливания с 1 до 3 ч незначительно (всего на 3-5 %).
Количественные данные о фазовом составе смесей после изотермической выдержки представлены в таблице. Анализ представленных данных показывает, что в прокаленных смесях I, III и IV одновременно с фазовым переходом анатаз-рутил образуется титанат никеля. Полного превращения диоксида титана в титанат никеля не происходит. При прокаливании в температурном интервале 800-850 °C оксид титана находится как в рутильной, так и в анатазной модификации. При термообработке смеси II механизм образования титаната никеля совершенно иной. В последнем случае происходит постепенное увеличение количества титаната никеля от времени и температуры изотермической выдержки. Фазового перехода анатаз-рутил в данном температур-
Сериков А.С., Гпадкое В.Е., Жеребцов Д. А., Колмогорцев А.М., Викторов В.В.
ном интервале не наблюдали. Полное превращение анатаза в титанат никеля в смеси II происходит в течение 3 ч при температуре 850 °C. Тогда как при температурах 800-850 °C в смеси I и IV образуется рутильная модификация, которая не взаимодействует с NiO.
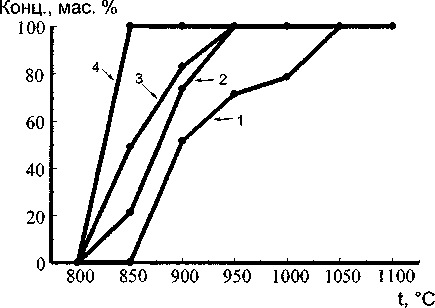
Рис. 2. Концентрация рутила, образующегося при изотермической выдержке из исходных оксидов: 1 - анатаз (ТЮЦ) после 1 ч прокаливания; 2 - анатаз (ГДТ) после 1 ч прокаливания; 3 - анатаз (TICI4) после 3 ч прокаливания; 4- анатаз (ГДТ) после 3 ч прокаливания
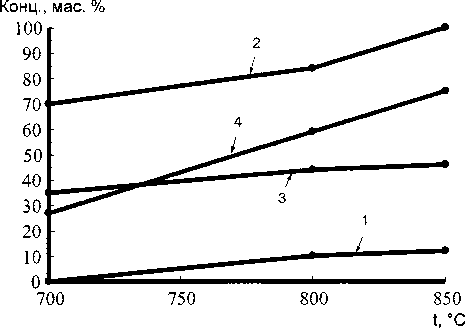
Рис. 3. Содержание титаната никеля в смесях после 3-часовой изотермической выдержки: 1 - смесь I;
2 - смесь II; 3 - смесь III; 4 - смесь IV
Количественный фазовый состав смесей I—IV после изотермической выдержки в течение 3 ч
|
Смеси |
тпр, °с |
Температура, °C |
|||
|
TiO2 (ан), мае. % |
ТЮ2 (рут), мае. % |
NiO, мае. % |
NiTiO3, мае. % |
||
|
I |
700 |
34 |
0 |
31 |
35 |
|
800 |
0 |
39 |
27 |
44 |
|
|
850 |
0 |
28 |
26 |
46 |
|
|
II |
700 |
16 |
0 |
15 |
70 |
|
800 |
8 |
0 |
8 |
84 |
|
|
850 |
0 |
0 |
0 |
100 |
|
|
III |
700 |
52 |
0 |
48 |
Следы |
|
800 |
31 |
16 |
41 |
10 |
|
|
850 |
0 |
46 |
42 |
12 ■ |
|
|
IV |
700 |
38 |
0 |
35 |
27 |
|
800 |
9 |
12 |
20 |
59 |
|
|
850 |
0 |
13 |
12 |
75 |
|
Магнитная восприичивость образцов смесей I и II увеличивается с увеличением температуры прокаливания, что указывает на возрастание парамагнитной фазы титаната никеля в смесях. Так для образца из смеси ТЮ2 (анатаз из ГДТ)-Ni(NO3)2-6H2O, полученного изотермической выдержкой при 700 и 800 °C, х = 13,ОТО-6 см3/г (содержание NiTiO3 - 3 5 %) и у = 14,5-10"6 см3/г (содержание NiTiO3 - 44 %), а для образца из смеси ТЮ2 (анатаз) TiCl4 -Ni(NO3)2-6H2O, прокаленного в тех же условиях, х = 20,9 10 6 см3/г (содержание NiTiO3 -70 %) и у =25,0-1 О*6 см3/г (содержание NiTiO3- 84 %) соответственно.
Выводы
Методами PC А, ДТА, масс-спектрометрического анализа исследован фазовый переход анатаз-рутил. Установлено, что температура фазового перехода зависит от предыстории получения оксида титана. Фазовый переход анатаз-рутил для TiO2, полученный из ГДТ, наблюдали на 100 °C ниже, чем анатаза, полученного из TiCl4. Исследовано образование титаната никеля из анатазной и рутильной модификации при взаимодействии с Ni(NO3)2 и (NiOH)2CO3 (в пересчете на NiO - эквимолярная смесь). Механизм взаимодействия существенно различен. При взаимодействии TiO2 (ГДТ) с нитратом никеля одновременно с фазовым переходом анатаз-рутил на-
Химия конденсированного состояния
блюдается образование титаната никеля. При этом полного превращения титаната никеля не происходит в температурном интервале 700-850 °C. Взаимодействие TiO2 (TiCl4) с нитратом никеля происходит без фазового перехода анатаз—рутил и образование титаната никеля заканчивается при 850 °C в течение 1 ч.
Список литературы Образования титана никеля в мелкодисперсной системе оксидов TiO2 (анатаз) -NiO
- Random fields and random anisotropics in the mixed ising-XY magnet FexCot-xTiO3/Q.J. Harris, Q. Feng, Y.S. Lee et al.//Phys. Rev. Lett. -1997. -Vol. 78, № 2. -P. 346-349.
- Fisch, R. Critical behavior of randomly pinned spin-density waves/R. Fisch//Physical Review -1995-Vol. 51-P. 11507-11514.
- Dharmaraj, N. Nickel titanate nanofibers by electrospinning/N. Dharmaraj, H.C. Park, C.K. Kim et al.//Materials Chemistry and Physics. -2004. -Vol. 87. -1. 1. -P. 5-9.
- Shimizu, Y./Y. Shimizu, K. Uemura, N. Miura et al.//Chem. Lett. -1988 -Vol. 67 -P. 1979.
- Phani, A.R. Structural characterization of nickel tantalum oxide synthesized by sol-gel spin coating technique/A.R. Phani, S. Santucci//Materials Letters. -2001. -Vol. 47. -1. 1-2. -P. 20-24.
- Newnhan, R.E. Crystal structure and magnetic properties of СоТiO3/R.E. Newnhan, J.H. Fang, R.P. Santoro//Acta Crystallogr. -1964. -Vol. 17. -P. 240-242.
- Ni, Y. Nickel titanate microtubes constructed by nearly spherical nanoparticles: Preparation, characterization and properties/Y. Ni, X. Wang, J. Hong//Materials Research Bulletin. -2009. -Vol. 44.-P. 1797-1801.
- Synthesis and characterization of titanates of the formula MTiO3 (M = Mn, Fe, Co, Ni and Cd) by co-precipitation of mixed metal oxalates/Y. M Sharma, M. Kharkwal, S. Uma, R. Nagarajan//Polyhedron. -2009. -Vol. 28. -P. 579-585.
- Structural characterization of NiTi03 nanopowders prepared by stearic acid gel method/M.S. Sadjadi, K. Zare, S. Khanahmadzadeh, M. Enhessari//Materials Letters. -2008. -Vol. 62. -P. 3679-3681.
- Low-temperature synthesis and characterization of (Zn,Ni)TiO3 ceramics by a modified sol-gel route/J. Luoa, X. Xing, R. Yu et al.//Journal of Alloys and Compounds. -2006. -Vol. 420. -P. 317-321.
- Беленький, Е.Ф. Химия и технология пигментов/Е.Ф Беленький, И.В Рискин. -Л.: Химия, 1974.-656 с.


