Оценка анксиолитической активности оптических изомеров 3-зам ещенных 4-(1н-тетразол-1-ил)бутановых кислот
Автор: Ковалев Н.С., Бакулин Д.А., Саблина Л.А., Воронцов М.Ю., Быкова А.С., Резников А.Н., Климочкин Ю.Н.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 1 (69), 2021 года.
Бесплатный доступ
3-пара-толилзамещенная ГАМК (толибут) оказывает нейропротекторное, обезболивающее, миорелаксирующее, противотревожное и противосудорожное действие и представляет собой рацемат. Клиническое применение толибута ограничено узкой терапевтической широтой. Одним из способов снижения его токсичности может быть подход, заключающейся в модификации структуры ГАМК, в частности замене аминогруппы на фрагмент тетразола. Тетразолильный заместитель может использоваться в качестве биоизостерического аналога различных функциональных групп. Целью данной работы является исследование анксиолитической активности тетразолильных производных ГАМК с толильным и фенильным радикалом в p-положении. Исследование было проведено на крысах линии Wistar. Была произведена оценка анксиолитического действия (R)- и (S)-энантиомеров 3-арилзамещенных 4-(1Н-тетразол-1-ил)бутановых кислот. По результатам исследования было отмечено наличие анксиолитической активности у (R)-изомера 3-(4-метилфенил)-4-(1Н-тетразол-1-ил)бутановой кислоты в условиях конфликтной ситуации, сопоставимой с таковой у толибута и фенибута.
Гамк, толибут, фенибут, энантиомеры, анксиолитическая активность, крысы
Короткий адрес: https://sciup.org/142229367
IDR: 142229367 | УДК: 615.214.2:547.466.3
Anxiolytic activity of optical isomers of 3-substituted 4- (1n-tetrazol-1-yl) butanoic acids
Racemate of 3-para-tolyl-substituted GABA (tolibut) has neuroprotective, analgesic, muscle relaxant, anti-anxiety and anticonvulsant effects. The clinical application of tolibut is limited by a narrow therapeutic range. One of the ways to reduce its toxicity can be the approach of modifying the structure of GABA, in particular, replacing the amino group with a tetrazole fragment. The tetrazolyl substituent can be used as a bioisosteric analogue of various functional groups. The aim of this work is to study the anxiolytic activity of tetrazolyl derivatives of GABA with tolyl and phenyl radicals in the beta position. The study was performed on Wistar rats. The anxiolytic action of the (R)- and (S)-enantiomers of 3-aryl-substituted 4-(1H-tetrazol-1-yl) butanoic acids was evaluated. According to the results of the study, the presence of anxiolytic activity in the (R) -isomer of 3-(4-methylphenyl) -4-(1H-tetrazol-1-yl) butanoic acid in a conflict situation was noted, comparable to that in tolibut and phenibut.
Текст научной статьи Оценка анксиолитической активности оптических изомеров 3-зам ещенных 4-(1н-тетразол-1-ил)бутановых кислот
Посредством последовательной структурной модификации молекулы ГАМК было создано значительное число лекарственных препаратов с психотропной активностью. Фенибут является фенильным производным ГАМК (включение фенильного радикала в β-положение структуры ГАМК увеличило её липофильность и соответственно повысило проницаемость через гематоэнцефалический барьер) и, являясь агонистом ГАМК, проявляет анксиолитическую и ноотропную активность, а также церебропротекторную активность в экспериментальных условиях [1, 6]. Препарат эффективен при лечении тревожных расстройств, депрессий, посттравматического стрессового расстройства. Структурные аналоги фенибута с толильным и 4-хлорфенильным заместителем в β-положении проявляют более выраженное анксиолитическое действие, большую активность в отношении ГАМК, а также у данных препаратов появляется дозозависимая миорелаксирующая активность, возможно, вызванная большим сродством к ГАМК-В рецептору.
Также исследования показывают аналогичный механизм действия у фенибута и габапентина, который широко используется для лечения тревожных расстройств и невропатической боли [6].
Толибут – пара -толилзамещенный аналог ГАМК, который, по результатам доклинических исследований, обладает достаточно широким спектром фармакологической активности: анальгетической [8], транквилизирующей [10], нейро-протекторной [12], седативной, миорелаксирующей. По многим фармакологическим эффектам толибут многократно превосходит фенибут, однако последний оказался менее токсичным и получил дальнейшее развитие с внедрением в практику [2]. Клиническое применение толибу-та ограничено узкой терапевтической широтой (LD 50 – 252 мг/кг).
Одним из способов её расширения может быть подход, заключающейся в модификации структуры ГАМК, в частности, замене аминогруппы на тетразольный цикл, который может использоваться в качестве биоизостерического аналога различных функциональных групп (карбоксильной и других) [13].
Многочисленные исследования способствовали акцентированию внимания на фармакологической активности индивидуальных энантиомеров давно известных препаратах.
Изучение активности отдельных энантиомеров фенибута и баклофена показало значительно большую активность ( R )-изомера и почти полное её отсутствие у ( S )-изомера. В дальнейшем как in vitro, так и in vivo, было выявлено, что все фармакологические эффекты фенибута реализуются посредством ( R )-изомера, в то время как ( S )-изомер оказался функционально неактивным [7]. Позже аналогичные результаты в in vitro и in vivo исследованиях были получены в отношении баклофена. Было подтверждено, что ( S )-изомер баклофена не обладает фармакологической активностью [9].
ЦЕЛЬ РАБОТЫ
Исследовать анксиолитическую активность ( S )- и ( R )-энантиомеров. 3-арилзамещенных 4-(1 Н -тетразол-1-ил)бутановых кислот (тетразолсодержащих аналогов фенибута и толибута).
МЕТОДИКА ИССЛЕДОВАНИЯ
Экспериментальное исследование проведено на 90 крысах-самцах линии Wistar, массой 200–230 г, в возрасте 6 месяцев.
Животные содержались в условиях вивария (ГОСТ Р 51849-2001) со свободным доступом к питьевой воде и пище (ООО «Лаборатор-корм», Москва).
Протокол исследования одобрен локальным этическим комитетом (Региональный исследовательский этический комитет Волгоградской области) № 2010-2019 02 апреля 2019 г.
С целью сравнения фармакологических свойств энантиомеров тетразолсодержащих аналогов фенибута и толибута в качестве препаратов сравнения использовались препараты фени-бут в дозе 20 мг/кг и толибут в дозе 10 мг/кг (см. табл.). Исследуемые соединения вводились в эквимолярных дозах 12 мг/кг и 25 мг/кг. Были сформированы следующие группы: контрольная, которым вводили физиологический раствор (плацебо), опытные, которым вводили ( R )-4-(1 Н -тетразол-1-ил)-3-фенилбутановую кислоту (ANR-05) и ее рацемат (ANR-06) (ANR-05 и 06) в дозах 12 и 25 мг/кг, опытные, которым вводили ( R )-4-(1 Н -тетразол-1-ил)-3-(4-метилфенил)бутано-вую кислоту (ANR-07) и ее рацемат (ANR-08) (ANR-07 и 08) в дозах 12 и 25 мг/кг, группа, получающих препарат сравнения толибут в дозе 10 мг/кг (наиболее активная доза, не вызывающая седативного эффекта) и группа, получавших препарат сравнения фенибут в дозе 20 мг/кг (наиболее активная доза). Исследуемые соединения вводили лабораторным животным однократно, внутрибрюшинно за 60 минут до выполнения поведенческих тестов.
Исследуемые соединения и препараты сравнения
|
Исследуемые соединения |
1/10 от Mr, мг/кг |
1/20 от Mr, мг/кг |
|
Фенибут |
20 |
|
|
ANR-05 |
25 |
12 |
|
ANR-06 |
25 |
12 |
|
Толибут |
10 |
|
|
ANR-07 |
25 |
12 |
|
ANR-08 |
25 |
12 |
Анксиолитическую активность исследуемых соединений оценивали в приподнятом крестообразном лабиринте «ПКЛ» и по методике конфликтной ситуации «вариант Vogel» [4, 5].
Соединения для исследования были получены по методикам, представленным в предыдущей работе [3], и предоставлены сотрудниками кафедры Органической химии ФГБОУ ВО «СамГТУ», г. Самара.
Статистическая обработка данных проводилась в MS Excel 2016 и Prism 6, статистический анализ осуществляли с использованием критериев Шапиро – Уилка, Краскела – Уоллиса и Дана.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
В тесте приподнятый крестообразный лабиринт (ПКЛ) 4-(1Н-тетразол-1-ил)-3-фенилбутано-вая и 4-(1Н-тетразол-1-ил)-3-(4-метилфенил)бу- тановая кислоты (в рацемической форме и в виде индивидуальных (R)-изомеров) незначи- тельно влияли на поведение животных в условиях переменной стрессогенности (см. рис.).
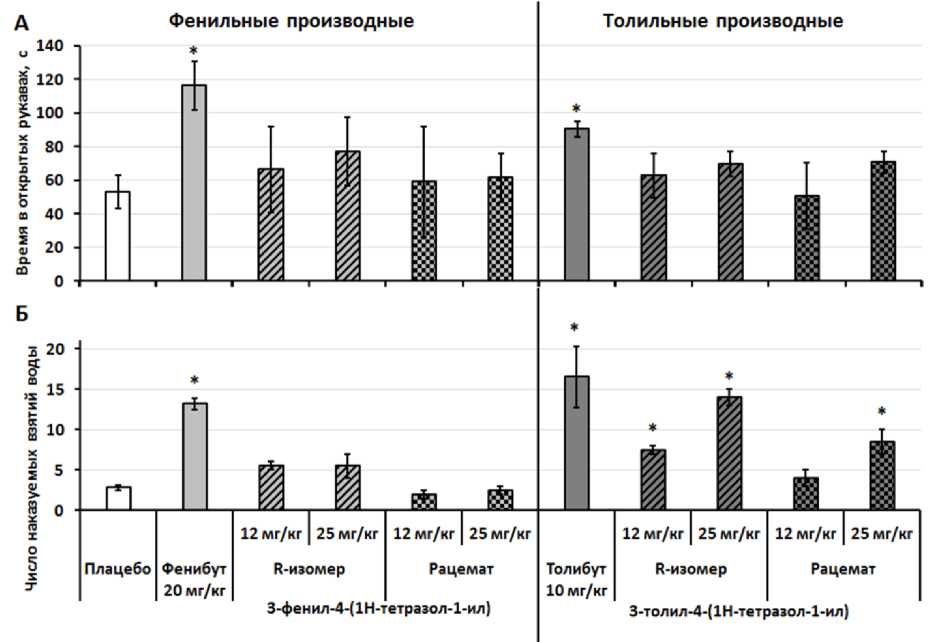
Рис. Продолжительность нахождения в открытых рукавах в тесте ПКЛ (а); количество наказуемых подходов в тесте конфликтной ситуации «вариант Vogel» (б)
Для оценки анксиолитической активности исследуемых соединений дополнительно к тесту ПКЛ был проведен тест конфликтной ситуации «вариант Vogel», в котором соединения вводили за 60 минут до начала тестирования.
Животные, которым вводили соединение ANR-08 (рацемическую 4-(1 Н -тетразол-1-ил)-3-(4-метилфенил)бутановую кислоту) совершали большее количество наказуемых взятий воды по мере увеличения вводимой дозы. Статистически значимые различия с контрольной группой животных достигаются в дозе 25 мг/кг, что свидетельствует о подавлении чувства тревоги перед аверсивным болевым раздражителем и снижении уровня тревоги.
Однако под действием ( R )-изомера 4-(1 Н -тетразол-1-ил)-3-(4-метилфе-нил)бутановой кислоты (ANR-07) животные совершали большее количество наказуемых взятий уже в дозе 12 мг/кг, и данный показатель возрастал по мере увеличения вводимой дозы.
Полученные результаты дают возможность сделать предположение о наличии анксиолитической активности у 4-(1Н-тетразол-1-ил)-3-(4- метилфенил)бутановой кислоты, более выраженной у (R)-изомера в сравнении с рацематом.
Рацемическая форма 4-(1 Н -тетразол-1-ил)-3-фенилбутановой кислоты (ANR-06) не оказывала противотревожных свойств: животные совершали сопоставимое с контрольной группой количество наказуемых взятий воды.
Группа животных, получающая ( R )-изомер 4-(1 Н -тетразол-1-ил)-3-фенилбутановой кислоты (ANR-05) обладала более выраженной анксиолитической активностью в сравнении с рацематом, однако уступало по эффективности как правовращающей, так и рацемической форме тет-разолильных производных ГАМК с толильным радикалом в β-положении (ANR-07 и ANR-08).
Тревожные расстройства характеризуются иррациональным неконтролируемым страхом и стойким чувством тревоги, сопровождаются нарушениями в модуляции мозговых цепей, регулирующих эмоциональные реакции на потенциально опасные стимулы. Множество работ доказывает, что мозговые цепи в миндалине содержат ингибирующие сети γ-аминомаслянной кислоты, и этот нейротрансмиттер играет ключе- вую роль в модуляции как нормальных, так и патологических тревожных реакций. Взаимодействие с аллостерическими сайтами на поверхности ГАМК рецепторов позволяет регулировать уровень ингибирования нейронов в миндалине. Именно этот механизм является основной мишенью многих классов анксиолитиков. Изменения уровней эндогенных модуляторов этих аллостерических сайтов, а также изменения в составе субъединиц рецептора ГАМК-А могут являться механизмом, посредством которого уровень нейронального торможения подавляется в патологических состояниях тревоги [11].
Толибут как препарат с доказанным анксиолитическим, нейропротекторным, седативным и рядом других свойств [9, 11, 13] может являться перспективным средством для лечения тревожных расстройств. Выраженный анксиолитический и седативный эффект толибута может способствовать нормализации чрезмерных эмоциональных и тревожных реакций, которые часто сопровождаются повышенной возбудимостью.
Проведенное исследование нейротропной активности энантиомеров 3-замещенных 4-(1 Н -тетразол-1-ил)бутановых кислот показало, что ( R )-изомер 4-(1 Н -тетразол-1-ил)-3-(4-метилфенил)бу-тановой кислоты обладает умеренной анксиолитической активностью.
ЗАКЛЮЧЕНИЕ
4-(1 Н -тетразол-1-ил)-3-(4-метилфенил)бута-новая кислота обладает более выраженным анксиолитическим действием в сравнении с 4-(1 Н -тетразол-1-ил)-3-(4-метилфенил)бутановой кислотой. Противотревожное действие наиболее выражено в условиях конфликтной ситуации у ( R )-изомера и проявлялось на сопоставимом уровне с препаратами толибут и фенибут.
[и др.] // Экспериментальная и клиническая фармакология. – 2016. – Т. 79, № 4. – С. 18 – 25. – Текст : непосредственный.
Список литературы Оценка анксиолитической активности оптических изомеров 3-зам ещенных 4-(1н-тетразол-1-ил)бутановых кислот
- Волотова Е. В., Филина И. С., Бакулин Д. А. [и др.] // Экспериментальная и клиническая фармакология. – 2016. – Т. 79, № 4. – С. 18 – 25. – Текст : непосредственный.
- Перфилова В. Н., Тюренков И. Н. // Вестник Волгоградского государственного медицинского университета. – 2005. – № 1 (13). – С. 30 – 33. – Текст : непосредственный.
- Резников А. Н., Островский В. А., Климочкин Ю. Н. // Журнал органической химии. – 2018. – Т. 54, № 11. – С. 1699 – 1704. – Текст : непосредственный.
- Султанова К. Т., Яковлев Д. С., Мальцев Д. В. [и др.] // Вестник Волгоградского государственного медицинского университета. – 2018. – № 3 (67). – С. 28 – 32. – Текст : непосредственный.
- Таран А. С., Мальцев Д. В., Яковлев Д. С. [и др.] // Волгоградский научно-медицинский журнал. – 2017. – № 1 (53). – С. 24 – 26. – Текст : непосредственный.
- Ahuja T., Mgbako O., Katzman C., Grossman A. // Case Rep Psychiatry. – 2018. – Vol. 2018. – P. 9864285. – Direct text.
- Dambrova M., Zvejniece L., Liepinsh E. [ et al.] // Eur J Pharmacol. – 2008. – Vol. 583 (1). – P. 128 – 134. – Direct text.
- Dmitriev A. V., Andreev N. I. // Farmakol Toksikol. – 1987. – Vol. 50 (1). – P. 24 – 27. – Direct text.
- Lorrai I., Maccioni P., Gessa G. L., Colombo G. // Front Psychiatry. – 2016. – Vol. 7. – P. 68. – Direct text.
- Morozov I. S., Kovalev G. I., Maisov N. I. [et al.] // Pharm Chem J. – 1977. – Vol. 11. – P. 10 – 12. – Direct text.
- Nuss P. // Neuropsychiatr Dis Treat. – 2015. – Vol. 11. – P. 165 – 175. – Direct text.
- Tyurenkov I. N., Borodkina L. E., Bagmetova V. V. [et al.] // Bull Exp Biol Med. – 2016. – Vol. 160 (4). – P. 465 – 469. – Direct text.
- Voitekhovich S. V., Ivashkevich O. A., Gaponik P. N. // Russian Journal of Organic Chemistry. – 2013. – Vol. 49. – P. 635 – 654. – Direct text.


