Оценка барьерной функции чернозема и серой почвы в рамках экспериментального загрязнения ионами меди
Автор: Иовчева А. Д., Семенков И. Н.
Журнал: Бюллетень Почвенного института им. В.В. Докучаева @byulleten-esoil
Рубрика: Статьи
Статья в выпуске: 116, 2023 года.
Бесплатный доступ
Целью работы была сравнительная оценка устойчивости гумусовых горизонтов чернозема квазиглееватого и серой почвы к смоделированному загрязнению медью. Для оценки сорбционной емкости почв и создания необходимых уровней загрязнения в почвы внесена Cu в виде растворов ацетатов с концентрацией от 2 до 200 мг/л (что соответствует внесению 20-2 000 мг/кг Cu). Показано, что изотермы адсорбции Cu достоверно аппроксимируются уравнением Лэнгмюра. При этом полученные значения максимальной адсорбции (Cmax) и константы Ленгмюра (KL) для чернозема выше, чем для серой почвы. Это свидетельствует о более высокой поглотительной способности и более прочном удержании сорбированной черноземом Cu по сравнению с серой почвой, что связано, по-видимому, с более высоким содержанием и составом органического вещества, тяжелосуглинистым гранулометрическим составом и нейтральным значением рН чернозема. Методом последовательных селективных экстракций установлено, что в незагрязненных почвах более 50% Cu находится в прочно связанном состоянии. Оценка распределения Cu по фракциям при уровне загрязнения > 200 мг/кг свидетельствует о слабом увеличении содержания биодоступных (обменных и кислоторастворимых) форм металла для чернозема, значительном - для серой почвы при 200 мг/кг. При загрязнении около 2 000 мг/кг Cu в обеих почвах преобладают пулы биодоступных и связанных с (гидр)оксидами Fe и Mn форм. Фактор подвижности не превышает 10% для чернозема и 25% для серой почвы в исходном и загрязненном (200 мг/кг) состояниях, что указывает, соответственно, на малую и среднюю биодоступность Cu в них. При загрязнении в 2 000 мг/кг фактор подвижности достигает 25% в черноземе и более 40% в серой почве, что свидетельствует о среднем и высоком риске миграции Сu в сопредельные среды.
Поглотительная способность почв, ацетаты меди, последовательное экстрагирование, геохимический барьер, фактор подвижности
Короткий адрес: https://sciup.org/143180770
IDR: 143180770 | УДК: 631.412 | DOI: 10.19047/0136-1694-2023-116-76-108
Assessment of the barrier function of chernozem and luvisol under their experimental contamination by copper ions
The aim of the work was to assess the ecological resistance of topsoils of Chernozem and Luvisol to modeled copper contamination. To determine the sorption capacity of soils and to obtain the required levels of contamination the experiment was carried out. Soils were contaminated by the Cu acetate solutions with concentrations from 20 to 200 mg/L, which corresponds to the input of 20-2 000 mg/kg of Cu. Approximation of Cu adsorption isotherms by the Langmuir equation was statistically significant. The obtained values of maximum adsorption (Cmax) and Langmuir constant (KL) for Chernozem were higher than for Luvisol. This indicates a higher adsorption capacity and stronger retention of adsorbed Cu in Chernozem compared with Luvisol. This fact can be explained by the higher content and composition of organic matter, the heavier texture and the neutral pH value of Chernozem. By the method of sequential selective extractions, it was found that in uncontaminated soils, more than 50% of Cu is strongly bounded to silicate fraction (>50%). Assessment of Cu fractionation at different levels of contamination reveals a slight increase in the percentage of Cu bioavailable forms (exchangeable and acid-soluble) in Chernozem at 200 mg/kg and its significant increase in Luvisol at 200 mg/kg. At contamination of about 2 000 mg/kg Cu, both soils are characterised by a predominance of pools of bioavailable and bound to (hydr)oxide of Fe and Mn forms. The mobility factor does not exceed 10% for Chernozem and 25% for Luvisol in the native and contaminated by 200 mg/kg soils, which indicates low and medium bioavailability of Cu in them, respectively. Contamination by 2 000 mg/kg of Cu increased the mobility factor up to 25% in Chernozem and up to 40% in Luvisol, which means the medium and high risk of Cu migration into the adjacent environments.
Текст научной статьи Оценка барьерной функции чернозема и серой почвы в рамках экспериментального загрязнения ионами меди
Поглотительная способность определяет две важнейшие функции почв. С одной стороны, она является геохимическим барьером на пути миграции различных загрязнителей, в том числе тяжелых металлов (ТМ); с другой – ближайшим резервом биодо-ступных макро- и микроэлементов, необходимых для развития растений. Сорбционная способность почв – непостоянная величина. Она зависит от состава и свойств почв: содержания органического вещества (Сорг), доли тонкодисперсных фракций, рН, насыщенности основаниями и прочих. Вместе с тем буферная емкость почв (способность выполнять протекторные функции) ограничена уровнем ее загрязнения ТМ. Она снижается по мере заполнения сорбционных позиций на поверхности почвенных частиц. Тип адсорбции при этом меняется со специфического на неспецифический, что обеспечивает слабую прочность связи адсорбированных катионов с поверхностью и их высокую способность к обмену (Kabala, Singh, 2001; Пинский, 2020; Ладонин, 2016) . Поэтому важно определять те предельные уровни загрязнения, выше которых почва перестает функционировать как защитный барьер.
Многие ТМ относятся к категории микроэлементов, которые необходимы биоте в малых концентрациях, но токсичны в высоких. Медь является биофильным элементом, участвующим в процессах фотосинтеза, дыхания и фиксации азота в растениях, синтеза гемоглобина у животных (Ильин, Сысо, 2001). Ее дефицит в сельскохозяйственных культурах приводит снижению их устойчивости к неблагоприятным внешним условиям, ухудшению свойств семян, снижению объема урожая. В то же время Cu является одним из приоритетных для изучения ТМ (Kabata-Pendias, 2011) и относится к элементам 2 класса опасности, согласно нормативным документам (СанПиН 1.2.3685-21).
Основные источники поступления Cu в почвы – это горнодобывающие, обогатительные и медеплавильные металлургические предприятия (Kabata-Pendias, 2011; Barsova et al., 2019; Бори- сочкина, 2021) . Фоновое содержание меди может варьировать от первых десятков мг/кг в почвах лесостепной зоны (Burachevskaya et al, 2020; Ильин, Сысо, 2001; Борисочкина, 2021; Иовчева и др., 2022) до первых сотен мг/кг в почвах на богатых металлами породах (Narwal et al, 1999; Kabala, Singh, 2001; Kabata-Pendias, 2011; Опекунова и др., 2017; Semenkov, Koroleva, 2020) . При этом содержание меди в загрязненных промышленными предприятиями почвах лесостепной зоны может колебаться от нескольких сотен (Kabala, Singh, 2001; Burachevskaya et al, 2020; Опекунова и др., 2017) до тысяч мг/кг (Tatsiy, 2012; Barsova et al., 2019) . Лимитирующие показатели содержания меди в почвах разных стран в основном варьируют от первых десятков (16 мг/кг; учитывает риск миграции из почвы в грунтовые воды) для ЮАР до первых сотен (100 – 300 мг/кг) в почвах Финляндии, России, Чехии и Нидерландов (Kabata-Pendias, 2011; Barsova et al., 2019; Ильин, Сысо, 2001; Семенков, Королева, 2019) . В некоторых странах, согласно Семенкову, Королевой (2019) , при нормировании учитывается функциональная зона, поэтому лимитирующие показатели содержания Cu могут составлять как первые десятки (Германия, Канада) и сотни (США) мг/кг в почвах селитебных территорий, так и тысячи мг/кг (США, Австралия) в почвах промышленных зон.
Высокая природная вариабельность содержания меди в почвах, часто превышающая как установленные нормативы, так и региональный фон, усложняет оценку экологического состояния конкретного объекта. Кроме того, существующий норматив по содержанию биодоступных форм Cu в почве представлен одной цифрой – 3 мг/кг (СанПиН 1.2.3685-21), в отличие от ОДК, значение которого зависит от рН и гранулометрического состава (СанПиН 1.2.3685-21). Таким образом, норматив по подвижным формам Cu совсем не учитывает разницу в буферности разных почв по отношению к данному металлу (Ладонин, 2016). Предложенная модель зависимости опасности загрязнения почвы от ее буферных свойств (Ильин, Сысо, 2001) до настоящего времени не получила широкого признания. Вклад индивидуальных свойств почв при разработке нормативов содержания в них ТМ и для прогноза экологических рисков можно оценивать количественно, определяя способность почв к удержанию определенной дозы поллютанта (Sipos, 2009). Для этого необходимо накапливать экспериментальные данные по оценке параметров сорбционной емкости почв разных природных зон.
С другой стороны, для оценки устойчивости почвы к загрязнению необходимо также оценивать прочность удерживания ТМ почвенными компонентами, соотношение их мобильных и связанных форм. С этой целью проводят последовательное или параллельное экстрагирование форм ТМ для понимания механизмов образования различных соединений и качественной оценки их мобильности в почве (Tessier et al., 1979; Narwal et al., 1999; Gleyzes et al., 2002; Kabala, Singh, 2001; Ghrefat et al., 2012; Ладонин, 2016) , что позволяет выделить как самые мобильные или “биодо-ступные” формы, которые могут поглощаться растениями и мигрировать в грунтовые воды, так и наиболее прочно связанные формы в составе устойчивых почвенных минералов (Tessier et al., 1979; Burachevskaya et al., 2020; Ладонин, 2016) . Высокая доля “биодоступных” соединений ТМ (извлекаемых нейтральными солями и слабокислотными буферными растворами) свидетельствует об опасности их миграции в сопредельные с почвой среды (Kabala, Singh, 2001; Ghrefat et al., 2012; Barsova et al., 2019; Burachevskaya et al., 2020) .
Из форм, выделяемых в рамках процедур последовательного экстрагирования, к “биодоступным” относят – обменную фракцию и фракцию кислоторастворимых (например, карбонатных) соединений ТМ, которая в том числе может содержать вытесненные из почвы их специфически сорбированные формы (Narwal et al., 1999; Tessier et al., 1979; Gleyzes et al., 2002; Ладонин, 2016). Фракцию водорастворимых соединений металлов иногда выделяют отдельно, однако зачастую объединяют с обменной, так как содержание обеих в фоновых почвах часто около или ниже предела обнаружения (Narwal et al, 1999; Kabala, Singh, 2001; Sipos, 2009). Извлекаемые после кислоторастворимой восстанавливае- мая (ТМ, связанные с (гидр)оксидами Fe и Mn) и окисляемая (ТМ, хемосорбированные органическим веществом, а также их труднорастворимые соли) фракции относительно прочно связаны с почвой, их высвобождение может быть вызвано только кардинальной сменой условий ее функционирования (Tessier et al, 1979; Narwal et al, 1999; Ладонин, 2016). Для форм, связанных с (гидр)оксидами железа и марганца, – это сдвиг рН в сторону сильнокислой реакции или установление восстановительных условий среды на длительное время. Для форм, связанных с органическим веществом, – это минерализация большей части органического вещества (Tessier et al., 1979; Gleyzes et al., 2002).
Стоит отметить, что у всех экстракционных методов есть серьезные ограничения: слабая селективность, перераспределение элементов между фазами в процессе экстракции, разнообразие схем и, как следствие, ограниченная сопоставимость данных, полученных различными исследователями (Narwal et al., 1999; Kabala, Singh, 2001; Ладонин, 2016) . Извлекаемая при экстрагировании фракция в первую очередь определяется свойствами экстрагента, его способностью разрушать те или иные связи между элементом и сорбционной позицией или растворять соли ТМ (Tessier et al., 1979; Narwal et al., 1999; Gleyzes et al., 2002; Burachevskaya et al., 2020; Ладонин, 2016) . Однако многие экстрагенты имитируют состав почвенного раствора или корневых экссудатов растений, следовательно, в той или иной степени позволяют оценить порядки поступления биодоступных форм ТМ из почвы в сопредельные среды. В то же время реактивы, использующиеся для извлечения форм, специфически связанных с (гидр)оксидами Fe, Mn и органическим веществом, крайне отличаются от состава почвенных растворов и грунтовых вод, следовательно, определяют порядки содержания и тип соединений металлов, не представляющих экологического риска в отсутствие выраженного смещения pH и Eh почвы при ее загрязнении ТМ.
Цель данной работы – провести сравнительную оценку устойчивости серой почвы и чернозема квазиглееватого к разным уровням смоделированного в лабораторных условиях загрязнения образцов хорошо растворимыми солями меди.
ОБЪЕКТЫ И МЕТОДЫ
Объекты исследования – гумусовые горизонты (верхние 0– 15 см) серой малогумусированной почвы и чернозема квазиглее-ватого, которые сформировались в пределах лесостепной зоны, в разных климатических и геолого-геоморфологических провинциях. Классификация почв проведена согласно Полевому определителю почв России (2008) .
Образцы серой почвы, сформировавшейся под лесной растительностью, отобраны на территории опытно-полевой станции ИФХиБПП РАН (Пущино), расположенной в пределах Среднерусской возвышенности в зоне умеренного климата. Почвообразующие породы – моренные суглинки. Чернозем квазиглееватый сформировался под разнотравно-злаковой растительностью в пределах лесостепной зоны Барабинской равнины в пределах участка, расположенного в 11 км к западу от города Барабинска, в зоне континентального климата. Почвообразующие породы – озерноаллювиальные суглинки.
Химический анализ основных свойств чернозема проводился в Эколого-геохимическом центре географического факультета МГУ, а серой почвы – в ЦКП ПНЦБИ РАН. Были определены величины pH в почвенной суспензии (соотношение почва : дистиллированная вода как 1 : 2.5) потенциометрическим методом в динамических условиях (приборы: “Эксперт-рН” – Россия и Sartorius – Швейцария). Гранулометрический состав чернозема был установлен методом лазерной дифрактометрии (ЛД) на приборе “Analysette-22 MicroTec plus” (Fritsch, Германия). Гранулометрический состав серой почвы был определен методом седиментации по Горбунову (1971) . Из-за разницы методик почвы могут быть сопоставимы по грансоставу качественно, исходя из полевого описания почв. Определение содержания органического углерода (Cорг) в обеих почвах выполнено согласно методу бихро-матного окисления с титриметрическим окончанием (Walkley, Black, 1934) . Оценка содержания карбонатов (<1%) проведена по отсутствию вскипания в полевых условиях.
В черноземе содержание подвижной формы меди (CuААБ) определено ранее (Иовчева и др., 2022) с использованием ацетат- но-аммонийного буфера (ААБ; pH = 4.8; соотношение почва : раствор – 1 : 5). Общее содержание ТМ с использованием стандартных образцов российских почв измерено рентген-флуоресцентным методом: в черноземе – на анализаторе “Axios” (“PANalytical”, Нидерланды) в ИГЕМ РАН, а в серой почве – на приборе Спектроскан Макс-GV (НПО Спектрон Россия) в ЦКП ПНЦБИ РАН.
В ходе работы проведены эксперименты по сорбции меди образцами исследуемых почв методом серий растворов. Образцы почвы растирали резиновым пестиком и просеивали через сито с диаметром ячеек – 1 мм. Навески серой почвы и чернозема заливали растворами ацетата меди Cu(CH 3 COO) 2 ∙Н 2 О с концентрациями 2, 4, 8, 12, 20, 40, 80, 100, 150 и 200 мг/л (от 0.03 до 3 ммоль/л) при соотношении почва : раствор – 1 : 10, что соответствует концентрации внесенной Cu в интервале 20–2 000 мг/кг. Широкий диапазон вносимых доз элемента позволяет смоделировать переход от допустимых концентраций Cu в нейтральных почвах лесостепи (меньше ОДК = 132 мг/кг) к значениям, характерным для почв, загрязненных промышленными выбросами.
Суспензии встряхивали в течение 4 ч, после чего выдерживали в состоянии покоя в течение 20 ч для достижения равновесия в системе. Затем образцы центрифугировали и фильтровали с помощью вакуумного насоса через мембранный фильтр из ацетата целлюлозы с диаметром пор 45 мкм. Определение содержания Cu в фильтрате (равновесном растворе), проведено методом атомноабсорбционной спектрометрии на приборе “AAnalyst 400” фирмы PerkinElmer (США) в ЦКП ПНЦБИ РАН. В ходе сорбционного эксперимента фиксировали значения рН исходных растворов ацетатов Cu и равновесных растворов потенциометрическим методом (pH-анализатор фирмы Sartorius, Швейцария). Количество поглощенных катионов рассчитано по разности между содержанием Cu в исходном и в равновесном растворах.
Следует отметить, что поглощение катионов почвой возможно не только на поверхности твердофазных частиц (адсорбция), но и в объеме (абсорбция). Однако считается, во-первых, что адсорбционный механизм вносит основной вклад в общий процесс сорбции металлов почвами. Во-вторых, самые известные уравне- ния (Лэнгмюра, Фрейндлиха), описывающие перераспределение ионов между твердой и жидкой фазами почвы, выведены для процессов, происходящих на поверхности твердой фазы (Пинский, 2020). В связи с этим при анализе результатов сорбционного эксперимента авторы далее будут использовать термин “адсорбция”.
Для расчета параметров адсорбции использовали уравнения Лэнгмюра (1) и Фрейндлиха (2):
CCu,ads
K l x Cmax xC cu .
1+KLxCCu ’
где C Cu, ads – количество поглощенных катионов (ммоль/кг), C Cu – концентрация катионов в равновесном растворе (ммоль/л).
В уравнении Лэнгмюра: Cmax – максимальная адсорбция Cu (ммоль/кг) и К L – константа сродства (л/ммоль). Величина C max характеризует наибольшее возможное, но конечное количество обменных позиций на поверхности адсорбента. К L отражает прочность закрепления катионов в почве. В уравнении Фрейндлиха K F характеризует прочность связи сорбтива с сорбентом, а степень 1/n – форму изотермы. Таким образом, уравнение Лэнгмюра подразумевает ограниченность поглощения вещества на поверхности частиц, в то время как уравнение Фрейндлиха описывает безграничную адсорбцию. Если почвы описываются одним типом уравнения, то по сопоставлению значений его параметров можно сравнить их способность к поглощению исследуемого катиона.
Для оценки фракционного состава Cu в исходных и загрязненных 200 и 2 000 мг/кг почвах в трехкратной повторности проведено последовательное экстрагирование в соответствии со схемой Tessier et al. (1979) , одной из наиболее часто применяемых (Kabala, Singh, 2001; Gleyzes et al., 2002; Sipos, 2009; Ghrefat et al., 2012; Burachevskaya et al., 2020; Борисочкина, Колчанова, 2021) . Выделены фракции (табл. 1): F1 – обменная, F2 – кислоторастворимая (извлекает как связанные с карбонатами, так и специфически сорбированные формы; Tessier et al., 1979; Narwal et al., 1999;
Gleyzes et al., 2002) , F3 – связанная с (гидр)оксидами Fe и Mn, F4 – связанная с органическим веществом. Содержание Cu в остаточной фракции ( F5 ) рассчитано как разность между общим содержанием Cu и ее содержанием во фракциях F1 – F4, так как высокая точность определения доли прочносвязанных форм в данном исследовании не требовалась. Для извлечения обменных форм был использован в качестве экстрагента ацетат натрия (NaOAc) с pH = 8 вместо обычно используемого MgCl2. Измерение концентрации Cu в вытяжках также проведено методом атомноабсорбционной спектрометрии в ЦКП ПНЦБИ РАН.
Наиболее простые в применении и активно используемые методы сравнительной оценки биодоступности металлов в почве основаны на учете доли самых легко экстрагируемых фракций (водорастворимой, обменной и кислоторастворимой) с помощью различных экологических индикаторов. К ним относятся анализ значений фактора подвижности – Mobility Factor (MF) (Salbu et al., 1998; Kabala, Singh, 2001) или фактора биодоступности – Bioavailability Factor (BAF), учет рисков с помощью Risk Assessment Code (RAC). MF представляет собой отношение самых подвижных фракций (водорастворимой, обменной и кислоторастворимой) к общей сумме всех фракций, выраженное в процентах (Salbu et al., 1998) . BAF, согласно Kidd et al. (2007) , – аналогичное MF отношение всех форм металла, экстрагируемых 0.11 M CH3COOH (что соответствует сумме F1 и F2, выделяемых по Tessier et al. (1979) согласно Burachevskaya et al. (2020) ), к общему содержанию металла, выраженное в процентах. RAC упоминается в работе Ghrefat et al. (2012) как метод оценки риска транслокации металлов в сопредельные среды в зависимости от доли биодо-ступных фракций от общего содержания (то есть от значений MF или BAF).
В данном исследовании коэффициент MF был подсчитан для исходных образцов, а также для образцов, загрязненных 200 и 2 000 мг/кг. Также была проведена оценка риска транслокации металлов из почв в сопредельные среды с использованием RAC. Согласно RAC, если содержание F1 + F2 ≤ 10%, то экологические риски очень малы.
Таблица 1. Модифицированная cхема Tessier с соавторами (1979) для последовательного фракционирования ТМ
Table 1. Modified scheme of sequential extraction of HM forms based on Tessier et al. (1979) extraction scheme
|
Фракция |
Выделяемые формы |
Соотношение почва : раствор |
Способ определения |
|
F1 |
Обменные (и легкорастворимые) |
1 : 8 |
1М NaCH 3 COO, pH = 8.2; взбалтывание в течение 1 ч при комнатной температуре |
|
F2 |
Кислоторастворимые |
1 : 8 |
1M NaOAc, доведенный до рH = 5.0; взбалтывание в течение 5 ч при комнатной температуре |
|
F3 |
Связанные с (гидр)оксидами Fe и Mn |
1 : 20 |
0.04 M раствор NH 2 OH·HCl в 25%-ой (v/v) CH 3 COOH; нагревание до 96 ± 3 ºС в течение 8 ч при периодическом взбалтывании |
|
F4 |
Связанные с органическим веществом |
1 : 20 |
3 мл 0.02 М HNO3 и 5 мл 30% H2O2, отрегулированной до pH = 2 с помощью HNO3; нагревание до 85 ± 2 °С в течение 2 ч при периодическом перемешивании. Дополнительные 3 мл 30% H2O2 (pH = 2); повторное нагревание до 85 ± 2 °С в течение 3 ч при периодическом перемешивании. После охлаждения – добавление 5 мл 3.2 М NH 4 OAc в 20% (v/v) HNO 3 , разбавление H 2 O до 20 мл и непрерывное перемешивание в течение 30 мин. |
|
F5 |
Прочносвязанные |
1 : 25 |
Содержание в F5 определяли по разности между общим содержанием и содержанием F1 , F2 , F3 , F4 |
Значение MF ≤ 30% отражает средний риск миграции металла в сопредельные среды. Если MF = 31–50%, то, согласно RAC, подвижность металлов в почве достаточно большая, чтобы оценивать риск транслокационного загрязнения как высокий. При MF > 50% вероятность попадания элемента из почвы в пищевые цепи считается крайне высокой (Ghrefat et al., 2012) .
Статистическая обработка результатов и построение изотерм адсорбции проведены в программах Excel 2010 и SigmaPlot 12.5. Значимость регрессионной модели оценена с помощью критерия Фишера и с учетом коэффициента детерминации при уровне значимости α = 0.05. Оценка значимости параметров проводилась с применением критерия Стьюдента при α = 0.05 и α = 0.1.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Основные характеристики гумусовых горизонтов почв представлены в таблице 2. Согласно полевым описаниям оба гумусовых горизонта серой почвы (AY) и чернозема (AU) имеют среднесуглинистый гранулометрический состав. Метод седиментации подтверждает полевое описание для AY. Однако гумусовый горизонт чернозема (AU), скорее, следует отнести к тяжелосуглинистому типу, так как по методу ЛД в нем содержится 51% физической глины. Это значение попадает в отрезок хорошей сопоставимости результатов ЛД и седиментационного методов для степного типа почвообразования, в котором для первого возможно применение градаций классификации Качинского (Юдина и др., 2020) . Содержание карбонатов в обоих образцах невелико, что характерно для промытых гумусовых горизонтов почв лесостепной зоны.
Горизонт AY характеризуется близким к нейтральному рН и низким содержанием Сорг = 1.2%, что может быть связано с эрозионными процессами, окультуриванием почвы и расположением в северной части лесостепной зоны. Горизонт AU характеризуется нейтральной реакцией, содержит около 3% Сорг, при этом обладает хорошей зернисто-комковатой структурой, его общая щелочность не превышает 0.05% (Иовчева и др., 2022). Общее содержание меди в гумусовых горизонтах как чернозема, так и серой почвы, составляет около 17 мг/кг, что не превышает ОДК для суглинистых почв.
Таблица 2. Основные характеристики исследуемых почв
Table 2. Main properties of investigated soils
|
Почва (горизонт) |
рН |
с орг, % |
Физическая глина, % |
CaCO 3 , % |
Cu общ , мг/кг |
CuААБ, мг/кг |
|
Серая (AY) |
5.7 |
1.2 |
35 |
<1% |
17 |
н. д. |
|
Чернозем (AU) |
6.9 |
2.8 |
51 |
17 |
0.1 0.03–0.1 |
Примечание. Над чертой дано среднее арифметическое по 3 повторностям, под чертой – максимум и минимум.
Note. Above the line is mean (n ≥ 3), below the line is maximum and minimum.
Оценка поглотительной способности чернозема и серой почвы по отношению к Cu
В целях оценки устойчивости гумусовых горизонтов исследуемых почв к загрязнению было проведено сравнение способностей серой почвы и чернозема квазиглееватого адсорбировать Cu из растворов ацетатов. Рассчитанные значения параметров уравнений адсорбции Cu черноземом и серой почвой представлены в таблице 3.
Регрессионная модель, описывающая адсорбцию Cu серой почвой с помощью уравнения Лэнгмюра, оценивается как рабочая, а ее параметры определены как значимые (α = 0.05). Несмотря на большую величину ошибки определения параметров (табл. 3), модель адсорбции Cu черноземом на основе уравнения Лэнгмюра и параметр Cmax также признаны значимыми (α = 0.05). Значение параметра K L может быть признано достоверным при α = 0.1. Увеличение количества экспериментальных точек и рабочего диапазона может скорректировать модель адсорбции Cu черноземом и повысить качество аппроксимации.
Таблица 3. Аппроксимация экспериментальных данных уравнениями адсорбции Лэнгмюра и Фрейндлиха
Table 3. Approximation of experimental data by Langmuir and Freundlich adsorption equations
|
Почва |
Параметры уравнений адсорбции |
||
|
Лэнгмюр |
|||
|
max |
K L |
R2 |
|
|
серая |
32.8 ± 1.5 |
17.3 ± 2.1 |
0.99 |
|
чернозем |
56.2 ± 15.5 |
112.6 ± 50.6 |
0.91 |
|
Фрейндлих |
|||
|
K F |
1/n |
R2 |
|
|
серая |
58.7 ± 6.8 |
0.5 |
0.96 |
|
чернозем |
809.4 ± 475.6 |
0.7 |
0.86 |
Уравнение Фрейндлиха хорошо описывает экспериментальные данные, полученные для серой почвы, регрессионная модель и ее параметры значимы при α = 0.05. Аппроксимация данных по адсорбции Cu черноземом показывает значимость регрессионной модели и параметра 1/n при α = 0.05. Значение K F невозможно определить достоверно при выбранных в исследовании уровнях значимости. Из сказанного вытекает, что использование модели Ленгмюра для описания адсорбции Cu исследуемыми почвами является более предпочтительным, поэтому в статье приведена иллюстрация изотерм, описанных этим уравнением (рис. 1).
В соответствии с рисунком 1 изотерма адсорбции Cu серой почвы имеет типичную “ленгмюровскую” форму (Пинский, 2020), то есть близкий к линейному начальный участок, постепенное вы-полаживание кривой в области более высоких концентраций 400– 800 мг/кг (6.3–12.6 ммоль/кг) и стремление к насыщению. Изотерма адсорбции Cu черноземом целиком расположена вблизи оси ординат и имеет слабо выпуклую форму. На ней невозможно выделить область насыщения, что означает, что во всем исследуемом диапазоне концентраций идет интенсивное поглощение Cu. Так при внесении более 400 мг/кг Cu для чернозема доля поглощенного вещества от внесенного составляет более 99%, для серой почвы – снижается от 99 до 92%. Вместе с тем достоверность аппрокси- мации изотермы адсорбции Cu черноземом уравнением Лэнгмюра свидетельствует о вероятном достижении предела насыщения при более высоких уровнях загрязнения.
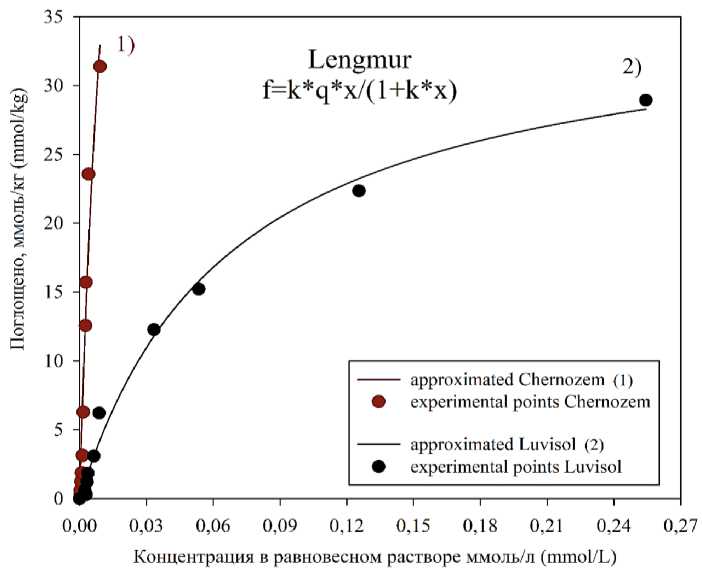
Рис. 1. Изотермы адсорбции Сu черноземом (1) и серой почвой (2).
Fig. 1. Cu adsorbtion isoterms for Chernozem (1) and Luvisol (2).
Аппроксимация полученных в результате эксперимента данных показывает (табл. 3), что у чернозема поглотительная способность по отношению к Cu выше, чем у серой почвы (Сmax., черн. > Сmax., сер.). Прочность удерживания Cu также выше у чернозема (КL, черн. >> КL, сер.; α = 0.1), что может быть связано с особыми свойствами гумусовых соединений в его составе. Известно, что медь характеризуется способностью достаточно прочно связы- ваться органическим веществом почв (Kabata-Pendias, 2011). Таким образом, чернозем демонстрирует более высокую устойчивость, по сравнению с серой почвой, к загрязнению ацетатами Cu, но достоверно определена эта способность лишь для исследованного диапазона вносимых концентраций загрязнителя.
Известно, что адсорбция ТМ почвами часто сопровождается изменением рН суспензий, как в большую, так и в меньшую сторону от исходного рН контактирующего с почвой раствора. Характер изменений определяется кислотно-основной буферностью каждой конкретной почвы, которая зависит от таких свойств как наличие карбонатов, состав органического вещества, ЕКО и пр. Подкисление равновесных растворов связано с десорбцией содержащихся в ППК ионов Н+ (особенно это характерно для функциональных групп Сорг почв) при увеличении концентрации сорбированных ионов ТМ, в данном случае Cu, а также с адсорбцией ионов металлов в сольватной (гидратной) оболочке (Пинский, 1998) . Кроме того, использованный в данном исследовании Cu(CH3COO)2∙Н2О (соль слабой кислоты и слабого основания), подвергается частичному или полному гидролизу, с образованием слабого основания (например, CuOH+) и уксусной кислоты. Поскольку константы нестойкости данного основания много меньше константы ионизации кислоты (pKd 1,осн = 6.0, а pKd кисл = 4.76), то в растворе образуется избыток ионов Н+, который и вызывает подкисление (Лурье, 1989) .
Результаты измерений pН исходных Cu(CH3COO)2∙Н2О и равновесных растворов представлены на рисунке 2, согласно которому при внесении ≥ 400 мг/кг Cu pH фильтратов серой почвы становится меньше, чем рН исходных растворов. Добавление Cu(CH 3 COO) 2 ∙Н 2 О к навескам чернозема квазиглееватого практически во всем диапазоне значений вызывает сдвиг рН в слабощелочную область, только при внесении 2 000 мг/кг Cu рН фильтрата и исходного раствора становятся равны.
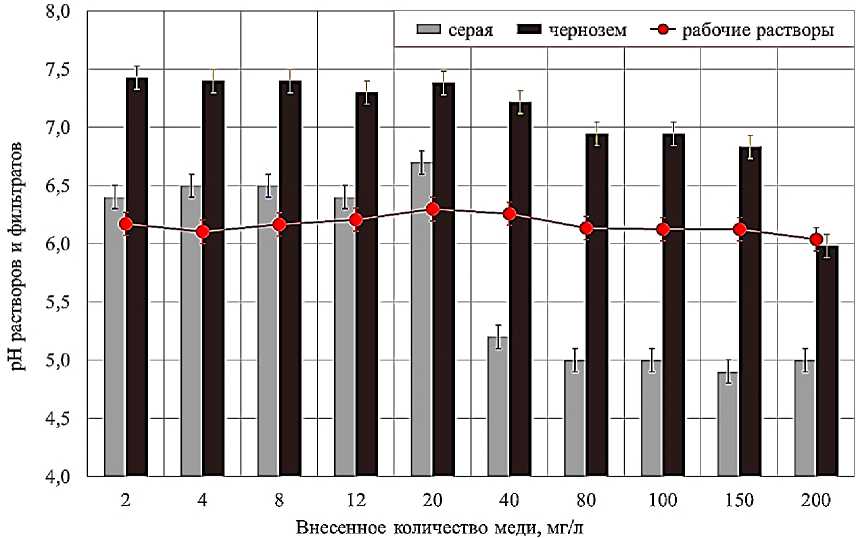
Рис. 2. pH растворов Cu(CH3COO)2∙Н2О разной концентрации и соответствующих им равновесных растворов.
Fig. 2. pH of Cu(CH 3 COO) 2 ∙Н 2 О solutions, being added, and of equilibrium solutions corresponding to them.
Серая почва устойчива к изменению рН лишь при невысоких уровнях загрязнения (≤ 200 мг/кг Cu). При внесении ≥ 400 мг/кг наблюдается подкисление равновесных растворов до pH ≈ 5. Можно предположить, что при таком уровне загрязнения меняется механизм адсорбции катионов. Если Cu сорбируется специфически (с нарушением сольватной оболочки) при внесении 20–200 мг/кг, то “высвободившиеся” в результате гидролиза аце-тат-ионы (и иные десорбированные в равновесный раствор лиганды) связывают H+, поэтому не происходит выраженного падения рН фильтратов (рис. 2). В случае смены механизма адсорбции на неспецифический (в форме сольватных комплексов) при внесении ≥ 400 мг/кг Cu, в равновесном растворе будет увеличиваться концентрация H+ за счет возросшего вытеснения из ППК и более интенсивного гидролиза ацетата Cu. При увеличении вносимой концентрации Cu ≥ 800 мг/кг падение рН фильтрата серой почвы прекращается, что может свидетельствовать об уменьшении количества десорбированных H+ и заполнении обменных позиций, так как стабилизация pH совпадает с началом выполаживания изотермы адсорбции Cu серой почвой.
Оценка изменения рН равновесных растворов показала, что способность к адсорбции Cu у серой почвы значительно ниже, чем у чернозема. Уже при концентрациях ≥ 40 мг/л Cu процессы гидролиза начинают сильно влиять на рН системы в целом (рис. 2). В случае с черноземом, когда более 99% Cu находится в поглощенном состоянии, эти процессы оказывают относительно слабое влияние на систему, но рН фильтратов постепенно снижается до рН рабочих растворов по мере увеличения уровня загрязнения почвы. Таким образом, чернозем проявляет большую буферность к загрязнению растворимыми солями Cu, чем серая почва, что может определяться нейтральным значением рН, более высоким содержанием и иным составом его Сорг, более тяжелым гранулометрическим составом.
Следует отметить, что проведенный эксперимент имеет ограничения, он моделирует поступление в почву Cu в составе легкорастворимых солей, в то время как основная форма поступления ТМ от промышленных предприятий – это твердофазные малорастворимые соединения (Kabata-Pendias, 2011; Ладонин, 2016) .
Однако, во-первых, в естественных условиях происходит медленное растворение вышеуказанных форм с последующим переходом ТМ в почвенный раствор, взаимодействующий с твердой фазой почвы. То есть может происходить вторичная иммобилизация металлов за счет адсорбции. Во-вторых, загрязнение почвы возможно также в результате воздействия сточных вод (Ghrefat et al., 2012) или применения удобрений, содержащих повышенные концентрации ТМ (Kidd et al., 2007) . В этом случае такие потенциально токсичные элементы как Cu могут поступать в почву в растворенном виде и взаимодействовать с лигандами, в том числе ацетатами, в составе почвенного раствора. Кроме того, проведенный эксперимент длился всего несколько дней, в то время как трансформация внесенных в почву малорастворимых соединений ТМ может длиться несколько лет.
Фракционный состав соединений Cu в исходных и загрязненных черноземе и серой почве
Для оценки прочности закрепления Cu в исследуемых почвах было проанализировано соотношение ее подвижных и связанных форм (табл. 4). Следует отметить, что для выделения обменной фракции (F1) Tessier с соавторами (1979) в основном использовали в качестве эктрагента раствор MgCl2. При этом реагент NaOAc c pH = 8.0 также был предложен и опробован авторами методики для извлечения подвижных форм. Предпочтение было отдано MgCl2, так как Tessier с соавторами (1979) считали его менее способным растворять карбонаты и нарушать соотношение обменной (F1) и так называемой карбонатной (F2) форм. Выбор в пользу MgCl2 был принят на основе меньших концентраций Ca, перешедших в вытяжку F2 после использования MgCl2 на первом этапе экстрагирования. Однако, во-первых, большее количество высвобожденного Ca при использовании NaOAc может быть также связано с реакциями комплексообразования, ионного обмена и гидролиза легкорастворимых солей. Во-вторых, Tessier с соавторами (1979) подвергали экстрагированию донные осадки (с содержанием карбонатов около 2%), и уже в последующих исследованиях предложенная схема стала использоваться для анализа почв (Gleyzes et al., 2002). В более поздних работах было показа- но, что однократная вытяжка MgCl2 не экстрагирует полностью всю сумму катионов ППК, способных к обмену (Narwal et al., 1999), поэтому было создано значительное количество модификаций схемы Tessier с соавторами (1979), в которых сильнее всего варьируют экстрагенты для самых подвижных фракций, а выбор исследователей основывается на особенностях исследуемого объекта и задачах исследования (Gleyzes et al., 2002).
В настоящем исследовании сочтено более целесообразным использовать NaOAc c pH = 8.0 для экстракции F1, а затем NaOAc c pH = 5.0 – для F2 ; так как по экстрагирующим свойствам эти реактивы ближе к ААБ с pH = 4.8, который используется в нормировании подвижных форм Cu в России (СанПиН 1.2.3685-21) , а исследуемые образцы практически не содержат карбонатов. При параллельной обработке почвы 1 М NH4Cl, CH3COOH и ААБ с pH = 4.8 Ладониным (2016) было выявлено, что более 80% от суммы обменной (доступной растениям) Cu извлекается ацетат-ионом за счет комплексообразования и лишь около 20% – за счет вытеснения ионом аммония. Основываясь на полученных в исследовании Ладонина (2016) данных, можно предположить, что суммарная концентрация подвижной Cu в вытяжках NaOAc с разным рН ( F1 + F2 ) должна быть близка к ее концентрации в вытяжке ААБ c pH = 4.8.
Суммарная концентрация Cu (0.3 мг/кг) в F1 + F2 чернозема (табл. 4) превышает концентрацию в FААБ (0.1 мг/кг; табл. 2), но при близком порядке значений. Из-за большого разброса значений при концентрации Cu в F1 и F2 , близкой к нижнему пределу обнаружения прибора (0.05 мг/л), различия признаны незначимыми. Руководствуясь вышеупомянутыми доводами и полученными данными о близости значений Cu ААБ и Cu в F1 + F2 , авторы посчитали возможным в данном исследовании сравнить с ПДК Cu суммарное содержание биодоступных форм Cu в черноземе квази-глееватом при разных уровнях загрязнения.
По результатам фракционирования установлено, что максимальная доля Cu в обеих нативных почвах приходится на остаточную фракцию (60% – для серых почв, 80% – для черноземов; табл. 4). Распределение Cu между другими фракциями серой незагрязненной почвы относительно равномерно. По 11–12% приходится на пулы обменных, связанных с (гидр)оксидами Fe и Mn и с органическим веществом форм Cu. Исключение составляет фракция F2, содержание которой практически в два раза меньше, чем F1, F3 и F4. Возможно, это связано с крайне низким содержанием карбонатов или иных связывающих Cu компонентов, которые извлекаются NaOAc с pH = 5.0. В тоже время наибольшая часть обменных форм, по-видимому, извлекается NaOAc с pH = 8.0 за счет комплексообразования.
Содержание относительно непрочно связанных форм ( F1 – F3 ) в нативном черноземе практически на порядок меньше (составляет первые проценты), чем в серой почве, а содержание в остаточной фракции намного больше (80%). Около 17% Cu связано с С орг почвы. Кажущаяся схожей с серой почвой тенденция превышения F1 над F2 в черноземе не может быть достоверно определена. Разброс содержания Cu в F1 и F2 очень высок, а полученные значения зачастую ниже ПО.
Содержание биодоступных форм ( F1 + F2 ) в серой почве составляет 3 мг/кг, в черноземе – менее 0.5 мг/кг. Сумма наиболее подвижных форм в серой почве не превышает 18%, а в черноземе – 2%. Таким образом, способность прочно удерживать Cu у чернозема значительно выше, чем у серой почвы.
Преобладание Cu в составе прочносвязанных (> 60%) форм характерно для нативных или слабо загрязненных черноземов и серых почв, что подтверждается работами Sipos (2009) , Burachevskaya et al. (2020) , Борисочкиной и Колчановой (2021) . Выявление F4 как второго по значимости пула Cu в почвах отмечено для фоновых черноземов миграционно-сегрегационных ( F5Cu = 64%; F4Cu = 19%) в работе Burachevskaya et al., (2020) и для Luvisols ( F5 Cu = 93%; F4 Cu = 6%) с высоким содержанием С орг , согласно Sipos (2009) . Для черноземов глинисто-иллювиальных аг-роселитебных ландшафтов (Борисочкина, Колчанова, 2021) наблюдается сходное с анализируемой серой почвой распределение слабоподвижных форм: на F3 и F4 приходится примерно равная доля содержания Cu (6.2–6.4%). Однако, в отличие от серой почвы, в них ничтожно мала (< 1%) доля обменных форм Cu.
Таблица 4. Фракционный состав Cu в исходных и загрязненных черноземе и серой почве
Table 4. Fractional composition of Cu in native and polluted Chernozem and Luvisol
|
Почва (внесено, мг/кг) |
Общее содержание Cu, мг/кг |
Содержание Cu во фракциях, мг/кг |
||||
|
F1 |
F2 |
F3 |
F4 |
F5 |
||
|
серая (0) |
17 |
2.0 |
1.0 |
2.0 |
1.9 |
10.1 |
|
чернозем (0) |
0.2 |
0.1 |
0.2 |
2.9 |
13.6 |
|
|
0.03–0.4 |
0.03–0.3 |
0.07–0.6 |
2.2–4.1 |
12.8–14.6 |
||
|
серая (200) |
212.9 |
5.7 |
43.8 |
89.1 |
55.6 |
18.71 |
|
чернозем (200) |
216.2 |
1.6 |
4.1 |
50.5 |
99.4 |
60.6 |
|
0.9–2.3 |
3.9–4.2 |
48.7–52.9 |
96.5–101.2 |
57.2–64.4 |
||
|
серая (2000) |
1855.4 |
178.1 |
693.5 |
752.2 |
151.8 |
79.9 |
|
162.6–204.9 |
585.6–761.2 |
733.6–768.3 |
145.6–163.5 |
31.7–144.6 |
||
|
чернозем (2000) |
2011.2 |
69.4 |
507.9 |
853.1 |
405.9 |
175.0 |
|
64.8–73.3 |
485.3–529.6 |
797.7–936.4 |
398.9–416.0 |
112.4–212.2 |
||
Примечание. Над чертой полужирным среднее арифметическое (n ≥ 3), под чертой – максимум и минимум.
Note. Above the line is mean in bold (n ≥ 3), below the line is maximum and minimum.
При внесении 200 мг/кг Cu (рис. 3) в серой почве возрастает до 42% доля связанных с (гидр)оксидами Fe и Mn форм, а кислоторастворимых и связанных с органическим веществом – до 21– 26%. При этом доля Cu в остаточной фракции снижается до 9%. Подобное распределение указывает на уменьшение буферной емкости почвы и риск транслокации Cu в сопредельные среды.
В черноземе при внесении 200 мг/кг почвы снижается до 28% доля прочно связанных с силикатной частью форм Cu. Увеличивается до 46% доля форм, связанных с органическим веществом, и до 23% – с (гидро)оксидами Fe и Mn. Наиболее подвижные ( F1Cu + F2Cu ) формы продолжают составлять первые проценты (рис. 3). Содержание наиболее подвижных форм ( F1 Cu + F2 Cu ) – 5.7 мг/кг (табл. 4) превышает ПДК (3 мг/кг) почти в 2 раза, что указывает на возможный, но слабый риск загрязнения сопредельных сред, учитывая относительно высокую потребность растений в Cu.
Схожее с изучаемым черноземом квазиглееватым распределение слабоподвижных фракций отмечается для чернозема миграционно-сегрегационного, загрязненного ≈ 300 мг/кг Cu (Burachev- skaya et al., 2020) . По сравнению с нативным, в нем ниже доля F5Cu (43% против фоновых 64%), выше доля форм Cu в F4 (29% против 19%) и в F3 (18% против 12%). Однако для загрязненного чернозема миграционно-сегрегационного наблюдается более высокая доля биодоступных форм (10% против фоновых 5%) в сравнении с черноземом квазиглееватым (5% при содержании Cu > 200 мг/кг).
Близкая к чернозему квазиглееватому картина распределения Cu по фракциям наблюдается также в Luvisol (Kabala, Singh, 2001), где для верхнего горизонта почвы (Сорг = 1.5%), подверженного слабому аэрогенному загрязнению (Cu = 96.9 мг/кг), доля Cu в F4 составляет около 50%, а в F5 – 30%. Отличие заключается в выраженной доле F2 (15%) и ничтожной – F3 (около 4%). Также близкие тренды изменения фракционного состава при загрязнении были обнаружены для окультуренной супесчаной Umbrisol с содержанием Сорг > 5% (Kidd et al., 2007), которую удобряли в течение нескольких лет ферментированным осадком сточных вод (содержание Cu в осадке – 230 мг/кг). По сравнению с контролем, в обрабатываемой почве выше общее содержание Cu (132 вместо исходных 12 мг/кг), меньше доля Сu в F5 (45% – окультуренная, 78% – контроль) и выше – в F4 (53% – окультуренная, 15% – контроль).
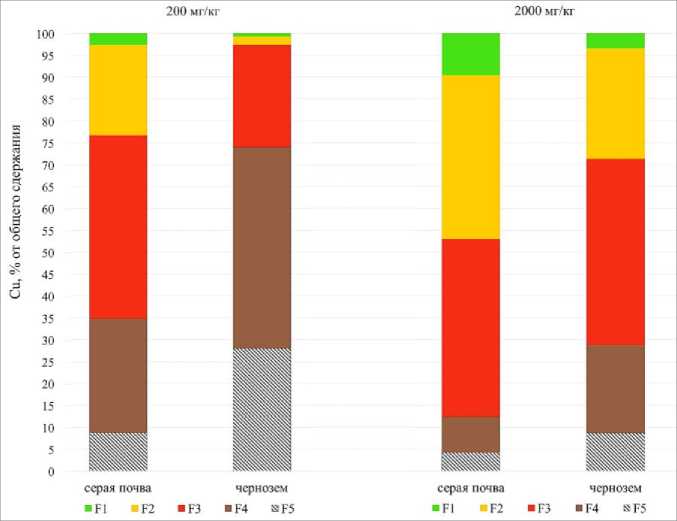
Рис. 3. Долевое распределение Cu (в %) по фракциям в почвах, загрязненных 200 и 2 000 мг/кг.
Fig. 3. Distribution of Cu (%) by fractions in soils contaminated by 200 and 2 000 mg/kg.
При уровне загрязнения в 2 000 мг/кг в обеих почвах доля прочно связанных форм Cu снижается до первых процентов, сильно увеличивается доля кислоторастворимых (≈ 20–35%) и связанных с (гидр)оксидами Fe и Mn (≈ 40%) форм Cu. Доля Cu в F4 снижается до 9% в серой почве и до 20% – в черноземе. Суммарная доля биодоступных форм Cu в обеих почвах составляет > 25%.
Схожее распределение Cu по фракциям отмечено для верхнего горизонта Luvisol с содержанием С орг < 1%, подверженного сильному аэрогенному загрязнению (Cu = 369 мг/кг) (Kabala, Singh, 2001). Доля прочносвязанных форм Cu в нем составляет около 5%, F4 Cu составляет около 17%, F3 Cu – 32%. Сумма биодоступных форм более 40% ( F1 Cu ≈ 16%, F2 Cu – 30%).
На основе абсолютных значений (табл. 4) также можно сделать вывод о том, что обе почвы демонстрируют неспособность прочно удерживать поглощенное количество Cu (сумма F1 Cu + F2Cu составляет десятки и сотни мг/кг) при уровне загрязнения 2 000 мг/кг, следовательно, происходит превышение предела буферной емкости обеих исследованных почв и увеличивается риск миграции поллютанта в другие компоненты ландшафта.
По итогам анализа фракционного состава почв хотелось бы подчеркнуть следующее: 1) основная доля Cu в нативных почвах, по-видимому, находится в форме неизвестных прочносвязанных соединений; 2) с ростом уровня загрязнения увеличивается абсолютное и относительное содержание биодоступных форм Cu, и уменьшается – прочносвязанных. Факт увеличения в первую очередь непрочно связанных ( F1 – F3 ) форм Cu при загрязнении почв ее растворимыми солями объясняется тем, что адсорбция является первым и наиболее быстрым этапом сложного многостадийного процесса трансформации экзогенных соединений ТМ в почвах (Пинский, 2020) . Согласно теоретическим представлениям, общая скорость трансформации определяется наиболее медленной стадией (Пинский, 2020) , следовательно, времени проведенного эксперимента недостаточно для завершения этого процесса и наблюдения последующих этапов.
Оценка экологических рисков и биодоступности Cu
Для серой почвы MF ≈ 18% (табл. 5), что достаточно много для фоновой почвы и указывает на ее невысокую буферную способность в совокупности с возможностью достаточного обеспечения растений Cu за счет средней биодоступности. Фактор подвижности Cu в черноземе составляет 1.6%. Это очень низкое значение, указывающее на ограничение доступности металла растениям и отсутствие риска транслокационного переноса. Получен- ный для чернозема результат согласуется с оценкой подвижности Cu (MF < 2%) для фоновых Luvisols (Sipos, 2009). Оба полученных значения MF согласуются с выводами других исследователей о том, что суммарная доля Cu в F1 и F2 в фоновых почвах составляет 10–20% или меньше (Narwal et al., 1999; Kabala, Singh, 2001; Kidd et al., 2007; Sipos, 2009).
Таблица 5. MF рассчитанный для нативных и загрязненных почв.
Table 5. MF calculated for native and contaminated soils
|
Почва |
Величина MF* в исследуемых почвах, % |
||
|
Незагрязненные |
Внесено 200 мг/кг |
Внесено 2 000 мг/кг |
|
|
серая |
17.9 |
23.3 |
47.0 |
|
чернозем |
1.6 |
2.6 |
28.7 |
Примечание. *MF – mobility factor (фактор подвижности). Note. *MF – mobility factor.
MF для серой почвы при общем Cu > 200 мг/кг составляет 23%, следовательно опасность транслокации подвижных форм элемента в сопряженные с почвой среды оценивается как средняя, согласно RAC ( F1Cu + F2Cu > 10% ), при этом суммарное абсолютное содержание F1 и F2 в серой почве при уровне загрязнения > 200 мг/кг составляет около 50 мг/кг. Подобные значения MF > 20% могут наблюдаться как в фоновых, так и в загрязненных почвах (Kabala, Singh, 2001; Ghrefat et al., 2012) . Для чернозема MF = 2.6%, что указывает на низкую биодоступность Cu и, согласно RAC, на слабую опасность миграции элемента в сопредельные среды. Низкая биодоступность Cu (BAF = MF < 5%) при общем содержании более 130 мг/кг отмечена в работе Kidd et al. (2007) для окультуренной супесчаной Umbrisol.
Фактор подвижности Cu при загрязнении в 2 000 мг/кг для чернозема составляет > 25%, а для серой > 45%. Таким образом, согласно RAC, для чернозема наблюдается средний риск миграции подвижных форм Cu в грунтовые воды и передвижения по пищевым цепям, а для серой почвы ‒ высокий (Ghrefat et al.,
2012) . Значения MF выше 30% для загрязненных почв получены в исследовании Kabala, Singh (2001) .
ВЫВОДЫ
Результаты эксперимента по адсорбции меди серой почвой и черноземом квазиглеевым достоверно аппроксимируются уравнением Лэнгмюра. Экспериментально подтверждена более высокая адсорбционная емкость чернозема по сравнению с серой почвой. Прочность удержания форм Cu, вероятно, также выше в черноземе (если допустить значимость KL при α = 0.1). Лучшая адсорбция Cu черноземом, по сравнению с серой почвой, определяется, по-видимому, нейтральным значением рН, более высоким содержанием и иным составом С орг , тяжелосуглинистым гранулометрическим составом.
В результате последовательного экстрагирования выявлено, что в нативных почвах основная доля Cu находится в прочно связанном состоянии (> 50%). В черноземе также значительна доля Cu, связанной с Сорг (17%), что подтверждает его важную роль в механизмах иммобилизации данного элемента. При возрастании уровня загрязнения в обеих почвах уменьшается доля прочносвязанных форм Cu. При уровне загрязнения в 200 мг/кг в черноземе увеличивается доля Cu во фракции органического вещества (до 46%), а в серой почве до 42% – связанной с (гидро)оксидами Fe, Mn, и до 21–26% – в кислоторастворимой и связанной с органическим веществом фракциях. При внесении 2 000 мг/кг в обеих почвах значительно увеличивается доля и абсолютное содержание кислоторастворимых и связанных с (гидр)оксидами Fe, Mn форм Cu, нарушаются барьерные функции.
MF ≤ 25% для обеих почв в исходном и загрязненном 200 мг/кг состояниях, что указывает на малый и средний риск увеличения биодоступности Cu. При загрязнении около 2 000 мг/кг MF > 25%, что означает средний для чернозема и высокий для серой почвы риск миграции Сu в грунтовые воды и по пищевым цепям.
Список литературы Оценка барьерной функции чернозема и серой почвы в рамках экспериментального загрязнения ионами меди
- Борисочкина Т.И., Колчанова К.А. Геохимия тяжелых металлов почв урбанизированных ландшафтов зон воздействия металлургических предприятий. // Экология и промышленность России. 2021. Т. 25. № 10. С. 50-56.
- Горбунов Н.И. Методика подготовки почв к минералогическим анализам. // Методы минералогического и микроморфологического изучения почв. М.: Наука, 1971. С. 5-15.
- Ильин В.Б. Сысо А.И. Микроэлементы и тяжелые металлы в почвах и растениях Новосибирской области. Новосибирск: Издательство СО РАН, 2001. 229 с.
- Иовчева А.Д., Кречетов П.П., Семенков И.Н. Засоление как фактор дифференциации подвижных форм тяжелых металлов в почвах Барабинской лесостепи // Вестник Московского университета. 2022. Серия 5. География. № 3. С. 108-118.
- Ладонин Д.В. Формы соединений тяжелых металлов в техногенно-загрязненных почвах: Автореф. дис. … докт. биол. наук. М., 2016. 42 с.
- Лурье Ю.Ю. Справочник по аналитической химии. М.: Химия, 1989. 448 с.
- Опекунова М.Г., Сомов В.В., Папян Э.Э. Загрязнение почв в районе воздействия горнорудных предприятий Башкирского Зауралья // Почвоведение. 2017. № 6. С. 744-758.
- Пинский Д.Л. К вопросу о механизмах ионообменой адсорбции тяжелых металлов почвами // Почвоведение. 1998. № 11. С. 1348-1355.
- Пинский Д.Л. Современные представления о механизмах поглощения тяжелых металлов почвами // Эволюция, функционирование и экологическая роль почв как компонента биосферы. Пущино: Товарищество научных изданий КМК, 2020. С. 55-64.
- Полевой определитель почв России. М.: Почвенный ин-т им. В.В. Докучаева, 2008. 182 с.
- СанПиН 1.2.3685-21. “Гигиенические нормативы и требования к обеспечению безопасности и (или) безвредности для человека факторов среды обитания”. 2021. 469 c.
- Семенков И.Н., Королева Т.В. Международные системы нормирования содержания химических элементов в почвах: принципы и методы (обзор) // Почвоведение. 2019. № 10. С. 1259-1268.
- Юдина А.В., Фомин Д.С., Валдес-Коровкинa И.А, Чурилинa Н.А., Александрова М.С., Головлева Ю.А., Филиппов Н.В., Ковда И.В., Дымов А.А., Милановский Е.Ю. Пути создания классификации почв по гранулометрическому составу на основе метода лазерной дифракции // Почвоведение. 2020. № 11. С. 1353-1371.
- Barsova N., Yakimenko O., Tolpeshta I., Motuzova G. Current state and dynamics of heavy metal soil pollution in Russian Federation - A review // Environmental Pollution. 2019. Vol. 249. P. 200-207. https://doi.org/10.1016/j.envpol.2019.03.020.
- Burachevskaya M., Minkina T., Bauer T., Mandzhieva S., Gülser C., Kızılkaya R., Sushkova S., Rajput V. Assessment of extraction methods for studying the fractional composition of Cu and Zn in uncontaminated and contaminated soils // Eurasian Journal of Soil Science. 2020. Vol. 9. Iss. 3. P. 231-241. https://doi.org/10.18393/ejss.734601.
- Ghrefat H.A., Yusuf N., Jamarh A., Nazzal J. Fractionation and Risk Assessment of Heavy Metals in Soil Samples Collected along Zerqa River, Jordan // Environ. Earth Sci. 2012. Vol. 66. P. 199-208. https://doi.org/10.1016/j.envpol.2019.03.020.
- Gleyzes C., Tellier S., Astruc M. Fractionation studies of trace elements in contaminated soils and sediments: a review of sequential extraction procedures // Trends Anal. Chem. 2002. Vol. 21. P. 451-467. https://doi.org/10.1016/S0165-9936(02)00603-9.
- Kabala C., Singh B.R. Fractionation and mobility of copper, lead, and zinc in soil profiles in the vicinity of a copper smelter // Journal of Environmental Quality. 2001. Vol. 30. P. 485-492. https://doi.org/10.2134/jeq2001.302485x.
- Kabata-Pendias A. Trace Elements in soils and plants. Y.: CRC Press, 2011. 505 p.
- Kidd P.S., Domínguez-Rodríguez M.J., Díez J., Monterroso C. Bioavailability and plant accumulation of heavy metals and phosphorus in agricultural soils amended by long-term application of sewage sludge // Chemosphere. 2007. Vol. 66. P. 1458-1467. https://doi.org/10.1016/j.chemosphere.2006.09.007.
- Narwal R.P., Singh B.R., Salbu B. Association of cadmium, zinc, copper, and nickel with components in naturally heavy metal‐rich soils studied by parallel and sequential extractions // Communications in Soil Science and Plant Analysis. 1999. Vol. 30. Iss. 7-8. P. 1209-1230. https://doi.org/10.1080/00103629909370279.
- Salbu B., Krekling T., Oughton D.H. Characterization of radioactive particles in the environment // Analyst. 1998. Vol. 123. P. 843-849. https://doi.org/10.1039/A800314I.
- Sipos P. Distribution and sorption of potentially toxic metals in four forest soils from Hungary // Cent. Eur. J. Geoscience. 2009. Vol. 1. Iss. 2. P. 183-192. https://doi.org/10.2478/v10085-009-0009-4.
- Semenkov I.N., Koroleva T.V. Heavy metals content in soils of Western Siberia in relation to international soil quality standards // Geoderma regional. 2020. Vol. 21. P. e00283. https://doi.org/10.1016/j.geodrs.2020.e00283.
- Tatsiy Yu.G. Ecological and Geochemical Evaluation of Environmental Pollution within the Operating Area of the Karabash Copper-Smelting Plant // Tyumen State University Herald. 2012. Vol. 12. P. 81-86.
- Tessier A., Campbell P.G.C., Bisson M. Sequential extraction procedure for the speciation of particulate trace metals // Anal. Chem. 1979. Vol 51. P. 844-851. https://doi.org/10.1021/ac50043a017.
- Walkley A., Black I.A. An examination of the Degtjareff method for determining soil organic matter and a proposed modification of the chromic acid titration method // Soil Sci. Journal. 1934. Vol. 27. P. 29-37. https://doi.org/10.1097/00010694-193401000-00003.


