Оценка детоксицирующей эффективности экстракта сапропеля при интоксикации птиц Конфидором Экстра
Автор: Бойко Т.В., Насырова И.А., Гонохова М.Н., Водолага В.С.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Сельскохозяйственные науки
Статья в выпуске: 6, 2017 года.
Бесплатный доступ
В статье дана оценка детоксицирующей эффективности экстракта сапропеля при отравлении птиц Конфидором Экстра® (КфЭ). Исследования проведены на пятисуточных петушках породы белый леггорн, подобранных по приниципу аналогов и разделенных на че-тыре группы по пять голов в каждой. Цыпля-та первой группы находились на стандартном рационе и потребляли воду водопроводную. Вторая группа цыплят с водой ежедневно в течение 14 дней потребляла экстракт сапро-пеля масляный в дозе 1 мл на 100 мл воды. Цыплята третьей группы получали водный 0,001%-й раствор КфЭ. Птицы четвертой группы на фоне интоксикации КфЭ получали ежедневно экстракт сапропеля масляный в дозе 1 мл на 100 мл воды. Через 14 суток про-водили убой животных. В результате прове- денных исследований было установлено, что общее состояние цыплят на протяжении все-го периода наблюдения было удовлетвори-тельным, несмотря на периодически реги-струемую диарею у птиц, получавших пести-цид и лекарственное средство. При анализе биохимических показателей крови было уста-новлено снижение концентрации мочевой кис-лоты на 18,5 % (р=0,009) у цыплят, потреб-лявших в течение двух недель раствор сапро-пеля масляный, и повышение данного показа-теля у цыплят, интоксицированных КфЭ, на 29,5 % (р
Экстракт сапропеля масляный, конфидор экстра, детоксикация, кonfidor eхtra®
Короткий адрес: https://sciup.org/14084929
IDR: 14084929 | УДК: 619:615
The assessment of sapropel extract detoxifying efficiency at Кonfidor Eхtra® intoxication in poultry
In the study the assessment of sapropel extract detoxification potency in the case of poultry poison-ing with Кonfidor Eхtra® (KFE) is given. The re-searches have been conducted on five-day White Leghorn cockerels matched on the analogue prin-ciple and divided into four groups of five specimens in each. The chickens of the first group were fed a standard diet and consumed tapwater. The second group of chickens consumed water with sapropel oil extract in the dose of 1 ml per 100 ml of water with-in 14 days. The chickens of the third group received 0.001 % aqueous KFE-solution. The specimens of the fourth group on the background of KFE intoxi-cation received daily sapropel oil extract at the dose of 1 ml per 100 ml of water. In 14 days the animals were slaughtered. As a result of studies it was found out that general condition of chickens during the observation period was satisfactory de-spite occasional diarrhea in the specimens who received pesticide and medicine. The analysis of blood biochemical parameters has shown the re-duction of uric acid concentration by 18.5 % (р=0.009) well as an increase in this indicator by 29.5 % (p
Текст научной статьи Оценка детоксицирующей эффективности экстракта сапропеля при интоксикации птиц Конфидором Экстра
Введение. Важной частью эффективного ведения сельского хозяйства является химический метод контроля численности вредителей. Современный рынок инсектицидов, применяемых в растениеводстве, ветеринарии, медицине и быту, представлен преимущественно фосфорорганическими соединениями, синтетическими пиретроидами, авермектинами и неоникотинои-дами. Неоникотиноиды (НН) – интенсивно развивающийся класс инсектицидов, акарицидов и фунгицидов, широко используемых в растениеводстве на посевах зерновых, плодовых и овощных культур. Одним из первых представителей этого класса является имидаклоприд (Ик), препараты на основе которого успешно применяют в растениеводстве и в быту для борьбы с муравьями и термитами, в ветеринарной медицине – против экто- и эндопаразитов, а в животноводстве – для обработки помещений [1, 2]. В токсикологическом отношении НН являются нейротропными ядами, механизм действия которых основан на взаимодействии с никотиновыми ацетилхолиновыми рецепторами постсинаптических мембран, что приводит к нарушению проведения нервного импульса и гибели насекомых. Обладая высокой липофильностью, НН легко проникают через биологические мембраны и временно депонируются в органах и тканях организма [3, 4].
Несмотря на то, что пестициды являются необходимым инструментом обеспечения эффективности проводимых мероприятий по борьбе с вредителями и возбудителями болезней, попадая в организм животных и человека в виде остаточных количеств с кормами или продуктами питания, водой, воздухом, а также через кожу при обработках, они неизбежно оказывают влияние на организм. Высокая контаминация кормов ксенобиотиками различного происхождения является основной причиной включения в рационы для животных средств с детоксицирующей активностью. Наряду с широким использованием углеродных сорбентов перспективным направлением в ветеринарной медицине является изучение детоксицирующей активности препаратов на основе сапропеля [5]. Экспериментально подтверждено, что продукты, получаемые из сапропеля, обладают антиоксидантным, антисептическим, гепатопротекторным и иммуномодулирующим эффектом, что послужило теоретической предпосылкой для проведения данных исследований.
Цель исследования. Определение детоксицирующей активности экстракта сапропеля при интоксикации птиц Конфидором Экстра®.
Объекты, материалы и методы исследования. Петушки пятисуточного возраста породы белый леггорн, массой 40,0 г; экстракт сапропеля масляный (ЭСМ); инсектицидный препарат Конфидор Экстра® (имидаклоприд, 70%. Bayer-CropScience, Германия). Методы – клинические, гематологические, гистологические, статистические. ЭСМ изготовлен на кафедре фармацевтической технологии, биотехнологии ФГБОУ ВПО «ОмГМУ» методом двухфазной экстракции [6]. Исследования на петушках проведены в виварии Института ветеринарной медицины и биотехнологии ФГБОУ ВО «Омский ГАУ». Содержание и уход за ними осуществляли в соответствии с требованиями по надлежащей практике при работе с лабораторными животными [7]. Для проведения эксперимента птиц разделили на четыре группы по пять голов в каждой. Цыплята первой группы (контроль 1) находились на стандартном рационе для молодняка птиц, поение осуществляли из автоматических поилок водопроводной водой. Второй группе цыплят (контроль 2) в воду ежедневно в течение 14 дней вносили ЭСМ в дозе 1 мл на 100 мл воды. Цыплята третьей группы (контроль 3) получали водный 0,001%-й раствор КфЭ весь период наблюдения. Птицам четвертой группы (опыт) на фоне интоксикации КфЭ ежедневно с водой выпаивали ЭСМ в дозе 1 мл на 100 мл воды. Оценку детоксицирующей активности ЭСМ проводили с учетом клинического статуса животных, показателей живой массы, реакции биохимических маркеров сыворотки крови, гистологической картины печени. Биохимические показатели определяли в химико-токсикологическом отделе Омской областной ветеринарной лаборатории на биохимическом анализаторе-автомате «Konelab20», используя реагенты фирмы Human (Германия) и Sentinel (Италия). Кусочки печени фиксировали в 4%-м нейтральном растворе формальдегида, обезвоживали в спиртах восходящей концентрации и заливали в парафин. Парафиновые срезы толщиной 3–5 мкм получали на ротационном микротоме LaboCut 4055 (фирма Slee, Германия), окрашивали гематоксилином и эозином. Микрофотосъемку гистологических препаратов проводили на микроскопе Альтами БИО 1Т с цифровой окулярной камерой UCMOS0300KPA. Статистический анализ цифровых данных проводили с помощью пакета прикладных статистических программ Statistica 6.0. Сравнение медиан про- водили используя U-критерий Mannа-Whitney. Различия считали значимыми при p<0,05.
Результаты исследования и их обсуждение. Общее состояние птиц контрольных и опытной групп на протяжении всего периода наблюдения было удовлетворительным. У птиц контрольной группы 1 помет был сформирован, темно-коричневого цвета, моча была белого цвета, вязкой консистенции, у цыплят остальных групп отмечали полужидкий помет от темно-коричневого до черного цвета, моча была без видимых изменений. Состояние перьевого покрова у цыплят всех групп было удовлетворительным. Через неделю во всех контрольных группах наблюдали прирост массы тела, причем наибольшее значение данный показатель отмечали у цыплят второй группы, в воду которым добавляли ЭСМ (р<0,05). Через две недели медианы массы тела цыплят во всех группах имели одинаковое значение, за исключением животных третьей контрольной группы, которые весь период наблюдения получали 0,001%-й раствор КфЭ – у них отмечали снижение массы тела на 4 % (р<0,05).
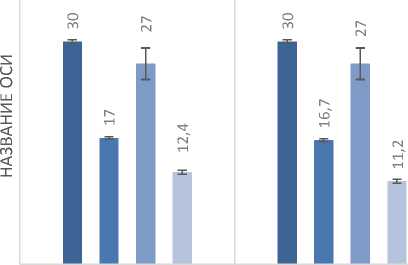
При анализе биохимических показателей сыворотки крови было установлено снижение концентрации мочевой кислоты на 18,5 % (р=0,009) у цыплят, потреблявших в течение двух недель ЭСМ в дозе 1 мл/100 мл воды, повышение концентрации мочевой кислоты у цыплят, получавших 0,001%-й раствор КфЭ в течение всего периода наблюдения, на 29,5 % (р<0,05), в общий белок (г/л) альбумин (г/л)
ГРУППА № 1 ГРУППА № 2
опытной группе (КфЭ+ЭСМ) регистрировали повышение данного показателя на 56 % (р<0,05) по сравнению с группой контроля 1.
Известно, что мочевая кислота является конечным продуктом пуринового и белкового обмена. Снижение данного показателя во второй контрольной группе могло быть обусловлено развитием гидропической дистрофии в печени птиц, признаки которой регистрировали гистологическими методами. Повышение данного показателя у птиц третьей контрольной и опытной групп, интоксицированных КфЭ, свидетельствует о развитии у них признаков мочекислого диатеза, что может быть следствием нефротоксического эффекта пестицида. При этом важно отметить, что экстракт сапропеля, вводимый в организм птиц на фоне интоксикации неонико-тиноидом, способствует более интенсивному накоплению мочевой кислоты в организме птиц, что в прогностическом отношении следует рассматривать как неблагоприятный фактор.
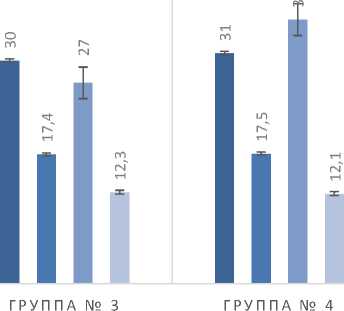
При анализе некоторых других биохимических показателей сыворотки крови птиц контрольных и опытной групп существенных отклонений не регистрировали (рис. 1). Следует отметить повышение концентрации креатинина у цыплят опытной группы на 18,3 % (р<0,05) по сравнению с группой контроля 1, что может указывать на развитие нефропатии, обусловленной в том числе высокой концентрацией мочевой кислоты в организме.
группы
Рис. 1. Медианы биохимических показателей сыворотки крови птиц: 1-я группа - контроль 1 (вода водопроводная); 2-я группа - контроль 2 (ЭСМ); 3-я группа - контроль 3 (0,001%-й раствор Конфидора Экстра ® ); 4-я группа - опыт (0,001%-й раствор Конфидора Экстра ® + ЭСМ)
креатинин(мкмоль/л) глюкоза(ммоль/л)
При патолого-анатомическом вскрытии птиц контрольных и опытной групп отмечали однотипную картину, при этом макроскопических изменений во внутренних органах отмечено не было. При анализе гистологической картины печени птиц контрольной группы 1 гепатоциты имели полигональную форму, цитоплазма однородная, оксифильно окрашена, ядро округлой формы, окрашено базофильно, в нем опреде- лялись одно или два ядрышка. Встречались двуядерные гепатоциты. Синусоидные капилляры расширены умеренно и содержали эритроциты, повреждений эндотелия не было зафиксировано (рис. 2). Междольковая соединительная ткань слаборазвита. Регистрировали небольшие скопления клеток лимфоидного ряда вокруг центральной вены.
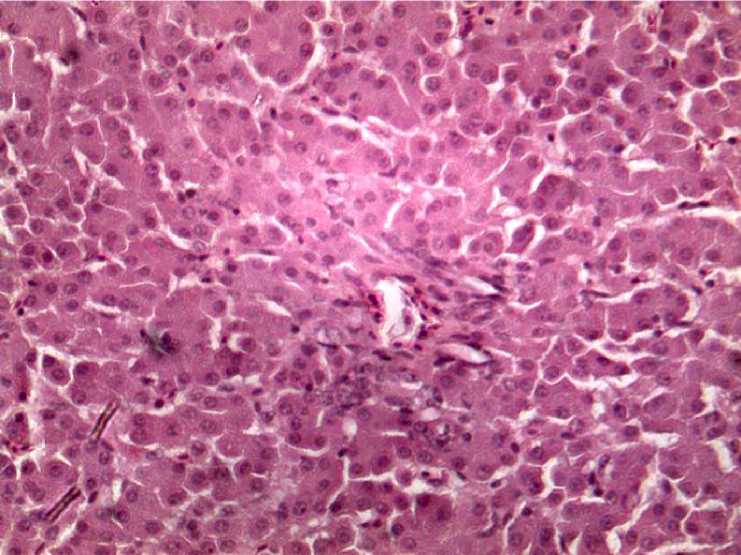
Рис. 2. Печень птиц контрольной группы 1. Гематоксилин и эозин, ×150
В печени птиц контрольной группы 2 гепатоциты находились в состоянии гидропической дистрофии – увеличены в объеме, цитоплазма их заполнена вакуолями, ядра, как правило, смещены на периферию, иногда с признаками вакуолизации (рис. 3). Синусоидные капилляры были расширены. Разрастание междольковой соединительной ткани не регистрировали, скопление лимфоидных клеток в печеночных дольках встречали редко.
Гистологическая картина печени цыплят контрольной группы 3 характеризовалась расширением синусоидных капилляров. Цитоплазма большинства клеток была оксифильно окрашена, ядра клеток были просветленные, содержали несколько ядрышек. Дистрофические изменения в гепатоцитах регистрировали редко (рис. 4). Небольшие скопления клеток лимфоидного ряда обнаруживали вокруг центральной вены.
В печени птиц опытной группы регистрировали гепатоциты в состоянии дистрофии, некробиоза и некроза, при этом ядра клеток отсутствовали или находились в состоянии пикно-за (рис. 5). Границы между клетками не дифференцировались.
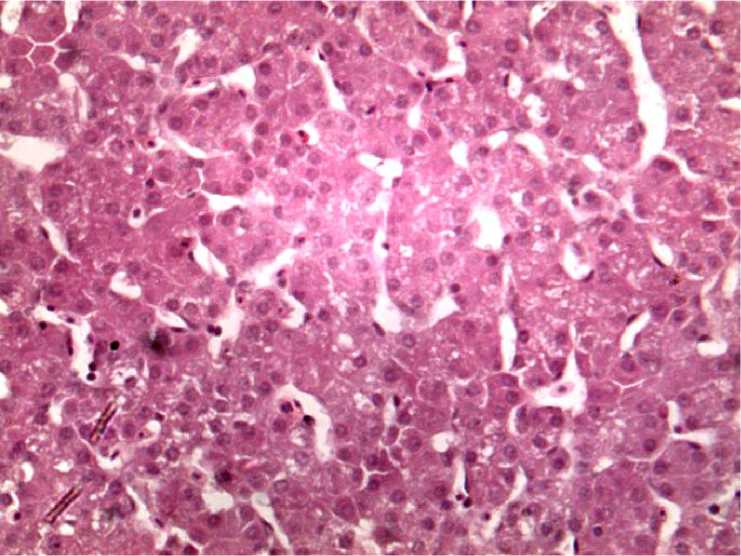
Рис. 3. Печень птиц контрольной группы 2. Расширение синусоидных капилляров, гидропическая дистрофия гепатоцитов. Гематоксилин и эозин, ×150
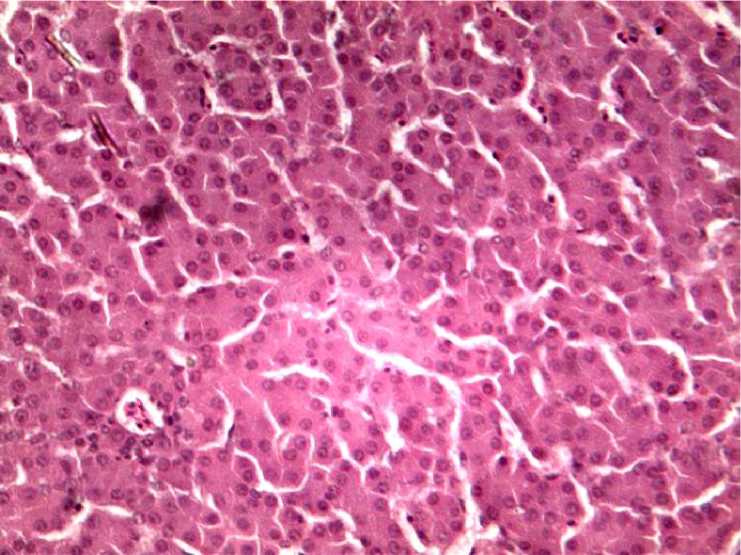
Рис. 4. Печень птиц контрольной группы 3. Расширение синусоидных капилляров. Гематоксилин и эозин, ×150
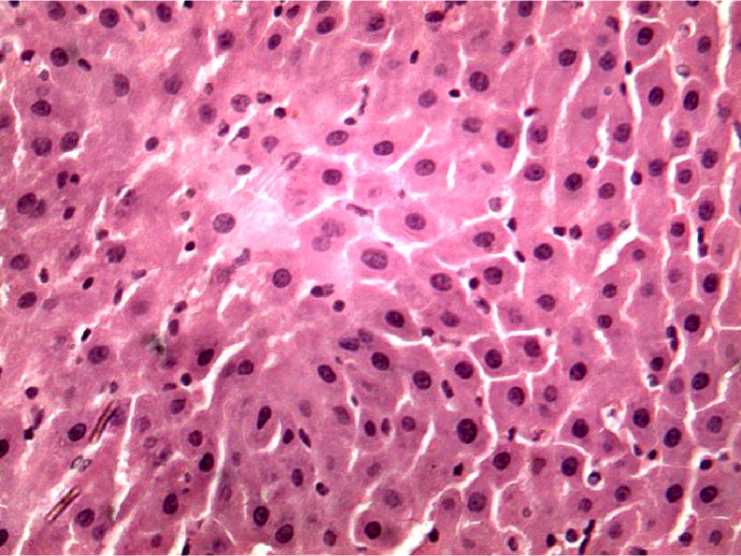
Рис. 5. Печень птиц опытной группы. Участки гепатоцитов в состоянии дистрофии, некроза и некробиоза. Гематоксилин и эозин, ×300
Регистрировали единичные двуядерные гепатоциты. Скопление мононуклеарных клеток обнаруживали на периферии печеночной дольки. Синусоидные капилляры умеренно расширены и заполнены кровью.
Выводы. Ежедневное поение цыплят 0,001%-м раствором КфЭ в течение двух недель способствует снижению массы их тела на 4 %, повышению уровня мочевой кислоты на 29,5 %. Гистологическая картина печени характеризуется преимущественно расширением синусоидных капилляров.
Ежедневное выпаивание цыплятам в течение 14 дней ЭСМ в дозе 1 мл на 100 мл воды способствует снижению мочевой кислоты на 18,5 %; гистологическая картина печени характеризуется признаками гидропической дистрофии.
На фоне интоксикации КфЭ ежедневное выпаивание ЭСМ в дозе 1 мл на 100 мл воды способствует увеличению уровня мочевой кислоты (на 56%) и креатинина (на 18,3%), что может быть обусловлено нарушением выделительной функции почек. Гистологические изменения в печени свидетельствуют о развитии дистрофических, некробиотических и некротических процессов в органе.
Таким образом, результаты проведенных исследований указывают на отсутствие детоксицирующего эффекта ЭСМ в дозе 1 мл на 100 мл воды на фоне интоксикации птиц КфЭ. Напротив, регистрируемые отклонения биохимических показателей сыворотки крови и структурные изменения в печени свидетельствуют о развитии гепато- и нефропатии у экспериментальных животных.
Список литературы Оценка детоксицирующей эффективности экстракта сапропеля при интоксикации птиц Конфидором Экстра
- Захаренко В.А. Пестициды в аграрном сек-торе России конца ХХ -начала ХХI века//Агрохимия. -2008. -№ 11. -С. 86-96.
- Лопатина Ю.В., Еремина О.Ю. Примене-ние инсектицидов группы неоникотиноидов в ветеринарии//С.-х. биология. Сер. «Био-логия животных». -2005. -№ 6. -С. 14-24.
- Токсикологическая характеристика неони-котиноидов/Т.В. Бойко, Л.К. Герунова, В.И. Герунов //Вестник Омск. гос. аграр. ун-та. -2015. -№ 4 (20). -С. 49-54.
- Бойко Т.В. Токсикокинетические особенно-сти неоникотиноида Конфидора Экстра® в организме крыс//Вестник НГАУ. -2013. -№ 1 (26). -С. 74-79.
- Применение сапропеля и продуктов его переработки в ветеринарии/В.И. Зайнчковский, В.Д. Конвай, Е.И. Войщатынский //Сапропель и продукты его перера-ботки: мат-лы Междунар. науч.-практ. конф. -Омск: Изд-во ОМГАУ, 2008. -С. 44-45.
- Насырова И.А. Разработка малоотходной технологии лекарственных и парафарма-цевтических средств на базе сапропелей Омского Прииртышья//Фармация Казах-стана: интеграция науки, образования и производства: мат-лы Междунар. науч.-практ. конф. -Шымкент, 2009. -Т. 2. -С. 68-73.
- ГОСТ 33215-2014. Руководство по содер-жанию и уходу за лабораторными живот-ными. Правила оборудования помещений и организации процедур. -URL: www.internet-law.ru/gosts/gost/61242/. Literatura


