Оценка интраоперационного метаболизма миокарда у детей первого года жизни при коррекции врожденных пороков сердца в условиях искусственного кровообращения
Автор: Углова Елена Владимировна, Князькова Любовь Георгиевна, Ломиворотов Владимир Николаевич, Горбатых Юрий Николаевич, Синельников Юрий Семенович, Шунькин Анатолий Васильевич, Афанасьев Иван Сергеевич, Корнилов Игорь Анатольевич
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Врожденные пороки сердца
Статья в выпуске: 3 т.13, 2009 года.
Бесплатный доступ
Изучены некоторые особенности метаболизма миокарда у 40 детей раннего возраста с ИБС, оперированных в условиях искусственного кровообращения с применением кристаллоидной фармакологической/химической кардиоплегии (ФХК) (11 больных), кровяной кардиоплегии (14 больных) и раствора «Кустодиол» (15 больных). Проведена комплексная оценка интраоперационного содержания глюкозы, лактата, пирувата, свободных жирных кислот (СЖК), неорганического фосфора (НФ) в образцах артериальной крови и крови коронарного синуса. Выявлено, что динамика изучаемых биохимических показателей при сравнении показателей артериальной и венозной (коронарный синус) крови носила однонаправленный характер. Статистических различий этих показателей у больных с ацианотическим и синим пороками сердца не наблюдалось. Несмотря на применение средств кардиопротекции, выявлены утилизация глюкозы и некоторые признаки гипоксии миокарда за счет лактата и пирувата в крови коронарного синуса при одновременном повышении этих сред в артериальной крови. При анализе продукции/экстракции энергетических сред установлено, что метаболические пути в миокарде переключаются на разных этапах репарации ИБС. Интраоперационные и реперфузионные нарушения сердечного метаболизма в виде гипоэргоза и лактацидоза можно рассматривать как факторы риска сердечной недостаточности в раннем послеоперационном периоде.
Кардиохирургия, метаболизм, миокард, врожденные пороки сердца, искусственное кровообращение, первый год жизни
Короткий адрес: https://sciup.org/142233512
IDR: 142233512 | УДК: 616.12-089.168.1-053.3
Evaluation of intraoperative myocardial metabolism in infants when repairing congenital heart diseases under extracorporeal circulation
Some features of myocardial metabolism were studied in 40 CHD infants operated under extracorporeal circulation with the use of crystalloid pharmacological/ chemical cardioplegia (FCC) (11 patients), blood cardioplegia (14 patients) and "Custodiol" solution (15 patients). A complex evaluation of intraoperative content of glucose, lactate, pyruvate, free fatty acids (FFA), inorganic phosphor (IP) in arterial blood and coronary sinus blood samples was carried out. It was found out that dynamics of biochemical parameters under study when comparing the values of arterial and venous (coronary sinus) blood was of a unidirectional nature. Statistical differences of these parameters in patients with acyanotic and blue heart diseases were not observed. Despite the use of cardiac protection techniques, glucose utilization and some symptoms of myocardium hypoxia because of lactate and pyruvate in the coronary sinus blood, alongside a simultaneous increase of these media in arterial blood, were revealed. While analyzing the production/extraction of energy media, the metabolic pathways in the myocardium were found to switch at different stages of CHD repair. Intraoperative and reperfusion disturbances of cardiac metabolism in the form of hypoergosis and lactacidosis can be considered as risk factors of cardiac insufficiency in the early postoperative period.
Текст научной статьи Оценка интраоперационного метаболизма миокарда у детей первого года жизни при коррекции врожденных пороков сердца в условиях искусственного кровообращения
Современный уровень требований к обеспечению операций на открытом сердце у детей с ВПС предполагает адекватную кардиопротекцию при длительных сроках выключения сердца из кровообращения. Изучение интраоперационного метаболизма миокарда на этапах аноксии и реперфузии, особенно у детей с функционально незрелым миокардом, представляется крайне актуальным. В связи с этим представлялось целесообразным определить общую направленность метаболических сдвигов миокарда в период фармакологически контролируемой аноксии, изучить использование энергетических субстратов непосредственно после восстановления коронарного кровотока и окончания реперфузии. Опубликованы единичные работы, показывающие, что при применении ФХКП при коррекции ВПС у детей старшего возраста [12] и раствора «Custodiol» [2] у детей первого года жизни имеются гипоксические расстройства метаболизма миокарда.
МАТЕРИАЛ И МЕТОДЫ
Обследовано 40 пациентов с ВПС (26-ДМЖП, 10-ТФ, ДОМС от ПЖ-2, ДМПП-2). Средний возраст детей 12±0,7 месяцев. Исследования проводились на следующих этапах: в начале анестезии - 0) исходный этап, 1) перед окклюзией аорты (АО) на фоне ИК, 2) непосредственно после восстановления сердечной деятельности, 3) 20-30-я мин реперфузии. Для защиты миокарда у 11 пациентов использовалась ФХКП и у 14 - кровяная кардиоплегия, по принятой в клинике методике, у 15 -раствор «Custodiol». Средняя продолжительность окклюзии АО составила 51,3±3,2 мин, ИК -95,1±4,4 мин. ИК проводилось в режиме умеренной гипотермии (средняя ректальная температура 31,3±0,4 °С). Анестезиологическое обеспечение включало комбинированную внутривенную и ингаляционную анестезию в составе базовых анестетиков: фентанил, изофлюран (в последнее время севофлюран); гипнотиков: дормикум (в последнее время пропофол); миорелаксантов-ардуан.
Забор проб крови производили из артерии и вены в начале на исходном этапе; из артериальной магистрали аппарата искусственного кровообращения (АИК) и коронарного синуса (КС) на 1этапе; из артериальной магистрали АИК и коронарного синуса на 2 этапе; из артериальной магистрали АИК и коронарного синуса на 3этапе. Метаболизм миокарда оценивался по содержанию глюкозы, лактата, пирувата, СЖК, неорганического фосфора в притекающей и оттекающей от сердца крови. На основе этих данных рассчитывалось процентное соотношение пациентов с экстракцией и продукцией метаболитов миокардом. Всем больным в послеоперационном периоде регистрировались ЭКГ и ЭхоКГ.
Статистическую обработку данных проводили с помощью пакета компьютерных программ ОFFICE XP, пакета статистических программ STATISTICA 6.0. В качестве статистически значимых считали результаты при достижении уровня значимости р<0,05, для оценки тенденции использовали уровень p<0,1. Методы статистики: для определения силы связи между параметрами вычислялся коэффициент корреляции Спирмена, различия между двумя группами оценивали непараметрическими критериями Манна-Уитни, Уилкок-сона. Если число сравниваемых групп превышало две, использовали непараметрический тест Краскелла-Уоллиса, для сравнения средних значений, которые нормально распределены, использовался критерий Стьюдента, для сравнения долей использовался z- критерий.
РЕЗУЛЬТАТЫ
Исследование динамики содержания глюкозы в артериальной крови показало статистически значимое возрастание ее концентрации на фоне ИК перед окклюзией АО в 2 раза по сравнению с исходным.
После снятия зажимов с аорты и восстановления сердечной деятельности, а также на 30-й мин реперфузии уровень глюкозы оставался в притекающей крови достоверно высоким по сравнению с исходным (р<0,001) (табл. 1). Аналогичная динамика содержания глюкозы выявлена в крови коронарного синуса (табл. 2), с той лишь разницей, что перед окклюзией АО и на 30-й мин реперфузии в крови КС уровень глюкозы был достоверно выше, чем в артерии (р<0,001).
Содержание лактата в артериальной крови перед коррекцией порока в 2 раза превышало исходное (р<0,001). После снятия зажимов с аорты и восстановления сердечной деятельности отмеча лось дальнейшее нарастание концентрации лактата и к 30-й мин реперфузии она оставалась на том же уровне (табл. 1). Аналогичная динамика содержания лактата выявлена в крови коронарного синуса (табл. 2), однако после восстановления сердечной деятельности концентрация этого метаболита в крови КС была достоверно выше, чем в притекающей артериальной крови (р<0,001).
Содержание пирувата в артериальной крови характеризовалась повышением на 2-м этапе относительно исходного и доокклюзионного с даль-
Таблица 1
Динамика показателей углеводных и липидных субстратов метаболизма миокарда в артериальной крови на этапах коррекции ВПС в условиях ИК у детей первого года жизни, ммоль/л
|
Этап- |
Глюкоза |
Медиана |
Лактат |
Медиана |
Пируват |
Ме- |
СЖК |
Ме- |
Фосфор |
Медиана |
||
|
N М±т |
N М±т |
N |
М±т |
диана |
N |
М±т |
диана |
N М±т |
||||
|
Исходный |
36,00 4,33±0,27 |
4,1 |
35,00 1,41±0,12 |
1,2 |
37,00 |
0,27±0,02 |
0,25 |
36,00 |
0,72±0,08 |
0,58 |
37,00 1,37±0,05 |
1,35 |
|
1 |
40,00 8,59±0,36 |
8,25 |
38,00 2,99±0,15 |
2,78 |
40,00 |
0,26±0,01 |
0,26 |
38,00 |
0,89±0,09 |
0,74 |
38,00 1,25±0,04 |
1,24 |
|
2 |
37,00 9,38±0,50 |
8,1 |
36,00 3,48±0,18 |
3,40 ***. ### |
37,00 |
0,30±0,02 |
0,30 ***. ### |
35,00 |
0,91±0,10 |
0,74 |
35,00 0,98±0,05 |
0,97 ***. ### |
|
3 |
37,00 9,32±0,50 |
8:4 |
35,00 3,68±0,23 |
3,77 ***. ### |
39,00 |
0,38±0,02 |
0,38 ***. ###, @@@ |
37,00 |
0,99±0,08 |
0,87 |
35,00 0,94±0,07 |
0,94 ***. ### |
Таблица 2
Динамика показателей углеводных и липидных субстратов метаболизма миокарда в крови коронарного синуса на этапах коррекции ВПС в условиях ИК у детей первого года жизни, ммоль/л
|
Этап- |
глюкоза |
Ме диана |
Лактат |
Ме-диана |
Пируват |
Ме- |
СЖК Ме- |
Фосфор |
Ме- |
||||
|
N |
М±т |
N |
М±т |
N |
М±т |
диана |
диа- N М±т на |
N |
М±т |
диана |
|||
|
Исходный |
31,00 4,31±0,28 4,0 |
32,00 |
1,67±0,1 |
1,44 |
34,00 |
0,28±0,02 |
0,27 |
31,00 0,87±0,11 0,71 |
32,00 |
1,47±0,06 |
1,44 |
||
|
1 |
37,00 |
9,47±0,5 |
8:7 |
38,00 |
3,13±0,19 |
3,01 |
40,00 |
0,27±0,02 |
0,27 |
38,00 0,97±0,09 0,82 |
36,00 |
1,21±0,05 |
1,22 ::: ### |
|
2 |
35,00 |
9,63±0,5 |
8:1 |
35,00 4,02±0,19 |
4,06 ::: ### |
35,00 |
0,34±0,02 |
0,31 ::: ### |
33,00 0,85±0,09 0,81 |
33,00 |
1,01±0,05 |
1,0 ::: ### |
|
|
3 |
37,00 |
9,61±0,5 |
8,8 |
34,00 |
3,49±0,15 |
3,58 *** , # |
39,00 |
0,37±0,02 |
0,35 ::: ###, @@@ |
35,00 0,85±0,08 0,76 |
35,00 |
1,04±0,07 |
1,1 ::: ### |
Исходный - начало анестезии; 1 - перед окклюзией АО на фоне ИК; 2 - сразу после восстановления сердечной деятельности; 3 - 30-я минута реперфузии
-
* статистически значимое различие между исходным этапом и последующими; # статистически значимое различие между 1 этапом и 2,3 этапом; @ статистически значимое различие между 2 этапом и 3 этапом;
-
*, #, @ p<0,05 (p-уровень значимости); **, ##, @@ p<0,01; ***, ###, @@@ p<0,001
нейшим нарастанием к 30-й мин реперфузии (р<0,001) (табл. 1). Аналогичная динамика содержания пирувата выявлена в крови коронарного синуса (табл. 2). Обнаружено, что после восстановления сердечной деятельности концентрация пирувата в крови КС была статистически значимо отличалась (выше) от артериальной (р<0,01).
Мы не выявили корреляции исследуемых параметров с длительностью пережатия аорты.
Уровень неорганического фосфата в артериальной крови непосредственно после восстановления сердечной деятельности имел статистически значимое различие (снижение) относительно исходного (р<0,001) и доокклюзионного периода (р<0,001) с сохранением низких показателей к 30й мин реперфузии (табл.1). Аналогичная динамика содержания неорганического фосфора выявлена в крови коронарного синуса без достоверных артериовенозных различий на всех этапах исследования (табл. 2).
Концентрация свободных жирных кислот в артериальной крови имела статистически значимое различие (повышение) перед окклюзией АО (р<0,001), сохраняясь на данном уровне до окончания реперфузии (табл. 1). Уровень СЖК в крови коронарного синуса оставался таким же высоким, как и в артериальной крови, статистически достоверных артериовенозных различий по концентрации СЖК на этапах исследования не зарегистрировано (табл. 2).
Установлено, что динамика изменений исследуемых биохимических параметров в притекающей к сердцу артериальной крови и крови коронарного синуса имела четкий однонаправленный характер. Мы не выявили статистических различий по всем представленным показателям между пациентами с цианотическими и бледными пороками.
Оценка распределения доли пациентов по соотношению продукции и экстракции энергетических субстратов миокардом на этапах коррекции ВПС показала, что перед окклюзией АО, на фоне ИК в режиме умеренной гипотермии (средняя ректальная температура 31,3±0,4 °С) отмечалась продукция глюкозы миокардом у 63±8% пациентов, лактата у 61±8%, пирувата у 50±8%, СЖК у 55±8% и экстракция фосфора у 67±8% пациентов. Непосредственно после восстановления сердечной деятельности (2 этап) доля пациентов с продукцией лактата в коронарный синус составила 83±8%, что статистически отличалось в сторону прироста от 1 этапа (р<0,05) и в 65±8% случаев наблюдалось продукция пирувата без статистических отличий с 1 этапом. Экстракция глюкозы выявлена у 63±8% пациентов, что статистически значимо отличалось, увеличилось по сравнению с 1 этапом (р<0,01), СЖК - у 62±8%, фосфора в 50±8% случаев, без статистических отличий с 1 этапом. На этапе реперфузии миокард продуцировал глюко зу у 70±8% пациентов, что статистически отличалось в сторону прироста от 2 этапа (р<0,01). Доля пациентов с экстракцией лактата увеличилась до 68±8% по сравнению со 2 этапом (р<0,001), пирувата - до 64±8% (р<0,01) и наблюдалось экстракция СЖК у 66±8%, фосфора - у 53±8% пациентов, без статистически значимых различий со 2 этапом (рисунок).
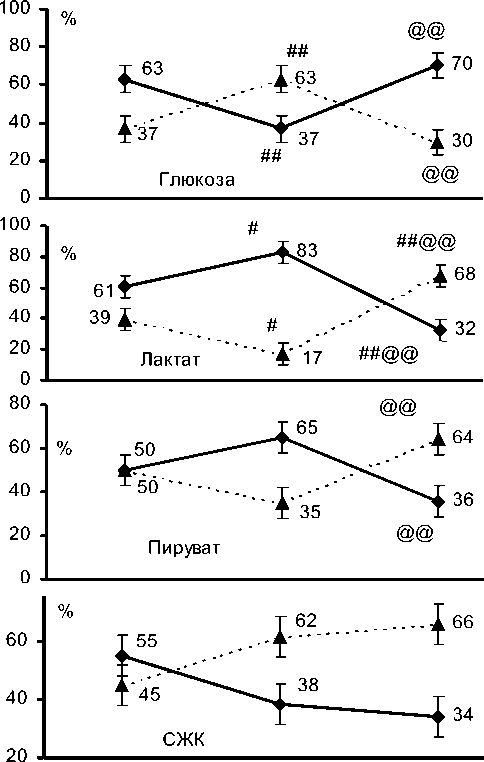
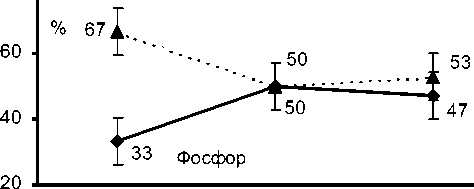
1 этап 2 этап 3 этап
♦ продукция ---А ■■ экстракция
1 этап - перед окклюзией АО на фоне ИК; 2 этап -сразу после восстановления сердечной деятельности; 3 этап - 30 минута реперфузии.
Процент больных по соотношению продукции - экстракции миокардом энергетических субстратов на этапах коррекции ВПС у пациентов первого года жизни.
ОБСУЖДЕНИЕ
В обычном режиме деятельности миокард предпочтительно использует для синтеза АТФ свободные жирные кислоты (60-90%),тогда как оставшаяся часть (10-40%) приходится на окисление глюкозы. В здоровом сердце практически все количество (>95%) АТФ синтезируется в процессе окислительного фосфорилирования в митохондриях и лишь небольшая часть образуется путем анаэробного гликолиза [24]. При увеличенной нагрузке сердечная мышца утилизирует глюкозу, при окислении которой образуется больше АТФ, чем при окислении СЖК. Известно также, что сердце может использовать в качестве энергетических субстратов недоокисленные метаболиты глюкозы лактат и пируват.
Фармакологически контролируемая аноксия миокарда и реперфузия при операциях на открытом сердце вызывает ряд метаболических изменений в сердечной мышце, затрагивающих субстратное обеспечение физиологических функций [8, 17]. Нами установлено, что перед окклюзией аорты на фоне искусственного кровообращения имеются нарушения использования энергетических субстратов сердечной мышцей. Снижение экстракции глюкозы миокардом, несмотря на повышенный уровень ее в артериальной крови, по-видимому, связано с действием на организм экстремальных факторов операционного периода и повышенной резистентностью тканей к инсулину вследствие высокого уровня в крови стрессовых гормонов. Имеются данные о снижении утилизации глюкозы миокардом перед коррекцией ВПС на глубине охлаждения с предпочтительным использованием лактата и жирных кислот в качестве энергетических субстратов [12]. С позиций изменений метаболического состояния миокарда период охлаждения у детей первого года жизни, по нашим данным, характеризовался появлением группы пациентов (61±8%), у которых регистрировалось выведение лактата в кровь коронарного синуса. Это свидетельствовало о развитии гипоксических нарушений в сердечной мышце еще до основного этапа операции, что по мнению ряда авторов связано с непосредственным влиянием гипотермии на миокард [6, 29].
Несмотря на применяемые методы кардиопротекции, у большинства пациентов первого года жизни после снятия зажима с аорты повышенный уровень лактата в крови коронарного синуса может свидетельствовать о его анаэробной природе и подавлении окислительных процессов в миокарде. Выраженную продукцию лактата миокардом на аналогичном этапе операции отмечали и при коррекции клапанных пороков сердца [3, 4], и после операций аорто-коронарного шунтирования. [1, 10, 13], а также при коррекции ВПС в условиях бесперфузионной гипотермии с применением ФХКП у детей старшего возраста [12], при коррекции ВПС в условиях гипотермической перфузии у пациентов первого года жизни с применением ФХКП и раствора «Custodiol» [2].
Увеличение концентрации пирувата в крови коронарного синуса, зарегистрированное нами после снятия зажима с аорты, по-видимому, связано с нарушением включения пирувата в цикл Кребса, что может быть обусловлено снижением активности пируватдегидрогеназы вследствие уменьшения активности инсулина. Полагают, что именно снижение чувствительности тканей к инсулину под влиянием контринсулярных гормонов является причиной уменьшения потребления не только глюкозы, но и лактата и пирувата х [27].
Эта точка зрения подтверждена клиническими наблюдениями и хорошим эффектом лечения раствором, содержащим глюкозу, инсулин, калий (ГИК-смесь) [28]. Известно, что применение препаратов, непосредственно активирующих окисление пирувата, приводило к устранению последствий ишемии, восстановлению ионного гомеостаза и улучшению сократительной активности миокарда [22], По результатам некоторых исследований внутрикоронарная инфузия пирувата приводила к быстрому повышению фракции выброса левого желудочка и минутного объема сердца у пациентов с дилятационной кардиомиопатией. Данный эффект исчезал сразу же после прекращения инфузии [16].
Анализ использования оперированным сердцем энергетических субстратов показал, что значительное снижение доли пациентов с потреблением глюкозы с 63±8% от начала восстановления коронарного кровотока до 30±8% к 30-й мин реперфузии сменяется продукцией этого субстрата соответственно с 37±8 до 70±8% больных, что подтверждает имеющиеся данные о снижении утилизации миокардом энергетических субстратов в постишемическом периоде [26]. Такое переключение с потребления глюкозы миокардом при возобновлении кровотока на ее выведение в кровь коронарного синуса к 30-й мин реперфузии может свидетельствовать о нарушении окислительного фосфорилирования и образования АТФ вследствие повреждения митохондрий. Оно может быть связано с реперфузионной и реоксигенационной активацией перекисного окисления липидов (ПОЛ), приводящего к структурной модификации биологических мембран. Поскольку продукты ПОЛ увеличивают проницаемость липидного бислоя мембран, особенно для ионов H и Са, это может приводить к избытку Са в цитоплазме и накоплению его в митохондриях, что способствует разобщению окисления с фосфолированием и дефициту АТФ [7]. Кардиомиоцит при снижении способности митохондрий осуществлять синтез АТФ может оказаться в условиях энергетического голода (гипоэргоза) [5, 14].
Возрастание доли пациентов с потреблением сердцем свободных жирных кислот по сравнению с потреблением глюкозы к 30-й мин реперфузии отражает существование обратной зависимости между этими субстратами в их влиянии на миокард. Считают, что увеличение концентрации СЖК в системной циркуляции при реперфузии ишемизированного миокарда является одним из главных факторов, приводящих к повышению активности окисления СЖК в сердце, в результате чего резко снижается активность окисления глюкозы [19, 21]. Таким образом, еще одним существенным фактором разобщения гликолиза и окислительного фосфорилирования в этот период является гиперлипидемия, что приводит к избыточному синтезу и накоплению лактата и протонов в клетке [18]. Нельзя исключать и того факта, что экстракция СЖК может быть связана не только с использованием в качестве энергетического источника, но и как субстрата в процессах ПОЛ. По современным данным медикаментозное торможение окисления СЖК и стимуляция окисления глюкозы способны улучшать эффективность работы сердца в условиях ишемии [9]. Кроме того, применение глюкозо-инсулинового раствора способствует снижению концентрации циркулирующих жирных кислот и улучшению сократительной функции сердца [25]. Инфузия ГИК-смеси в периоде реперфузии должна начинаться как можно раньше, поскольку при этом наилучшим образом используется «терапевтическое окно», позволяющее инсулину эффективно блокировать поступление жирных кислот в миокард [17].
Значительное снижение доли пациентов с продукцией лактата с 83±8% от начала восстановления коронарного кровотока до 32±8% к 30-й мин реперфузии сменяется потреблением этого субстрата соответственно от 17±8 до 68±8% больных.
Наши данные о потреблении миокардом лактата, пирувата в качестве энергетических субстратов на этапе реперфузии у большей доли больных первого года жизни сопоставимы с ранее представленными данными после коррекции ВПС у пациентов старшего возраста [12].
Способность миокарда экстрагировать лактат, являющийся эффективным источником энергии для аэробного гликолиза позволяет повысить экономичность потребления кислорода в миокарде на 16-26% [20]. По данным некоторых авторов снижение утилизации лактата у ряда пациентов в этот период совпадало с развитием сердечной недостаточности [3], в тоже время по данным других авторов переключение метаболизма на захват и окисление углеводов, в том числе и лактата, приводило к улучшению функции левого желудочка [15]. По-видимому, следует считать включение лактата в процесс метаболизма у детей первого года жизни на этапе реперфузии прогностически благоприятным признаком, тем более, что нормальный метаболизм сердечной мышцы в данной возрастной группе предполагает предпочтительное использование лактата и глюкозы в качестве энергетических субстратов [11]. Снижение содержания неорганического фосфата как в артериальной, так и в венозной крови коронарного синуса после восстановления сердечной деятельности и на 30-й мин реперфузии может свидетельствовать о его использовании в реакциях окислительного фосфорилирования и образования АТФ.
ВЫВОДЫ
-
1. Интраоперационная динамика метаболических показателей в артериальной крови и крови коронарного синуса у детей первого года жизни при коррекции ВПС носит однонаправленный характер и представлена гипергликемией, лактатемией, пи-руватемией и гипофосфатемией.
-
2. Метаболизм миокарда непосредственно после восстановления сердечной деятельности при сравнении количественных показателей в артерии и коронарном синусе характеризуется продукцией лактата и пирувата, что отражает гипоксические изменения в миокарде и преобладание анаэробного пути обмена, а также продукцией глюкозы на момент реперфузии, что свидетельствует о нарушении утилизации глюкозы.
-
3. Субстратное обеспечение оперированного сердца при оценке доли пациентов с экстракцией -продукцией характеризуется переключением метаболических путей с экстракции глюкозы и продукции лактата на этапе восстановления коронарного кровотока относительно доокклюзионного периода на потребление лактата и пирувата на фоне нарушения утилизации глюкозы на этапе реперфузии по сравнению с этапом восстановления сердечной деятельности.
-
4. Использование лактата на этапе реперфузии можно рассматривать в качестве экономичного энергетического субстрата для оперированного сердца у детей первого года жизни, совпадающего с возрастными особенностями метаболизма сердечной мышцы.
-
5. Интраоперационные и реперфузионные нарушения метаболизма миокарда в форме гипоэргоза и лактацидоза у детей первого года жизни при кардиохирургических вмешательствах являются факторами риска развития сердечной недостаточности в раннем послеоперационном периоде.
Список литературы Оценка интраоперационного метаболизма миокарда у детей первого года жизни при коррекции врожденных пороков сердца в условиях искусственного кровообращения
- Бокерия Л.A., Нисневич Э.Д., Лушкин A.B., Сигаев И.Ю., Крюченков Н.Б., Мовсесян Р.Р.//Грудная и сердечно-сосудистая хирургия, 2000. № 4. С. 25-28.
- EDN: RWZOBP
- Бокерия Л.А., Шебаев Г.А., Нисневич Э.Д., Егорова И.Ф., Ким А.И., Мовсесян Р.Р.//Бюллетень НЦ ССХ им. А.Н. Бакулева РAMH, 2002, Т. 3, № 11. С. 223-223.
- EDN: VTMQIX
- Дементьева И.И., Бабалян Г.В., Соловова Л.Е.//Cor et vasa, 1982. V. 24. P. 16-26.
- EDN: XLXUDR
- Дементьева И.И., Белоус А.Е., Трекова Н.А. Андрианова М.Ю., Мильчаков В.И.//Клиническая и лабораторная диагностика, 1997. Т. 6. С. 53.
- Долгих В.Т. Повреждение и защита сердца при острой смертельной кровопотере. Омск. Изд. ОГМА. 2002. 203 с.


