Оценка эффективности методов нейромодуляции в лечении спастических синдромов у пациентов с позвоночно-спинномозговой травмой
Автор: Смолькин А.А., Нинель В.Г., Коршунова Г.А.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Травматология и ортопедия
Статья в выпуске: 4 т.10, 2014 года.
Бесплатный доступ
Цель; оценить эффективность методов нейромодуляции и определить их роль в комплексной реабилитации пациентов со спастическими синдромами после позвоночно-спинномозговой травмы. Материал и методы. В основу работы положено изучение и лечение 105 пациентов со спастическими синдромами после травмы спинного мозга, которым для лечения спастического синдрома последовательно применяли электростимуляцию спинного мозга, эпидуральную лекарственную терапию в сочетании с электронейростимуляцией и локальную гипотермию спинного мозга. Результаты. Последовательное применение методов нейромодуляции у пациентов со спастическими синдромами после травмы спинного мозга дает возможность в 88,6% случаев добиться положительных результатов. Заключение. Полученные результаты позволяют оценить эффективность нейро-модуляционных методик и определить их роль в комплексной реабилитации пациентов со спастическими синдромами после травмы спинного мозга.
Нейромодуляция, спастический синдром, травма спинного мозга
Короткий адрес: https://sciup.org/14918023
IDR: 14918023
Evaluationof efficiency of methods of neuromodulation in the treatment of spastic syndromes in patients with spinal cord injury
Objective: to evaluate the efficiency of the neuromodulation methods and to determine their role in complex rehabilitation of patients with spastic syndromes after spinal cord injury. Material and methods: Based on the study and treatment of 105 patients with spastic syndromes after injury of the spinal cord, electrical stimulation of the spinal cord, epidural drug therapy in combination with electrical nerve stimulation and local hypothermia spinal cord have been consistently applied for the treatment of spastic syndrome. Results: Consistent use of methods of neuromodulation in patients with spastic syndromes after spinal cord injuries are given in 88,6% of cases to obtain positive results. Conclusion: The obtained results allow to estimate efficiency of neuromodulation methods and to determine their role in complex rehabilitation of patients with spastic syndromes after spinal cord injury
Текст научной статьи Оценка эффективности методов нейромодуляции в лечении спастических синдромов у пациентов с позвоночно-спинномозговой травмой
1 Введение . Повреждения позвоночника составляют 15-20% от числа всех травм опорно-двигательной системы, при этом почти в 80% случаев возникают повреждения спинного мозга. Пациенты с данной травмой представляют собой наиболее тяжелый контингент пострадавших, о чем свидетельствует высокий процент инвалидизации, который, по данным литературы, составляет от 50 до 80% [1]. В 60-78% случаев у больных, перенесших грубое повреждение спинного мозга выше поясничного утолщения, развивается спастический синдром. Подобная ситуация значительно усугубляет и без того их тяжелое состояние, а самое главное, она препятствует проведению реабилитационных мероприятий, направленных на восстановление двигательных функций спинного мозга [2, 3].
Лечение пациентов с чрезмерной спастичностью мышц начинают с применения различных антиспастических средств на фоне физиотерапии и лечебной физкультуры. Вместе с тем клинический опыт указывает на малую эффективность консервативной
терапии при выраженном спастическом синдроме у пострадавших после позвоночно-спинномозговой травмы (ПСМТ). В отдельных случаях для локального воздействия на спазмированную мышцу используют препарат ботулинического токсина. Он на время блокирует пораженную мышцу и в какой-то степени корригирует работу нейромышечного аппарата. Однако применение нервно-мышечных блокад у пациентов, перенесших ПСМТ, весьма проблематично [4].
Хирургические вмешательства у пациентов со спастическим синдромом, направленные на деструкцию различных структур спинного мозга (ризотомия, миелотомия, локальное введение химических агентов и др.), в настоящее время применяются в исключительных случаях. Это связано, во-первых, с высоким риском получения нежелательных осложнений, во-вторых, с широким применением функциональных методик (электростимуляция спинного мозга и интратекальное введение лекарственных препаратов — опиатов и баклофена), осуществляемых с помощью генераторов импульсного тока и дозирующих устройств [5].
Интратекальная инфузия лекарственных препаратов, несмотря на высокую эффективность, со- пряжена с нагноением, риском прекращения подачи этих препаратов либо их избыточного поступления, образованием псевдоменингоцеле и гранулемы на внутреннем конце катетера, требующих удаления имплантированной помпы. Нередко развиваются и более грозные витальные осложнения, которые могут привести к летальному исходу [6].
В настоящее время незаслуженно забыта локальная гипотермия спинного мозга, которая относится к методам функциональной нейрохирургии. Она не только может эффективно купировать посттравматические спастические синдромы, но и является реальной альтернативой деструктивным оперативным вмешательствам и лекарственной терапии [7].
Цель работы : оценить эффективность методов нейромодуляции и определить их роль в комплексной реабилитации пациентов со спастическими синдромами после позвоночно-спинномозговой травмы.
Материал и методы. В основу работы положено углубленное изучение и лечение 105 пациентов с чрезмерной спастичностью мышц после перенесенной позвоночно-спинномозговой травмы. Из них лиц мужского пола 80 (76,1%), женского 25 (23,9%). Основную массу составили пострадавшие молодого трудоспособного возраста. Большинство пациентов (70 человек, или 66,6%) поступили в нейрохирургический стационар через год и более после ПСМТ, 35 (33,4%) человек госпитализированы в ранние сроки (до года) с момента травмы после безуспешного консервативного лечения. Всем больным проведено комплексное обследование соматического и неврологического статусов, включающее электрофизиологические и лучевые методы диагностики. В целях сравнения электронейромиографических данных, регистрируемых у пациентов с травмой спинного мозга, осложнённой спастическим синдромом, нами обследовано 10 практически здоровых добровольцев (5 лиц мужского и 5 — женского пола) в возрасте от 25 до 45 лет. Полученные показатели электрофизиологического исследования были приняты за условную норму.
Для объективизации тяжести функциональных нарушений спинного мозга пациентов использовали шкалу ASIA / IMSOP (American Spinal Injury Association / International Medical Society of Paraplegia). В зависимости от выраженности чувствительных и двигательных выпадений она ранжирована на 5 классов: «А» — полное нарушение проводимости, «В» — неполное нарушение проводимости, «С» — частичное нарушение (сила мышц менее трех баллов), «D» — частичное нарушение (сила основных мышц 3 балла и более) и «E» — двигательная и чувствительная функции в норме. У всех пациентов (n=105) определяли степень спастичности мышц по международной модифицированной шкале Ашворта, которая позволяет условно оценить уровень мышечного тонуса при осуществлении пассивных движений конечностью от 1 до 5 баллов [8].
О функциональном состоянии сегментарного аппарата спинного мозга судили по данным электронейромиографии (ЭНМГ), которую выполняли на электромиографе «Keypoint» фирмы «Dantek» (Дания; CША). В работе использовали такие показатели, как амплитуды Н-рефлекса и М-ответа, а также их процентное соотношение (Н / М·100).
Обзорную рентгенографию позвоночника выполняли всем пациентам с ПСМТ (n=105) с применением стандартных укладок. В отдельных случаях (n=35) для уточнения положения металлоконструкций в костных структурах и состояния позвоночного канала проводили компьютерную томографию на аппарате «Aquilion 64» фирмы «Toshiba» (Япония).
Травматические изменения в спинном мозге на уровне повреждения визуализировали на 1,5 Тл магнитно-резонансном томографе (МРТ) «Echelon» фирмы «Hitachi» у больных с травматической болезнью спинного мозга (n=66) при отсутствии внешних и внутренних факторов, препятствующих получению достоверной информации.
Для купирования спастического синдрома у пострадавших после ПСМТ использовали следующие методы нейромодуляции: электростимуляцию спинного мозга (ЭССМ); комплексную лекарственную и электроимпульсную нейромодуляцию; локальную гипотермию спинного мозга (ЛГСМ).
Методика электростимуляции спинного мозга . Для осуществления этого метода электроды в эпидуральное пространство спинного мозга устанавливали таким образом, чтобы контактные площадки противоположных полюсов находились на 1–2 позвонка выше и ниже сегментов поясничного утолщения, а также справа и слева от средней линии. Параметры импульсного тока подбирали индивидуально на основании изменений показателей электронейромиографии: использовали преимущественно ток частотой 100 Гц, длительностью 0,2 мс, а амплитуду увеличивали плавно до появления устойчивого Н-рефлекса, что обычно соответствовало амплитуде 8–10 В. Для осуществления ЭССМ применяли электроды и портативные генераторы импульсного тока фирмы «Medtronic» (США). Сеансы длительностью по 30–40 мин проводили 3–4 раза в день, курс ЭССМ продолжался 4–5 недель.
Методика эпидуральной лекарственной терапии и электроимпульсной нейромодуляции . Данный способ нейромодуляции выполняли путем имплантации в эпидуральное пространство на уровне сегментов поясничного утолщения электродов и стандартного катетера, предназначенного для пери-дуральной анестезии. Катетер располагали между электродами на уровне Th12-L1 позвонков. Приготовленную лекарственную смесь, содержащую 2 мл 0,01%-ного раствора клофелина, 2,0 мл 1%-ного раствора морфина гидрохлорида и 20,0 мл изотонического раствора хлорида натрия, через катетер вводили с помощью стационарных («ВЭДА-3», Россия) либо портативных («WalkMed» фирмы «McKinley», США) дозаторов. Инфузию лекарственной смеси осуществляли со скоростью от 0,1 до 0,5 мл/ч. Аппликацию указанных препаратов проводили круглосуточно на протяжении 10–12 суток на фоне сеансов электроимпульсной нейромодуляции по следующей схеме: первые трое суток скорость введения составляла 1 мл/ч, в последующие двое суток — 0,5 мл/ч и в оставшиеся 5–7 суток — 0,1 мл/ч. Методика ЭССМ оставалась прежней, ее осуществляли импульсами длительностью 0,2 мс, частотой 100 Гц и амплитудой импульсного тока от 8 до 10 В. Длительность сеанса составляла 30–40 мин, сеанс повторяли 3–4 раза в день.
Методика локальной гипотермии спинного мозга. На заключительном этапе нейромодуляцион-ного лечения выполняли ЛГСМ путем пункционного введения в субарахноидальное пространство охлажденного от 0° до +4°С 0,9%-ного раствора хлорида натрия. Метод осуществляли инфузионным или перфузионным способом в условиях операционной под общим интубационным наркозом. В положении больного на левом боку с приведенными к животу ногами и приподнятым до 30° изголовьем пунктировали субарахноидальное пространство между L3 и L4 позвонками и эвакуировали 60–80 мл ликвора. Затем шприцем емкостью 20 мл пробно вводили 10–20 мл охлажденного до 18–22°С раствора хлорида натрия со скоростью 10 мл/мин. Убедившись в отсутствии осложнений со стороны сердечно-сосудистой системы, с той же скоростью осуществляли инфузию еще 40–60 мл раствора, но при более низкой его температуре от 0 до +2°С. Для выполнения перфузионного способа субарахноидальное пространство пунктировали на нескольких уровнях, при этом иглу, через которую осуществляли перфузию, располагали между L3и L4 позвонками, а остальные выше — над сегментами поясничного утолщения (на уровне Th10-L2 позвонков). Охлажденный до температуры 0 — +2°С раствор хлорида натрия в количестве 1500–2000 мл вводили на протяжении 60–120 мин. Во время ЛГСМ осуществляли электрофизиологический мониторинг в целях предупреждения нежелательных реакций со стороны сердечно-сосудистой системы.
Статистическую обработку полученных результатов осуществляли методом вариационной статистики с вычислением средней арифметической (М), ошибки средней арифметической (m) и среднеквадратического отклонения (σ) при нормальном характере распределения вариационных рядов; для определения достоверности различий вычисляли доверительный коэффициент t-критерий Стьюдента и определяли по табличным данным величину вероятности (р). Различия считали достоверными при p≤0,05.
Результаты. Эффективность методов нейромодуляции в лечении спастического синдрома у пострадавших с последствиями ПСМТ оценивали по снижению чрезмерной спастичности мышц в баллах, состоянию сегментарного аппарата поясничного утолщения при ЭНМГ-обследовании, степени неврологического дефицита (шкала ASIA / IMSOP) и структурным изменениям спинного мозга на магнитно-резонансной томограмме.
Традиционно исходы лечебных мероприятий подразделяются на отличные, хорошие, удовлетворительные и неудовлетворительные результаты. Однако, учитывая функциональную направленность применяемых методик и трудности оценки спастических синдромов у пострадавших с ПСМТ, мы принимали во внимание только положительный и неудовлетворительный результаты. Для этого сравнивали усредненную сумму баллов до и после лечения и вычисляли коэффициент эффективности лечения (Кэфл.) по следующей формуле: Кэфл.=Σдо / Σпосле, где Кэфл. — коэффициент эффективности лечения; Σдо — сумма баллов до и Σпосле — после выпол- нения лечебных мероприятий. Если Кэфл.=2 или >2, то лечебный эффект оценивали как положительный. Если Кэфл.<2, то лечебный результат считали неудовлетворительным.
Ранги «A» и «B», «C» и «D» шкалы ASIA / IMSOP нами были объединены в «АВ» и «CD», поскольку при наличии спастического синдрома по клинико-неврологическим данным четко ранжировать пострадавших в рамках указанной классификационной схемы не представлялось возможным. Оказалось, что 58 (55,2%) пациентов соответствовали группе «АВ» и клинически у них наблюдались спастические тетра- и параплегии, а 47 (44,8%) — группе «CD» со спастическими тетра- и парапарезами.
Во время магнитно-резонансного томографического (МРТ) обследования у 66 пострадавших зарегистрированы следующие результаты. Из 42 пациентов с тетра- и параплегией у 30 (71,4%) на томограммах обнаружены рубцово-кистозные изменения спинного мозга, у 6 (14,3%) выявлены обширные очаги ушиба, у 4 (9,5%) — гематомиелия и у 2 (4,8%) — признаки размозжения нервной ткани. Из 24 пострадавших с тетра- и парапарезом у 18 (75,0%) выявлены небольшие очаги ушиба, у 4 (16,6%) — умеренный атрофический процесс и у 2 (8,4%) — МРТ-признаки наличия мелких участков глиозных изменений в спинном мозге с кистозным компонентом.
Чрезмерная мышечная спастичность по шкале Ашворта у 58 пациентов с тетра- и параплегией (группа «АВ») в среднем составила 4,5±0,06 балла, а у 47 пациентов с частичным повреждением спинного мозга (группа «CD») средние цифры спастичности мышц были на уровне 3,8±0,07 балла.
Показатели ЭНМГ-обследования функционального состояния сегментарного аппарата поясничного утолщения спинного мозга перед проведением лечебной нейромодуляции представлены в табл. 1. На электронейромиограммах у 58 пациентов со спастической тетра- и параплегией обнаружено достоверное повышение амплитуды Н-рефлекса (p<0,01), снижение амплитуды М-ответа (p=0,05) и увеличение процентного отношения Н-рефлекса к М-ответу (p<0,001).
У 47 пострадавших с тетра- и парапарезом (группа «CD») амплитуды H-рефлекса (p<0,05) и M-ответа (p<0,001) были меньше контрольных значений, при этом величина процентного соотношения H-рефлекса к M-ответу не отличалась от данных контрольной группы (p>0,05). При сравнении групп «АВ» и «CD» оказалось, что у больных с тетра- и параплегиями амплитуда Н-рефлекса (р1<0,05) и величина процентного соотношения Н-рефлекса к М-ответу (р1<0,001) достоверно меньше, чем у пациентов с тетра- и парапарезом (табл. 1).
Таблица 1
Электромиографические показатели до начала лечения
|
Обследованные группы |
Изучаемые показатели (М ± m) |
||
|
Амплитуда Н-рефлекса, мВ |
Амплитуда М-ответа, мВ |
Соотношение Н/М, % |
|
|
Контрольная (n=10) |
1,09±0,1 |
2,53±0,2 |
42,8±2,1 |
|
«АВ» (n=58) |
1,48±0,1 p<0,01 |
1,82±0,3 p=0,05 |
81,3±3,2 p<0,001 |
|
«CD» (n=47) |
0,62±0,17 p < 0,05 р <0,05 |
1,12±0,3 p < 0,001 р >0,05 |
55,3±6,5 p > 0,05 p <0,001 |
П р и м еч а н и е : р — достоверность по сравнению с показателями контрольной группы; p1 — достоверность к показателями группы «АВ».
Степень спастичности мышц по шкале Ашворта у больных с ПСМТ до и после электронейромодуляции в зависимости от исходов лечения
Таблица 2
|
Категория |
Группа «АВ» |
Группа «CD» |
||
|
Кол-во пациентов |
Степень спастичности |
Кол-во пациентов |
Степень спастичности |
|
|
До лечения |
58 |
4,5±0,3 |
47 |
3,8±0,2 |
|
Положительный результат |
23 |
2,1±0,15*** |
36 |
1,5±0,1* |
|
Неудовлетворительный результат |
35 |
3,2±0,1***ллл |
11 |
3,1±03 |
П р и м еч а н и е : * — достоверность по отношению к степени спастичности мышц до проведения ЭССМ (*** — р<0,001); ^ — достоверность по отношению к степени спастичности в группе с положительными результатами лечения (^^^ — р<0,001).
Результаты ЭССМ оценивали по изменению степени спастичности мышц по шкале Ашворта до и после проведения курса электростимуляции (табл. 2).
Согласно данным, представленным в табл. 2, у 23 (39,7%) пациентов группы «АВ» получено достоверное (р<0,001) снижение уровня спастичности мышц. Результат ЭССМ у этих пациентов считали положительным, так как коэффициент эффективности лечения (Кэфл.=2,14) был больше «2». У 35 (60,3%) больных коэффициент эффективности лечения (Кэфл.=1,4) был меньше «2», что свидетельствовало об отсутствии эффекта, однако выраженность спастического синдрома была значимо снижена (р<0,001) по сравнению с данными степени спастичности до проведения ЭССМ. В то же время степень спастичности мышц пациентов с неудовлетворительными результатами оказалась существенно выше, чем в группе больных с удовлетворительными исходами лечения (р<0,001).
В группе «Cd» у 36 (76,6%) больных после 4-недельного курса ЭССМ достигнут положительный результат. У них, наряду с достоверным (р<0,001) снижением уровня спастичности, отмечалось повышение коэффициента эффективности лечения до «2,5» (Кэфл.>2). У 11 (23,4%) пациентов коэффициент эффективности лечения оказался равным «1,23» (Кэфл.<2), и они были отнесены к неудовлетворительным результатам.
В оценке эффективности ЭССМ весьма демонстративными оказались электронейромиографиче-ские показатели. Так, у 23 (39,7%) пострадавших группы «АВ» с положительным клиническим эффектом после 4 недель ЭССМ процентное соотношение максимальных амплитуд Н/М снизилось более чем в 1,5 раза, т.е. наблюдалась тенденции к нормализации рефлекторной деятельности сегментарного аппарата поясничного утолщения спинного мозга. Напротив, у 35 (60,3%) пациентов этой же группы с неудовлетворительными результатами после ЭССМ соотношение максимальных амплитуд Н/М снизилось лишь на 13% по сравнению с исходными данными.
В группе «CD» у 36 (76,6%) пациентов с положительными клиническими результатами процентное отношение амплитуд Н/М уменьшилось на 14,8% и соответствовало данным нижней нормы. У 11 (23,4%) пострадавших с тетра- и парапарезом заметной динамики этих ЭНМГ-показателей не наблюдалось (рис. 1).
Таким образом, общие положительные исходы после 4-недельного курса ЭССМ зарегистрированы у 59 (56,2%), а неудовлетворительные — у 46 (43,8%) пациентов.
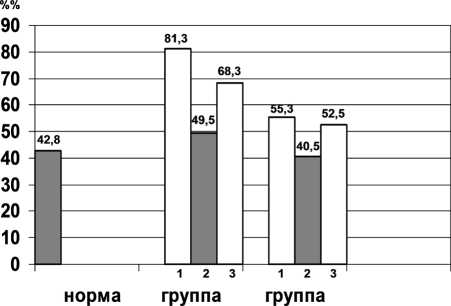
"АВ" "CD"
Рис. 1. Динамика процентного соотношения максимальных амплитуд Н/М по данным ЭНМГ: 1 — до лечения; 2 — положительный результат после курса ЭССМ; 3 — неудовлетворительный исход после курса ЭССМ
Результаты эпидуральной лекарственной терапии и электроимпульсной нейромодуляции изучены у 46 (43,8%) пострадавших, из которых у 35 (33,3%) наблюдалась тетра- и параплегия, а у 11 (10,5%) имелся тетра- и парапарез (табл. 3).
Из данных табл. 3 следует, что при эффективном лечении пациентов с тетра- и параплегией (группа «АВ») положительный результат получен у 13 (12,4%) человек (р<0,001), о чем свидетельствовало снижение уровня спастичности мышц (Кэфл=2,1). В случаях неудовлетворительного исхода после комплексной лекарственной и электроимпульс-ной нейромодуляции у 22 (20,9%) пострадавших уменьшение интенсивности спастического синдрома не наблюдалось и коэффициент эффективности был равен «1» (Кэфл.<2). В группе «CD» у 8 (7,6%) больных с тетра — и парапарезом при положительных результатах после эпидуральной лекарственной терапии и электроимпульсной нейромодуляции наблюдалось достоверное (р<0,01) снижение уровня спастичности, при этом коэффициент эффективности составил «2,2» (Кэфл.>2). У 3 (2,9%) пациентов эффект от эпидуральной аппликации лекарственной смеси и электроимпульсной нейромодуляции результат оказался неудовлетворительным (Кэфл.<2).
Динамика электронейромиографических показателей после курса комплексной лекарственной и электроимпульсной нейромодуляции представлена на рис. 2.
Обнаружено, что у 13 (12,4%) пострадавших группы «АВ» с положительным клиническим эффектом после 4-недельной комплексной лекарственной и
Таблица 3
Степень спастичности мышц по шкале Ашворта у больных с ПСМТ до и после эпидуральной лекарственной терапии и электронейромодуляции в зависимости от исходов лечения
|
Категория |
Группа «АВ» |
Группа «CD» |
||
|
Кол-во пациентов |
Степень спастичности |
Кол-во пациентов |
Степень спастичности |
|
|
До лечения |
35 |
3,2±0,1 |
11 |
3,1±0,2 |
|
Положительный результат |
13 |
1,5±0,05*** |
8 |
1,4±0,1*** |
|
Неудовлетворительный результат |
22 |
3,0±0,1^^ |
3 |
2,8±0,1^ |
П р и м еч а н и е : * — достоверность по отношению к степени спастичности мышц до проведения ЭССМ (*** — р<0,001); ^ — достоверность по отношению к степени спастичности в группе с положительными результатами лечения (^^ — р<0,01).
электроимпульсной нейромодуляции соотношение максимальных амплитуд Н/М снизилось в 1,7 раза, т.е. наблюдалась тенденции к нормализации рефлекторной деятельности сегментарного аппарата поясничного утолщения спинного мозга. У 17 (37,0%) пациентов этой же группы с неудовлетворительными результатами после лечения соотношение максимальных амплитуд Н/М снизилось лишь на 13% по сравнению с исходными данными. В группе «CD» (n=11) у 8 (7,6%) пациентов электронейромиографи-ческие данные не были столь показательными, но все-таки положительный клинический результат сопровождался снижением процентного соотношения максимальных амплитуд Н/М на 10,2%, а при неудовлетворительном исходе это соотношение Н/М, напротив, увеличилось на 9,9%,
Таким образом, общие положительные исходы комплексного лекарственного и электроимпульсно-го нейромодуляционного воздействия на сегменты поясничного утолщения спинного мозга регистрировались у 21 (20,0%), а неудовлетворительные у 25 (23,8%) пациентов.
На заключительном этапе пациентам (n=25), у которых предыдущие нейромодуляционные методики не оказали положительного эффекта, была выполнена локальная гипотермия спинного мозга, причем у 22 (88,0%) из них наблюдалась параплегия (группа «АВ») в результате повреждения грудного, а у 3 (12,0%) отмечался тетрапарез (группа «CD») после травмы шейного отдела позвоночника. Степень спа-
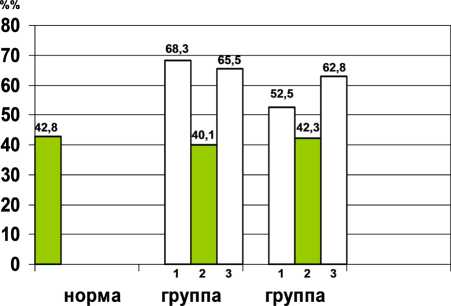
Рис. 2. Динамика процентного соотношения максимальных амплитуд Н/М по данным ЭНМГ: 1 — до лечения; 2 — положительный результат; 3 — неудовлетворительный результат после курса комплексной лекарственной и электроимпульс-ной нейромодуляции стичности мышц перед выполнением ЛГСМ у всех 25 (23,4%) пострадавших равнялась 2,9±0,1 балла, а после операции у 13 (12,4%) пациентов она составила 1,4±0,05 балла. Коэффициент эффективности лечения у них равнялся «2,07» (Кэфл.>2). У этих больных по клиническим и электронейромиографическим данным отмечалось отчетливое снижение мышечного тонуса в конечностях, что соответствовало положительному результату. В итоге после выполнения ЛГСМ у 13 (12,4%) больных достигнут положительный результат, а 12 (11,4%) пациентам эффекта от лечения получить не удалось.
Обсуждение. В обсуждении результатов применения различных нейромодуляционных методик с целью купирования спастических синдромов у пациентов с последствиями ПСМТ нами, как и другими клиницистами [9], учитывались следующие моменты. Во-первых, механизмы их терапевтического воздействия на нейрональные структуры спинного мозга далеко не одинаковы, а самое главное — эти механизмы до сих пор изучены недостаточно. Во-вторых, результаты лечения зависят от характера структурных изменений на уровне травмы спинного мозга и тяжести его функциональных нарушений. В-третьих, отсутствует простая и достаточно надежная система оценки тяжести спастического синдрома и результатов лечения пациентов, вследствие чего у клиницистов возникают серьезные трудности в оценке истинного состояния пациентов, что значительно влияет на интерпретацию эффективности лечебных мероприятий. Тяжесть неврологической симптоматики оценивалась по шкале ASIA / IMSOP, получившей статус международных стандартов в качестве классификации неврологического дефицита при ПСМТ. Однако оценка степени тяжести травматического поражения спинного мозга в остром и более отдаленном периодах травматической болезни спинного мозга по данной классификационной схеме вызывала большие трудности. Это связано с тем, что в остром периоде у пострадавших наблюдался спинальный шок, а в более позднем периоде двигательные выпадения выявить оказалось крайне затруднительно, поскольку они перекрывались и маскировались возникновением спастических сокращений в мышцах конечности и непроизвольных движениях в них. Поэтому больные с клиникой спастической тетра- и параплегии и грубыми, обширными изменениями структуры спинного мозга на МРТ нами были объединены в одну группу «АВ», а пациенты с тетра- и парапарезом в группу «CD». На эти трудности при определении тяжести неврологических расстройств и их соответствие ха- рактеру травматических изменений в спинном мозге на МРТ указывают и другие авторы [10].
Степень спастичности мышц нами оценивалась по модифицированной шкале Ашворта, основанной на 5-балльной системе. Однако, несмотря на широкое применение в клинической практике из-за ее простоты и доступности, она не лишена субъективизма, поскольку зависит от квалификации и опыта клинициста. В этой связи для цифровой интерпретации результатов лечения нами предложен коэффициент эффективности лечения (Кэфл.), который позволяет путем сравнения усредненной суммы баллов до и после лечения достаточно просто и полноценно оценить полученные результаты лечения болевых и спастических синдромов [11]. Согласно имеющимся сведениям в литературе, для оценки степени спастичности многие авторы предлагают использовать электронейромиографию [12]. Нейрофизиологические исследования показывают, что у пациентов с травматической болезнью спинного мозга в сегментарном аппарате на поясничном уровне образуются новые патологические нейрональные связи, закрепляющие патологические рефлексы, и оценить по данным ЭНМГ динамику гиперактивности альфа- и гамма-мотонейронов становится крайне затруднительно [13]. Однако в настоящем исследовании установлено, что при положительных результатах у пациентов отмечается четкая тенденция к нормализации процентного соотношения максимальных значений амплитуд Н-рефлекса к М-ответу.
В группе пострадавших с тетра- и параплегией положительный результат при электростимуляции спинного мозга удалось получить только у одной трети. Напротив, у пациентов с тетра- и парапарезом клиническая эффективность этого метода наблюдалась у подавляющего большинства пострадавших. В доступной литературе четкого объяснения этим фактам нами не обнаружено [14]. Однако, опираясь на многолетний клинический опыт, можно предположить, что при воздействии электрическими импульсами на нейронный аппарат поясничного утолщения спинного мозга у пациентов при частичном его повреждении возникает эффект одновременной стимуляции структуры нервной системы на супрасегмен-тарном уровне [15]. Отсутствие эффекта от ЭССМ у пациентов группы «АВ», по-видимому, обусловлено не только грубыми морфологическими изменениями в спинном мозге, выявляемыми при магнитно-резонансной томографии, но и длительностью существования спастического синдрома. Большое значение имеют и морфофункциональные процессы в нейронном аппарате спинного мозга, развивающиеся ниже его повреждения, о формировании которых имеются подтверждения в отечественной и зарубежной литературе [16].
С учетом клинического опыта нами разработана методика комплексного лечения спастических синдромов, заключающаяся в эпидуральной электростимуляции спинного мозга и введении в его эпидуральное пространство субтерапевтических доз клофелина и морфина. Применение этой комбинированной методики позволило получить положительный эффект у пациентов, где одна электронейростимуляция не принесла желаемого результата.
В первые несколько часов и даже суток у большинства (более чем у 90%) пациентов после локальной гипотермии спинного мозга тонус в мышцах нижних конечностей полностью отсутствовал. И мы затруднялись данный результат лечения оценивать как положительный, поскольку развитие вялой тетра- и/или параплегии создавало ряд нежелательных проблем, связанных с возникновением дисфункции мочевого пузыря и кишечника, а также усугублением двигательных нарушений вплоть до полного их исчезновения у пациентов с частичным поражением спинного мозга.
Выводы:
-
1. При оценке эффективности методов нейромодуляции в лечении спастических синдромов необходимо не только опираться на степень снижения спастичности мышц по шкале Ашворта и динамику показателей ЭНМГ-обследования, но и учитывать данные неврологического статуса до и после лечения, а также характер структурных изменений на магнитно-резонансных томограммах.
-
2. Электростимуляция является высокоэффективным методом купирования спастических синдромов у пациентов с частичным травматическим поражением спинного мозга.
-
3. Комбинированная методика нейромодуляции позволяет купировать спастический синдром у той части больных, где электростимуляция спинного мозга оказалась неэффективной.
-
4. Локальную гипотермию спинного мозга необходимо в основном использовать у пациентов с полным повреждением спинного мозга, поскольку у них она оказалась достаточно эффективной.
-
5. Последовательное применение методов нейромодуляции у пациентов со спастическими синдромами после травмы спинного мозга позволяет в 88,6% случаев получить положительные результаты с возможностью дальнейшего проведения реабилитационных мероприятий.
Список литературы Оценка эффективности методов нейромодуляции в лечении спастических синдромов у пациентов с позвоночно-спинномозговой травмой
- Беков M.M., Лобода В.A., Верещако А. В. Хирургическое лечение больных с травмой грудного и смежных отделов позвоночника и спинного мозга в многопрофильном стационаре. В сб.: Всероссийская научно-практическая конференция «Поленовские чтения». СПб., 2009; с. 86-89
- Древаль О.H., Черных И.А., Басков А.В. и др. Особенности клиники и хирургического лечения больных со спастическим и болевым синдромами после позвоночно-спинномозговой травмы Вопросы нейрохирургии им. акад. Н.Н. Бурденко 2007; (3): 10-15
- Biering-Siurensen F, Nielsen JB, Klinge К. Spasticity-as-sessment: a review. Spinal Cord 2006; 44 (12): 708-722
- Воробьева О.В. Применение центральных миорелаксантов в клинике нервных болезней. Лечение заболеваний нервной системы. 2011; 1 (6): 3-9
- Филатов B.C. Иванов B.C., Фатыхова Э.Ф. Использование хронической эпидуральной стимуляции поясничного утолщения спинного мозга в реабилитации детей со спастическими синдромами. В сб.: Материалы Международной научно-практической конференции по нейрореабилитации в нейрохирургии. Казань, 2012; с. 276-278
- Зеелигер А., Берснев В. П. Интратекальное применение баклофена при спастических и хронических болевых синдромах. Неврологический вестник им. академика В.М. Бехтерева 2008; (4): 121-124
- Щуковский В.В. Локальная спинномозговая гипотермия при чрезмерной мышечной спастичности и тяжких болевых синдромах туловища и конечностей. В сб.: Материалы III научно-практической конференции общества «Спинной мозг». Саратов, 2004; с. 22-24
- Haas ВМ, Bergstrom Е, Jamous A, Bennie A. The inter rater reliability of the original and of the modified Ashworth scale for the assessment of spasticity in patients with Spinal Cord injury. Spinal Cord 1996; 34 (9): 560-564
- TatorCH, Minassian K, MushahwarVK. Spinal cord stimulation: therapeutic benefits and movement generation after spinal cord injury. Handb Clin Neurol 2012; 109: 283-296
- Холин А.В., Макаров А.Ю., Мазуркевич E.A. Магнитная резонансная томография позвоночника и спинного мозга. СПб., 1995; 132 с.
- Нинель В.Г., Норкин И.А., Пучиньян Д.М. и др. Методика измерения интенсивности нейрогенной хронической боли туловища и конечностей. Боль 2005; (3): 19-23
- Королев A.A., Суслова Г.А., Королев А.А., Суслова ГА. Оценка выраженности спастичности в нейрореабилитации. Успехи современного естествознания 2011; (4): 89-89
- Лившиц А.В. Хирургия спинного мозга. М.: Медицина, 1990; 352 с.
- Решетняк В.К. Корковый контроль антиноцицептивных структур при рефлекторной аналгезии: автореф. дис... д-ра мед. наук. М., 1989; 49 с.
- Яфарова Г.Г., Балтина ТВ., Плещинский И.Н. Функциональное состояние двигательных центров спинного мозга в условиях его травматического повреждения. Нижнекамск: Изд-во НФ МГЭИ, 2008; 74 с.


