Оценка эффективности седатации у детей с ДЦП в раннем послеоперационном периоде после многоуровневых одномоментных оперативных ортопедических вмешательств
Автор: Евреинов Вадим Викторович, Томов Ахмед Даутович, Попков Дмитрий Арнольдович
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 4, 2015 года.
Бесплатный доступ
Цель. Проведение сравнительной оценки седативного эффекта дексмедетомидина и мидазолама в раннем послеоперационном периоде в отделении реанимации и интенсивной терапии у детей с ДЦП после выполнения многоуровневых одномоментных вмешательств, сопровождающихся реконструктивными вмешательствами на тазобедренном суставе. Материалы и методы. Проведена сравнительная оценка эффективности седатации дексмедетомидином и мидазоламом у 14 детей с ДЦП в раннем послеоперационном периоде после многоуровневых одномоментных оперативных ортопедических вмешательств, которые были разделены на 3 сопоставимые группы. Для оценки степени седатации использовали шкалу Ramsay, шкалу оценки возбуждения - седатации Richmond. Послеоперационное обезболивание во всех группах осуществлялось посредством введения в эпидуральное пространство ропивокаина 0,2 % через установленный ранее эпидуральный катетер. Результаты. Показано, что в 1 группе (без седатации) дети взволнованы, беспокойны, и комфорта ребенку достичь не удается. Во 2 (седатация дексмедетомидином) и 3 (седатация мидазоламом) группах уровень седатации был достоверно выше, чем в контрольной группе и достигал легкой и средней степени. Заключение. Таким образом, дексмедетомидин и медазолам являются эффективными препаратами для седатации детей с ДЦП в ОРИТ в раннем послеоперационном периоде, и достоверных преимуществ в достижении поверхностной седатации между ними не выявлено.
Дети, детский церебральный паралич, ортопедические вмешательства, послеоперационный период, седатация
Короткий адрес: https://sciup.org/142121859
IDR: 142121859 | УДК: 615.214.24:616.831-009.11-053.2-089.168.1-089.5 | DOI: 10.18019/1028-4427-2015-4-36-41
Sedation effectiveness evaluation in children with cerebral palsy in the early postoperative period after acute multilevel surgical orthopedic interventions
Purpose. To make a comparative evaluation of Dexmedetomidine and Midazolam sedative effect in children with cerebral palsy (CP) in the early postoperative period in Resuscitation and Intensive Care Unit (RICU) after performing multilevel acute interventions accompanied by reconstructive procedures of the hip. Materials and Methods. We made a comparative evaluation of the effectiveness of sedation with Dexmedetomidine and Midazolam in 14 children with CP in the early postoperative period after multilevel acute surgical orthopedic interventions who divided into three comparable groups. Ramsay Scale, Scale of Excitement Evaluation - Richmond sedation used in order to evaluate sedation level. Postoperative analgesia in all the groups performed by 0.2 % Ropivacaine infusion into the epidural space using a previously set epidural catheter. Results. As demonstrated, the children in the Group 1 (without sedation) were excited, anxious, they felt uncomfortable. In Groups 2 (sedation with Dexmedetomidine) and 3 (sedation with Midazolam) the level of sedation was significantly higher than in the control group, it attained light and moderate levels. Conclusion. Thus, Dexmedetomidine and Midazolam appeared to be effective preparations to sedate the children with CP staying in RICU in the early postoperative period, and no significant advantages in achieving surface sedation not revealed between them.
Текст научной статьи Оценка эффективности седатации у детей с ДЦП в раннем послеоперационном периоде после многоуровневых одномоментных оперативных ортопедических вмешательств
Частота встречаемости спастического паралича у детей в странах Западной Европы и Северной Америки составляет, в среднем, 2-3 случая на 1000 [1, 2].
У детей с тяжелыми формами ДЦП (IV и V уровень по GMFCS [1]) частота подвывихов и вывихов бедер варьирует от 2,6 до 28 % [3]. В настоящее время концепция оперативного лечения таких ортопедических осложнений подразумевает выполнение многоуровневых одномоментных вмешательств, сопровождающихся реконструкциями тазобедренного сустава (бедренного и ацетабулярного компонента), тено- и апоневротомиями в области тазобедренного, коленного и голеностопного суставов, пересадками сухожилий [3, 4]. Объем оперативного вмешательства и, соответственно, выраженный болевой синдром в сочетании с эмоциональной возбудимостью детей способствуют резкому увеличению спастичности мускулатуры, которая, в свою очередь, увеличивает болевой синдром. Для предотвраще- ния данной ситуации необходимы особые требования к сопровождению данной категории пациентов в раннем послеоперационном периоде и наблюдение в первые сутки в отделении реанимации и интенсивной терапии (ОРИТ) [5]. Вышесказанное заставляет рассматривать вопросы седативной терапии и послеоперационного обезболивания в едином комплексе, персонализировать выбор седативных препаратов в ОРИТ с учетом их фармакокинетическими и фармакодинамическими свойствами, а также сопутствующей патологии пациентов.
Цель работы – проведение сравнительной оценки седативного эффекта дексмедетомидина и мидазолама в раннем послеоперационном периоде в отделении реанимации и интенсивной терапии у детей с ДЦП после выполнения многоуровневых одномоментных вмешательств, сопровождающихся реконструктивными вмешательствами на тазобедренном суставе.
Ш Евреинов В.В., Томов А.Д., Попков Д.А. Оценка эффективности седатации у детей с ДЦП в раннем послеоперационном периоде после многоуровневых одномоментных оперативных ортопедических вмешательств // Гений ортопедии. 2015. № 4. С. 36-41.
МАТЕРИАЛЫ И МЕТОДЫ
В данном проспективном исследовании все дети (14 человек – 8 девочек, 6 мальчиков), страдающие спастической диплегией тяжелой формы, имели одно- или двусторонние вывихи и подвывихи бедер (у четырех пациентов были выполнены вмешательства только на одной стороне, у 10 – последовательно с обеих сторон, с интервалом не менее 30 дней), по поводу которых было произведено, в общей сложности, 24 многоуровневых оперативных вмешательства. С точки зрения двигательных возможностей по GMFCS пациенты относились к IV уровню в 12 случаях и к V уровню в 2 случаях. В таблице 1 представлены элементы оперативного вмешательства, выполненные у пациентов в различных группах.
Все пациенты в зависимости от вида послеоперационной седатации в отделении реанимации и интенсивной терапии были разделены на 3 группы, сопоставимые между собой по возрасту, полу и объему хирургического вмешательства. В группе 1 седатация в послеоперационном периоде не проводилась, в группе 2 осуществлялась дексмедетомидином, в группе 3 – мидазоламом. Средний вес по группам составлял 18 кг, 16,25 кг и 14,75 кг соответственно. Возраст на момент вмешательства варьировал от 4 до 12 лет, составляя в среднем 7,1 года для первой группы, 7,6 года – для второй и 7,1 – для третьей. Рандомизацию на группы проводили методом таблицы случайных чисел. Оценка глубины седатации, а также эффективность аналгезии проводилась четырехкратно за сутки: через 2, 6, 10, 18 часов после оперативного вмешательства.
Операционно-анестезиологический риск по классификации американской ассоциации анестезиологов (ASA) у 11 пациентов соответствовал 2 классу, у 3 пациентов 3 классу.
В группе 1 дети были оперированы под общей анестезией с ИВЛ в сочетании с эпидуральной аналгезией ропивокаином 0,5 % в дозе 2 мг/кг, введенным через эпидуральный катетер диаметром G19, установленный на уровне дерматома, соответствующего операции [6, 7]. Использовался набор препаратов, дозы которых рассчитывались, исходя из массы тела: пропофол, фентанил, рокурония бромид, севоран. Фентанил вводился однократно, только на момент интубации трахеи. По окончании операции всех пациентов будили на операционном столе и переводили в отделение реанимации и интенсивной терапии. Послеоперационное обезболивание в ОРИТ проводилось посредством введения в эпидуральное пространство через катетер ропивокаина 0,2 % в дозировке 0,3 мг/кг/час с помощью эластомерной помпы или дозатора для микроструйного введения лекарств [8, 10-12]. Седатация не проводилась.
В группе 2 анестезиологическое пособие при оперативных вмешательствах и послеоперационное обезболивание было идентичным группе 1. Седатация в раннем послеоперационном периоде в отделении реанимации и интенсивной терапии проводилась дексмедетомидином
20 % путем внутривенного введения раствора (200 мкг дексмедетомидина, разведенного в 38 мл физиологического раствора) с помощью микроструйного дозатора со скоростью 0,4 мкг/кг/час [9, 13, 14]. Дексмедетомидин (дексдор) является селективным агонистом α2-адренорецепторов с широким спектром фармакологических свойств. Обладает симпатолитическим эффектом, реализующимся за счет снижения высвобождения норадреналина симпатическими нервными окончаниями. Седативный эффект опосредован снижением возбуждения в голубоватом месте – ядре с преобладанием норадренергических нейронов, расположенном в стволе головного мозга.
В группе 3 также интраоперационное и послеоперационное обезболивание было подобно обезболиванию пациентов 1-й и 2-й групп. Седатация в раннем послеоперационном периоде в отделении реанимации и интенсивной терапии проводилась мидазоламом 0,5 % путем внутривенного введения раствора (5 мг мидазолама, разведенного в 19 мл физиологического раствора) с помощью микроструйного дозатора со скоростью 0,04 мг/кг/час [15]. Мидазолам – это бензодиазепин короткого действия, стимулирующий ионотропные рецепторы ГАМК, расположенные в центральной нервной системе. Мидазолам (дормикум) связывается с рецепторами бензодиазепинов на каналах для ионов хлора, что приводит к активации рецептора ГАМК и снижению возбудимости подкорковых структур головного мозга. Вследствие этого мидазолам оказывает седативное и снотворное действие, а также анксиолитическое, противосудорожное и центральное миорелаксирующее действие.
Добровольное письменное согласие на седатацию дексмедетомидином или мидазоламом в раннем послеоперационном периоде в отделении реанимации и интенсивной терапии от родителей или официальных опекунов получено.
Кроме того, у больных всех групп в динамике контролировали ЧСС, АД, SpO2, показатели крови.
Для оценки послеоперационной аналгезии использовали рейтинговую шкалу оценки боли по изображению лица Вонга-Бейкера для детей старше 3 лет, объективную шкалу боли Hanallah и соавторов для оценки послеоперационной боли, шкалу боли Riley [16, 17, 18]. Для оценки степени седации в раннем послеоперационном периоде использовали шкалу Ramsay, шкалу оценки возбуждения – седатации Richmond [19, 20, 21]. Все исследования по шкалам проводили через 2, 6, 10 и 18 часов после операции – в период пребывания ребенка в отделении реанимации и интенсивной терапии.
Статистические исследования проводились с применением программы Attestat®. Для описательной статистики были определены средние значения показателей и их стандартные отклонения. Сравнение между выборками осуществлялось с применением критериев Стьюдента и Манна-Уитни.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Во всех группах в послеоперационном периоде средний объем инфузионно-трансфузионных средств составил 1018,4±180 мл. Дренажная кровопотеря была в среднем 103,3±23,96 мл. В течение 1-х суток послеоперационного периода больные получали стандартную инфузионную терапию, в состав которой входили кристаллоидные растворы, коллоидные препараты. Донорскую эритроцитарную массу применяли у 3 больных. Судя по диурезу и ЦВД, значимой гиповолемии, которая могла бы влиять на показатели гемодинамики, у детей в 1-е сутки после операции не было.
В 1-й группе у детей после пробуждения и на всем протяжении до конца нахождения в ОРИТ был достоверно учащен пульс: ЧСС через 2 часа – 123±16,5 в ми- нуту, через 6 часов – 116±20 в минуту, через 10 часов – 112,6±11,8 в минуту, через 18 часов – 119,6±14 в минуту. Средние значения АД составили: через 2 часа САД – 130±0,08 мм рт. ст., ДАД – 71,3±9,8 мм рт. ст., через 6 часов САД – 134,3±12,1 мм рт. ст., ДАД – 66,7±5,7 мм рт. ст., через 10 часов САД – 131,3±11,6 мм рт. ст., ДАД – 68±7,2 мм рт. ст., через 18 часов САД – 136,3 мм рт. ст., ДАД – 74,3±5,1 мм рт. ст.
Интенсивность боли по шкале Вонга-Бейкера составила: через 2 часа – 0,75±0,7 балла, через 6 часов – 0,75±0,7 балла, через 10 часов – 0,5±0,5 балла, через 18 часов – 0,87±0,35 балла; по шкале Riley – 3,75±2,54 балла, 3,12±2,1 балла, 3,71±2,56 балла, 1,87±1,8 балла и по шкале Hanallah – 2±1,19 балла, 1,6±1,18 балла, 1,25±0,7 балла, 1,12±0,6 балла соответственно, что расценивалось как отсутствие боли или незначительная болезненность.
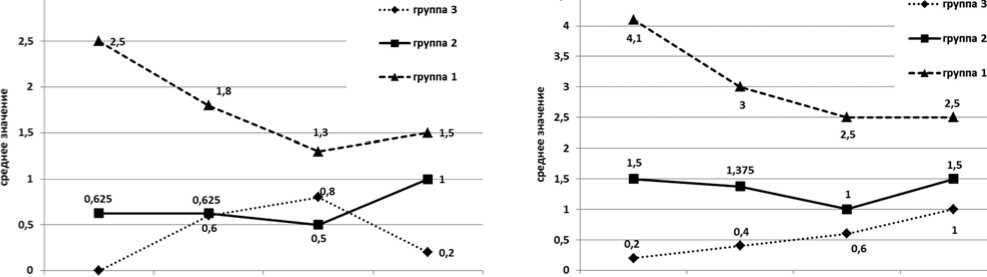
У пациентов 2-й группы, у которых седатация обеспечивалась дексмедетомидином, не наблюдалось учащения пульса (табл. 1) по отношению к первой группе, а показатели артериального давления не увеличивались. При оценке боли получены следующие результаты: по шкале Вонга-Бейкера через 2 часа – 0,5±0,75 балла, через 6 часов – 0,25±0,46 балла, через 10 часов – 0,25±0,46 балла, через 18 часов – 0,5±0,75 балла; по шкале Riley (рис. 1) – 1,5±1,5 балла, 1,37±1,3 балла, 1±1,19 балла, 1,5±1,41 балла; по шкале Hanallah (рис. 2) – 0,63±0,9 балла, 0,63±0,9 балла, 0,5±0,75 балла, 0,75±1,16 балла, что интерпретировалось как полное отсутствие боли.
В 3-й группе пациентов, седатированных мидазоламом, отмечено также достоверное снижение ЧСС, САД и ДАД по отношению к контрольной группе, но менее выраженное по отношению ко 2-й группе (табл. 2). При оценке боли по шкалам получены следующие результаты: по шкале Вонга-Бейкера 0 баллов за все время наблюдения, по шкале Riley через 2 часа – 0,13±0,35 балла, через 6 часов – 0,25±0,7 балла, через 10 часов – 0,63±0,91 балла, через 18 часов – 0,63±1,76 балла; по шкале Hanallah – 0 баллов, 0,63±0,91 балла, 1±1,06 балла, 0,13±0,35 балла, что соответствует полному отсутствию боли.
Таблица 1
Показатели гемодинамики в раннем послеоперационном периоде в исследуемых группах
|
Время |
Группа |
САД мм рт. ст. |
ДАД мм рт. ст. |
ЧСС в мин. |
|
Через 2 часа |
1 группа |
130,3±0,08 |
71,3±9,8 |
123±16,5 |
|
2 группа |
110,8±4,4 |
67,7±11,09 |
101,5±17,1 |
|
|
3 группа |
107,4±9,5 |
63,2±15,6 |
118±9,9 |
|
|
Через 6 часов |
1 группа |
134,3±12,1 |
66,7±5,7 |
116±20 |
|
2 группа |
100,4±12,7 |
55±8,2 |
93,1±11,6 |
|
|
3 группа |
107,4±14,05 |
67,4±13,1 |
119±13,1 |
|
|
Через 10 часов |
1 группа |
131,3±11,6 |
68±7,2 |
112,6±11,8 |
|
2 группа |
104,3±17,4 |
56,7±8.7 |
93,7±14,4 |
|
|
3 группа |
106,4±14,2 |
57,8±9,4 |
115,4±14,05 |
|
|
Через 18 часов |
1 группа |
136,3±10 |
74,3±5,1 |
119,6±14 |
|
2 группа |
98,6±8,2 |
54±9,4 |
101,1±10,6 |
|
|
3 группа |
107,2±9,5 |
70,2±10,8 |
120,6±4,7 |
Таблица 2
Элементы оперативных вмешательств
|
Элемент вмешательства |
Группа 1 |
Группа 2 |
Группа 3 |
|
Деротационно-варизирующая остеотомия бедра |
8 |
8 |
8 |
|
Ацетабулопластика |
3 |
3 |
4 |
|
Теномиотомия аддукторов |
6 |
7 |
6 |
|
Удлинение сгибателей коленного сустава |
4 |
5 |
5 |
|
Низведение надколенника |
4 |
4 |
5 |
|
Апоневротомия икроножных мышц |
7 |
6 |
6 |
|
Пересадка сухожилий на стопе |
3 |
2 |
3 |
|
Артроэрез по Grice |
3 |
2 |
2 |
|
Подтаранный артродез |
0 |
2 |
0 |
|
Коррекция hallux valgus |
0 |
2 |
0 |
S т------------------------------------------------------------ 4,5
Через 2 часа Через 6 часов Через 10 часов Через 18 часов Через 2 часа Через 6 часов Через 10 часов Через 18 часов
Рис. 1. Оценка болевого синдрома по шкале Hanallah Рис. 2. Оценка болевого синдрома по шкале Riley
После перевода из операционной в отделение реанимации и интенсивной терапии параллельно с оценкой боли проводилась оценка степени седатации. Балльная оценка седатации с динамикой по времени для каждой группы представлена в таблице 3.
В группе 1 пациенты за весь период наблюдения бодрствовали, были беспокойны, взволнованны. За время нахождения в ОРИТ пациенты группы 2 были сонливы, не полностью бдительны, реагировали открыванием глаз на голос. В третьей группе все пациенты находились в состоянии легкой седатации, дремали, но реагировали на прикосновение или громкий звук. В группах 2 и 3 в период через 2, 6 и 10 часов после операции уровень седатации был достоверно выше, чем в контрольной группе. В более позднее время (18 часов после операции) не было различий по уровню седатации между первой и второй группой при оценке по шкале Richmond и первой и третьей группой – по шкале Ramsay (табл. 3).
Таблица 3
Изменения оценки степени седатации в раннем послеоперационном периоде в группах
|
Группа |
2 часа |
6 часов |
10 часов |
18 часов |
||||
|
Шкала Ramsay |
Шкала Richmond |
Шкала Ramsay |
Шкала Richmond |
Шкала Ramsay |
Шкала Richmond |
Шкала Ramsay |
Шкала Richmond |
|
|
Группа 1 |
1,8±0,46 |
0,6±0,74 |
1,9±0,83 |
0,0±0,53 |
2,3±1,04 |
0,4±0,52 |
2,4±1,06 |
-0,5±0,93 |
|
Группа 2 |
3,8±0,461sw |
-1,5±0,761sw |
3,9±0,351sw |
-1,8±0,461sw |
3,5±1,071sw |
-1,8±0,461sw |
3,5±0,761sw |
-1,5±1,20 |
|
Группа 3 |
4,0±0,761sw |
-2,1±0,831sw |
3,3±1,491s |
-1,9±0,831sw |
4,0±1,411sw |
-2,4±0,741sw |
3,5±1,19 |
-1,9±0,831sw |
Примечание: 1 – достоверная разница с группой 1 (p<0,05), S – достоверная разница по критерию Стьюдента, w – достоверная разница по критерию Манна-Уитни.
ДИСКУССИЯ
Реконструктивные оперативные вмешательства при подвывихах и вывихах бедра у детей с тяжелыми формами детского церебрального спастического паралича являются необходимостью и имеют целью предотвратить раннее развитие коксартроза, протекающего со значительным болевым синдромом, облегчить уход за ребенком, улучшить или создать условия для возможности сидения и вертикали-зации такого пациента, ликвидировать неудобства укладки пациента, ведущие часто к трофическим нарушениям, а в некоторых случаях – вернуть ребенку способность самостоятельно передвигаться с использованием вспомогательных средств [22, 23]. Столь сложные и травматичные вмешательства выполняются, как правило, у детей, имеющих ряд сопутствующих хронических заболеваний внутренних органов, что требует поиска путей снижения тяжести оперативного вмешательства и оптимизации анестезиологического пособия, а также седатации в раннем послеоперационном периоде [2, 5, 24, 25]. Особенно это необходимо при выполнении одномоментных многоуровневых оперативных вмешательств у детей с тяжелыми формами спастического паралича (SEMLS – single-event multilevel ortopaedic surgery), подразумевающих две и более хирургических процедуры на сухожильно-мышечном аппарате и/или костях двух и более анатомических областей во время одного оперативного вмешательства, одной госпитализации, сопровождающейся одним ранним реабилитационным периодом [26, 27]. Проведение адекватной седа-тации в раннем послеоперационном периоде способствует уменьшению спастичности у детей с церебральным параличом, что, в свою очередь, способствует снижению болевого синдрома и обеспечивает раннее начало реабилитационных мероприятий, являющихся основополагающим нехирургическим компонентом системы многоуровневых одномоментных оперативных вмешательств у пациентов с ДЦП [22, 26, 27].
Целью седативной терапии в ОРИТ является обеспечение физического и психологического комфорта [28, 29, 30]. Психомоторное возбуждение у детей с тяжелыми нарушениями психического развития при отсутствии или недостаточной седатации осложняет ранний послеоперационный период, увеличивает риск самопроизвольного удаления катетеров, дренажей и подвергает непосредственной опасности самих пациентов [17, 30]. Наконец, недостаточная седатация может оставить у пациентов стойкие травмирующие воспоминания о пребывании в ОРИТ [13].
Ранее проведенные исследования показали эффективность дексмедетомидина и мидазолама с точки зрения проведения седативной терапии в раннем послеоперационном периоде у кардиохирургических пациентов [14].
В нашем исследовании мы также обнаружили достоверно высокий уровень седатации у данной категории пациентов после выполнения объемных оперативных вмешательств. Применяемые при исследовании дексмедетомидин и мидазолам обеспечивали необходимую степень седатации при минимальных эффективных дозировках в условиях продленной эпидуральной аналгезии.
С другой стороны, в нашей серии не удалось выявить различий в седативном эффекте между исследуемыми препаратами. В группах 2 и 3 была достигнута легкая или умеренная степень седации у детей с ДЦП на протяжении раннего послеоперационного периода.
Важно отметить, что ни у одного из пациентов, получавших дексмедетомидин и мидазолам в описанных выше дозировках в раннем послеоперационном периоде через микроструйный дозатор, не выявлено эпизодов угнетения дыхания, не получено каких-либо значимых осложнений в виде гипотонии или брадикардии.
ВЫВОДЫ
-
1. Дексмедетомидин и мидазолам являются эффективными препаратами, используемыми для достижения легкой или средней степеней седатации в ОРИТ у
- детей с ДЦП после многоуровневых одномоментных оперативных ортопедических вмешательств.
-
2. В нашем исследовании достоверных преимуществ
-
3. Оба препарата могут быть использованы для се-
- датации детей со спастическими формами ДЦП сразу же после перевода из операционной в ОРИТ в раннем послеоперационном периоде.
между дексмедетомидином и мидазоламом в достижении поверхностной седатации у детей с ДЦП не выявлено.
Список литературы Оценка эффективности седатации у детей с ДЦП в раннем послеоперационном периоде после многоуровневых одномоментных оперативных ортопедических вмешательств
- Development and reliability of a system to classify gross motor function in children with cerebral palsy/R. Palisano, P. Rosenbaum, S. Walter, D. Russell, E. Wood, B. Galuppi//Dev. Med. Child.Neurol. 1997. Vol. 39, No 4. P. 214-223.
- Irgens L.M. The Medical Birth Registry of Norway. Epidemiological research and surveillance throughout 30 years//Acta Obstet. Gynecol. Scand. 2000. Vol. 79, No 6. P. 435-439.
- Long term follow-up after one-stage reconstruction of dislocated hips in patients with cerebral palsy/W.N. Sankar, D.A. Spiegel, J.R. Gregg, B.J. Sennett//J. Pediatr. Orthop. 2006. Vol. 26, No 1. P. 1-7.
- McNerney N.P., Mubarak S.J., Wenger D.R. One-stage correction of the dysplastic hip in cerebral palsy with the San Diego acetabuloplasty: results and complications in 104 hips//J. Pediatr. Orthop. 2000. Vol. 20, No 1. P. 93-103.
- Попков Д.А., Попков А.В., Аранович А.М. Сравнительное исследование результатов реконструктивных вмешательств на 45 тазобедренных суставах у 25 детей со спастическим церебральным параличом//Гений ортопедии. 2013. № 1. С. 48-54.
- Осипова Н.А. Антиноцицептивные компоненты общей анестезии и послеоперационной анальгезии//Анестезиология и реаниматология. 1998. № 5. С. 11-15.
- Diordiev A.V., Aizenberg V.L. Peripheral regional block role in orthopedics in pediatric patients with cerebral palsy//Anesteziol. Reanimatol. 2013. No 1. P. 45-48.
- Гельфанд Б.Р., Кириенко П.А., Черненко Л.Ю. Постоперационное обезболивание//Рус. мед. журн. 2003. № 12. С. 707-713.
- Козлов И.А. Агонист альфа 2 адренорецепторов дексмедетомидин в практике современной седации//Общая реаниматология. 2013. № 2. С. 55-65.
- Овечкин А.М., Морозов Д.В., Жарков И.П. Контролируемое обезболивание и седация в послеоперационном периоде: реалии и возможности//Вестн. интенсив. терапии. 2012. № 4. С. 1-12.
- Буров Н.Е. Послеоперационное обезболивание//Рус. мед. журн. 2003. № 21. С. 1172-1177.
- Effectiveness of an anesthetic continuous-infusion device in children with cerebral palsy undergoing orthopaedic surgery/K. Muthusamy, S.M. Recktenwall, R.M. Friesen, J. Zuk, J. Gralla, N.H. Miller, J.L. Galinkin, F.M. Chang//J. Pediatr. Orthop. 2010. Vol. 30, No 8. P. 840-845.
- Keating G.M., Hoy S.M., Lyseng-Williamson K.A. Dexmedetomidine: a guide to its use for sedation in the US//Clin. Drug Investig. 2012. Vol. 32, No 8. P. 561-567.
- Еременко А.А., Чернова Е.В. Применение дексмедетомидина для внутривеннойседации и лечения делирия в раннем послеоперационном периоде у кардиохирургических пациентов//Анестезиология и реаниматология. 2013. № 5. С. 4-7.
- A pharmacokinetic study of midazolam in paediatric patients undergoing cardiac surgery/H.M. Mathews, I.W. Carson, S.M. Lyons, I.A. Orr, P.S. Collier, P.J. Howard, J.W. Dundee//Br. J. Anaesth. 1988. Vol. 61, No 3. P. 302-307.
- Wong’s Essentials of Pediatric Nursing/D.L. Wong, M. Hockenberry-Eaton, D. Wilson, M.L. Winkelstein, P. Schwartz. 6th ed. St. Louis: Mosby Inc., 2001. P. 1301.
- Comparison of caudal and ilioinguinal/iliohypogastric nerve blocks for control of post-orchiopexy pain in pediatric ambulatory surgery/R.S. Hanallah, L.M. Broadman, A.B. Belman, M.D. Abramowitz, B.S. Epstein//Anesthesiology.1987. Vol. 66, No 6. P. 832-834.
- Reliability and validity of preverbal pain assessment tools/B.A. Joyce, J.G. Schade, J.F. Keck, J. Gerkensmeyer, T. Raftery, S. Moser, G. Huster//Issues Compr. Pediatr. Nurs.1994. Vol. 17, No 3. P. 121-135.
- Controlled sedation with alphaxalone-alphadolone/M.A. Ramsay, T.M. Savege, B.R. Simpson, R. Goodwin//Br. Med. J. 1974. Vol. 2, No 5920. P. 656-659.
- The Richmond Agitation-Sedation Scale: validity and reliability in adult intensive care unit patients/C.N. Sessler, M.S. Gosnell, M.J. Grap, G.M. Brophy, P.V. O’Neal, K.A. Keane, E.P. Tesoro, R.K. Elswick//Am. J. Respir. Crit. Care Med. 2002. Vol. 166, No 10. P. 1338-1344.
- Monitoring sedation status over time in ICU patients: reliability and validity of the Richmond Agitation-Sedation Scale (RASS)/E.W. Ely, B. Truman, A. Shintani, J.W. Thomason, A.P. Wheeler, S. Gordon, J. Francis, T. Speroff, S. Gautam, R. Margolin, C.N. Sessler, R.S. Dittus, G.R. Bernard//JAMA. 2003. Vol. 289, No 22. P. 2983-2991.
- Krebs A., Strobl W.M., Grill F. Neurogenic hip dislocation in cerebral palsy: quality of life and results after hip reconstruction//J. Child. Orthop. 2008. Vol. 2, No 2. P. 125-131.
- Popkov D., Journeau P., Popkov A. Comparative study on results of reconstructive surgery in 45 hip joints of 25 children with cerebral palsy//Eur. Orthop. Traumatol. 2014. Vol. 5, No 1. P. 57-63.
- Bladder and bowel control in children with cerebral palsy: case-control study/M. Ozturk, F. Oktem, N. Kisioglu, M. Demirci, I. Altuntas, S. Kutluhan, M. Dogan//Croat. Med. J. 2006. Vol. 47, No 2. P. 264-270.
- Burns A.M., Shelly M.P., Park G.R. The use of sedative agents in critically ill patients//Drugs. 1992. Vol. 43, No 4. P. 507-515.
- Результаты многоуровневых одномоментных оперативных вмешательств у пациентов с детским церебральным параличом/А.М. Аранович, А.В. Попков, А.А. Щукин, С.Н. Медведева, В.В. Евреинов, А.Н. Третьякова, А.Г. Третьякова, А.Г. Зыков, О.В. Климов, Э.М. Парфенов, P. Lascombes, Д.А. Попков//Гений ортопедии. 2013. № 4. С. 53-59.
- Single-event multilevel surgery for children with cerebral palsy: a systematic review/J.L. McGinley, F. Dobson, R. Ganeshalingam, B.J. Shore, E. Rutz, H.K. Graham//Dev. Med. Child. Neurol. 2012. Vol. 54, No 2. P. 117-128.
- Козлов И.А. Современные подходы к седации в отделениях реанимации и интенсивной терапии//Неотложная медицина. 2013. № 1. С. 22-31.
- Riker R.R., Fraser G.L. Adverse events associated with sedatives, analgesics, and other drugs that provide patient comfort in the intensive care unit//Pharmacotherapy. 2005. Vol. 25, No 5. Pt. 2. P. 8S-18S.
- Dexmedetomidine vs midazolam for sedation of critically ill patients: a randomized trial/R.R. Riker, Y. Shehabi, P.M. Bokesch, D. Ceraso, W. Wisemandle, F. Koura, P. Whitten, B.D. Margolis, D.W. Byrne, E.W. Ely, M.G. Rocha; SEDCOM (Safety and Efficacy of Dexmedetomidine Compared with Midazolam) Study Group//JAMA. 2009. Vol. 301, No 5. P. 489-499.


