Оценка экспрессии PD-l1 у пациентов с уротелиальным раком, имеющих противопоказания к назначению препаратов платины
Автор: Завалишина Л.Э., Повилайтите П.Е., Раскин Г.А., Андреева Ю.Ю., Петров А.В., Харитонова Е.А., Пугач И.М., Франк Г.А., Румянцев А.А., Тимофеев И.В., Тюляндин С.А.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Собственные исследования
Статья в выпуске: 1 т.9, 2019 года.
Бесплатный доступ
Введение. Уротелиальный рак во всем мире находится на 7 и 17 местах среди всех злокачественных опухолей у мужчин и женщин соответственно. Появление новых иммунотерапевтических препаратов открывает новые возможности для лечения таких пациентов, особенно учитывая группу пациентов, имеющих противопоказания к назначению препаратов платины. Применение иммуноонкологических препаратов требует определения экспрессии PD-L1, для которого используются различные диагностические системы. Актуальным является вопрос о сопоставлении результатов определения экспрессии PD-L1 разными методами. Материалы и методы. Исследования проведено на 100 образцах операционного и биопсийного материала уротелиального рака. Для исследования были использованы два клона антител 22C3 и SP142 с соответствующими системами детекции. Оценивалась экспрессия PD-L1 в опухолевых и иммунных клетках. Результаты. Исследование показало высокое совпадение негативного PD-L1 статуса опухоли, выявленного при использовании обоих диагностикумов (92% и 97%) и низкое совпадение результатов по позитивному PD-L1 статусу (67% и 43%)...
Уротелиальный рак, оценка экспрессии pd-l1, ингибиторы контрольных точек, непереносимость препаратов платины
Короткий адрес: https://sciup.org/140243808
IDR: 140243808
Assessment of PD-l1 expression in patients with urothelial cancer with contraindications to platinum-based therapy
Background. Urothelial cancer ranks 7th and 17th of all the malignant tumors in males and females, respectively. Development of new immunotherapeutic drugs provides new possibilities in treatment of such patients, especially the patient population in whom platinum-based therapy is contraindicated. Administration of immunooncology drugs requires determination of PD-L1, for which various diagnostic systems are used. The question regarding correlation of results of determination of PD-L1 expression remains of concern. Materials and Methods. The study was performed on 100 samples of surgical and biopsy samples of urothelial cancer. Two clones of 22C3 and SP142 with corresponding detection systems were used for the study. PD-L1 expression was assessed in tumor and immune cells. Results. The study demonstrated a high correlation of negative PD-L1 tumor status determined using both diagnostic agents (92 % and 97 %) and low correlation of results of positive PD-L1 status (67 % and 43 %). Conclusions. Thus, if a negative result of PD-L1 status of urothelial cancer is obtained using any of the diagnostic agents studied, repeated test with the other antibody is not required. If positive status is obtained in one test, the patient may have a negative status in the other test, which allows recommending a repeated testing in borderline cases using a test, recommended for the medicinal product untended for treatment.
Текст научной статьи Оценка экспрессии PD-l1 у пациентов с уротелиальным раком, имеющих противопоказания к назначению препаратов платины
Уротелиальный рак мочевого пузыря во всем мире находится на 7 и 17-м местах среди всех злокачественных новообразований у мужчин и женщин соответственно. С каждым годом частота встречаемости данного злокачественного новообразования в российской популяции возрастает. Выбор вариантов лечения метастатического уротелиального рака, характеризующегося плохим прогнозом, до последних лет был весьма ограничен. Большой проблемой терапии уротелиального рака является также и то, что более 50% пациентов с прогрессирующей уротелиальной карциномой не могут получить высокотоксичную химиотерапию на основе цисплатина в качестве терапии первой линии из-за неудовлетворительного состояния и сопутствующих заболеваний [1]. Замена цисплатина карбоплатином не дает желаемого увеличения эффективности, и, кроме того, 20% больных не могут получить или прерывают лечение карбоплатином [2]. Новым подходом к терапии этих злокачественных опухолей стала разработка новых подходов, а именно иммунотерапия, т.е. применение ряда препаратов, влияющих на ключевые точки противоопухолевого иммунитета. Опухолевые клетки умеют уклоняться от иммунной системы организма с помощью различных механизмов, в том числе путем гиперэкспрессии лиганда программированной клеточной смерти PD-L1. Этот процесс как на опухолевых клетках, так и на иммунных клетках микроокружения в различных типах рака, в том числе и в уротелиальном.
Атезолизумаб — первый ингибитор контрольных точек, одобренный для лечения пациентов с местно-распространенным или метастатическим уротелиальным раком после прогрессирования на платиносодержащей химиотерапии. Одобрение атезолизумаба в первой линии терапии больных, которые не подлежат лечению цисплатином, было основано на результатах крупного исследования II фазы IMvigor211, в котором принимали участие 123 пациента из 47 исследовательских центров [3]. Атезолизумаб применяли в стандартной схеме (1200 мг внутривенно каждый 21 день до прогрессирования). Основной конечной точкой, оцениваемой в исследовании, была объективная частота ответа, как во всей популяции больных, так и у пациентов с экспрессией PD-L1. Медиана наблюдения составила 17,2 месяца. Оцененная объективная частота ответа 23% во всей популяции и 28% у пациентов с выраженной экспрессией PD-L1 достоверно превышала исторический контроль. Ответы были долговременными; медиана продолжитель- ности ответа не была достигнута. Медиана общей выживаемости составила 15,9 месяцев [4].
В этом исследовании PD-L1 положительный статус опухоли определяли как наличие 5% и более окрашенных иммунных клеток, инфильтрирующих опухоль. Определение экспрессии PD-L1 проводилось иммуногистохимическим методом с помощью моноклональных антител SP142 (Ventana). Для оценки биомаркеров использовались архивные парафиновые блоки ткани опухоли, фиксированной формалином.
Вторым иммуноонкологическим препаратом, который применяется для терапии этой группы пациентов, стал пембролизумаб [4]. Решение об ускоренном одобрении пембролизумаба в качестве терапии первой линии было принято более года назад на основе результатов 2 фазы клинического исследования KEYNOTE-052 [4]. В нём участвовали 370 пациентов, которым невозможно было назначить лечение на основе цисплатина. Все пациенты получали пембролизумаб (200 мг, внутривенное введение каждые 3 недели). Основной конечной точкой была скорость объективного ответа. При медиане наблюдения 11,5 месяцев показатель объективного ответа составил 28,9%, медиана продолжительности ответа не была достигнута [5]. Медиана общей выживаемости от начала назначения пембролизумаба составила 11,5 месяцев, показатели 6 — и 12-месячной общей выживаемости оказались 67.2% и 47,5% соответственно. PD-L1 в сочетании с положительной оценкой в 10% и более ассоциировался с более высокой частотой ответов (47,3%) и лучшей общей выживаемостью (18,5 месяцев). Частота ответов была существенно выше у пациентов с экспрессией PD-L1 и составила 39%.
В данном исследовании PD-L1- положительный статус опухоли определялся как процентное содержание клеток (опухолевых клеток, макрофагов или лимфоцитов), экспрессирующих PD-L1 в биопсии опухоли в 10% и более. Определение проводилось иммуногистохимическим методом с помощью клона моноклональных антител 22C3 (Agilent Technologies) на тканях, фиксированных формалином и залитых в парафин. Использовался закрытый набор для фармакодиагностики PD-L1 IHC 22C3 PharmDx (Dako, Inc.)
Замена химиотерапии ингибиторами контрольных точек прошла всесторонне успешно. В исследованиях IMvigor210 и KEYNOTE-052 только 8% и 5% пациентов прекратили лечение атезолизумабом и пембролизумабом, соответственно, из-за неприемлемой токсичности. Частота серьезных нежелательных явлений составила 16% для обоих препаратов. Помимо снижения токсичности, применение атезолизумаба и пембролизумаба позволило повысить эффективность за счет увеличения скорости ответа в два раза по сравнению с химиотерапией у всех больных, а у пациентов с наличием позитивного PD-L1 статуса опухоли — в 3 раза. Таким образом, результаты этих клинических исследований показали, что больные, которые ранее не могли получать лечение, теперь получили более эффективную возможность терапии.
Однако эти исследования продемонстрировали и объективные трудности при тестировании статуса PD-L1 у больных уротелиальным раком, которые возникали из-за наличия различных диагностических и аналитических систем, а также инструментальных платформ, на которых проводятся исследования. Кроме того, для различных клонов антител (22С3 и SP142) существуют разные пороговые значения (cut-off) и способы оценки наличия положительной реакции, разработанные производителями диагностических наборов. Не решен однозначно вопрос и о том, в каких клетках необходимо оценивать экспрессию PD-L1 — только в опухолевых (ОК), только в иммунных (ИК), или и в ОК, и в ИК. Рекомендации производителей строго регламентируют применение одного конкретного диагностикума для конкретного лекар- ственного препарата. Поэтому вопрос гармонизации результатов при использовании различных диагностических систем остаётся крайне актуальным, особенно с учетом того, что исследования по гармонизации использования различных диагностических тестов проведены в основном для немелкоклеточного рака легкого, а для уротелиального рака такие исследования немногочисленны и проведены на ограниченных выборках. В настоящее время во многих отделениях патологической анатомии в России имеются в наличии не все автоматизированные платформы и реагенты для in vitro диагностики, а использование всех диагностикумов для каждого случая является финансово затратным. Отсутствие единой методики определения рецептора PD-L1 усложняет процесс отбора пациентов для иммунотерапии уротелиального рака. Отсутствие единых диагностических рекомендаций может отрицательно влиять на выбор терапии и как следствие — на эффективность лечения и выживаемость пациентов. Таким образом, правильная диагностика и, следовательно, правильная терапия не только влияют на эффективность лечения, но и на снижение стоимости лечения. Поэтому актуальным остается вопрос о сопоставлении результатов, полученных с помощью различных диагностикумов, инструментов и систем оценки результатов.
Задачей многоцентрового совместного исследования, проведенного Российским обществом клинической онкологии (RUSSCO) и Российским обществом патологоанатомов, являлось сравнение результатов иммуногистохимической оценки экспрессии PD-L1 опухолевыми и иммунными клетками при использовании диагностических систем (22С3 и SP142) двух производителей (Agilent Technologies и Ventana), применение различных систем оценки результатов тестирования, изучение сопоставимости результатов количественной оценки экспрессии PD-L1 статуса опухоли при использовании различных пороговых значений положительного статуса [6]. В связи с наличием различных cut-off, принятых в настоящее время, и с появлением результатов новых клинических исследований, возможно изменение ныне существующих критериев оценки, поэтому определение фактического количества позитивно окрашенных ОК и ИК с помощью 2 исследуемых антител является актуальной задачей данного исследования.
Материалы и методы
Материалом для исследования послужили 100 образцов операционного и биопсийного материала уротелиального рака мочевого пузыря, предоставленных кафедрой патологической анатомии РМАНПО (60 случаев) и Ростовского патологоанатомического бюро (40 случаев). Пациенты были преимущественно мужского пола (89%), средний возраст — 63 года (29–87 лет), стадия Т1–45% (45/100), Т2–45% (45/100), по степени дифференцировки опухоли в 47% случаев (47/100) были высокодифференцированными (High Grade). Все парафиновые блоки содержали достаточное количество материала для исследования экспрессии белка 2 антителами с использованием как позитивного, так и негативного контролей.
Исследование проводилось иммуногистохимическим методом с использованием набора PD-L1 IHC 22C3 PharmDx (Dako, Inc.) и антител PD-L1 SP142 с системой детекции OptiView DAB IHC Detection Kit c амплификацией сигнала (Ventana Medical Systems, Inc.). С каждого образца опухоли делали по 2 среза для исследования и контрольные срезы для негативного контроля. В качестве контроля применяли стекла c образцами клеточных культур (NCL-H226-позитивная клеточная линия и MCF-7 — негативная клеточная линия), образцы ткани миндалины (для 22С3 и SP142) и плаценты (для SP142) в каждом цикле постановки реакции. Для всех антител применялся автоматизированный метод иммуногистохимического исследования, для 22С3 исследование проводилось на автостейнере Avtostainer Link 48 (ASL48) (Dako, Inc.) с использованием оптимизированного закрытого протокола, заложенного в автоматизированную платформу. Для постановки реакции с антителом SP142 (Ventana Medical Systems, Inc.) использовался иммуногистостейнер VENTANA BenchMark ULTRA (Ventana Medical Systems, Inc.) по протоколам, рекомендованным в инструкциях к антителам и системой внешнего контроля качества NordiQC.
На первом этапе анализа оценивалась правильность окрашивания позитивных и негативных клеточных линий и позитивного тканевого контроля (ткань миндалины и плаценты). Затем проводили оценку иммуногистохимических реакций на образцах уротелиального рака. Для каждого антитела наличие фактической иммуногистохимической реакции как в ОК, так и в ИК оценивали визуально (Manual Scoring), а также оценивали PD-L1 статус опухоли по пороговым значениям (cut-off), рекомендованным в настоящее время для рака мочевого пузыря: 22С3: отношение ОК+ИК, экспрессирующих PD-L1, ко всем клеткам в образце ≥10%, а для SP142: ИК≥5%. Также для каждого из антител применяли точки отсечения в 1%, 10%, 25% и 50% для ОК и ИК.
В соответствии с рекомендациями по оценке результатов экспрессии PD-L1 оценивалось только наличие мембранного окрашивания в опухолевых и иммунных клетках независимо от его интенсивности.
Все полученные препараты анализировались визуально независимо друг от друга 4 патоморфологами и затем сканировались для создания цифрового архива изображений. При расхождении в оценке препаратов специалисты принимали консенсусное решение.
Все полученные результаты были подвергнуты статистической обработке с определением корреляционных коэффициентов Пирсона.
Результаты
В результате иммуногистохимического исследования было получено 200 препаратов с иммуногистохимическими реакциями с 2 антителами 22C3 и SP142.
При использовании cut-off в 1% экспрессии на ОК было выявлено 22 позитивных образца (78 — негативных) при использовании антитела 22C3 и 8 позитивных образцов (92 — негативных) при использовании антитела SP142. При использовании более высоких значений cut-off (10, 25 и 50%) все антитела выявляли 6–7% положительных образцов (6 — SP142, 7–22C3), кроме того, уменьшалось число позитивных образцов при cut-off25 и 50% до 4–5%.
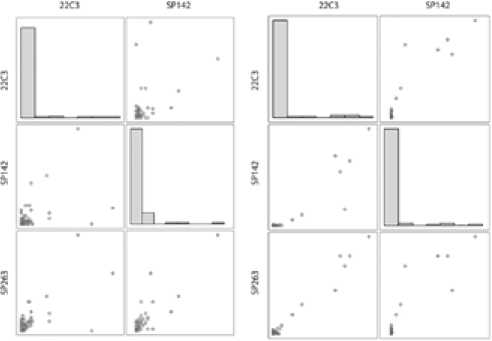
Анализ экспрессии PD-L1 в ИК был проведен с использованием аналогичного подхода. Диагностикум на основе антитела 22С3 идентифитицировал как позитивные 50 образцов из 100 и SP142–42 из 100. Повышение порогового значения для ИК приводило к резкому уменьшению числа позитивных случаев: при 10%-барьере выявлено 3 (SP142) и 6 (22C3) случаев из 100. Дальнейшее повышение пороговых значений приводило к уменьшению позитивных случаев примерно вдвое. Рисунок 1 отражает корреляцию между тестами по экспрессии PD-L1 на ИК и ОК.
После непосредственной оценки на препаратах количества ОК и ИК, окрашенных анти-PD-L1 антителами, PD-L1 статус образца уротелиального рака определяли в соответствии с принятыми в настоящее время cut-off для каждого маркера. Определение PD-L1 статуса опухоли с использованием этих критериев выявило наличие различного количества позитивных случаев при использовании двух анти-PD-L1 антител: для SP142–9% и 22С3–11 % из 100 исследованных случаев. Различалось и количество выявляемых по наличию мембранного окрашивания клеток. Однако
ИММУННЫЕ КЛЕТКИ ОПУХОЛЕВЫЕ КЛЕТКИ
Sutter Hot MMrix
|
2X3 |
5P1« |
|
|
2X3 |
1.00 |
0.50 |
|
SP142 |
030 |
1.00 |
|
S₽X3 |
069 |
035 |
|
2X3 |
«■142 |
|
|
2X3 |
LOO |
0.93 |
|
SP142 |
0.93 |
1.00 |
|
$Р2« |
0.99 |
0.91 |
Рисунок 1.
Таблица 1. Согласие между тестами 22C3 и SP142 в негативных и позитивных случаях на основании стандартных cut-off
Сопоставление результатов PD-L1 статуса, полученного при использовании разных оценочных систем, выявило следующие закономерности:
-
1. Пациенты с негативным статусом по SP142 имеют также негативный статус по 22С3 в 92% случаев;
-
2. Пациенты с негативным статусом по 22С3 имеют также негативный статус по SP142 в 97% случаев;
-
3. Пациенты с позитивным статусом по SP142 имеют также позитивный статус по 22С3 в 67% случаев;
-
4. Пациенты с позитивным статусом по 22С3 имеют также позитивный статус по SP142 в 43% случаев;
Обсуждение
Сложность в тестировании статуса экспрессии PD-L1 при уротелиальном раке обусловлена наличием различных диагностических реагентов, оценочных систем, рекомендациями производителей о жесткой привязке диагностикума к лекарственному препарату. Наличие таких различных подходов обусловливает необходимость исследования конкордантности между различными диагностикумами и изучение возможности использования разных диагностических систем для определения чувствительности к препарату и/или прогноза ответа на терапию [7].
Для немелкоклеточного рака легкого был уже проведен ряд подобных исследований по гармонизации применения диагностических антител — 22C3, 28.8, SP263 и SP142 (исследования Blueprint, Germany Study и др). Анализ этих работ показал сходные результаты, выявившие высокое совпадение данных, полученных с помощью антител 22C3, 28.8 и SP263.
Антитела показали меньшую согласованность результатов с другими антителами, но большую выявляемость экспрессии на ИК по сравнению с другими диагностикумами. Клон SP142 позиционируется как антитело для лучшего обнаружения именно ИК. Для уротелиального рака для SP142 приняты cut-off только для ИК. Системы оценки реакции для клонов 22C3, 28.8, SP263 были в первую очередь валидированы для оценки PD-L1 статуса на ОК.
В представляемом исследовании были изучены 100 образцов уротелиального рака, которые были окрашены с помощью 2 антител — 22C и SP142, применяемых в практике для назначения пембролизумаба и атезолизумаба у больных уротелиальным раком, ранее не получавших терапию и не являющихся кандидатами для лечения препаратами платины. Результаты независимой оценки экспрессии PD-L1 4 патологами были проанализированы как по совпадению выявляемости экспрессии PD-L1 на ИК и ОК разными антителами, так и по совпадению PD-L1 статуса пациентов по критериям cut-off, рекомендованным для каждого теста.
Количество опухолей с позитивным статусом по существующим оценочным критериям составило для SP142–9% и для 22C3–11%. Полученные результаты несколько ниже в сравнении с другими исследованиями [8]. Так, по данным М. Treiakova с соавторами, среди 235 образцов от 156 пациентов с уротелиальным раком были обнаружены 56 позитивных образцов (23,8%). Однако в нашем исследовании не проводился отбор пациентов по другим критериям, кроме наличия уротелиального рака и минимума клинических данных (пол, возраст, стадия и степень дифференцировки опухоли), поэтому меньшее число пациентов с позитивным статусом может быть связано с меньшим количеством исследованных случаев и наличием в представленной выборке Т1 стадии почти в половине образцов (45%). Стоит отметить, что главной целью работы было сравнение уровня экспрессии при использовании различных диагностикумов в одном и том же образце опухоли, поэтому отбор пациентов по стадии или сравнение уровня экспрессии между первичной опухолью и метастазами не представлялись целесообразными, так как не соответствовали основной задаче. Оценка экспрессии в ткани метастазов для чистоты эксперимента (создание однородной группы больных) не проводилась. Нужно подчеркнуть, что в настоящее время как в исследованиях по эффективности ингибиторов контрольных точек, так и в практической деятельности в большинстве случаев оценка экспрессии PD-L1 проводится в ткани первичной опухоли, забор которой для иммуногистохимического анализа является достаточно простым у больных уротелиальным раком [3–6]. Однако возможное появление в будущем данных о дискордантности экспрессии PD-L1 на клетках первичной опухоли и метастазов может повлиять на существующий подход [9].
В нашем исследовании было обнаружено более высокое число окрашенных ИК по сравнению с ОК со всеми маркерами (45% vs 8% SP142, 55% vs 24% 22C3). Коэффициенты корреляции Пирсона были для ИК — 0,5 между SP142/22C3 и для ОК — 0,93. В единственном крупном исследовании по сравнению экспрессии PD-L1, выявляемого различными тестами, М. Treiakova с соавторами указывают коэффициенты корреляции для всех образцов как 0,76–0,9 и 0,69–0, 86 — для позитивных случаев. Наиболее высокое совпадение результатов обнаружено для пар 22С3/28.8 и 28.8/E1L3. N и более низкое для пар 22C3/SP142 и 28.8/SP142, что сходно с результатами, полученными при исследованиях по гармонизации для НМРЛ. Аналогично для ИК наибольшие совпадения были для 22C3/28.8–0,85, 22C3/E1L3. N — 0,74. В целом тест SP142 во всех образцах имел значительно более низкую конкордантность SP142/22C3/28.8/E1L3. N — 0,3–0,38. В нашем исследовании коэффициент корреляции был несколько выше — от 0,5, но также мал для вывода о совпадении результатов. Наш анализ согласованности результатов для негативных и позитивных образцов различался. Так, для негативных образцов по 2 тест-системам было получено высокое совпадение результатов — 0,91 для SP142/22C3. Такие результаты позволяют считать, что оба маркера (22С3 и SP142) при использовании существующих систем оценки достоверно и с разницей менее чем 10% (9% — 0%) позволяют определить пациентов с негативным PD-L1 статусом без проведения повторного исследования с другими маркерами и решить вопрос о лекарственной терапии. При определении согласованности результатов для позитивного PD-L1 статуса опухоли были получены значительные расхождения результатов между 22С3 и SP142–43%. М. Treiakova с соавторами показали схожие результаты. Такое расхождение в выявлении опухолей с позитивным статусом экспрессии не позволяет рекомендовать использование только одного антитела для определения чувствительности к иммунотерапии. При обнаружении позитивного статуса по одному тесту пациент может иметь негативный статус по другому тесту с вероятностью 44–57%.
В заключение надо отметить, что проведенное исследование подтвердило возможность применения двух диагностических систем для определения PD-L1 статуса уротелиального рака с целью определения чувствительности к иммунотерапии. Использование диагностических систем с антителами SP142 и 22C3 по рекомендованным протоколам, системам оценки и инструментальным платформам показало, что при негативном статусе пациента по одному тесту он будет иметь негативный статус и по другому тесту, причем с высокой вероятностью в 97–100%. При обнаружении позитивного статуса по одному тесту пациент может иметь отрицательный статус с другим тестом с вероятностью 44–57%, что позволяет рекомендовать использовать повторное тестирование, особенно в пограничных случаях, с тестом, рекомендованным для предполагаемого к лечению препарата.
Список литературы Оценка экспрессии PD-l1 у пациентов с уротелиальным раком, имеющих противопоказания к назначению препаратов платины
- Tsimafeyeu I, Tjulandin S. First-line checkpoint inhibitors in PD-L1-positive patients with advanced urothelial carcinoma. BJU Int. 2018 Nov 20. 627 DOI: 10.1111/bju.14
- Sonpavde G, Galsky MD, Latini D, Chen GJ. Cisplatin-ineligible and chemotherapy-ineligible patients should be the focus of new drug development in patients with advanced bladder cancer. Clin Genitourin Cancer 2014; 12: 71-73.
- Powles T, Duran I, van der Heijden MS, et al. Atezolizumab versus chemotherapy in patients with platinum-treated locally advanced or metastatic urothelial carcinoma (IMvigor211): a multicentre, open-label, phase 3 randomised controlled trial. Lancet. 2018 Feb 24;391 (10 122):748-757.
- Balar AV, Galsky MD, Rosenberg JE, et al. Atezolizumab as first-line treatment in cisplatin-ineligible patients with locally advanced and metastatic urothelial carcinoma: a single-arm, multicentre, phase 2 trial. Lancet. 2017 Jan 7; 389 (10 064): 67-76.
- Balar AV, Castellano D, O'Donnell PH, et al. First-line pembrolizumab in cisplatin-ineligible patients with locally advanced and unresectable or metastatic urothelial cancer (KEYNOTE-052): a multicentre, single-arm, phase 2 study. Lancet Oncol. 2017 Nov; 18 (11): 1483-1492.
- Vuky J, Balar AV, Castellano D, O'Donnell PH, et al. Updated efficacy and safety of KEYNOTE-052: A single-arm phase 2 study investigating first-line pembrolizumab (pembro) in cisplatin-ineligible advanced urothelial cancer (UC). Journal of Clinical Oncology 36, no. 15_suppl (May 2018) 4524-4524 DOI: 10.1200/JCO.2018.36.15_suppl.4524
- Zavalishina L, Tsimafeyeu I, Povilaitite P, et al. RUSSCO-RSP comparative study of immunohistochemistry diagnostic assays for PD-L1 expression in urothelial bladder cancer. Virchows Arch. 2018. https://doi.org/10.1007/s00 428-018-2453-7.
- Tretiakova M, Fulton R, Kocherginsky M, et al. Concordance study of PD-L1 expression in primary and metastatic bladder carcinomas: comparison of four commonly used antibodies and RNA expression. Mod Pathol. 2018 Apr;31 (4):623-632.
- Burgess EF, Livasy C, Hartman A, et al. Discordance of high PD-L1 expression in primary and metastatic urothelial carcinoma lesions. Urol Oncol. 2019 Jan 16. pii: S1078-1439 (19) 30 002-X. doi: 10.1016/j.urolonc.2019.01.002. .


