Оценка количества ДНК разных групп микроорганизмов в генетических горизонтах темно-серой почвы
Автор: Железова А.Д., Кутовая О.В., Дмитренко В.Н., Тхакахова А.К., Хохлов С.Ф.
Журнал: Бюллетень Почвенного института им. В.В. Докучаева @byulleten-esoil
Статья в выпуске: 78, 2015 года.
Бесплатный доступ
Молекулярно-биологическими методами проведено исследование структуры микробного сообщества в профиле темно-серой почвы Luvic Retic Greyzemic Phaeozem (Loamic), Московская область, Каширский район. Микроорганизмы играют ведущую роль в преобразовании органического вещества почвы, их основная масса сосредоточена в верхней части профиля. В связи с этим большинство почвенных микробиологических исследований проводится для верхних горизонтов. Однако изучение микробного сообщества нижней части профиля представляет не только теоретический, но и практический интерес в связи с возрастающей интенсивностью эрозионных процессов. Методом количественной полимеразной цепной реакции в реальном времени оценено количество ДНК бактерий, архей и микромицетов в горизонтах исследуемой почвы. Исследован материал кротовины, находившейся на глубине 80 см. Наибольшее количество ДНК бактерий и архей выявлено в верхнем гумусово-аккумулятивном горизонте (9.6 × 10 8 и 9 × 10 7 копий/г почвы соответственно). С увеличением глубины наблюдалось плавное снижение количества ДНК бактерий и архей, что связано с изменением физико-химических условий в почве. ДНК микромицетов распределялись по профилю равномерно (5.0-9.4 × 10 7 копий/г почвы). Показатели содержания ДНК разных групп микроорганизмов в материале кротовины были близки к нижним минеральным горизонтам. Это может быть объяснено инфильтрацией воды через кротовину с элюированием микроорганизмов в период переувлажнения почв. Определяющими факторами, влияющими на количество ДНК микроорганизмов, являются элементарные почвенные процессы: биогенно-аккумулятивный в верхних горизонтах, глинисто-иллювиальный и гумусово-иллювиальный в нижних горизонтах темно-серой почвы.
Пцр (полимеразная цепная реакция), профильное распределение микроорганизмов, бактерии, археи, микромицеты
Короткий адрес: https://sciup.org/14313614
IDR: 14313614 | УДК: 631.4;574.472
Еstimаtiоn оf DNА quаntitу in diffеrеnt grоuрs оf miсrооrgаnisms with in gеnеtiс hоrizоns оf thе dаrk-grау sоil
Molecular-biological methods permitted to study the structure of the microbial community in the profile of dark-gray soil (Luvic Retic Greyzemic Phaeozem) in Kashira district of the Moscow region. Microorganisms playing an important role in transformation of the soil organic matter are mainly concentrated in the topsoil and the major microbiological studies are related to this part of the soil profile. However, the study of the microbial community in the lower soil horizons is not only of theoretical but also practical interest in view of increasing the intensity of erosion processes. The method of quantitative polymerase chain reaction was used to estimate the DNA quantity of bacteria, archespores and micromycetes in horizons of the above soil. Under study was also the crotovina material at a depth of 80 cm. The highest DNA quantity of bacteria and archespores proved to be in the upper humus-accumulative horizon (9.6 × 10 8 and 9 × 10 7 copy/g of soil respectively). Their quantity was decreased downwards the profile, what is connected with changes in the physic-chemical conditions of soil. DNA of micromycetes was evenly distributed throughout the soil profile (5.4-9.4 × 10 7 copy/g). In the crotovina material the DNA content of different microorganisms groups was close to that in lower mineral soil horizons. This may be explained by water infiltration through the crotovina accompanying by eluviation of microorganisms in the period of soil wetting. The factors affecting the DNA amount of microorganisms are elementary soil processes including the biogenic-accumulative process in the upper soil horizons, clay-illuvial and humus-illuvial processes in the lower horizons of the dark-gray soil.
Текст научной статьи Оценка количества ДНК разных групп микроорганизмов в генетических горизонтах темно-серой почвы
Согласно Единому государственному реестру почвенных ресурсов России (2014), серые лесные почвы (серые и темно-серые по “Классификации и диагностике…”, 2004 г.) занимают территорию в 41 млн га. Это зональный тип почв, формирующийся под травянистыми широколиственными лесами лесостепной зоны в плакорных условиях. По географическому положению они находятся в зоне умеренно континентального климата с близким соотношением количества годовых осадков и испаряемости (коэффициент увлажнения около 1), что благоприятствует их сельскохозяйственному использованию. На серых лесных почвах находится 11.8% от общей площади сельскохозяйственных угодий и 14.9% от общей площади пашни страны. Текстурно-дифференцированный профиль серой лесной почвы формируется в результате сложной комбинации элементарных почвенных процессов ( ЭПП ), охватывающих всю толщу профиля или его часть и выраженных в разной степени в зависимости от условий рельефа и климата (Урусевская и др., 1987). Серые почвы естественных ценозов хорошо оструктурены (Базыкина, 2012). Интенсивность гумусона-копления и биогенной аккумуляции зольных элементов наиболее сильно проявляется в темно-серых лесных почвах. Поступление органических остатков в почву ближе к южной границе зоны распространения серых лесных почв уравновешивается скоростью разложения опада, результатом является отсутствие лесной подстилки. Миграция гумусовых веществ в форме металлоорганических и закисных соединений приводит к увеличению мощности органо-минерального горизонта и обусловливает появление второго гумусового горизонта, что имело место в исследуемом профиле. Однако существует и гипотеза реликтового происхождения второго гумусового горизонта (Добровольский, 1993). Процессы лессиважа, иллитизации и оглинивания определяют формирование элювиального горизонта и некоторые особенности морфологии нижних текстурных горизонтов.
Деятельность микроорганизмов тесно связана с проявлением и интенсивностью многих почвенных процессов и режимов: биохимического, окислительно-восстановительного, водно-воздушного, а также с деструкцией и преобразованием минералов. Благоприятный термический режим и водно-физические свойства лесных почв оказывают существенное влияние на почвенно- микробиологические процессы. Температура +15ºС редко наблюдается в слоях глубже 40 см от поверхности, а +20ºС отмечается редко даже в поверхностных слоях в течение вегетационного периода. Перепад температуры в суточном цикле в поверхностном слое серой почвы под лесом не превышает 15ºС (Базыкина, 2012), что сказывается на высокой численности микроорганизмов в серых почвах и скорости их метаболизма.
Микробное сообщество играет ведущую роль в процессах почвообразования, затрагивающих превращения органического вещества, поэтому основная масса почвенных микроорганизмов сосредоточена в верхней части профиля. В минеральных горизонтах микробиологические процессы протекают не так активно. Однако изучение микробного сообщества нижней части профиля представляет не только теоретический, но и практический интерес, в связи с проявлением эрозионных процессов и возможным выходом на поверхность минеральных горизонтов. Кроме того, имеются данные, свидетельствующие о равномерном распределении микробной биомассы по профилю серой лесной почвы (Полянская и др., 1995).
Для исследования биомассы и структуры микробного сообщества почвы применяются классические методы почвенной микробиологии: субстрат-индуцированное дыхание, фумигацию, люминесцентную микроскопию, посев на питательные среды (Василенко и др., 2014). В настоящее время все большее распространение получают новые методы, основанные на анализе ДНК микроорганизмов, выделенных из почвы. Преимуществом этих методов является высокая чувствительность и информативность. Кроме того, только молекулярно-биологическими методами учитываются некультивируемые формы микроорганизмов (Манучарова, 2010).
Цель работы – количественный анализ ДНК бактерий, архей и микромицетов, выделенных из генетических горизонтов естественной темно-серой почвы, и определение зависимости их распределения по профилю от химических показателей почвы.
ОБЪЕКТЫ И МЕТОДЫ
Образцы темно-серой почвы отобрали на Богословском стационаре Почвенного института (Московская область, Каширский район; координаты разреза: 54°46′37.52″N 38°01′55.34″E) в июне
2014 г. в лесном массиве в районе с. Ледовские Выселки (1 км) и с. Елькино (1 км) (рис. 1). Растительность на данном участке представлена дубом черешчатым ( Quercus robur ), липой ( Tilia cordata ), березой ( Betula sp. ), осиной ( Populus tremola ) в древесном ярусе, лещиной ( Corylus avellana ) и рябиной ( Sorbus aucuparia ) в подлеске, зеленчуком ( Galeobdolon luteum ), будрой ( Glechoma hederacea ), геранью ( Geranium pratense ), снытью ( Aegopodium podagraria ) в напочвенном покрове. Описание разреза темно-серой почвы со вторым гумусовым горизонтом:
AU. Темно-серый с буроватым оттенком, свежий, тяжелосуглинистый, разделяется на слои: 0-15, 15-30, 30-40 см:
0-15 см, рыхлый, комковато-зернистый, очень много корней, перерыт почвенной фауной (черви, мыши), много копролитов, переход по структуре;
15-30 см, темно-серый с буроватым оттенком, неоднородный по плотности и структуре, комковато-порошистый, местами уплотнен, встречаются зоогенные зоны с копрогенной структурой, очень много корней тонких и до 2 см, встречаются кротовины, переход по плотности и структуре;
30-40 см, прерывистый, встречается фрагментарно, темно-серый с бурым оттенком с белесыми скелетанами, уплотнен, комковато -порошистая структура, местами неясноплитчатый (угловатые плитки), комковато-плитчатая, переход по структуре, окраске и наличию скелетанов.
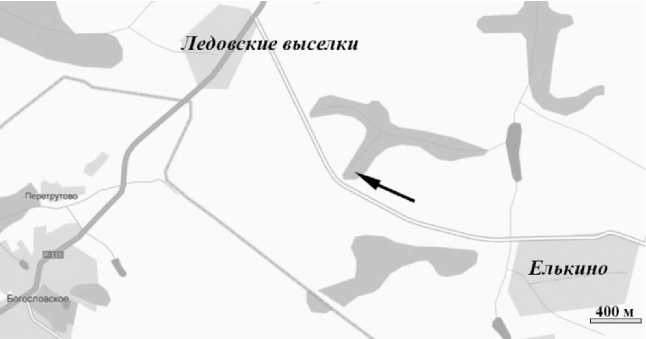
Рис. 1. Схема расположения разреза (указан стрелкой) темно-серой почвы.
BEL (hh), 40–55(60) см. Окраска неравномерная (темно-серая, белесая, бурая до углистого), тяжелосуглинистый, плотный, пористый, очень много ходов червей (крупных) 5–6 на см2, структура ореховатая, местами неясноплитчатая, по границам, на разломе темные гумусовые кутаны и обильные белесые скелетаны; структура многопорядковая, большие “орехи” распадаются на мелкие; нижняя граница языковатая, волнистая, переход по окраске и структуре.
BT1, 55(60)–85 см. Бурый с серыми глинисто-гумусовыми кутана-ми с редкими белесоватыми скелетанами, плотный, влажный. На глубине 80 см обнаружена кротовина, заполненная тёмным материалом. Структура – ореховато-призматическая, в отличие от предыдущего горизонта призмы имеют вертикальную ориентацию, структура аналогична гор. BEL (hh), структурные отдельности крупнее.
BT2, 85–110 см. Окраска неоднородная, бурый с серыми потеками, более увлажнен, тяжелосуглинистый до глинистого, структура глыбисто-призматическая, много гумусовых потеков, вязкий плотный, корней меньше.
BT3, 110–140 см. Похож на предыдущий, но встречаются орт-штейны, примазки, структура неясно-глыбистая, переход постепенный, встречаются темные гумусовые потеки (по ходам корней или морозобойным трещинам).
BC, > 140 см. Темно-бурый, плотный, тяжелый лёссовидный суглинок.
По совокупности признаков почва классифицирована как темно-серая со вторым гумусовым горизонтом (Классификация …, 2004) и Luvic Retic Greyzemic Phaeozem (Loamic) по Классификации WRB (IUSS Working …, 2014).
Образцы для микробиологического анализа отобрали из трех стенок разреза, из середины каждого генетического горизонта. Химический анализ почвенных образцов проводили в испытательном центре Почвенного института им. В.В. Докучаева, результаты представлены в таблице.
Выделение ДНК из образца почвы. ДНК из замороженных образцов выделяли из 0.2 г почвы после механического разрушения с использованием стеклянных шариков в экстрагирующем буфере, содержащем 350 мкл раствора А (натрий-фосфатный буфер – 200 мМ, изоцианат гуанидина – 240 мМ, pH 7), 350 мкл раствора Б (Трис-HCl – 500 мМ, SDS – 1% по массе от объема, pH 7) и 400 мкл смеси фенола с хлороформом (1 : 1). Разрушение образ ца проводили в течение 40 с на гомогенизаторе Precellys 24 (Bertin Technologi-
Химические свойства темно-серой почвы со вторым гумусовым горизонтом
Количественную оценку ДНК бактерий, архей и грибов осуществляли методом полимеразной цепной реакции (ПЦР) в реальном времени. Для определения концентрации очищенного препарата почвенной ДНК реакцию проводили в амплификаторе iCycler (Biorad) с измерением интенсивности флуоресценции реакционной смеси на каждом цикле. Реакционную смесь готовили из препарата SuperMix Eva Green Biorad (концентрированный буфер с дезоксирибонуклеотидами, полимеразой Sso7d-fusion, MgCl2, красителем EvaGreen и стабилизаторами).
Проводили калибровку зависимости интенсивности флуоресценции от логарифма концентрации ДНК стандартных растворов, по которой определяли концентрацию ДНК образцов с помощью программного обеспечения CFX Manager. В качестве стандартов для бактерий использовали растворы клонированных фрагментов рибосомального оперона Esherichia coli, для архей – штамма FG-07 Halobacterium salinarum, для грибов – штамма дрожжей Saccharomyces cerevisae Meyen 1B-D1606. Определяли концентрацию ДНК консервативных участков, присутствующих в генетическом материале любых бактерий, архей (участок 16s ДНК) и грибов (участок 18s ДНК) и пересчитывали в количество копий данных участков на грамм почвы для бактерий, архей и грибов по уравнению:
A = 4500 Q , где Q – концентрация ДНК в растворе, рассчитанная по калибровочному графику программой CFX Manager; А – количество копий консервативного участка ДНК на грамм почвы (далее – копий/г почвы); 4500 – коэффициент пересчета, выведенный с учетом исходной навески образца и манипуляций с экстрактом ДНК, выделенным из почвы.
По полученным данным (количеству копий/г почвы) можно сделать заключение об абсолютной численности микроорганизмов в горизонтах, приближенной к реальным показателям. Число рибосомальных оперонов в геномах бактерий, грибов и архей варьирует в широких пределах, но при пересчете по усредненным показателям распределение численности бактерий, архей и микро-мицетов в разных горизонтах остается неизменным (Андронов и др., 2012).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Наибольшее количество бактериальной ДНК (9.6 × 108 ко-пий/г почвы) обнаружено в гор. AU на глубине 0–15 см. В нижней части гор. AU количество бактериальной ДНК уменьшилось в 4 раза (2.5 × 108 копий/г почвы), далее по профилю наблюдалось плавное уменьшение до 8.1 × 107 копий/г почвы в гор. ВС (рис. 2).
Аналогичная картина наблюдалась с количеством ДНК архей, которое варьировало в пределах 9 × 107 – 6 × 106. В гор. AU количество ДНК архей было распределено неравномерно: выявлен локальный максимум на глубине 30–40, что может быть обусловлено высокой гетерогенностью почвенной среды в пределах данного горизонта. Следует отметить, что в изучаемой почве количество бактериальной ДНК в верхнем гор. AU на порядок превышает количество ДНК архей и микромицетов. Французскими исследователями (Gangneux et al, 2011) было получено другое соотношение между количеством ДНК грибов и бактерий (около 1 : 1) для гли-
А Б
AU (0-15)
AU (15-30)
AU (30-40)
BEL (40-55)
BT 1 (55-85)
BT 2 (85-110)
BT 3 (110-140)
BC (>140)
Кротовина (80)

0 2 4 6 8 1012

■
I
0 2 4 6 8 10
В

× 107 копий/г почвы
× 108 копий/г почвы × 107 копий/г почвы
Рис. 2. Количество ДНК бактерий (А), архей (Б) и микромицетов (В), распределение по глубине и горизонтам темно-серой почвы.
нистых почв сельскохозяйственных территорий. Нижняя часть исследуемого профиля (от 55 см) по сравнению с верхней обеднена микроорганизмами. Сокращение количества ДНК по профилю обусловлено сменой условий среды (уменьшением количества органического вещества, изменением химического состава и физических характеристик). В исследуемом профиле с глубиной количество ДНК бактерий и архей достаточно резко снижается. Наличие ДНК микроорганизмов в нижних почвенных горизонтах не всегда связано с их биологической активностью, некоторую долю может составлять неактивная экзоцеллюлярная ДНК, принесенная из верхних горизонтов (Agnelli et al, 2004).
ДНК грибов распределялись по профилю без статистически значимых различий между горизонтами. Их количество варьировало в пределах (5–9.4) × 107 копий/г почвы. Известно, что в основном грибная биомасса сосредоточена в подстилке и в верхней части гор. А (Fierer et al., 2003; Baldrian et al., 2013). Тем не менее, грибные споры распределены равномерно во всех минеральных горизонтах серой лесной почвы (Полянская и др., 1995). Равномерное распределение грибной биомассы по генетическим горизонтам может быть объяснено трофической связью микромицетов
Бюллетень Почвенного института им. В.В. Докучаева. 2015. Вып. 78. с подземной корневой массой древесных растений на данном участке, отсутствием конкурентов за трофические ресурсы в нижних почвенных горизонтах и возможной консервацией ДНК грибов из-за низкой интенсивности биологических процессов.
Определение количества ДНК проведено и для материала кротовины на глубине около 80 см (гор. BT1). Несмотря на морфологическую схожесть материала кротовины с материалом верхних горизонтов (темно-серая окраска, комковато-зернистая структура), количество бактериальной, архейной и грибной ДНК в ней было низким и находилось на уровне количества ДНК нижних минеральных горизонтов почвообразующей породы (бактерии – 4.6 × 107; археи – 3.6 × 106; микромицеты – 7.9 × 107 копий/г почвы). Присутствие кротовин в почвенном разрезе связано с засыпкой нежилой норы поверхностными выбросами почвенных млекопитающих. По таким ходам животных происходит активная инфильтрация воды с элюированием микроорганизмов в период переувлажнения почвы. Низкие количественные показатели ДНК микроорганизмов также могут быть связаны с угнетением микробного сообщества темноокрашенного материала кротовины при попадании его в нетипичные условия (отсутствие поступления органических веществ, изменение водно-воздушных и температурных условий жизнедеятельности).
Таким образом, можно говорить об относительно большем содержании бактерий и архей в верхних горизонтах темно-серой почвы и о равномерном распределении микромицетов по профилю. Как и следовало ожидать, для верхней части профиля имеется схожая тенденция в распределении количества ДНК (бактерий и архей) и содержания гумуса и азота. Верхние горизонты характеризуются высокой биогенностью за счет процессов преобразования органического вещества, связанных с деятельностью микроорганизмов (минерализацией растительных остатков, синтезом гумусовых веществ, биогенной аккумуляции микро- и макроэлементов). Для нижней части профиля обнаружена обратная зависимость количества ДНК архей от содержания обменных оснований, подвижного К2О, рН водной вытяжки, что может быть обусловлено экологическими особенностями этой группы (экстремофиль-ность, ацидофильность). Факторы, влияющие на количество ДНК микроорганизмов, в нижних минеральных и верхних органоген- ных горизонтах различаются и связаны с ЭПП, проходящими в генетических горизонтах серой почвы. В верхних горизонтах синхронно проходят биогенно-аккумулятивные процессы (разложение поступающих растительных и животных остатков, гумусооб-разование и аккумуляция гумусовых веществ) и процессы минерализации гумуса, а также элюирование гумусовых веществ вниз по профилю. Формирование нижних текстурных горизонтов обусловливается глинисто-иллювиальным (лессиваж) и гумусоиллювиальным процессами, которые определяют морфологические особенности этих горизонтов – появление глинистых и гумусовых кутан на гранях структурных отдельностях и присутствие второго гумусового горизонта.
ЗАКЛЮЧЕНИЕ
Методами молекулярной биологии впервые получены количественные показатели численности микроорганизмов по профилю темно-серой почвы. Верхняя часть гумусово-аккумулятивного гор. AU 0–15 см является наиболее биогенной. В ней обнаружено значительное количество ДНК бактерий и архей (9.6 × 108 и 9 × × 107 копий/г почвы соответственно). ДНК микромицетов распределяется по профилю равномерно от 5 × 107 до 9.4 × 107 ко-пий/г почвы. Высокая биологическая активность и количество ДНК прокариотной группы микроорганизмов верхних горизонтов связаны с почвенно-биологическими и биохимическими процессами трансформации органических веществ, поступающих в почву.
Благодарности. Выбор объекта исследования и местоположение эталонного разреза темно-серой почвы осуществлен сотрудником Богословского стационара В.Н. Дмитренко. Описание разреза и характеристика почвы проведены С.Ф. Хохловым. Работа выполнена при финансовой поддержке РНФ № 14-26-00079.
ESTIMATION OF DNA QUANTITY IN DIFFERENT GROUPS OF MICROORGANISMS WITHIN GENETIC
Список литературы Оценка количества ДНК разных групп микроорганизмов в генетических горизонтах темно-серой почвы
- Андронов Е.Е., Петрова С.Н., Пинаев А.Г., Першина Е.В., Рахимгалиева С.Ж., Ахмеденов К.М., Горобец А.В., Сергалиев Н.Х. Изучение структуры микробного сообщества почв разной степени засоленности с использованием T-RFLP и ПЦР с детекцией в реальном времени//Почвоведение. 2012. № 2. С. 173-183.
- Андронов Е.Е., Пинаев А.Г., Першина Е.В., Чижевская Е.П. Выделение ДНК из образцов почвы (методические указания). СПб.: ВНИИСХМ РАСХН, 2011. 27 с.
- Базыкина Г.С. Гидрологическая деградация автоморфных почв в агроландшафтах//Бюл. Почв. ин-та им. В.В. Докучаева. 2012. Вып. 70. С. 43-55.
- Василенко Е.С., Кутовая О.В., Тхакахова А.К., Мартынов А.С. Изменение численности микроорганизмов в зависимости от величины агрегатов миграционно-мицелярного чернозема//Бюл. Почв. ин-та им. В.В. Докучаева. 2014. Вып. 73. С. 85-97.
- Добровольский Г.В. Разнообразие генезиса и функций лесных почв//Почвоведение. 1993. № 9. С. 5-12.
- Единый государственный реестр почвенных ресурсов России. Версия 1.0. Коллективная монография. М.: Почв. ин-т им. В.В. Докучаева, 2014. 768 с.
- Классификация и диагностика почв России. Смоленск: Ойкумена, 2004. 342 с.
- Манучарова Н.А. Молекулярно-биологические аспекты исследований в экологии и микробиологии. М. Изд-во Моск. ун-та, 2010. 47 с.
- Полянская Л.М., Гейдебрехт В.В., Степанов A.Л., Звягинцев Д.Г. Распределение численности и биомассы микроорганизмов по профилям зональных типов почв//Почвоведение. 1995. № 3. С. 322-328.
- Урусевская И.С., Соколова Т.А., Шоба С.А., Багнавец О.С., Куйбышева И.П. Морфологические и генетические особенности профиля светло-серой лесной почвы на покровных суглинках//Почвоведение. 1987. № 4. С. 5-16.
- Agnelli A., Ascher J., Corti G., Ceccherini M.T., Nannipieri P. Distribution of microbial communities in a forest soil profile investigated by microbial biomass, soil respiration and DGGE of total and extracellular DNA//Soil Biol. Biochem. 2004. P. 859-868.
- Baldrian P., Vetrovsky T., Cajthaml T., Dobiasova P., Petrankova M., Snajdr J., Eichlerova I. Estimation of fungal biomass in forest litter and soil//Fungal ecology. 2013. P. 1-11.
- Fierer N., Schimela J.P., Holden P.A. Variations in microbial community composition through two soil depth profiles//Soil Biol. Biochem. 2003. P. 167-176.
- Gangneux C., Akpa-Vinceslas M., Sauvage H., Desaire S., Houot S., Laval K. Fungal. bacterial and plant dsDNA contributions to soil total DNA extracted from silty soils under different farming practices: Relationships with chloroform-labile carbon//Soil Biol. Biochem. 2011. P. 431-437
- IUSS Working Group WRB. World Reference Base for Soil Resources 2014. International soil classification system for naming soils and creating legends for soil maps. World Soil Resources Reports No. 106. FAO, Rome. 2014. 181 p.


