Оценка потенциальных радиологических рисков населения при реализации проекта "Прорыв" Госкорпорации "Росатом". Часть 1. Рекомендации МКРЗ
Автор: Чекин С.Ю., Меняйло А.Н., Ловачв С.С., Селва Н.Г., Корело А.М., Туманов К.А., Иванов В.К.
Рубрика: Научные статьи
Статья в выпуске: 4 т.29, 2020 года.
Бесплатный доступ
Понятие «радиационный ущерб» (radiation detriment) активно обсуждается в Публикации 103 МКРЗ, вышедшей в 2007 г. с учётом накопленных данных в области радиационной эпидемиологии. При расчёте радиационного ущерба используются модели показателей радиационных рисков, идентифицированных на данных наблюдения за японской когортой лиц, переживших в 1945 г. атомные бомбардировки городов Хиросима и Нагасаки. Модели показателей радиационных рисков включают зависимость от пола и возраста облучённых лиц. Дальнейшие вычисления радиационного ущерба МКРЗ проводит для специально определённой стандартной популяции, усредняя результаты расчётов по возрасту при облучении. Концепция радиологического ущерба разрабатывалась для наиболее полного выражения вреда здоровью человека, включая его потомков, от ионизирующего облучения, с учётом потерь продолжительности и качества жизни. Однако, областью применения радиационного ущерба МКРЗ является определение эффективной дозы и её нормирование для целей радиационной защиты. В статье проводится анализ концепции радиационного ущерба с точки зрения возможностей расширения области её применения. Показано, что методика расчёта радиационного ущерба МКРЗ может быть обобщена с учётом российских медико-статистических данных, оценок доли летальности и потерь лет здоровой жизни, с учётом пола и возраста. Такой обобщённый радиационный ущерб в дальнейшем будет называться «радиологический ущерб», чтобы подчеркнуть возможность его привязки к конкретной облучённой популяции. Величину популяционно-специфического радиологического ущерба можно использовать для оценки уровней радиологической защиты конкретного населения, а не только для сравнения источников ионизирующих излучений по их действию на стандартную популяцию. В частности, величина радиологического ущерба может быть использована для количественной характеристики потенциального вреда здоровью населения при реализации проекта «Прорыв» Госкорпорации «Росатом».
Мкрз, модель
Короткий адрес: https://sciup.org/170171552
IDR: 170171552 | УДК: 614.876 | DOI: 10.21870/0131-3878-2020-29-4-33-47
Potential radiological risk for the population during implementation of the Rosatom Proryv project. Part 1. ICRP recommendations
The concept “radiation detriment” has been debated intensively in the pages of the ICRP Publication 103 (2007), new radiation epidemiological data obtained after 2007 have also been brought into discussion. For radiation detriment calculation radiation risk models based on data of the study of Japanese cohort of atomic bombings survivors were used. Models developed for estimating radiation risk factors take account of gender and age at exposure. Now ICRP has estimated radiation detriment in specially designed standard population by averaging the estimates based on age at exposure. The concept “radiation detriment” was developed for quantification of the overall harm to health of humans and their offspring from stochastic effects of low-level radiation on different parts of the body, reduction in life expectancy and reduced quality of life. In addition, radiation detriment is used to assess effective dose and its standardization for radiological protection. In the paper, the concept “radiation detriment” is assessed with regard to the possibility of extending the area of its application. The applicability of technique for calculation of radiation detriment is possible to be extended with account of Russian health and statistical data, lethality fraction estimates, years of life lost, gender and age. The extended “radiation detriment” will be renamed as “radiological detriment”, that will highlight the possibility of quantifying potential harm to a specific irradiated population. The magnitude of population-based radiological detriment may be used not only for matching sources of ionizing radiation by their impact on the standard population, but also for estimating the level of radiological protection of the specific population. The level of radiological detriment may be used for quantification of potential harm to the public health in the implementation of the Rosatom project “Proryv”.
Текст научной статьи Оценка потенциальных радиологических рисков населения при реализации проекта "Прорыв" Госкорпорации "Росатом". Часть 1. Рекомендации МКРЗ
Реализуемый в настоящее время Госкопорацией «Росатом» приоритетный проект «Прорыв» нацелен на достижение принципиально нового качества ядерной энергетики, ориентированного на разработку и промышленную реализацию замкнутого ядерного топливного цикла на базе реакторов на быстрых нейтронах. При этом вопросы радиоэкологии и радиологической защиты требуют, естественно, рассмотрения и принятия решений с учётом национальных и международных стандартов, принятых в последние годы.
В настоящее время считается, что воздействие ионизирующего излучения на организм человека может быть причиной развития детерминированных и стохастических эффектов, вли-
Чекин С.Ю.* – зав. лаб.; Меняйло А.Н. – вед. научн. сотр., к.б.н.; Ловачёв С.С. – мл. научн. сотр.; Селёва Н.Г. – инженер, к.б.н.; Корело А.М. – ст. научн. сотр.; Туманов К.А. – зав. лаб., к.б.н.; Иванов В.К. – зам. директора по научн. работе МРНЦ им. А.Ф. Цыба, гл. радиоэколог ПН «Прорыв», Председатель РНКРЗ, чл.-корр. РАН, д.т.н. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России, ООО «НПК «Мединфо».
яющих на его здоровье: качество и длительность жизни. При так называемых детерминированных реакциях тканей [1] тяжесть их поражения зависит от дозы облучения, и зависимость «доза-эффект» не вполне строго, для практических целей радиологической защиты, считается пороговой. Порог определяется как доза, вызывающая определённый эффект у 1% облучённых индивидуумов [1]. К детерминированным эффектам относятся, например, помутнение хрусталика, катаракта, незлокачественные поражения кожи, временная или постоянная стерильность, мукозиты, некрозы, нарушения кроветворения. Для стохастических эффектов доза облучения влияет только на вероятность развития эффекта, а зависимость «доза-эффект» считает беспо-роговой [1]. К стохастическим эффектам относится развитие рака (злокачественных новообразований) различных локализаций, а также вредных для здоровья генетических последствий среди потомков облучённых лиц, называемых наследственными эффектами [1].
Основная цель радиологической защиты – исключить развитие детерминированных эффектов и снизить, насколько это возможно, риск стохастических эффектов. Рекомендации по достижению этой цели разрабатывает Международная комиссия по радиологической защите (МКРЗ).
Для количественной оценки вреда для здоровья человека от стохастических эффектов действия радиации МКРЗ использует многомерную концепцию радиационного ущерба (radiation detriment), в основе которой лежат оценки риска (вероятности) развития конкретных стохастических эффектов и тяжести связанных с ними последствий для здоровья [2]. В частности, при одной и той же дозе облучения оценки радиационного ущерба различаются для различных локализаций рака. Поэтому актуальные до настоящего времени Рекомендации МКРЗ (Публикация 103) [3], утверждённые 21 марта 2007 г., подчёркивают, что «дозы в органах и тканях, а не эффективные дозы, требуются для оценки вероятности индукции рака у облучённых индивидуумов».
Концепция радиационного ущерба разрабатывалась с целью сравнения вреда для здоровья человека от воздействия радиации с вредом от других воздействий. Величина радиационного ущерба используется при обосновании дозовых ограничений и пределов для целей радиологической защиты, а также для сравнения последствий различных вариантов распределения эквивалентной дозы в организме при определении эффективной дозы на основе взвешивающих коэффициентов тканей w T [3]. Современное представление об указанном подходе дано в работе Hamada N. и Fujimichi Y. (2014 г.) [4].
Вычисление радиационного ущерба является сложным процессом, для которого требуется информация из различных источников и соглашения различных экспертных сообществ о конкретных способах вычислений. В 2016 г. Рабочая группа 102 МКРЗ начала разработку современной методологии вычисления ущерба, которая в 2020 г. близка к завершению. Частью работы этой группы явилось описание истории развития концепции радиационного ущерба МКРЗ [5]. Целью данной статьи является анализ основных особенностей вычисления радиационного ущерба, использовавшихся в различных публикациях МКРЗ, с точки зрения его применения для оценки потенциальных радиологических рисков населения при реализации проекта «Прорыв» Госкорпорации «Росатом».
Методы расчёта радиационного ущерба и исходные данные
В самом общем виде концепция радиационного ущерба была сформулирована в Публикации 22 МКРЗ [2]: «Ущерб населению определяется как математическое понятие ожидаемого ущерба от облучения с учётом не только вероятности развития любого негативного последствия, но также тяжести этих последствий. Так, если pi – вероятность развития негативного эффекта i, тяжесть которого выражается как весовой коэффициент gi, тогда ущерб G в группе из P человек можно выразить как G=P^ipigi».
Количественные значения радиационного ущерба для стохастических эффектов впервые были представлены в Публикации 26 МКРЗ [6] в предположении линейной беспороговой (ЛБП) зависимости между дозой и риском. Ущерб (называвшийся «risk factor», коэффициент риска) выражался через вероятность летальных раков и серьёзных наследственных эффектов для следующих тканей: для гонад (с учётом наследственных эффектов), красного костного мозга, кости, лёгких, щитовидной железы, молочной железы, а также для группы тканей со специальным названием «прочие ткани». Усреднённые по полу и возрасту коэффициенты риска для летальных раков варьировали от 0,5 x 10 -3 Зв-1 (для рака кости и рака щитовидной железы) до 5 х 10-3 Зв-1 (для «прочих тканей»). Для наследственных эффектов в последующих двух поколениях коэффициент риска принимался равным 10-2 Зв-1. Однако, для целей радиационной защиты индивидуумов средний коэффициент риска для рака был определён на уровне 10-2 Зв-1, а для значимых наследственных эффектов - на уровне 4 х 10-3 Зв-1 [6].
Дозовый предел при равномерном облучении всего тела человека Публикация 26 МКРЗ [6] определяет при дополнительном условии логнормального вероятностного распределения годовых доз (годовых дозовых эквивалентов) в группе лиц. В данном случае МКРЗ считает, что установленный для индивидуума предел годового облучения 50 мЗв будет соответствовать среднему (в группе облучённых лиц) значению годового дозового эквивалента 5 мЗв. Радиационный ущерб (риск летальных раков и наследственных эффектов) от такого годового облучения в среднем будет равен 0,7 х 10-4, и только для нескольких лиц из облучённой группы ущерб достигнет значения 7 х 10-4. Такие величины радиационного ущерба МКРЗ рассматривала как приемлемые, так как в наиболее безопасных отраслях индустрии средний уровень профессиональной смертности составлял около 10-4 в год. Определение дозового предела было основано на принципе равенства ущерба, независимо от того, равномерно или неравномерно облучено тело человека:
L W t H t 5 H wbL ' (1)
T где wT – весовой коэффициент, отношение радиационного ущерба для ткани T к радиационному ущербу при равномерном облучении тела; HT – годовой дозовый эквивалент для ткани T; Hwb,l=50 мЗв – рекомендованный предел годового дозового эквивалента при равномерном облучении всего тела.
Для сравнения различных профессиональных рисков в Публикации 27 МКРЗ [7] использовались оценки обусловленных (различными факторами, связанными с работой) потерь продолжительности жизни персонала. Считалось, что в среднем один случай смертельного рака приводит к потере 16 лет жизни (включая 1 год дожития от заболевания до смерти). В Публикации 45 МКРЗ [8] были более подробно рассмотрены данные по летальности рака различных локализаций.
Начиная с 1977 г., в связи с новыми методами расчёта риска развития радиационно-индуцированного рака у населения, а также новыми экспериментальными данными, полученными на лабораторных животных и культурах клеток, возникла необходимость переоценки риска развития радиационно-индуцированного рака, что было отражено в Публикации 60 МКРЗ [9]. Кроме того, Публикация 60 МКРЗ внесла изменения в методику вычисления ущерба, учтя риск не смертельных случаев рака: радиационный ущерб D=Fх(2-к), где F - риск летальных раков, а к - их доля от общего числа раков (смертельных и не смертельных), называемая долей летальности.
В Публикации 103 МКРЗ [1] был изменён метод расчёта радиационного ущерба, разработанный ранее в Публикации 60 [9]. Новый метод основан на расчёте радиационных рисков заболеваемости, а не на смертности. В Приложении А Публикации 103 МКРЗ [1] представлен метод вычисления радиационного ущерба, но он не детализирован до такой степени, которая позволила бы полностью воспроизвести расчёты. Ниже метод вычисления радиационного ущерба представлен более подробно.
Последовательность вычисления радиационного ущерба представлена в табл. 1. Первый этап – вычисление номинального риска, являющегося оценкой радиационно-обусловленного пожизненного риска, усреднённого по полу, возрасту и региону (проживания) для различных типов рака, суммированного с риском серьёзных наследственных заболеваний в первых двух поколениях. Второй этап связан с учётом летальности, качества жизни для не смертельных случаев рака и числа потерянных лет жизни. На втором этапе не рассматривается зависимость от дозы облучения, но учитывается тяжесть заболевания, характерная для рака различных локализаций.
Таблица 1
Этапы вычисления радиологического ущерба согласно Публикации 103 МКРЗ [1, 5]
|
Этап расчёта |
Входные данные |
Расчётные показатели |
|
Этап 1: учёт облучения, номинальные риски по органам и тканям |
Фоновые показатели заболеваемости и смертности, модели радиационных рисков, половозрастное распределение облучённого населения или когорты |
Функция выживаемости, пожизненный радиационный риск, применение фактора DDREF, риск наследственных эффектов |
|
Этап 2: не зависит от облучения |
Доли летальности, коэффициенты качества жизни, потерянные годы жизни |
Взвешенная сумма по органам и тканям |
|
Результат |
Радиационный ущерб |
|
Модели показателей радиационных рисков (риск в год) по локализациям рака были получены на основе анализа заболеваемости в японской когорте лиц, переживших атомную бомбардировку и находившихся под медицинским наблюдением с 1958 по 1998 гг. включительно [10] (так называемая когорта LSS – Life Span Study). Для каждой локализации рака показатель радиационного риска моделировался с использованием моделей избыточного относительного показателя риска (ERR, от англ. Excess Relative Rate) и избыточного абсолютного показателя риска (EAR, от англ. Excess Absolute Rate):
X(s,a,e,d) = Xo (s,a,e)[1 + ERR(s,a,e,d)]
X (s,a,e,d) = Xo (s,a,e) + EAR(s,a,e,d)
с использованием единого функционального представления для ERR и EAR
ER (s,a,e,d) = pd exp [« (e - 30/10) +aIn (a /70)] , где e - возраст при облучении (годы); a - достигнутый возраст (годы); d - доза (Гр), Хо - исходный (базовый) риск рака; ER – избыточный показатель риска (ERR или EAR).
Значения параметров в и a в формуле (3), использованные для вычисления номинальных рисков МКРЗ [1], представлены в табл. 2. Предполагалось, что латентный период для солидных раков составляет 10 лет: ER =0, если a – e <10 лет.
Таблица 2 Коэффициенты моделей радиационных рисков заболеваемости Публикации 103 МКРЗ [1]
Для общего представления о модифицирующем влиянии возраста на избыточные показатели риска на рис. 1 и 2 приведены возрастные зависимости ERR и EAR для заболеваемости всеми солидными раками в совокупности, рассчитанные по формуле (3) с численными значениями параметров из табл. 2.
При оценке моделей показателей риска лейкемии также были использованы данные когорты LSS. Величина риска вычислялась с использованием модели EAR, сходной с моделью Preston et al. [11], при линейно-квадратичной зависимости показателя риска от дозы. Для вычисления радиационного риска лейкемии минимальный латентный период составлял 2 года.
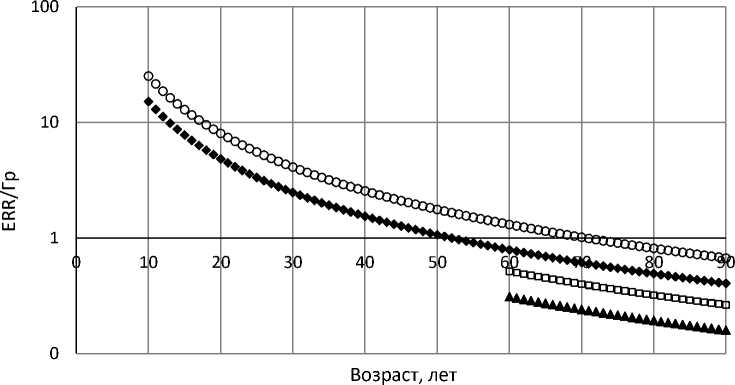
♦ ERR, муж., до 1 года при облучении о ERR, жен., до 1 года при облучении
▲ ERR, муж., 50 лет при облучении □ ERR, жен., 50 лет при облучении
Рис. 1. Коэффициент избыточного относительного показателя риска (ERR/Гр) для всех солидных раков в зависимости от возраста при облучении и достигнутого возраста.
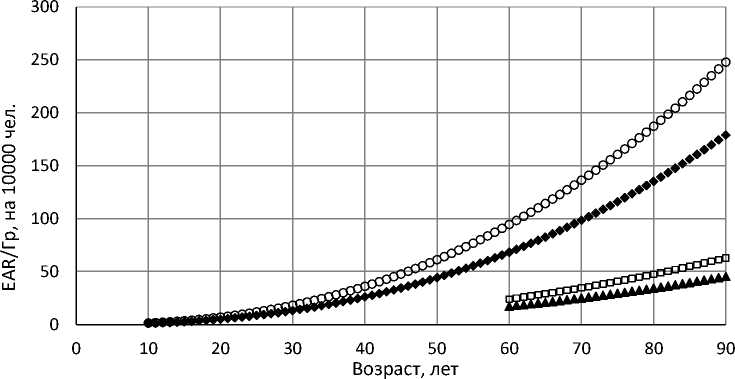
♦ EAR, муж., до 1 года при облучении о EAR, жен., до 1 года при облучении
▲ EAR, муж., 50 лет при облучении □ EAR, жен., 50 лет при облучении
Рис. 2. Коэффициент избыточного абсолютного показателя риска (EAR/Гр, на 10000 чел.) для всех солидных раков в зависимости от возраста при облучении и достигнутого возраста.
Для расчёта радиационных рисков в произвольной популяции, отличной от тех, по которым оценивались параметры моделей избыточных показателей (2), использовались взвешенные средние радиационных рисков, рассчитанных по моделям ERR и EAR . Для рака молочной железы и для лейкозов использовалась только модель EAR, для рака щитовидной железы – только модель ERR, для рака лёгкого отношение весов моделей ERR:EAR = 0,3:0,7, и для остальных локализаций солидных раков – ERR:EAR = 0,5:0,5.
В основе определения некоторых метрик пожизненного радиационного риска лежит определение риска радиационно-индуцированного рака (REIC, от англ. Risk of Exposure-Induced Cancer) [12]:
REIC(s,e,d)= J [EAR* (s,a,e,d)S (s,a,e,d)]da , (4)
a=e+L где s – пол; e – возраст при облучении (годы); d – доза облучения в возрасте e (Гр); a – достигнутый возраст (годы); L – латентный период развития радиационно-индуцированного рака (годы); EAR*(s,a,e,d) – избыточный абсолютный показатель риска, равный ^ (s,a,e)• ERR(s,a,e,d), либо EAR(s,a,e,d) из выражения (2) для избыточного показателя риска; S(s,a,e,d) – функция (вероятность) дожития без рака от возраста при облучении e до возраста а.
В Публикации 103 МКРЗ [1] используется упрощённая консервативная оценка REIC , называемая «пожизненный атрибутивный риск», LAR (от англ. Lifetime Attributable Risk), в которой функция дожития не зависит от дозы облучения:
LAR(s,e,d)= J [EAR* (s,a,e,d) S (s,a,e)~^а . (5)
a = e + L
Как показывает рис. 3, величина LAR незначительно превышает REIC : менее чем на 6% даже для доз облучения 1 Гр, которые могут встречаться только в аварийных ситуациях. При построении системы дозовых ограничений и пределов для целей радиологической защиты преимуществом метрики пожизненного риска LAR является её линейная зависимость от дозы облучения, если избыточный показатель риска EAR* в выражении (5) также линеен по дозе.
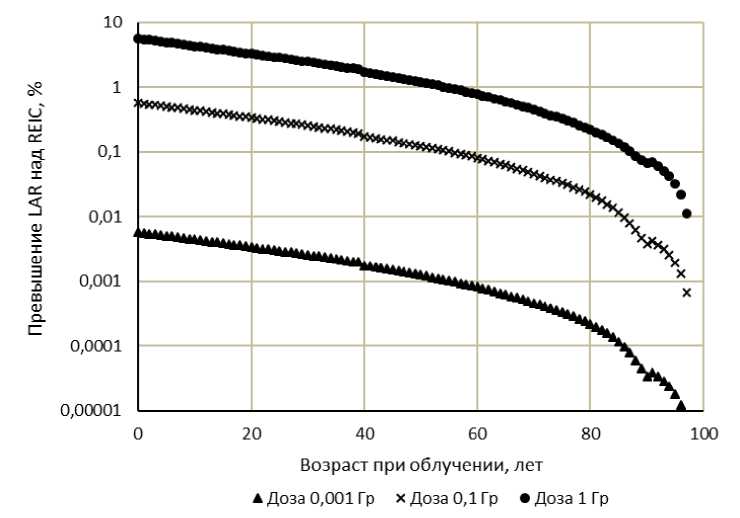
Рис. 3. Превышение величины LAR над REID для заболеваемости всеми солидными раками женского населения России при однократном гамма-облучении всего тела в дозах 0,001 Гр, 0,1 Гр и 1 Гр в зависимости от возраста при облучении.
Усреднённые по возрасту при облучении величины LAR рассчитывались для персонала (возраста при облучении от 18 до 64 лет) и для населения (возраста при облучении от 0 до 85 лет) для сценария однократного внешнего гамма-облучения всего тела человека в дозе 0,1 Гр.
Начина с Публикации 60 МКРЗ [9], для малых доз облучения (менее 0,5 Гр) и при пролонгированном облучении значение LAR для солидных раков, полученное по формуле (5), МКРЗ рекомендует уменьшать в 2 раза, применяя так называемый «фактор эффективности дозы и мощности дозы» DDREF =2 (Dose and Dose-Rate Effectiveness Factor). Для лейкемии такая корректировка LAR , как это декларирует МКРЗ, не используется, из-за линейно-квадратичной зависимости EAR от дозы.
Оценки радиационного риска наследуемых (hereditary) эффектов в Публикации 26 МКРЗ [6] ограничивались первыми двумя поколениями потомков облучённых лиц, в Публикации 60 МКРЗ [9] была сделана попытка учесть наследственные (heritable) эффекты во всех последующих поколениях, а Публикация 103 МКРЗ [1] опять вернулась к двум поколениям. В настоящее время радиационно-эпидемиологических данных для оценки радиационных рисков наследственных эффектов недостаточно для их статистически достоверной оценки, поэтому такие оценки во многом основаны на экспериментальных данных, полученных на животных и опубликованных в отчёте Научного комитета ООН по действию атомной радиации (НКДАР ООН) [13]. Коэффициент радиационного риска наследственных заболеваний для населения принят равным 20 случаям на 10 000 человек при внешнем гамма-облучении гонад в дозе 1 Гр, а риск для персонала – 12 случаев на 10 000 человек/Гр (60% от риска для населения) [1].
Современные значения коэффициентов номинального риска R по данным Публикации 103 МКРЗ [1] представлены в табл. 3. Суммарный коэффициент номинального радиационного риска составил 1715 случаев рака на 10 000 человек на 1 Зв для населения и 1179 случаев рака на 10 000 человек на 1 Зв – для персонала.
Таблица 3 Компоненты радиологического ущерба для населения и персонала, на основе данных Публикации 103 МКРЗ [1]
|
Орган/ткань |
Коэффициент номинального риска, число случаев на 10 000 чел. на 1 Зв, R a |
Доля летальности, k |
Минимальный вес не летальных раков, q min |
Фактор качества жизни для не летальных раков, q |
Относительная потеря лет жизни без рака, l |
Коэффициент радиационного ущерба, D |
Относительный радиационный ущерб |
|
Население (возраст 0-84 лет при облучении) |
|||||||
|
Пищевод |
15 |
0,928 |
0,1 |
0,935 |
0,87 |
13,1 |
0,023 |
|
Желудок |
79 |
0,829 |
0,1 |
0,846 |
0,88 |
67,7 |
0,118 |
|
Толстая кишка |
65 |
0,478 |
0,1 |
0,530 |
0,97 |
47,9 |
0,083 |
|
Печень |
30 |
0,954 |
0,1 |
0,959 |
0,88 |
26,6 |
0,046 |
|
Лёгкое |
114 |
0,890 |
0,1 |
0,901 |
0,80 |
90,3 |
0,157 |
|
Кость |
7 |
0,450 |
0,1 |
0,505 |
1,00 |
5,1 |
0,009 |
|
Кожа |
1000 |
0,002 |
0,0 |
0,002 |
1,00 |
4,0 |
0,007 |
|
Молочная железа |
112 |
0,294 |
0,1 |
0,365 |
1,29 |
79,8 |
0,139 |
|
Яичник |
11 |
0,566 |
0,1 |
0,609 |
1,12 |
9,9 |
0,017 |
|
Мочевой пузырь |
43 |
0,286 |
0,1 |
0,357 |
0,71 |
16,7 |
0,029 |
|
Щитовидная железа |
33 |
0,066 |
0,2 |
0,253 |
1,29 |
12,7 |
0,022 |
|
Красный костный мозг |
42 |
0,669 |
0,1 |
0,702 |
1,63 |
61,5 |
0,107 |
|
Прочие солидные раки |
144 |
0,490 |
0,1 |
0,541 |
1,03 |
113,5 |
0,198 |
|
Гонады (наследствен- |
20 |
0,800 |
0,1 |
0,820 |
1,32 |
25,4 |
0,044 |
|
ные заболевания) |
|||||||
|
Всего |
1715 |
574,2 |
1,000 |
||||
|
Персонал (возраст 18-64 лет при облучении) |
|||||||
|
Пищевод |
16 |
0,928 |
0,1 |
0,935 |
0,91 |
14,2 |
0,034 |
|
Желудок |
60 |
0,829 |
0,1 |
0,846 |
0,89 |
51,8 |
0,123 |
|
Толстая кишка |
50 |
0,478 |
0,1 |
0,530 |
1,13 |
43,0 |
0,102 |
|
Печень |
21 |
0,954 |
0,1 |
0,959 |
0,93 |
19,7 |
0,047 |
|
Лёгкое |
127 |
0,890 |
0,1 |
0,901 |
0,96 |
120,7 |
0,286 |
Продолжение таблицы 3
Коэффициенты номинального радиационного риска заболеваемости раком или наследственными заболеваниями конвертировали в соответствующие риски смертности путём умножения на долю летальности (коэффициент k в табл. 3). Оценки k были получены экспертным путём на основе анализа показателей 5-летней выживаемости для различных локализаций рака в период 1980-1985 гг. [14]. Оценка коэффициента номинального риска для рака кости в Публикацию 103 МКРЗ [1] была перенесена из Публикации 60 МКРЗ [6], а оценка коэффициента номинального риска для немеланомного рака кожи – из Публикации 59 МКРЗ [15]. Из-за ограниченности имевшихся радиационно-эпидемиологических данных коэффициенты радиационных рисков для этих двух локализаций рака были приняты независимыми от возраста или времени, прошедшего с момента облучения.
В Публикации 60 МКРЗ [9] вклад не летальных случаев рака в радиационный ущерб (D) принимался пропорциональным доле летальности к , и при к стремящемся к нулю ( к ^ 0) вклад в ущерб от не летальных раков также стремился к нулю ( D ^ 0). В Публикации 103 МКРЗ [1] считается, что при нулевой летальности ( k =0) вклад от не летальных раков в радиационный ущерб должен учитываться с коэффициентом q min >0, который характеризует потери качества жизни и определяется экспертным путём. Фактор качества жизни ( q ) для не летальных раков, называемый МКРЗ, по аналогии с Публикацией 60 МКРЗ [9], скорректированной долей летальности, определяется следующей формулой [1]:
q = ( 1- qmin )• k+qmin, (6)
где k – доля летальности; q min – минимальное значение фактора качества жизни для не летальных раков.
Вероятностные распределения по возрасту, при котором впервые устанавливается диагноз рака, различаются для разных локализаций рака. Относительные сокращения продолжительности жизни без диагноза рака, значения коэффициента / в табл. 3, определялись с использованием среднего числа потерянных лет здоровой (без рака) жизни для конкретной локализации рака, поделённого на среднее число потерянных лет здоровой жизни для всех раков (15,15 лет). Коэффициент / варьирует от значений / <1 для раков, встречающихся в поздний период жизни (0,71 для рака мочевого пузыря, 0,80 для рака лёгкого у населения), до значений / >1 для заболевших в ранний период жизни (1,63 для лейкемии и 1,29 для рака щитовидной или молочной железы). Для рака кости или кожи устанавливается значение / =1 (как среднее для всех раков), так как число лет сокращения жизни для этих локализаций не может быть определено как для других раков. Для гонад число потерянных лет жизни из-за тяжёлых генетических нарушений принимается равным 20 годам и коэффициент / =1,32.
Для вычисления коэффициента радиационного ущерба D для каждой локализации рака (включая наследственные эффекты для гонад) используется следующая формула:
D = [ R • k + R • (1 - к) • q ]• l, (7)
где R - коэффициент номинального риска (число случаев заболевания на 10 000 человек при однократном облучении в эквивалентной дозе 1 Зв); к - доля летальности; q - фактор качества жизни для случаев не летальных раков, вычисляемый по формуле (6); / - относительная потеря лет здоровой (без рака) жизни; коэффициент радиационного ущерба D имеет ту же размерность, что и коэффициент номинального риска R .
Набор коэффициентов радиационного ущерба для каждой локализации рака, нормированных на их сумму, т.е. набор относительных радиационных ущербов (последняя колонка в табл. 3) является основой при вычислении тканевых весовых коэффициентов w t в выражении (1) для определения дозового предела. Как показано в табл. 3, суммарный радиационный ущерб для населения равняется 574 случаям на 10 000 человек/Зв, а для персонала - 422 случаям на 10 000 человек/Зв. Наибольший вклад (относительный радиационный ущерб равен 0,198) в суммарный ущерб для населения вносят «прочие солидные раки» (14 локализаций: сноска б в табл. 3), а в суммарный ущерб для персонала - рак лёгкого (относительный радиационный ущерб равен 0,286).
Результаты анализа и обсуждение современной концепции радиационного ущерба
Радиационный ущерб, как и радиационные риски заболеваемости и смертности, зависит от локализации рака, возраста и пола облучённых лиц. Рассчитанные МКРЗ [1] коэффициенты номинального риска (табл. 3) предоставляют радиационные пожизненные риски заболеваемости для различных локализаций рака (а также для наследственных заболеваний). С учётом ле- тальности заболеваний, качества жизни при наличии этих заболеваний и потерянных лет здоровой жизни коэффициенты номинального риска пересчитываются в коэффициенты номинального радиационного ущерба по органам и тканям, а суммарный коэффициент номинального радиационного ущерба является суммой коэффициентов ущерба для каждой части тела (ткани или органа) и для возможных наследственных эффектов.
В Публикации 103 МКРЗ [1] фоновые показатели заболеваемости и смертности относятся к периоду эпидемиологических наблюдений в разных странах с 1993 по 1997 гг. Очевидно, что с тех пор показатели заболеваемости и смертности во всех странах существенно изменились из-за изменения образа жизни, совершенствования диагностических методов и повышения качества лечения, особенно для рака молочной железы и рака щитовидной железы. Обновление этих фоновых показателей дало бы более актуальную основу для системы радиологической защиты [16]. Более того, фоновая заболеваемость и смертность значительно варьируют не только от страны к стране, но и в пределах одной страны из-за генетических различий, различий в образе жизни и в уровне здравоохранения. Последние два фактора приводят к вариабельности фоновых показателей персонала по отраслям человеческой деятельности.
Использование адекватных для ситуаций облучения фоновых показателей заболеваемости и смертности является существенным условием корректной оценки радиационных рисков в силу того, что последние, являясь пожизненными вероятностями, получаются интегрированием по времени исходных показателей риска, и в процессе интегрирования небольшие, на первый взгляд, вариации показателей риска накапливаются и могут приводить к значимым вариациям пожизненных рисков.
В Публикации 103 МКРЗ [1] используются модели показателей радиационного риска, идентифицированные на основе данных наблюдения когорты LSS для 11 органов и тканей, которые были собраны с 1958 по 1998 гг. включительно [10, 11]. При наличии более современных или более адекватных для прогнозируемой когорты моделей показателей радиационного риска их использование при прогнозе пожизненных радиационных рисков в когорте является более обоснованным (с точки зрения статистики), чем использование устаревших фоновых показателей несуществующей в реальности композитной популяции МКРЗ [1].
Например, для прогноза пожизненных радиационных рисков российского населения обоснованным было бы использование моделей показателей радиационных рисков, идентифицированных на основе данных наблюдений в когорте жителей загрязнённых радионуклидами российских территорий (в результате аварии на Чернобыльской АЭС в 1986 г.).
В отношении облучения красного костного мозга на сегодняшний день остаётся нерешённым вопрос о расширении используемой в прогнозах группы злокачественных новообразований лимфатической и кроветворной тканей за счёт включения в этот прогноз лимфом и множественных миелом.
Для рака кости и немеланомного рака кожи оценки номинального радиационного риска до сих пор проводятся по моделям Публикаций 60 и 59 соответственно [9, 15]. Было бы желательно уточнить модели показателей риска для этих заболеваний. То же относится и к разработке моделей риска для мозга и слюнных желез, так как в настоящее время для этих органов специфических моделей оценки ущерба нет.
Анализ возможных наследственных эффектов основан на данных отчёта НКДАР ООН [13]. С того времени получены новые научные данные, поэтому необходимо провести анализ современных данных.
В современной схеме расчёта радиационного ущерба доля летальности от рака и оценки относительного сокращения продолжительности жизни основаны на устаревших статистических данных 1980-х годов [9, 14] и применяются без различия пола и возраста (используются одинаковые значения для населения и персонала). Очевидно, что при расчёте коэффициентов радиационного ущерба для российского населения должны использоваться российские оценки доли летальности и потерь лет здоровой жизни, в идеале – с учётом возраста, пола и территориальных групп населения.
Выводы
Радиационный ущерб является наиболее полной прогнозной оценкой вреда здоровью облучённых групп населения. Для его вычисления требуется обработка большого объёма эпидемиологической и медицинской информации, включая данные медицинской статистики и оценки параметров тяжести онкологических и наследственных заболеваний. Оценка величины радиационного ущерба базируется на последних мировых данных радиационно-эпидемиологических исследований зависимости «доза-эффект» и требует дальнейшего осмысления возможности её практического применения в области радиологической защиты населения и персонала.
В настоящее время методика расчёта радиационного ущерба находится на стадии усовершенствования [5], и становится всё более важным публикация процедур и результатов его вычисления для конкретных популяций в конкретных ситуациях облучения для понимания возможностей расширения области применения концепции радиационного ущерба за пределами оценки эффективных доз и их нормирования.
Анализ современной концепции радиационного ущерба, с точки зрения возможностей расширения области её применения, показывает, что методика расчёта радиационного ущерба МКРЗ может быть обобщена с учётом российских медико-статистических данных, оценок доли летальности и потерь лет здоровой жизни, с учётом пола и возраста. Такой обобщённый радиационный ущерб в дальнейшем будет называться «радиологический ущерб», чтобы подчеркнуть возможность его привязки к конкретной облучённой популяции. Величину популяционноспецифического радиологического ущерба можно использовать для оценки уровней радиологической защиты конкретного населения, а не только для сравнения источников ионизирующих излучений по их действию на стандартную популяцию. В частности, величина радиологического ущерба может быть использована для количественной характеристики потенциального вреда здоровью населения при реализации проекта «Прорыв» Госкорпорации «Росатом».
Следует отметить, что технология оценки радиационных рисков Публикации 103 МКРЗ [1] была ранее использована авторами для обоснования достижимости радиологической эквивалентности радиоактивных отходов и исходного уранового сырья при функционировании закрытого ядерного топливного цикла на базе реактора на быстрых нейтронах [17].
В следующей части настоящей статьи (часть 2) впервые показано, как методика расчёта популяционно-специфического радиологического ущерба используется для оценки уровня радиологической защиты населения, проживающего вблизи АО «СХК», в рамках проектного направления «Прорыв».
Настоящая работа выполнена в рамках ПН «Прорыв» Госкорпорации «Росатом».
Список литературы Оценка потенциальных радиологических рисков населения при реализации проекта "Прорыв" Госкорпорации "Росатом". Часть 1. Рекомендации МКРЗ
- ICRP, 2007. The 2007 Recommendations of the International Commission on Radiological Protection. ICRP Publication 103 //Ann. ICRP. 2007. V. 37, N 2-4. P. 1-332.
- ICRP, 1973. Implications of commission recommendations that doses be kept as low as readily achievable. ICRP Publication 22. Oxford: Pergamon Press, 1973. 18 p.
- ICRP, 1966. Recommendations of the International Commission on Radiological Protection. ICRP Publication 9. Oxford: Pergamon Press, 1966. 27 p.
- Hamada N., Fujimichi Y. Classification of radiation effects for dose limitation purposes: history, current situation and future prospects //J. Radiat. Res. 2014. V. 55. P. 629-640.
- Cléro E., Vaillant L., Hamada N., Zhang W., Preston D., Laurier D., Ban N. History of radiation detriment and its calculation methodology used in ICRP Publication 103 //J. Radiol. Prot. 2019. V. 39. P. R19-R35.
- ICRP, 1977. Recommendations of the International Commission on Radiological Protection. ICRP Publication 26 //Ann. ICRP. 1977. V. 1, N 3. P. 1-53.
- ICRP, 1977. Problems involved in developing an index of harm. ICRP Publication 27 //Ann. ICRP. 1977. V. 1, N 4. P. 1-24.
- ICRP, 1985. Developing a unified index of harm. ICRP Publication 45 //Ann. ICRP. 1985. V. 15, N 3. P. 1-64.
- ICRP, 1991. The 1990 Recommendations of the International Commission on Radiological Protection. ICRP Publication 60 //Ann. ICRP. 1991. V. 21, N 1-3. P. 1-201.
- Preston D.L., Ron E., Tokuoka S., Funamoto S., Nishi N., Soda M., Mabuchi K., Kodama K. Solid cancer incidence in atomic bomb survivors: 1958-1998 //Radiat. Res. 2007. V. 168, N 1. P. 1-64.
- Preston D.L., Kusumi S., Tomonaga M., Izumi S., Ron E., Kuramoto A., Kamada N., Dohy H., Matsui T., Nonaka H., Thompson D.E., Soda M., Mabuchi K. Cancer incidence in atomic bomb survivors: III. Leukaemia, lymphoma and multiple myeloma, 1950-1987 //Radiat. Res. 1994. V. 137 (Suppl. 2). P. S68-S97.
- Thomas D., Darby S., Fagnani F., Hubert P., Vaeth M., Weiss K. Definition and estimation of lifetime detriment from radiation exposures: principles and methods //Health Phys. 1992. V. 63, N 3. P. 259-272.
- United Nations Scientific Committee on the Effects of Atomic Radiation (UNSCEAR). Hereditary effects of radiation. UNSCEAR 2001 Report to the General Assembly with Scientific Annex. New York: United Nations, 2001.
- Cancer statistics review 1973-1986 including a report on the status of cancer control. NIH Publication No. 89-2789. Bethesda, MD: US Department of Health and Human Services, PHS, NIH, NCI, 1989.
- ICRP, 1992. The biological basis for dose limitation in the skin. ICRP Publication 59 //Ann. ICRP. 1992. V. 22, N 2. P. 1-104.
- Breckow J., Emami S., Amalhaf S., Beshgard A., Buermeyer J., Spruck K. Impact of updating the non-radiation parameters in the ICRP 103 detriment model //Radiat. Environ. Biophys. 2018. V. 57, N 2. P. 89-98.
- Иванов В.К., Чекин С.Ю., Меняйло А.Н., Максютов М.А., Туманов К.А., Кащеева П.В., Ловачёв С.С., Адамов Е.О., Лопаткин А.В. Радиационная и радиологическая эквивалентность РАО при двухкомпонентной ядерной энергетике //Радиация и риск. 2019. Т. 28, № 1. С. 5-25.


