Оценка предельно-допустимого воздействия на процессы самоочищения в экосистеме малого водотока
Автор: Злывко Алексей Сергеевич, Чеснокова Светлана Михайловна, Трифонова Татьяна Анатольевна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Водные ресурсы
Статья в выпуске: 1-4 т.16, 2014 года.
Бесплатный доступ
Приведены критерии выбора приоритетного загрязнителя эвтрофного водотока, по трансформации которого целесообразно проводить оценку процессов самоочищения. Рассмотрено влияние различных веществ на процессы нитрификации аммонийного азота и проведена оценка предельно допустимой нагрузки на водные объект по ингибированию процессов нитрификации с использованием метода лабораторного моделирования.
Водоток, загрязнитель, самоочищение, нитрификация, предельно-допустимая нагрузка, моделирование
Короткий адрес: https://sciup.org/148202933
IDR: 148202933 | УДК: 502.51(282)
Assessment the maximum-permissible impact on self-cleaning processes in the small waterway ecosystem
Criteria of choice the priority pollutant of eutrophic waterway on which transformation it is expedient to carry out an assessment of self-cleaning processes are given. Influence of various substances on processes of nitrification the ammonium nitrogen is considered and assessment of maximum-permissible loading on water object on inhibition the nitrification processes with use of a method of laboratory modeling is carried out.
Текст научной статьи Оценка предельно-допустимого воздействия на процессы самоочищения в экосистеме малого водотока
Цель работы: оценка характера и уровня загрязнения экосистемы р. Содышка соединениями биогенных элементов, ведущих факторов эвтрофикации водных объектов [4].
Так как процессы самоочищения в эвтрофных водных объектах зависят от природы приоритетного загрязнителя, который определяет характер процессов самоочищения, нами разработаны критерии выбора этого вещества. Для выбора приоритетного загрязнителя водного объекта нами предлагаются следующие критерии:
-
1) вклад в величину ИЗВ более 25%;
-
2) вклад загрязнителя в трофический статус водного объекта;
-
3) токсичность вещества для гидробионтов;
-
4) трансформация в водном объекте с образованием токсичных продуктов;
-
5) возможность поступления вещества как из антропогенных источников, так и за счет внутриводоемных процессов;
-
6) влияние загрязнителя на кислородный режим водного объекта.
В таблице 1 представлены данные по содержанию биогенных элементов в водах реки. В наибольшей степени перечисленным критериям в исследуемом водотоке отвечает ион аммония, так как его концентрация в водах реки изменяется от 2 до 11 ПДК. Соли аммония токсичны для многих гидробионтов, при их трансформации в аэробных условиях расходуется много кислорода и нарушается кислородный режим, образуются более токсичные нитрит-ионы и нитрозами-ны, они могут также образовываться в экосистеме за счет процессов аммонификации азотсодержащих органических соединений, а также в анаэробных условиях в донных отложениях и мигрировать в водную среду.
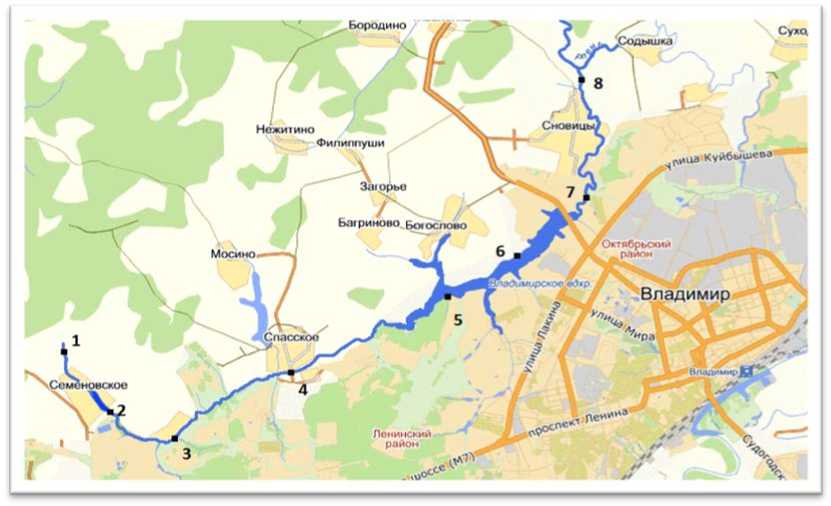
Рис. 1. Бассейн реки Содышка (1-8 пункты отбора проб):
1 – исток (с. Семеновское), 2 – до птицефабрики «Юрьевецкая», 3 – после птицефабрики «Юрьевецкая», 4 – с. Спасское, 5 – поселок РТС, 6 – водохранилище «Содышка», 7 – коллективные сады, 8 – устье (с. Сновицы)
Таблица 1. Пространственно-временная динамика содержания биогенных элементов в воде р. Содышка
|
№ р-ра |
Концентрация N NH4+, мг/дм3 |
Концентрация N NO3- , мг/дм3 |
Фосфор минеральный, мг/дм3 |
||||||
|
2009 г. |
2010 г. |
2011 г. |
2009 г. |
2010 г. |
2011 г. |
2009 г. |
2010 г. |
2011 г. |
|
|
1 |
0,50± |
2,4± |
0,06± |
0,17± |
0,88± |
0,025± |
0,056± |
0,25± |
0,07± |
|
0,032 |
0,087 |
0,004 |
0,038 |
0,096 |
0,002 |
0,003 |
0,013 |
0,005 |
|
|
2 |
0,55± |
1,4± |
0,09± |
0,20± |
0,79± |
0,047± |
0,07± |
0,23± |
0,07± |
|
0,012 |
0,063 |
0,004 |
0,053 |
0,064 |
0,003 |
0,004 |
0,038 |
0,005 |
|
|
3 |
0,89± |
4,3± |
0,56± |
0,45± |
3,5± |
0,174± |
0,18± |
1,37± |
0,2± |
|
0,060 |
0,056 |
0,030 |
0,061 |
0,118 |
0,004 |
0,003 |
0,040 |
0,004 |
|
|
4 |
0,79± |
3,7± |
0,34± |
0,31± |
1,2± |
0,08± |
0,15± |
0,19± |
0,1± |
|
0,078 |
0,108 |
0,021 |
0,040 |
0,087 |
0,04 |
0,0035 |
0,008 |
0,004 |
|
|
5 |
0,96± |
4,4± |
0,48± |
0,39± |
1,65± |
0,1± |
0,13± |
0,15± |
0,1± |
|
0,089 |
0,096 |
0,072 |
0,021 |
0,030 |
0,004 |
0,0036 |
0,0063 |
0,0035 |
|
Так как приоритетным загрязнителем экосистемы р. Содышка является азот аммонийный, актуальным явилось исследование процессов нитрификации, как одного из факторов самоочищения экосистемы от ионов аммония, как в натурных наблюдениях, так и в модельных опытах. В настоящее время процессы нитрификации наиболее полно изучены в почвах [5] и в аэротенках сооружений биологической очистки сточных вод [6]. Процесс нитрификации в аэробных условиях протекает в две стадии и осуществляется двумя группами бактерий:
NH 3 + O 2 + CO 2 → HNO 2 + [CH 2 O]
HNO 2 + O 2 + CO 2 → HNO 3 + [CH 2 O]
Первая группа (р. Nitrosomonas) окисляет ионы аммония до нитритов, вторая (р. Nitrobacter)
– нитриты до нитратов. Энергия, выделяемая при окислении аммиака и нитритов, используется ими для ассимиляции диоксида углерода и синтеза органического вещества. В водных экосистемах, богатых растворенным кислородом, ионы NH 4 + подвергаются быстрому окислению. Перевод катиона в анион ведет к подкислению вод и тем самым к повышению растворимости минералов (солей калия, магния, кальция и фосфорной кислоты).
NH 4 + + 2О 2 = 2NO 3 - + 2H+ +H 2 O
Для исследования процессов нитрификации в водных объектах в натурных условиях нами использовался индекс нитрификации. Индекс нитрификации в воде (Iнитр), характеризующий интенсивность процессов нитрификации в естественных условиях (натурных наблюдениях), рассчитывали по соотношению концентраций азота нитратного к азоту общему минеральному.
Iнитр = NNO3 * 100 / (NNO3- + NNO2- + NNH4+), где NNO3- – концентрация азота нитратного, мг/дм3; NNO2- –концентрация азота нитритного, мг/дм3; NNH4+ – концентрация азота аммонийного, мг/дм3;
На рис. 2 представлена пространственновременная динамика индекса нитрификации в водах р. Содышки в 2009-2011 гг. Из рис. 2 следует, что наиболее интенсивно процессы нитрификации протекали в 2010 г., что, по-видимому, связано с оптимальными для процессов нитрификации температурами воды.
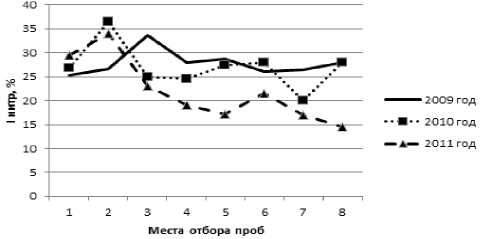
Рис. 2. Пространственно-временная динамика интенсивности процессов нитрификации в экосистеме р. Содышки
Наибольшие значения индекса нитрификации наблюдали с 2009 г. по 2010 г. в истоке и до прицефабрики «Юрьевецкая». В остальных исследованных участках водотока с 2009 по 2011 гг. происходит снижение интенсивности процессов нитрификации, что особенно заметно в устьевом створе и, вероятно, связано с высоким уровнем загрязнения воды токсичными для нит-рификаторов веществами.
Применение корреляционного анализа для выявления зависимости интенсивности процесса нитрификации (I нитр ) от гидрохимических показателей водотока в различных участках (рис. 2) и между отдельными гидрохимическими параметрами позволило установить, что на интенсивность нитрификации наиболее значимое влияние оказывают рН воды (r = 0,92), содержание в воде легко- и трудноокисляемых органических веществ (r соответственно равны 0,91 и – 0,94) и содержание в воде азота аммонийного (r = 0,77).
Исследование процессов нитрификации в экосистеме р. Содышки показало, что наиболее значимыми факторами, влияющими на интенсивность процессов нитрификации, являются соединения биогенных элементов и токсичные для микробиоценоза вещества. Поэтому представляло интерес изучение влияния на превращение азота аммонийного в модельных экспериментах солей аммония, а также анионных синтетических поверхностно-активных веществ (ПАВ) – приоритетных загрязнителей малых водотоков урбанизированных территорий в последние десятилетия. Для изучения влияния этих веществ на микробиоценоз были проведены лабораторные эксперименты с природной водой по моделированию процесса нитрификации. Суть модели заключалась в создании в лабораторных условиях среды, максимально приближенной к природной, но с учетом внесения в одинаковые объемы природной воды различных доз изучаемых веществ. Под воздействием нитрицифиру-ющей микробиоты, содержащейся в природной воде, происходила трансформация солей аммония в нитриты и нитраты.
Для реализации модельных экспериментов нами были отобраны пробы речной воды. Место отбора – водохранилище «Содышка». Выбор места отбора проб обусловлен наименьшим уровнем загрязнения воды солями аммония по сравнению с прочими участками водотока. Отбор проб производился с глубины 0,7-1,0 м. Затем в лаборатории вода была разлита по сосудам в количестве 8 литров в каждый. После того как температура воды сравнялась с комнатной, в пробы были введены различные дозы изучаемых компонентов.
Интенсивность процессов нитрификации оценивалась по степени превращения азота аммония (СП) в %:
СП = (Сн – Ск) * 100 / Сн , где Сн – концентрация азота аммонийного в модельном растворе сразу же после внесения дозы аммония, мг/дм3; Ск – концентрация азота аммонийного в модельном растворе после n суток экспозиции, мг/дм3.
График зависимости степени превращения (СП) азота аммонийного от его концентрации представлен на рис. 3. Кривая зависимости СП от дозы аммония имеет куполообразный вид с четко выраженной зоной оптимума и зонами стресса. Первая часть кривой, характеризующая процессы нитрификации в сосудах 1-5, что соответствует концентрациям аммония от 0 до 6 ПДК, показывает тенденцию к увеличению интенсивности нитрификации с увеличением содержания аммонийного азота в модельном растворе. Максимум функции приходится на шестой сосуд, которому соответствует концентрация азота аммония равная 8 ПДК. При таком содержании аммонийного азота степень превращения составляет 87%. На участке кривой, соответствующему 8-10 ПДК, наблюдается резкое торможение процесса нитрификации, а при содержании аммонийного азота 10-20 ПДК угнетение процесса менее резкое, что, вероятно, связано с адаптацией нитрифицирующих бактерий к солям аммония.
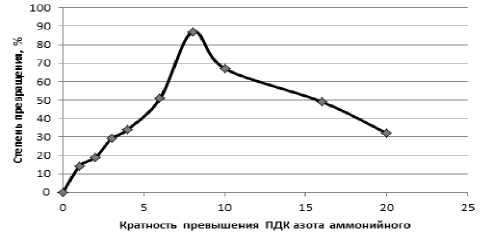
Рис. 3. Зависимость степени превращения азота аммонийного от его концентрации в системе
Основываясь на данных этой модели можно сделать вывод о том, что наиболее интенсивно процессы нитрификации протекают при концентрациях аммония равных 6-8 ПДК. Превышение этого интервала концентраций ведет к угнетению деятельности микробиоты и, как следствие, снижению интенсивности процессов нитрификации. Полученный характер дозоответной реакции можно, вероятно, объяснить тем, что при концентрациях аммонийного азота более 8 ПДК на процессы нитрификации начинает оказывать влияние дефицит кислорода в системе.
Одной из главных задач при оценке состояния водных экосистем является количественная оценка допустимых пределов антропогенного воздействия, при которых сохраняется устойчивость экосистемы [7-8]. Под допустимым антропогенным воздействием понимают нагрузку (складывающуюся из однородных или разнородных воздействий), которая не меняет качества окружающей природной среды или меняет ее в допустимых пределах, при которых не нарушается существующая экологическая система и не возникают неблагоприятные последствия в важнейших популяциях [9]. Из рис. 3 следует, что деятельность нитрифицирующих бактерий начинает угнетаться при концентрации аммонийного азота более 8 ПДК. Исходя из этого, предельно-допустимая нагрузка на исследуемую экосистему по аммонийному азоту равна 9 ПДК.
Приоритетными загрязнителями поверхностных вод в последние десятилетия стали анионные синтетические поверхностно-активные вещества (АСПАВ). Показано, что АСПАВ тормозят деятельность многих гидробионтов, участвующих в процессах самоочищения в экосистемах водных объектов [10]. Исходя из этого представляло интерес исследование влияния синтетических ПАВ – приоритетных загрязнителей водных объектов урбанизированных территорий, на процессы нитрификации в модельных экспериментах. Для лабораторного моделирования в качестве АСПАВ нами использовался додецилсульфат натрия (ДСН). Концентрация аммонийного азота во всех пробах воды при моделировании были равны 10 ПДК. График зависимости степени превращения азота аммонийного от концентрации ДСН представлен на рис. 4.
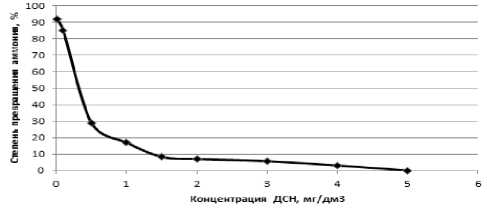
Рис. 4. Зависимость СП азота аммонийного от концентрации ДСН
Кривая зависимости СП азота аммонийного от концентрации ДСН представленная на рис. 4. На ней условно можно выделить 3 зоны. Первая зона – зона максимальной интенсивности процесса нитрификации (СП=92-85%). Она ограничена концентрациями ДСН равными от 0,01 мг/дм3 до 0,1 мг/дм3. Данный интервал концентраций ДСН оказывает минимальное влияние на деятельность нитрифицирующей микробиоты. Вторая зона – зона резкого угнетения деятельности нитрифицирующих организмов. Она соответствует концентрациям ДСН равным от 0,1 до 1,5 мг/дм3. В этом диапазоне концентраций действие ДСН на микробиоценоз характеризуется как острое токсическое. Наблюдается падение степени превращения аммония в 8,5 раз – от 85% до 10%. Третья зона – зона полного прекращения нитрификации. Начиная от точки соответствующей 2 мг/дм3 ДСН кривая дозоответной реакции практически не меняет своего характера, характеризуясь очень низкими значениями интенсивности нитрификации.
Таким образом, АСПАВ даже при незначительных концентрациях оказывают острое токсическое действие на нитрифицирующую микробиоту. Даже незначительные превышения ПДК ДСН в системе приводит к резкому снижению интенсивности процессов нитрификации. При концентрации ДСН 4,024 мг/дм3 нитрификация практически полностью прекращается. Если принять за предельно допустимую нагрузку величину фактора, приводящего к снижению деятельности нитрифицирующих бактерий на
50% [8], то по анионным синтетическим поверх- 2. ностно-активным веществам она составит 0,1 мг/дм3. 3
Выводы: .
-
1 . Разработаны критерии выбора приоритетного загрязнителя эвтрофного водотока, главным образом определяющего характер процес- 4. сов самоочищения в нем.
-
2 . Изучен уровень загрязнения малого эвтрофного водотока соединениями биогенных 5. элементов и органическим веществом и на основе разработанных критериев выбран приоритет- 6. ный загрязнитель, определяющий основной механизм самоочищения водного объекта.
-
3. Изучены процессы нитрификации в эв- 7. трофном водотоке с приоритетным загрязнителем – аммонийным азотом.
-
4. Методами лабораторного моделирования определены предельно-допустимые нагрузки на исследуемый водоток по азоту аммонийному и анионным синтетическим поверхностно-актив- 8.
ным веществам.
Научная публикация подготовлена в рамках государственного задания ВлГУ №2014/13 на выполнение государственных работ в сфере научной деятельности. 9.
Список литературы Оценка предельно-допустимого воздействия на процессы самоочищения в экосистеме малого водотока
- Синельников, В.Е. Механизм самоочищения водоёмов. -М.: Стройиздат, 1980. 250 с.
- Остроумов, С.А. Загрязнение, самоочищение и восстановление водных экосистем. -М.:МАКС-Пресс, 2005. 147 с.
- Эрнестова, Л.С. Самоочищающая способность природной воды как показатель экологического состояния водного объекта/Л.С. Эрнестова, И.В. Семенова//Водные ресурсы. 1994. № 2. С. 161-165.
- Хрисанов, Н.И. Управление эвтрофированием водоемов/Н.И. Хрисанов, Г.К. Осипов. -СПб.: Гидрометеоиздат, 1993. 278 с.
- Умаров, М.М. Микробиологическая трансформация азота в почве/М.М. Умаров, А.В. Кураков, А.Л. Степанов. -М.: ГЕОС, 2007. 264 с.
- Жмур, Н.С. Технологические и биохимические процессы очистки сточных вод на сооружениях с аэротенками. -М.: АКВАРОС, 2003. 512 с.
- Моисеенко, Т.И. Методологические подходы к нормированию антропогенных нагрузок на водоемы Субарктики (на примере Кольского Севера)//Проблемы химического и биологического мониторинга экологического состояния водных объектов Кольского Севера. -Апатиты: Кольский научный центр РАН, 1996. С. 7-23.
- Левич, А.П. Метод расчета экологически допустимых уровней воздействия на экосистемы (метод ЭДУ)/А.П. Левич, А.Т. Терехин//Водные ресурсы. 1997. №3. С. 328-335.
- Израэль, Ю.А. Экология и контроль состояния природной среды. -М.: Гидрометеоиздат, 1984. 560 с.
- Остроумов, С.А. Биологические эффекты при воздействии поверхностно-активных веществ на организм. -М.: МАКС-Пресс, 2001. 334 c.


