Оценка состояния генофондов популяций Pinus sylvestris L. на Урале и прилегающих территориях с использованием двух типов молекулярных маркеров
Автор: Чертов Н.В.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Генетика
Статья в выпуске: 1, 2025 года.
Бесплатный доступ
Исследовано состояние генофондов 11 популяций сосны обыкновенной (Pinus sylvestris L.) на Урале и прилегающих территориях с использованием двух типов высокополиморфных молекулярных маркеров. Анализ полиморфизма межмикросателлитных маркеров показал средний уровень генетического разнообразия вида (P95 = 1.000; I = 0.224; HE = 0.130; ne= 1.319). Анализ полиморфизма нуклеотидных последовательностей трех потенциально адаптивных локусов P. sylvestris выявил гаплотипическое разнообразие (Hd), равное 0.662, а нуклеотидное разнообразие (π) составило 0.004. Тест Таджимы показал наличие отклонений от нейтральности для локуса Pinus-12 (DT = -2.615), что указывает на возможное влияние селективных процессов. Наибольшим генетическим разнообразием обладает популяция из Чердынского (Ps_Ch) р-на (P95 = 0.970; I = 0.264; HE = 0.167; Hd = 0.661), а наименьшим - популяция из Мечетлинского (Ps_Mh) р-на (P95 = 0.853; I = 0.144; HE = 0.089; Hd = 0.650). Выявлены популяции с типичными (КГО 1.000) генофондами. Установлено, что у 7 изученных популяций P. sylvestris состояние генофондов удовлетворительное, а у 4 популяций наблюдается обеднение генофондов. Представленный подход позволяет выявить ключевые особенности их генофондов, необходимых для разработки мероприятий по сохранению и восстановлению генетических ресурсов сосны обыкновенной.
Полиморфизм днк, маркеры, оценка состояния генофондов, урал
Короткий адрес: https://sciup.org/147251168
IDR: 147251168 | УДК: 575.22 | DOI: 10.17072/1994-9952-2025-1-80-88
Evaluation of the state of gene pools of Pinus sylvestris L. populations in the Urals and adjacent territories using two types of molecular markers
The state of gene pools of 11 populations of Scots pine (Pinus sylvestris L.) in the Urals and adjacent territories was studied using two types of highly polymorphic molecular markers. Analysis of polymorphism of inter simple sequence repeats markers showed an average level of genetic diversity of the species (P95 = 1.000; I = 0.224; HE = 0.130; ne= 1.319). Analysis of polymorphism of nucleotide sequences of three potentially adaptive loci of P. sylvestris revealed haplotype diversity (Hd) equal to 0.662, and nucleotide diversity (π) was 0.004. Tajima test showed the presence of deviations from neutrality for the Pinus-12 locus (DT = -2.615), which indicates the possible influence of selective processes. The population from Cherdynsky (Ps_Ch) district has the highest genetic diversity (P95 = 0.970; I = 0.264; HE = 0.167; Hd = 0.661), and the population from Mechetlinsky (Ps_Mh) district has the lowest (P95 = 0.853; I = 0.144; HE = 0.089; Hd = 0.650). Populations with typical (CGO 1.000) gene pools were identified. It was found that the state of the gene pools of 7 studied populations of P. sylvestris is satisfactory, and depletion of the gene pools is observed in 4 populations. The presented approach allows us to identify the key features of their gene pools, which are necessary for the development of measures to preserve and restore the genetic resources of Scots pine.
Текст научной статьи Оценка состояния генофондов популяций Pinus sylvestris L. на Урале и прилегающих территориях с использованием двух типов молекулярных маркеров
Ускоряющиеся изменения климата, сопровождающиеся увеличением частоты и длительности засух, становятся причиной масштабных лесных пожаров, что наносит значительный ущерб лесным экосистемам и лесному хозяйству [Allen et al., 2010; Gauthier et al., 2015; Кузнецова и др., 2021]. Для понимания механизмов адаптации древесных растений к изменяющимся условиям важным направлением исследований становится изучение генетических основ адаптации популяций. Формирование генетической изменчивости и способность к адаптации зависят от взаимодействия эволюционных факторов и структуры популяций, что играет ключевую роль в приспособлении видов к новым экологическим вызовам [Eriksson, 1998; Namkoong, 2001; González-Martínez et al., 2006; Рябухина и др., 2019]. Оценка состояния генофондов лесообразующих видов растений позволяет определить подходы к сохранению генофондов видов на уровне отдельных популяций, а также выделить локальные популяции, наиболее перспективные для сохранения и воспроизводства вида. Однако популяционный подход в сохранении биоразнообразия растений остается слабо разработанным [Путенихин, 2013].
Сосна обыкновенная ( Pinus sylvestris L.) – второй по распространенности вид хвойных растений в мире, играет важную экономическую и экологическую роль [Floran et al., 2011]. Леса с ее преобладанием занимают 37% от общей площади мировых лесов и около 70% лесов Северного полушария [Mirov, 1967; Floran et al., 2011]. Этот вид отличается высокой генетической изменчивостью, которая определяет его количественные и качественные характеристики, включая признаки с адаптивным значением [Kavaliauskas et al., 2022; Чертов, 2024].
Для анализа гетерогенных природных популяций растений требуется молекулярно-генетическое исследование их генофондов с использованием как минимум двух типов высокополиморфных молекулярных маркеров, способных выявлять полиморфизм различных структурных элементов генома [Боронни-кова, 2013].
На Урале, прилегающих к нему территориях и на востоке Русской равнины ранее проводились исследования по оценке состояния генофондов P. sylvestris . Изучаемые популяции в целом характеризовались удовлетворительным состоянием генофонда [Сбоева, 2024]. Однако ранние исследования проводились с использованием только одного типа маркеров – ISSR (Inter-Simple Sequence Repeat) -маркеров. Использование двух типов маркеров позволяет повысить точность оценки состояния генофондов и получить более полные данные о генетическом разнообразии популяций.
Таким образом, цель настоящего исследования – оценка состояния генофондов популяций сосны обыкновенной на Урале и прилегающих территориях с использованием двух типов высокополиморфных молекулярных маркеров.
Материал и методы исследования
В качестве объектов исследования для оценки состояния генофондов на основании полиморфизма двух типов молекулярных маркеров были избраны 11 популяций (рисунок) сосны обыкновенной ( Pinus sylvestris L.; Pinaceae). Исследуемые популяции P. sylvestris расположены: Чердынский р-н ( Ps_Ch ), Гай-нский р-н ( Ps_Gn ), Усольский р-н ( Ps_Rm ), Кудымкарский р-н ( Ps_Ln ), Кишертский р-н ( Ps_Pr ), Большесосновский р-н ( Ps_Bl ), Пермский р-н ( Ps_Uk ), Добрянский р-н ( Ps_Pl ) (все – Пермский край); Каслинский р-н Челябинской обл. ( Ps_Ar ), Мечетлинский ( Ps_Mh ) и Салаватский ( Ps_Sl ) р-ны Республики Башкортостан.
Географические расстояния между популяциями варьировали от минимальных 61 км между PS_Uk и PS_Bl до максимальных 628 км между популяциями PS_Gn и PS_Sl . Сбор растительного материала проводили с деревьев, расположенных на расстоянии не менее 50–150 м друг от друга.
Для проведения исследования образцы растительных тканей были индивидуально отобраны с 31 дерева в каждой из исследуемых популяций. ДНК из образцов выделяли с использованием CTAB-метода [Rogers, Bendich, 1985], при этом масса сухого растительного материала для каждого образца составляла около 20 мг. Концентрацию и качество выделенной ДНК оценивали с помощью спектрофотометра NanoDrop™ 2000 (Thermo Fisher Scientific Inc., Уолтем, Массачусетс, США). Для проведения полимеразной цепной реакции (ПЦР) концентрацию ДНК в каждом образце приводили к уровню 10 нг/мкл.
Для оценки генетического разнообразия и структуры популяций применялся ISSR-анализ полиморфизма ДНК [Zietkiewicz et al., 1994]. Продукты ПЦР разделяли методом электрофореза на 1.7% агарозном геле в буфере 1×TBE при напряжении 120 В в течение 3 час. Для визуализации гели окрашивали бромистым этидием и фотографировали в ультрафиолетовом свете с использованием системы документации Gel Doc XR+ (Bio-Rad Laboratories, Inc., Hercules, Калифорния, США). Длину фрагментов определяли с помощью маркера молекулярной массы (100 п.н. + 1.5 + 3 Кб DNA Ladder, ООО «СибЭнзим-М», Москва, Россия) и программы Quantity One 1-D Analysis (Bio-Rad Laboratories, Inc.). Был проанализирован полиморфизм ISSR-маркеров с использованием в ПЦР 5 праймеров и проб ДНК 333 индивидуальных деревьев P. sylvestris. Для обеспечения достоверности результатов каждая ПЦР повторялась не менее трех раз.
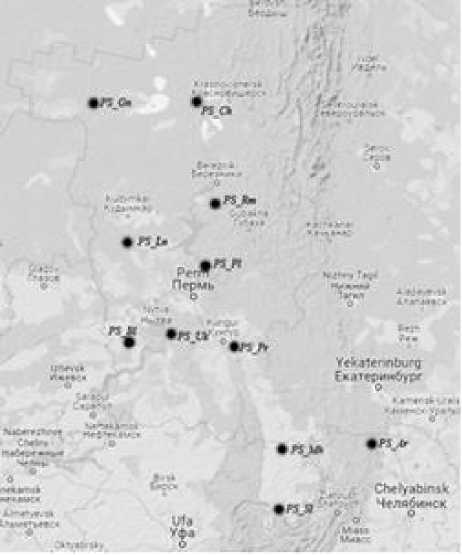
Карта-схема расположения изученных популяций P. sylvestris :
Ps_Ch –Чердынский р-н, Ps_Gn –Гайнский р-н, Ps_Rm –Усольский р-н, Ps_Ln –Кудымкарский р-н, Ps_Pr – Кишертский р-н, Ps_Bl – Большесосновский р-н, Ps_Uk – Пермский р-н, Ps_Pl – Добрянский р-н, Ps_Ar – Каслинский р-н, Ps_Mh –Мечетлинский р-н, Ps_Sl –Салаватский р-н
[Schemаtic map of the location of the studied populations of P. sylvestris :
Ps_Ch – Cherdynsky district, Ps_Gn – Gaynsky district, Ps_Rm – Usolsky district , Ps_Ln – Kudymkarsky district, Ps_Pr – Kishertsky district, Ps_Bl – Bolshesosnovsky district, Ps_Uk – Permsky district, Ps_Pl – Dobryansky district, Ps_Ar – Kaslinsky district, Ps_Mh – Mechetlinsky district, Ps_Sl – Salavatsky district]
Для изучения полиморфизма нуклеотидных последовательностей P. sylvestris проводилось секвенирование трёх локусов ( Pinus-11, Pinus-12, Pinus-15 ), выбранных ранее [Chertov et al., 2024]. Очистку продуктов ПЦР проводили смесью ферментов ExoI и FAST-AP («Fermentas», Литва) в отношении 0.5:1 из расчета 1.5 мкл ферментативной смеси на 5 мкл продуктов ПЦР. Реакцию проводили в амплификаторе GeneAmp PCRSystem 9700 («Applied Biosystems», США) по программе: 37°C – 30 мин., 80°C – 15 мин., охлаждение до 4°C.
Для сeквeнирования применяли набор BigDye® Terminator v3.1 Cycle Sequencing Kit («Applied Biosys-tems», США). В качeствe праймeра использованы сначала прямая, а затем обратная послeдоватeльности из пары, с которой была поставлeна ПЦР. Амплификацию проводили в термоциклере GeneAmp PCRSystem 9700 («Applied Biosystems», США) по программe: 5 мин. – 94°C, следующие 30 циклов (94°C – 30 сек., Т отж °C – 45 сек., 72°C – 2 мин.), 72оС – 10 мин. Очистку продуктов реакции сeквeнирования от нeвступивших в реакцию мeчeных нуклeотидов осуществляли с помощью набора BigDye® XTermina-torTM Purification Kit («Applied Biosystems», США). В исследовании использовался метод автоматического ферментативного секвенирования. Капиллярный электрофорез синтeзированных послeдоватeльностeй проведен в лаборатории молекулярных и генетических технологий кафeдры ботаники и гeнeтики растeний ПГНИУ (Россия) на 24-капиллярном гeнeтичeском анализаторe Genetic Analyzer 3500xL («Ap-plied Biosystems», США) в двух направлениях. Нуклеотидные последовательности трех локусов ДНК были секвенированы в среднем у восьми деревьев из каждой популяции.
В программе DNASP v5 [Librado, Rozas, 2009] были реконструированы гаплотипы и на основе сравнения их нуклеотидных последовательностей рассчитаны следующие показатели нуклеотидного поли- морфизма: число вариабельных сайтов (S), число гаплотипов в популяции (hn), общее гаплотипическое разнообразие (Hd) по М. Нею [Nei, 1973], нуклеотидное разнообразие (π), оценивающее среднее число парных различий между двумя последовательностями ДНК и являющееся мерой генетической изменчивости вида или популяции, параметр нуклеотидного разнообразия, вычисленный исходя из числа мутаций (θW), или оценка Уоттерсона [Nei, 1987].
Компьютерный анализ данных проведен по стандартным для молекулярно-генетического анализа программам [Yeh, Yang, Boyle, 1999; Peakall, Smouse, 2006]. Уровень внутрипопуляционного разнообразия оценивался с помощью показателей: среднее число морф (μ) и доля редких морф (h) [Животовский, 1980]. Выявление специфических особенностей генофондов проводилось с использованием метода расчета коэффициента генетической оригинальности (КГО) [Потокина, Александрова, 2008], модифицированного для дикорастущих древесных видов растений [Боронникова, 2013]. Для оценки состояния генофондов популяций сосны обыкновенной была взята за основу методика С.В. Боронниковой [2013].
Результаты и их обсуждение
Для оценки состояний генофондов 11 популяций сосны обыкновенной в регионе исследований были определены параметры генетического разнообразия. Доля полиморфных локусов ( P 95 ) в них варьировала от 0.719 до 0.970, а на общую выборку этот показатель составил 1,000. Следующий параметр, ожидаемая гетерозиготность ( H E ), находился в пределах от 0.089 до 0.141. Абсолютное число аллелей на локус ( n a ), а в данном случае на фрагмент ДНК на общую выборку, составило 2.000; для отдельных популяций этот параметр варьировался от 1.307 до 1.640. Эффективное число аллелей на локус ( n e ) на общую выборку равнялся 1.319, для отдельных популяций этот параметр был от 1.135 до 1.271 (табл. 1). В результате внутрипопуляционного анализа выявлено, что показатель разнообразия ( μ ) у изученных популяций находился в диапазоне от 1.632 до 1.761. Также была определена доля редких морф ( h ), отражающая сбалансированность генетической структуры популяции. Значения доли редких морф более 0.300 свидетельствует о нарушении генетической структуры популяции (табл. 1).
Таблица 1
|
Генетическое разнообразие изученных одиннадцати популяций P. sylvestris [Genetic diversity of the nine P. sylvestris populations studied] |
|||||||
|
Популяции |
P 95 |
H E |
n a |
n e |
I |
μ |
h |
|
Ps_Gn |
0.940 |
0.141 (0.013) |
1.627 (0.485) |
1.217 (0.287) |
0.228 (0.019) |
1.691 (0.005) |
0.155 (0.003) |
|
Ps_Pr |
0.969 |
0.169 (0.014) |
1.634 (0.483) |
1.271 (0.321) |
0.266 (0.021) |
1.761 (0.005) |
0.120 (0.002) |
|
Ps_Ln |
0.900 |
0.140 (0.013) |
1.614 (0.483) |
1.215 (0.284) |
0.227 (0.019) |
1.675 (0.006) |
0.162 (0.003) |
|
Ps_Ch |
0.970 |
0.167 (0.014) |
1.640 (0.481) |
1.263 (0.310) |
0.264 (0.020) |
1.756 (0.005) |
0.122 (0.002) |
|
Ps_Rm |
0.902 |
0.148 (0.013) |
1.608 (0.490) |
1.229 (0.294) |
0.236 (0.020) |
1.695 (0.005) |
0.153 (0.003) |
|
Ps_Ar |
0.719 |
0.106 (0.014) |
1.307 (0.463) |
1.178 (0.312) |
0.159 (0.021) |
1.639 (0.007) |
0.180 (0.003) |
|
Ps_Bl |
0.942 |
0.148 (0.014) |
1.529 (0.501) |
1.233 (0.300) |
0.231 (0.021) |
1.749 (0.005) |
0.126 (0.003) |
|
Ps_Mh |
0.853 |
0.089 (0.012) |
1.399 (0.491) |
1.135 (0.244) |
0.144 (0.017) |
1.632 (0.007) |
0.184 (0.003) |
|
Ps_Sl |
0.870 |
0.120 (0.014) |
1.438 (0.498) |
1.193 (0.298) |
0.188 (0.020) |
1.665 (0.006) |
0.167 (0.003) |
|
Ps_Uk |
0.823 |
0.083 (0.013) |
1.274 (0.448) |
1.136 (0.271) |
0.128 (0.019) |
1.683 (0.007) |
0.159 (0.004) |
|
Ps_Pl |
0.879 |
0.120 (0.014) |
1.399 (0.491) |
1.194 (0.304) |
0.184 (0.021) |
1.743 (0.006) |
0.128 (0.003) |
|
На общую выборку |
1.000 |
0.130 (0.004) |
2.000 |
1.319 (0.254) |
0.205 (0.006) |
- |
- |
Примечание: H E – ожидаемая гетерозиготность; n a – абсолютное число аллелей на локус; n e – эффективное число аллелей на локус; I – информационный индекс Шеннона; μ – показатель внутрипопуляционного разнообразия; h – доля редких морф; у всех вышеуказанных параметров в скобках даны стандартные отклонения.
Анализ генетического разнообразия в 11 популяциях P. sylvestris проведен на основании полиморфизма SNP-маркеров трех локусов. Полученные данные о гаплотипическом разнообразии ( Hd = 0.662) свидетельствуют о среднем уровне генетического разнообразия, что согласуется с результатами других исследований [Wachowiak at al., 2014; Wachowiak at al., 2024]. Нуклеотидное разнообразие (π = 0.004) и оценка Уоттерсона ( θ W = 0.013) также подтверждают наличие генетических различий между популяциями. Эти показатели указывают на стабильное генетическое состояние популяций с учетом их адаптации к различным условиям среды. С использованием теста Таджимы выявлено (табл. 2), что наибольшее отклонение от нейтральности наблюдалось для локуса Pinus-12 ( D T = -2.615). Отрицательное значение теста указывает на возможный избыток низкочастотных аллелей, что может быть результатом положительного отбора или демографических событий, таких как сокращение популяции или расширение ареала.
Таблица 2
Общее гаплотипическое и нуклеотидное разнообразие и статистика теста на нейтральность для трех локусов P. sylvestris
[Total haplotype and nucleotide diversity and neutrality test statistics for three P. sylvestris loci]
|
Локус |
Hd |
π |
θ W |
D T |
|
Pinus-11 |
0.737 (0.028) |
0.004 (0.000) |
0.006 |
-0.890 |
|
Pinus-12 |
0.630 (0.040) |
0.005 (0.001) |
0.032 |
-2.615 |
|
Pinus-15 |
0.620 (0.025) |
0.003 (0.000) |
0.002 |
0.925 |
|
Среднее |
0.662 (0.010) |
0.004 (0.002) |
0.013 |
- |
Примечание: Hd – общее гаплотипическое разнообразие; π – нуклеотидное разнообразие; θ W – оценка Уоттерсона или нуклеотидное разнообразие, вычисленное из числа мутаций; D T – коэффициент D- теста Таджимы; в скобках указаны стандартные отклонения.
В целом, по данным нуклеотидного разнообразия (табл. 3) наиболее генетически гетерогенными являются популяции Ps_Ar ( Hd = 0.697; π = 0.003; θ = 0.003 ), Ps_Bl ( Hd = 0.692; π = 0.003; θ = 0.003 ) и Ps_Ch ( Hd = 0.661; π = 0.004; θ = 0.013 ), а наименее – популяции Ps_Gn ( Hd = 0.472; π = 0.005; θ = 0.005 ) и Ps_Pr ( Hd = 0.478; π = 0.004; θ = 0.004 ).
Таблица 3
Общее гаплотипическое и нуклеотидное разнообразие популяций P. sylvestris [Total haplotype and nucleotide diversity of P. sylvestris populations]
|
Популяции |
Hd |
π |
θ |
|
Ps_Gn |
0.472 |
0.005 |
0.005 |
|
Ps_Pr |
0.478 |
0.004 |
0.004 |
|
Ps_Ln |
0.614 |
0.002 |
0.002 |
|
Ps_Ch |
0.661 |
0.004 |
0.003 |
|
Ps_Rm |
0.675 |
0.003 |
0.003 |
|
Ps_Ar |
0.697 |
0.003 |
0.003 |
|
Ps_Bl |
0.692 |
0.003 |
0.003 |
|
Ps_Mh |
0.650 |
0.003 |
0.004 |
|
Ps_Sl |
0.592 |
0.002 |
0.002 |
|
Ps_Uk |
0.659 |
0.003 |
0.003 |
|
Ps_Pl |
0.653 |
0.004 |
0.006 |
|
На общую выборку |
0.662 |
0.004 |
0.013 |
Примечание: Hd – общее гаплотипическое разнообразие; π – нуклеотидное разнообразие; θ W – оценка Уоттерсона или нуклеотидное разнообразие, вычисленное из числа мутаций.
Один из подходов к классификации внутрипопуляционного разнообразия по результатам молeкуляр-ного маркирования с определением коэффициента генетической оригинальности (КГО) был предложен E.К. Потокиной и Т.Г. Алeксандровой [2008] на примере изучения типичности и специфичности сортов вики посевной ( Vicia sativa L.). Для хвойных древесных видов растений этот подход применен С.В. Бо-ронниковой [2013]. Данный подход основан на принципе «взвешивания» признаков в зависимости от частоты их встречаемости.
Для оценки состояния генофондов популяций установленные при молекулярно-генетическом анализе параметры генетического разнообразия P. sylvestris разделены на четыре группы [Боронникова, 2013]. К первой (I) группе относятся «Основные показатели генетического разнообразия», т. е. доля полиморфных локусов ( P 95 ) и ожидаемая гетерозиготность ( H E ). Вторую группу (II) параметров генетического разнообразия составляют показатели внутрипопуляционного разнообразия, которые характеризуются на популяционном уровне информационным индексом Шеннона ( I ), показателем внутрипопуляционного разнообразия ( μ ) и на нуклеотидном уровне общим гаплотипическим разнообразием ( Hd ) . Генетическую структуру и дифференциацию популяций (группа III) предлагаем характеризовать показателем доля редких морф ( h ) , рассчитанным на основании полиморфизма ISSR ( h ISSR ) и SNP-маркеров ( h SNP ). Четвертая группа (IV) показателей отражает «специфику генофондов», которая оценивается коэффициентом генетической оригинальности (КГО), рассчитанным на основании полиморфизма ISSR-маркеров.
Для оценки состояния генофондов популяций каждому из вышеперечисленных параметров присваивались баллы в зависимости от их величины, что позволило ранжировать показатели генетического разнообразия популяций (табл. 4)
Баллы суммировались, и на основе полученной суммы давалась итоговая оценка состояния генофонда: «удовлетворительное состояние» (9–14 баллов), «обеднение генофонда» (5–8 баллов) или «деградация генофонда» (0–4 балла). Такой подход предоставляет всестороннюю оценку состояния генофондов 84
популяций, что позволяет оперативно выявлять популяции с риском утраты генетического разнообразия и необходимостью проведения мероприятий по их охране и восстановлению.
Таблица 4
Шкала оценки состояния генофондов популяций Pinus sylvestris L. [Scale for assessing the state of gene pools of Pinus sylvestris L. populations]
|
Параметр |
Высокое значение |
Среднее значение |
Низкое значение |
|
P 95 |
> 0.90 (2 балла) |
0.70–0.90 (1 балл) |
< 0.70 (0 баллов) |
|
H E |
> 0.15 (2 балла) |
0.10–0.15 (1 балл) |
< 0.10 (0 баллов) |
|
I |
> 0.25 (2 балла) |
0.15–0.25 (1 балл) |
< 0.15 (0 баллов) |
|
μ |
> 1.70 (2 балла) |
1.60–1.70 (1 балл) |
< 1.60 (0 баллов) |
|
Hd |
> 0.65 (2 балла) |
0.50–0.65 (1 балл) |
< 0.50 (0 баллов) |
|
hISSR |
< 0.10 (2 балла) |
0.10–0.20 (1 балл) |
> 0.20 (0 баллов) |
|
hSNP |
< 0.10 (2 балла) |
0.10–0.20 (1 балл) |
> 0.20 (0 баллов) |
Примечание: P 95 – доля полиморфных локусов; H E – ожидаемая гетерозиготность; I – информационный индекс Шеннона; μ – показатель внутрипопуляционного разнообразия; Hd – общее гаплотипическое разнообразие; h ISSR – доля редких морф, рассчитанная на основании ISSR маркирования; h SNP – доля редких морф, рассчитанная на основании SNP-маркирования.
Таким образом, бо́льшая часть изученных популяций (7 популяций) характеризуется высокими показателями генетического разнообразия и, соответственно, удовлетворительным состоянием генофондов (табл. 5). Четыре изученные популяции ( Ps_Ar, Ps_Mh, Ps_Sl, Ps_Uk ) характеризуются сниженным генетическим разнообразием и меньшей сбалансированностью генетической структуры, что свидетельствует об обеднении их генофондов.
Таблица 5
Оценка состояния генофондов популяций Pinus sylvestris L. [Assessment of the state of gene pools of Pinus sylvestris L. populations]
|
Популяция |
I. Основные показатели генетического разнообразия |
II. Внутрипопуляцион-ное разнообразие |
III. Генетическая структура и дифференциация |
IV. Специфика генофондов |
Оценка состояния генофондов |
||||||
|
P 95 |
He |
I |
μ |
Hd |
h issr |
hSNP |
КГО |
тип |
Балл |
Состояние |
|
|
Ps_Gn |
0.940 |
0.141 |
0.228 |
1.691 |
0.472 |
0.155 |
0.165 |
0.772 |
Т |
9 |
удовлет. |
|
Ps_Pr |
0.969 |
0.169 |
0.266 |
1.761 |
0.478 |
0.120 |
0.112 |
0.874 |
Т |
11 |
удовлет. |
|
Ps_Ln |
0.900 |
0.140 |
0.227 |
1.675 |
0.614 |
0.162 |
0.159 |
0.761 |
Т |
10 |
удовлет. |
|
Ps_Ch |
0.970 |
0.167 |
0.264 |
1.756 |
0.661 |
0.122 |
0.126 |
0.743 |
Т |
12 |
удовлет. |
|
Ps_Rm |
0.902 |
0.148 |
0.236 |
1.695 |
0.675 |
0.153 |
0.095 |
0.783 |
Т |
11 |
удовлет. |
|
Ps_Ar |
0.719 |
0.106 |
0.159 |
1.639 |
0.697 |
0.180 |
0.087 |
1.256 |
С |
7 |
обеднение |
|
Ps_Bl |
0.942 |
0.148 |
0.231 |
1.749 |
0.692 |
0.126 |
0.074 |
0.995 |
Т |
11 |
удовлет. |
|
Ps_Mh |
0.853 |
0.089 |
0.144 |
1.632 |
0.650 |
0.184 |
0.098 |
1.147 |
С |
6 |
обеднение |
|
Ps_Sl |
0.870 |
0.120 |
0.188 |
1.665 |
0.592 |
0.167 |
0.137 |
0.994 |
Т |
8 |
обеднение |
|
Ps_Uk |
0.823 |
0.083 |
0.128 |
1.683 |
0.659 |
0.159 |
0.124 |
1.182 |
С |
8 |
обеднение |
|
Ps_Pl |
0.879 |
0.120 |
0.184 |
1.743 |
0.653 |
0.128 |
0.134 |
1.494 |
С |
10 |
удовлет. |
Примечание: P 95 – доля полиморфных локусов; H E – ожидаемая гетерозиготность; I – информационный индекс Шеннона; μ – показатель внутрипопуляционного разнообразия; Hd – общее гаплотипическое разнообразие; h ISSR – доля редких морф, рассчитанная на основании ISSR маркирования; h SNP – доля редких морф, рассчитанная на основании SNP-маркирования; КГО – коэффициент генетической оригинальности; жирным выделены наибольшие значения показателей, наименьшие значения показателей выделены жирным курсивом.
С целью сохранения генофонда ценного лесообразующего вида растений P. sylvestris рекомендуется отбирать как популяции с типичными (базовыми) генофондами, так и популяции, обладающие специфическими особенностями генофондов, являющиеся резервом генетической изменчивости. Отбор при этом базируется на количественных характеристиках генетического разнообразия, рассчитанных на основании анализа полиморфизма высокополиморфных молекулярных маркеров [Боронникова, 2013]. Для отбора в качестве объектов сохранения генофондов могут быть рекомендованы популяции, обладающие высоким уровнем генетического разнообразия. Например, популяции PS_Pr и PS_Ch , характеризующиеся невысокими значениями КГО, т. е. типичным для местности генофондом и наибольшими показателями генетического разнообразия. Кроме того, популяции PS_Ar и PS_Uk , для которых характерно в целом обедненное состояние генофонда, но имеющие специфичные генофонды, могут быть рекомендованы для отбора в качестве резерва специфичных аллелей. Также, учитывая данные SNP-маркеров для отбора, следует рекомендовать популяции PS_Ar и Ps_ Bl , характеризующиеся высоким генетическим разнообразием в локусах потенциально адаптивных генов.
В целом, изученные популяции P . sylvestris демонстрируют средний уровень генетического разнообразия ( P 95 = 1.000; I = 0.224; H E = 0.130; n e = 1.319). Данный уровень генетического разнообразия ниже, чем у популяций Южного Урала ( H E = 0.239), Оренбургского Зауралья ( H E = 0.161) и некоторых популяций Восточно-Европейской равнины ( H E = 0.170) [Рябухина и др., 2019; Khanova et al., 2020; Сбоева, 2023].
Различия в уровнях генетического разнообразия могут быть обусловлены влиянием антропогенных факторов, в частности интенсивностью лесозаготовок и другими формами хозяйственной деятельности. Кроме этого, в данном исследовании изучен полиморфизм нуклеотидных последовательностей трех потенциально адаптивных локусов P . sylvestris , проведен анализ полиморфизма SNP-маркеров на популяционном уровне, что существенно дополняет подход к оценке состояния генофондов популяций P. sylvestris в регионе исследований.
Заключение
Состояние генофондов популяций сосны обыкновенной на Урале и прилегающих территориях демонстрирует значительное генетическое разнообразие исследованных популяций. Наибольшую генетическую устойчивость показывают популяции Ps_Pr и Ps_Ch , которые обладают высокой долей полиморфных локусов, ожидаемой гетерозиготностью и информационным индексом Шеннона. Эти популяции представляют собой базовый генофонд, который необходимо сохранять для поддержания адаптивного потенциала вида.
В то же время популяции с обеднением генофонда, такие как Ps_Uk и Ps_Mh , характеризуются низкими значениями ключевых показателей генетического разнообразия, что свидетельствует о снижении внутрипопуляционной изменчивости и возможной утрате адаптационных способностей. Эти популяции требуют внедрения мероприятий по поддержанию и восстановлению генетического разнообразия. Особое внимание следует уделить популяциям Ps_Ar и Ps_Bl , которые, несмотря на общий обедненный генофонд, демонстрируют уникальные аллели, способные стать резервом для адаптации вида в условиях изменяющегося климата.
Использование SNP-маркеров позволило более точно охарактеризовать адаптивные особенности популяций, выявив отклонения от нейтральности и указывая на наличие локусов, связанных с адаптацией к специфическим условиям среды. Эти данные подчеркивают необходимость интеграции нескольких типов молекулярных маркеров для комплексного анализа генетического разнообразия на популяционном уровне и оценки состояния генофондов популяций.
Полученные результаты имеют большое значение для разработки стратегий сохранения и управления генофондом сосны обыкновенной. Дифференцированный подход, включающий сохранение как типичных, так и специфичных популяций, позволит эффективно поддерживать генетическое разнообразие вида. В условиях усиливающегося воздействия антропогенных факторов и климатических изменений сохранение генетического ресурса сосны обыкновенной становится важной задачей для обеспечения устойчивости экосистем и сохранения биоразнообразия.


