Оценка состояния микроциркуляторного кровотока при эмболизации маточных артерий методом капилляроскопии
Автор: Завалко Александр Федорович, Нурмухаметова Эльмира Тимеровна, Антипов Евгений Валерьевич
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.26, 2018 года.
Бесплатный доступ
В настоящем исследовании описаны виды реакции микроциркуляторного русла у женщин с клиническими проявлениями постэмболизационного синдрома после лечения миомы матки методом эмболизации маточных артерий. Была проведена компьютерная капилляроскопия ногтевого ложа 3-го пальца руки у 78 женщин с миомой матки, поступивших в гинекологическое отделение на лечение малоинвазивным эндоваскулярным методом эмболизации маточных артерий. Исследование микроциркуляторного русла ногтевого ложа использовали в качестве метода оценки микроциркуляторного кровотока в организме в целом у пациенток в послеоперационном периоде. Изучение микроциркуляции проводили в динамике до эмболизации маточных артерий и после. У 96% пациенток в послеоперационном периоде возник постэмболизационный синдром различной степени тяжести, по которым пациентки были распределены на 3 группы. По данным капилляроскопии можно сделать предварительное заключение о наличии определенных изменений показателей микроциркуляции в динамике в зависимости от степени выраженности постэмболизационного синдрома. Метод капилляроскопии позволяет осуществлять прижизненное изучение микроциркуляции, исследовать реактивность сосудистых звеньев в зависимости от тяжести развития симптомов в послеоперационном периоде у пациенток.
Микроциркуляция, эмболизация маточных артерий, капилляроскопия
Короткий адрес: https://sciup.org/143177260
IDR: 143177260
The evaluation of the microcirculatory blood flow during uterine artery embolization by the method of capillaroscopy
This study describes the types of microcirculatory reaction in women with clinical manifestations of the postembolization syndrome after treatment of uterine fibromyoma by uterine artery embolization. A computerized capillaroscopy of the 3rd finger nail bed was conducted in 78 women with uterine myoma who were admitted to the gynecological department for treatment with the minimally invasive endovascular embolization of the uterine arteries. The study of the microvasculature of the nail bed was used as a method for assessing the microcirculatory blood flow in the body as a whole in patients in the postoperative period. The study of microcirculation was performed in dynamics before uterine artery embolization and after. In 96% of patients in the postoperative period, a postembolization syndrome of varying severity occurred, in which the patients were divided into 3 groups. According to capillaroscopy data, a preliminary conclusion can be made about the presence of certain changes in microcirculation indices in dynamics depending on the severity of the postembolization syndrome. The capillaroscopy method allows for the in vivo study of microcirculation, to investigate the reactivity of vascular units, depending on the severity of the development of symptoms in the postoperative period in patients.
Текст научной статьи Оценка состояния микроциркуляторного кровотока при эмболизации маточных артерий методом капилляроскопии
Завалко А.Ф., Нурмухаметова Э.Т., Антипов Е.В. Оценка состояния микроциркуляторного кровотока при эмболизации маточных артерий методом капилляроскопии// Морфологические ведомости.- 2018.- Том 26.- № 3.- С. 14-17. (26).03.14-17
Zavalko AF, Nurmukhametova ET, Antipov EV. The evaluation of the microcirculatory blood flow during uterine artery embolization by the method of capillaroscopy. Morfologicheskie Vedomosti – Morphological Newsletter. 2018 Oct 31;26(3):14-17. (26).03.14-17
Введение . Прогресс и достижения современной медицины позволяют все шире использовать в лечении пациентов малоинвазивные и высокоэффективные методы. Одним из них является эмболизация маточных артерий (далее - ЭМА) - малоинвазивный эндоваскулярный метод лечения миомы матки [1-2]. Его преимуществом является отсутствие необходимости общего наркоза, сохранение органа и его функции, сокращение продолжительности вмешательства, отсутствие многочисленных противопоказаний. Облитерация эмболами магистральных маточных сосудов в послеоперационном периоде у большинства пациенток вызывает постэмболизационный синдром (далее - ПС), продолжительность и выраженность которого варьирует от легкой до тяжелой степени тяжести [3-4]. В настоящее время микроциркуляторное русло кожи используется в качестве модели для исследования микроциркуляторного кровотока не только регионарно в определенной области, но и в организме в целом при различных заболеваниях, например, артериальной гипертонии, сердечной и почечной недостаточности, хронической венозной недостаточности нижних конечностей и других [5-6]. Известно, что искусственное нарушение микроциркуляции в области миоматозных узлов как рефлекторно, так и опосредованно через медиаторы может вызывать изменения микроциркуляции в других органах и тканях, усугубляя клиническую симптоматику ПС. Представляет интерес оценка реакции микроциркуляторного русла при различных вариантах течения (степени тяжести) ПС. Для оценки капиллярного кровообращения, тонуса сосудов и происходящих в них изменений используется компьютерная капилляроскопия ногтевого ложа - неинвазивный метод обследования и визуализации морфологии капилляров [7-8]. Компьютерная капилляроскопия зарекомендовала себя как информативный, неинвазивный и достаточно точный метод исследования и функциональной оценки микроциркуляторного русла. С его помощью можно прицельно изучить и визуализировать состояние и форму капилляров, плотность капиллярной сети, линейную и объемную скорости кровотока [9-10].
Цель исследования - оценить реактивные изменения микроциркуляторного русла ногтевой фаланги у женщин в зависимости от степени тяжести течения постэмболизационного синдрома.
Материал и методы исследования . В исследование были включены 78 пациентки в возрасте от 24 до 51 года, страдающие миомой матки и поступившие на лечение методом ЭМА. Группу исключения составили пациентки, страдающие сердечно-сосудистыми заболеваниями тяжелой степени, сахарным диабетом, атеросклеротическими изменениями тяжелой степени, хронической венозной недостаточностью, облитерирующим эндартериитом, болезнью Рейно, травмами, деформацией и инфекционными поражениями ногтевых фаланг. Общий размер матки у пациенток группы наблюдения варьировал от 7 до 15 недель беременности, размеры отдельных узлов варьировали от 21 до 96 мм в диаметре. У всех женщин диагностирована прогрессирующая миома, с наличием клинической симптоматики в виде менометроррагий, тянущих болей внизу живота различной интенсивности, учащенного мочеиспускания и запоров. Компьютерная капилляроскопия выполнялась трижды: до лечения ЭМА на 1-2 сутки после хирургического вмешательства и на 5 сутки. Исследование выполнялось в положении сидя после 15-минутного отдыха. При выполнении капилляроскопии соблюдались условия, рекомендованные в руководстве по эксплуатации используемого оборудования. Исследование проводилось при наличии добровольного информированного согласия пациента на исследование, с соблюдением необходимых этических требований, предъявляемых к исследованиям с участием человека. Капиллярный кровоток изучался в области эпонихия 3го пальца правой руки, для чего палец помещался в специальное устройство для его мягкой фиксации. При этом рука находилась на уровне сердца. Источником освещения объекта служила галогеновая лампа мощностью 50W. Видеозапись капиллярного кровотока проводилась по шести различным капиллярам продолжительностью 10 секунд для каждого. Информация, полученная при исследовании, обрабатывалась с помощью программного обеспечения, входящего в комплект к используемому оборудованию - компьютерному капилляроскопу КК4-01-«ЦАВ» (регистрационное удостоверение № ФСР 2010/06980 от 01 марта 2010 года) ЗАО Центр «Анализ веществ» (Москва) [9-10].
Протокол исследования капилляроскопии включал определение следующих параметров: плотность капилляров (1/N) - площадь, занятая микрососудами, 1 на мм2; периваскулярная зона, мкм; диаметр капилляра (артериальная часть), мкм; диаметр капилляра (средняя часть), мкм; диаметр капилляра (венозная часть), мкм; скорость движения эритроцитов (артериальная часть), мкм/с; скорость движения эритроцитов (венозная часть), мкм/с. В ближайшие часы после ЭМА у 96% обследуемых пациенток был диагностирован постэмболизационный синдром [11]. Наиболее выраженная клиническая симптоматика ПС зарегистрирована через 10-18 часов после вмешательства и до вторых суток послеоперационного периода. Основным клиническим проявлением ПС явился болевой симптом. По нашим наблюдениям боль максимальной интенсивности диагностирована через 12 часов после ЭМА, средняя продолжительности болевого симптома составила 31,4 часа, что соответствует данным других авторов [12-13]. С третьих суток ПС болевые ощущения постепенно уменьшались. К 5 суткам постэмболизационного периода боли стихали. Оценка степени тяжести ПС проводилась по балльной системе, предложенной коллективом исследователей под руководством Ю.Э. Доброхотовой [3], с выделением постэмболизационного синдрома легкой степени тяжести - до 7 баллов, средней степени тяжести - 8-14 баллов, тяжелой степени тяжести - 15-21 баллов. Выраженность болевой симптоматики оценивалась по визуально-аналоговой шкале (далее - ВАШ) от 0 до 10 баллов [14]. Все наблюдаемые пациенты были распределены на 3 группы, в зависимости от тяжести течения ПС. Постэмболизационный синдром легкой степени (I группа) наблюдался у 36 пациенток (46,2%), умеренной степени (II группа) - у 30 (38,4%), выраженной степени (III группа) - у 12 женщин (15,4%).
Результаты исследования и обсуждение . Распространенность и интенсивность проявления болевого симптома представлена на рис. 1. При оценке результатов капилляроскопии до ЭМА, на 1-2 сутки (в течение 12-36 ч) и на 5 сутки послеоперационного периода, было установлено, что к 5 суткам происходило восстановление нормальной микроциркуляции у 98% пациенток. При исследовании микроциркуляторного русла у пациенток с миомой матки до и после лечения были получены следующие данные. У 20 пациенток (25,6%) в течение первых - начале вторых суток боли были выраженными и составили 8-10 баллов, у 32 женщин (41%) - умеренно выраженными от 4 до 7 баллов, у 25 пациенток (32,1%) - слабо выраженными от 1 до 3 баллов, у 1 пациентки (1,3%) боли отсутствовали. К концу 2 суток (более 36 часов после ЭМА) три пациентки оценили боль как сильную, 16 - отметили умеренные боли, 51 - слабые боли, у 8 пациенток -боли отсутствовали. После 5 суток на умеренные боли жаловались только 2 пациентки, по поводу чего им проведено комплексное лечение постэмболизационного синдрома, слабые боли зарегистрированы у 25 (32,1%) пациенток, у остальных женщин (52 человек) - боли отсутствовали. Повышение лейкоцитов крови имело место у 41 женщин (52,6%). Кровянистые выделения из половых путей зарегистрированы у 54 пациенток (69,2%), в основном при наличии интерстициального и интерстициально-субмукозного расположения узлов. Гипертермия, 380С и более, наблюдалась у 12 пациенток с размерами узлов более 5,5 см. Максимальные клинические проявления постэмболизационного синдрома диагностировались в зависимости от тяжести на первые-вторые сутки.
При легкой степени ПС лечение заключалось в использовании папаверина, анальгетиков. В микроциркуляторном русле отмечалось снижение плотности капиллярной сети; уменьшение диаметров сосудов во всех звеньях капиллярной сети. В I группе, кроме уменьшения диаметра сосудов, также отмечалось уменьшение скорости кровотока в артериальном и венозном звеньях, что способствовало формированию перикапиллярного отека [5]. Несмотря на изменения показателей плотности капилляров и скорости эритроцитов до и после ЭМА, они оставались в пределах нормальных значений. Диаметры сосудов во всех отделах значительно уменьшились по сравнению с показателями до ЭМА, регистрируемые значения стали ниже нормы. У пациенток I группы при капилляроскопии был выявлен спазм сосудов , замедление скорости кровотока и увеличение периваскулярной зоны, что свидетельствовало о появлении отека на 2 сутки после ЭМА [11]. Указанные проявления, по-видимому, связаны с всасыванием продуктов некроза при локальной ишемии в сосудистое русло. На рис. 2 видна бледность, спазм сосудов после ЭМА.
При средней степени выраженности ПС во II группе клиническая картина характеризовалась: болями по шкале ВАШ до 7-8 баллов, повышением температуры тела от нормальных значений до 38оС, кровянистыми скудными выделениями; у 26 (86,6%) отмечался лейкоцитоз от 9х109/л до 11х109/л. При капилляроскопии выявлено уменьшение краевой плотности капилляров, плотности капилляров на единицу площади. Увеличение диаметра сосудов венозного отдела сопровождалось сужением сосудов переходного и артериального звеньев, при этом показатели оставались в пределах нормальных значений. Как видно на рис. 3 у пациентки «А» со средней степенью тяжести ПС отмечалась бледность и отек периваскулярной зоны, который был явно более выражен, чем у пациентки с легкой степенью ПС (рис. 2).
Основной Основной Основной Основной Основной Основной Основной Основной Основной
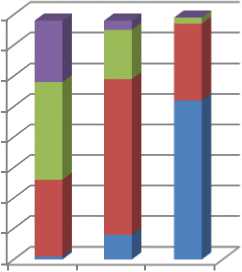
■ сильные
■ умеренные
■ слабые
■ нет болей
1 сутки 2 сутки 5 сутки
В III группе пациенток постэмболизационный синдром протекал с выраженным болевым симптомом (до 10 баллов по шкале ВАШ), купировался анальгетиками ненаркотического и наркотического действия. Температура повышалась 38оС и выше, лейкоцитоз составил 11,0×109/л и выше. Диагностировалась гиперфибриногенемия, нарушения со стороны желудочно-кишечного тракта, мочевыделительной системы, сердечно-сосудистой системы в виде тахикардии. Двум пациенткам была выполнена катетеризация мочевого пузыря. По данным капилляроскопии на 2 сутки отмечалось увеличение краевой плотности капиллярной сети и уменьшение плотности капиллярной сети на единицу площади Нами было зарегистрировано незначительное увеличение диаметров сосудов венозного звена и снижение на диаметров сосудов
Рис. 1. Распределение пациенток по выраженности болевого симптома после ЭМА.

А Б
Рис. 2. Капилляроскопия пациентки «М» с легкой степенью постэмболизационного синдрома до (А) и после (Б) эмболизации на 2 сутки наблюдения. Ув.:×200 (левый) и ×400 (правый) рисунки.

А Б
Рис. 3. Капилляроскопия пациентки «А» со средней степенью постэмболизационного синдрома до и после эмболизации на 2 сутки наблюдения. Ув.:×200 (левый) и ×400 (правый) рисунки.
артериального звена по сравнению с исходной картиной капилляроскопии до применения ЭМА. Сужение сосудов артериального звена капиллярной сети во II и III группах может служить показателем компенсаторной реакцией на развивающийся венозный застой [5].

Рис. 4. Капилляроскопия пациентки «Н» с выраженным постэмболизационным синдромом до и после эмболизации на 2 сутки наблюдение. Ув.:×200 (левый) и ×400 (правый) рисунки.
Во II и III группах наблюдаемых женщин установлена прямая корреляционная зависимость некоторых показателей капилляроскопии от уровня повышения температуры тела и степени интоксикации: увеличение скорости кровотока в венозном звене во II и III группах. Во всех трех группах отмечалось увеличение периваскулярной зоны сопряжено со степенью тяжести постэмболизационного синдрома. Полученные данные свидетельствуют большая степень интоксикации организма вызывает более выраженный отек в микроциркуляторном русле. Отек интерстиция развивается вследствие нарушения механизма поддержания гидростатического давления в капиллярах. Патологический процесс, характеризующийся объемным дефицитом капиллярного кровотока, приводит к повреждению механизмов регуляции гемодинамики в капиллярах, от которых зависит транскапиллярный перенос жидкости. Снижение интенсивности капиллярного кровотока приводит к развитию капиллярного стаза в метаболическом звене микроциркуляторного русла, снижается капиллярная перфузия, уменьшается функционирующая поверхность обменных микрососудов, развивается тканевая гипоксия. Все эти патофизиологические механизмы нарушения микроциркуляции приводят в дальнейшем к изменениям энергетического метаболизма в клетках, развивается ацидоз интерстициального и клеточного компартментов [5].
Заключение . Послеоперационный период после ЭМА характеризуется различной тяжестью течения и степенью клинических проявлений. Чем выше степень интоксикации, тем более выражен постэмболизационный синдром. Интоксикация сопровождается изменениями в микроциркуляторном капиллярном русле в виде периваскулярного отека; снижения скорости кровотока при отсутствии повышения температуры тела; спазма сосудов. При повышении температуры тела скорость кровотока увеличивается. Таким образом, компьютерная капилляроскопия позволяет объективно зарегистрировать ранние признаки нарушения состояния микроциркуляторного русла – спазм артериолярных сосудов, застойные явления в венулах, снижение интенсивности кровотока в капиллярном звене микроциркуляторного русла. С помощью неинвазивного прижизненного изучения микроциркуляции можно определять реактивность отдельных сосудистых звеньев микроциркуляторного русла. Таким образом биомикроскопия капилляров позволяет получить объективную оценку структурных параметров сосудистого русла.
Список литературы Оценка состояния микроциркуляторного кровотока при эмболизации маточных артерий методом капилляроскопии
- Savel'eva G.M., Breusenko V.G., Krasnova I.A., Kapranov S.A. Embolizatsiya matochnykh arteriy pri miome matki kak al'ternativa khirurgicheskomu lecheniyu // Mezhdunarodnyy meditsinskiy zhurnal. 2005.- № 1.- S. 74-79.
- Sidorova I.S. Mioma matki (sovremennye aspekty etiologii, patogeneza, klassifikatsii i profilaktiki).- M: MIA, 2003.- S. 5-66.
- Embolizatsiya matochnykh arteriy/ Pod red. E.Yu. Dobrokhotovoy.- SPb: Eksten Medikal, 2013.- 112s.
- Spencer EB, Stratil P, Mizones H. Clinical and Periprocedural Pain Management for Uterine Artery Embolization. Semin Intervent Radiol. 2013 Dec;30(4):354-63.
- Kozlov V.I. Kapillyaroskopiya v klinicheskoy praktike: monografiya.- M.: Prakticheskaya meditsina, 2015.- 232s.
- Sirotin B.Z., Zhmerenetskiy K.V. Mikrotsirkulyatsiya pri serdechno-sosudistykh zabolevaniyakh.- Khabarovsk, 2008.- 150s.
- Logina A.V., Supil'nikov A.A., Antipov E.V. Obzor metodov vozdeystviya na mikrotsirkulyatsiyu kozhi// Vestnik Meditsinskogo instituta «REAVIZ».- 2015.- №3(19).- S. 57-61.
- Logina A.V., Supil'nikov A.A., Antipov E.V., Stolyarov S.A. Vliyanie glikolevoy kisloty na mikrotsirkulyatsiyu krovi v kozhe pri vozrastnykh izmeneniyakh// Vestnik Meditsinskogo instituta «REAVIZ».- 2016.- №3 (23).- S. 106-110.
- Gurfinkel' Yu.I., Voeykov V.L., Kondakov S.E., Korol' O.A., Kufal' G.A. Ustroystvo dlya avtomaticheskoy registratsii dinamicheskikh kharakteristik protekaniya protsessa (komp'yuternyy kapillyaroskop). Patent RF na izobretenie № 2129266 ot 15.05.98.
- Gurfinkel' Yu.I., Voeykov V.L., Kondakov S.E., Korol' O.A., Kufal' G.A. Model'nyy eksperiment s dlitel'noy izolyatsiey: problemy i dostizheniya.- M.: Slovo, 2001.- S. 306-313.
- Kapranov S.A., Dobrokhotova Yu.E., Bobrov B.Yu., Alieva A.A. Postembolizatsionnyy sindrom pri endovaskulyarnom lechenii miomy matki// Mezhdunarodnyy zhurnal interventsionnoy kardioangiologii.- 2005.- № 7.- S. 24.
- Bruno J, Sterbis K, Flick P et al. Recovery after uterine artery embolization for leiomyomas: a detailed analysis of its duration and severity. J Vasc Interv Radiol. 2004;15(8):801-807.
- Pron G, Bennett J, Common A, Wall J, Asch M, Sniderman K. Ontario Uterine Fibroid Embolization Collaboration Group. The Ontario Uterine Fibroid Embolization Trial. Part 2. Uterine fibroid reduction and symptom relief after uterine artery embolization for fibroids. Fertil Steril 2003;791:120-127.
- Huskisson EC. Measurement of pain. Lancet. 1974 Nov 9;2(7889):1127-1131.
- Ivanova O.V., Soboleva G.N., Karpov Yu.I. Sostoyanie endoteliya pri arterial'noy gipertenzii i drugikh faktorakh riska razvitiya ateroskleroza// Kardiologiya.- 1997.- № 9.- S. 80-83.
- Logina A. V., Supilnikov A. A., Antipov E. V. review of the methods of influence on the microcirculation of the skin. Bulletin of medical Institute "REAVIZ": rehabilitation, doctor and health. 2015;3 (19):57-61.


