Оценка состояния микроциркуляторного русла кожи лица методом лазерной допплеровской флоуметрии
Автор: Давыдова А.В., Моррисон А.В., Утц С.Р., Меглинский И.В., Лычагов В.В.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Кожные болезни
Статья в выпуске: 2 т.8, 2012 года.
Бесплатный доступ
Цель: изучение и возможность оптимизации измерения микроциркуляции кровотока в коже человека методом лазерной допплеровской флоуметрии (ЛДФ) с учетом различных топографо-анатомических особенностей периферийного кровоснабжения биотканей. Материал и методы. Аппаратом ЛДФ обследованы 20 человек в возрасте от 20 до 56 лет без признаков поражения кожи. Аппарат ЛДФ имеет два источника излучения в красном световом диапазоне на длине волны 650±30 нм и в ближнеинфракрасном на длине волны 805±50 нм. Регистрация излучения осуществлялась четырьмя приемными волокнами, расположенными на расстояниях 1, 2, 3 и 4 мм от освещающего волокна. Состояние сосудов микроциркуляторного русла исследовали в четырех точках кожи лица: в середине лба, в области центра щеки справа и симметричной точке щеки слева и области подбородка. Рассчитывали среднее значение показателя микроциркуляции, его среднеквадратическое отклонение и коэффициент вариации. Результаты. Варьируя расстояние от освещающего до приемного волокна и длину волны падающего излучения, методом ЛДФ определены значения микроциркуляции на различных участках здоровой кожи лица. Методом Монте Карло сделаны оценки объема зондируемой ткани, пространственной локализации ЛДФ-сигнала в тканях и эффективной глубины детектирования. Установлено, что изменения ЛДФ-сигнала находятся в прямой зависимости от структурных особенностей строения микроциркуляторного русла, глубины залегания и плотности функционирующих капилляров. Заключение. Предложенный метод может быть использован для диагностики состояния биологического объекта в норме и при патологии, а также при оценке эффективности лечения различных дерматозов.
Кожа, кровоток, лазерная допплеровская флоуметрия, микроциркуляция, сосудистое русло
Короткий адрес: https://sciup.org/14917589
IDR: 14917589
Текст научной статьи Оценка состояния микроциркуляторного русла кожи лица методом лазерной допплеровской флоуметрии
-
1 Вв едение. В настоящее время в связи интенсивным развитием лазерных и оптических технологий наблюдается устойчивая тенденция развития методов изучения состояния тканевого кровотока [1]. Разработанные методы оптической микроскопии позволяют вести непосредственный визуальный мониторинг за состоянием микроциркуляции крови и объективно оценивать такие показатели, как морфология и тонус микрососудов, агрегатное состояние крови, а также выявлять различные внутри- и внесосудистые изменения и ряд других признаков, важных для патогенетической характеристики изучаемого процесса. Однако исследование микроциркуляторного русла методами оптической микроскопии существенно ограничено и возможно лишь на поверхности тканей (на глубине менее 300 мкм по толщине), обычно в ногтевом ложе или конъюнктиве глазного яблока.
Ультразвук с использованием эффекта Допплера обеспечивает необходимое пространственно-временное разрешение измерения скорости кровотока в сосудах различных тканей, но пространственное разрешение метода ограничено до 200 мкм по глубине зондирования. Магнитно-резонансная ангиография предоставляет в основном информацию о больших кровеносных сосудах, таких как коронарная артерия, и не даёт возможности регистрировать изменения кровотока в периферическом сосудистом русле. Недостатки оптической когерентной томографии (ОКТ): высокая чувствительность к непроизвольным движениям объекта исследования и невозможность реги страции значений потоков в лимфатических и крове
Адрес: г. Саратов, ул. Навашина, д.30, кв. 55.
Тел.: +79179861126.
носных сосудах менее 50 мкм в диаметре и скорости течения в них менее 100 мкм/с.
Наиболее чувствительным методом регистрации динамики процессов микроциркуляции крови в биотканях является метод диффузионной волновой спектроскопии [2]. А его аналог — метод лазерной допплеровской флуометрии (ЛДФ) на сегодняшний день, по-видимому, является наиболее доступным методом оценки состояния микроциркуляции кровотока и позволяет получить объективную информацию об усреднённых параметрах кровотока (перфузии) микро-циркуляторного русла с любого участка поверхности тела в режиме реального времени. Вместе с тем весьма актуальными остаются методологические проблемы анализа измеряемого допплеровского сигнала и оценки показателей кровотока на заданной глубине, что существенно ограничивает повседневное применение данной методики в клинической практике. Это обусловливает необходимость поиска новых подходов к анализу данных ЛДФ для более эффективной оценки состояния сосудистого русла и своевременной коррекции лечебного процесса.
Цель : изучение и возможность оптимизации измерения микроциркуляции кровотока в коже человека методом ЛДФ с учётом различных топографо-анатомических особенностей периферийного кровоснабжения биотканей.
Методы . Состояние сосудов микроциркуляторно-го русла на различных участках кожи лица проводили на базе аппарата ЛДФ (рис. 1), разработанного кафедрой оптики и биофотоники ФГБОУ ВПО «Саратовский государственный университет имени Н. Г. Чернышевского».
Рис. 1. Аппарат лазерной допплеровской флоуметрии
Аппарат ЛДФ, используемый в данном исследовании, включает два модуля: измерительный зонд и базовый блок, соединенных посредством гибкого кабеля. Измерительный зонд содержит освещающие и приемные оптические волокна, фотоприемники и предусилители сигнала. Базовый блок содержит лазерные модули, драйверы лазерных диодов и согласующие каскады усилителей. Доставка лазерного излучения от лазерных диодов к измерительному зонду осуществляется посредством оптического волокна. Соединительный кабель содержит оптическое волокно, сигнальные провода и провода питания усилителей. Питание драйверов лазерных диодов осуществляется от сети переменного тока 220 В, 50 Гц. Питание усилителей фототока осуществляется от двух батарей типа 6 F22.
В ЛДФ данной модификации используются два источника лазерного излучения в красном световом диапазоне на длине волны 650±30 нм и в ближнеинфракрасном на длине волны 805±50 нм с мощностью излучения 5 мВт и 2 мВ соответственно. Выбор длин волн зондирующего излучения основан на различии коэффициентов поглощения окисленной и восстановленной форм гемоглобина (рис. 2). Для красного света с длиной волны λ 1 = 650±30 нм поглощение восстановленного гемоглобина существенно превы-
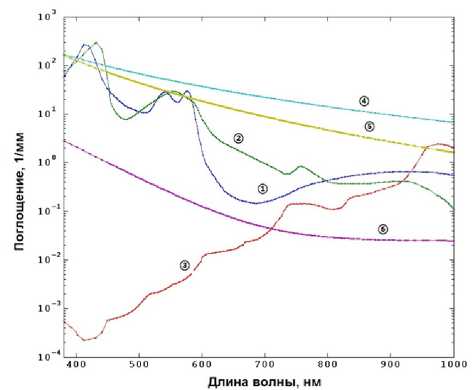
Рис. 2. Спектр поглощения различных составляющих биоткани. Поглощение основных хромофоров кожи человека в зависимости от длины волны оптического излучения:
1 — окисленный гемоглобин HbO2, 2 — восстановленный гемоглобин Hb, 3 — вода, 4 — эумеланин, 5 — феомеланин, 6 — прочие поглотители шает поглощение окисленного гемоглобина. В инфракрасной области при λ2=805±50 нм поглощение оптического излучения этими формами гемоглобина одинаково (изобестическая точка, см. рис. 2). Это позволяет разделять изменение ЛДФ-сигнала, связанного с изменением скорости эритроцитов или с физиологическими изменениями, обусловленными изменением оксигенации крови.
От источника света лазерное излучение посредством оптоволокна доставляется к исследуемому биологическому объекту. Внутри биологического объекта оптическое излучение претерпевает многократное рассеяние и переотражение на границах раздела клеточной структуры кожи и подкожных тканей, а также частично поглощается содержащимися в тканях хромофорами, такими, как окисленный и восстановленный гемоглобин, меланин, жир, вода — межклеточная жидкость, βкаротин, билирубин и др. [3]. Рассеянное и ослабленное за счет поглощения излучение детектируется на поверхности исследуемого биологического объекта (рис. 3). Регистрация осуществляется четырьмя приемными волокнами, расположенными на расстояниях 1, 2, 3, и 4 мм от освещающего волокна. Диаметр сердцевины освещающего и приемных волокон составляет 0,2 мм. Посредством оптоволокна сигнал обратно рассеянного оптического излучения доставляется на фотоприемник, который осуществляет линейное преобразование оптического сигнала I (Л) в электрический сигнал U (Л). Далее регистрируемый сигнал U (Л) проходит аналоговую обработку (усиление, фильтрацию и т.п.) в электронном блоке, оцифровывается и передается в компьютер для последующих математических преобразований и анализа. Управление прибором осу-
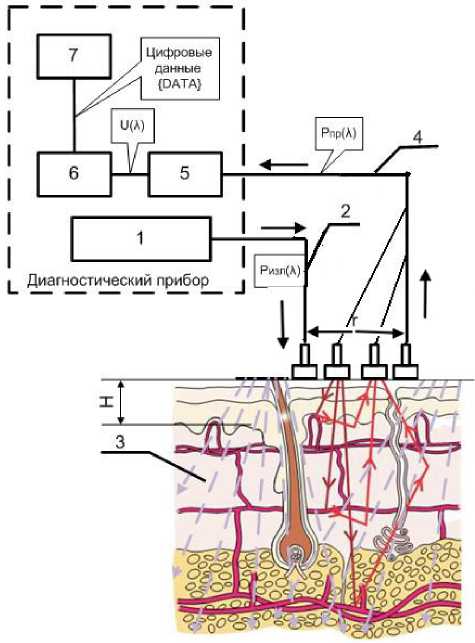
Рис. 3. Обобщённая функциональная схема измерений «на отражение» в ЛДФ ществляется посредством компьютерной программы FlowMeter.
Средние значения интенсивности и частоты флуктуаций интенсивности регистрируемого фотоприемником сигнала зависят от средней скорости движения рассеивающих частиц и их концентрации [4]. Для восстановления параметров микроциркуляции анализируется спектр фотоэлектрического сигнала U (λ) , представляющий собой распределение энергии P (ƒ) детектируемого излучения по частоте ƒ. Затем вычисляется нулевой и первый спектральные моменты, определяемые в общем виде для момента N -го порядка как M N = ƒ N P (ƒ) dƒ . Нулевой спектральный момент представляет собой среднюю энергию фотоэлектрического сигнала и пропорционален среднему объему крови, протекающему через исследуемый объем за единицу времени. Первый момент определяет средний объем перфузии — произведение среднеквадратичной скорости движения рассеивателей на их концентрацию. Отношение первого момента к нулевому представляет собой средневзвешенную частоту флуктуаций фотоэлектрического сигнала и пропорционален среднеквадратичной скорости движения рассеивающих свет частиц, т.е. эритроцитов.
Представленным методом ЛДФ были обследованы 20 человек в возрасте от 20 до 56 лет без признаков поражения кожи, с относительно стабильной центральной гемодинамикой и нормальными показателями, отражающими реологические свойства крови. В исследовании участвовали здоровые лица мужского и женского пола, в возрасте не моложе 18 и не старше 60 лет, у которых на протяжении 6 месяцев, предшествовавших исследованию: не было признаков кожных заболеваний; отсутствовали признаки анамнестических заболеваний, которые могли бы привести к стойкому нарушению функционального состояния сердечно-сосудистой и дыхательной систем; не была выявлена отягощенная наследственность по кожным заболеваниям. Критерии исключения включали: физиологическое состояние (например, беременность, лактация и др.); онкологические заболевания; прием фотосенсибилизаторов и антикоагулянтов; фотодерматит; декомпенсированные заболевания, которые могут повлиять на результаты измерений (например, органические поражения центральной нервной системы, декомпенсированная патология сердечно-сосудистой системы, эндокринологические и иммунологические нарушения, больные с острой почечной или печеночной недостаточностью, коллагенозы, патология органов зрения); нарушение целостности кожных покровов; вирусные и гнойничковые поражения кожи [5].
Все измерения проводились в положении лежа, после 10-минутной стабилизации гемодинамики в помещении при температуре 20-23 °С и неярком освещении. На кожу после ее предварительного обезжиривания спиртовым раствором прикладывался контактный накожный датчик диаметром 1,0 см. Затем осуществлялись пятикратные измерения кровотока с последующим их усреднением и последовательной записью 5-секудных разверток на жесткий диск персонального компьютера.
Последовательно измеряли кровоток по четырем основным точкам в течение 5 минут в каждой из них: в середине лба, в области центра щеки справа и симметричной точке щеки слева и области подбородка. Общая продолжительность одного исследования 30 минут.
Регистрировали и рассчитывали следующие показатели: среднее значение показателя микроцирку- ляции (ПМ) и его среднеквадратическое отклонение (σ), характеризующее переменную составляющую микроциркуляции, и коэффициент вариации (К). Статистическую обработку данных производили на компьютере с использованием пакетов программ для статистического анализа Excel и Statistica 6.0. Критический уровень достоверности (р) нулевой статистической гипотезы (об отсутствии значимых различий) принимали равным 0,05
Результаты. Диагностика состояния микроциркуляции крови осуществлялась методом ЛДФ с четырех приемных волокон на длинах волн 0,65 мкм и 0,805 мкм. Регистрируемая ЛДФ-грамма (графическая запись непрерывно регистрируемого в течение всего времени исследования ЛДФ-сигнала) содержит фрагменты с различными типами колебаний, отличающихся по частоте и амплитуде. Происхождение колебаний связано с пространственной ориентацией сосудов, а также с различными значениями числа эритроцитов и скорости кровотока, предопределяемых структурой капиллярного дерева в исследуемом участке ткани [6]. В этой связи возникает необходимость анализа пространственной локализации ЛДФ-сигнала в тканях кожи и определения парциальных вкладов различных элементов сосудистого русла дермальных слоев в детектируемом ЛДФ-сигнале.
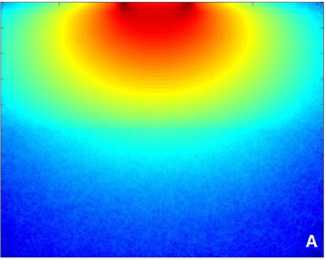
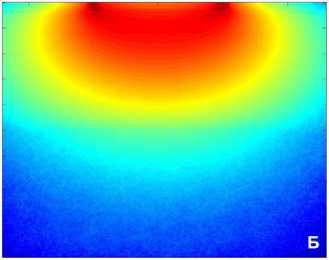
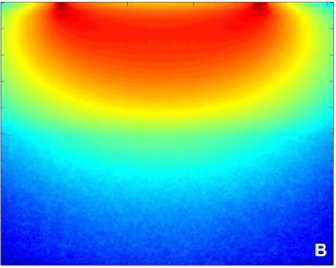
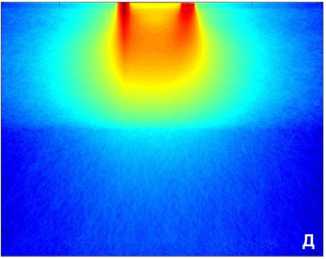
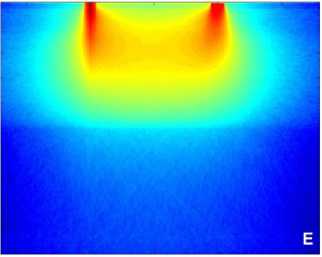
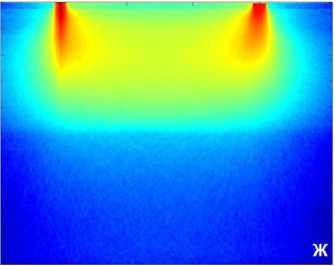
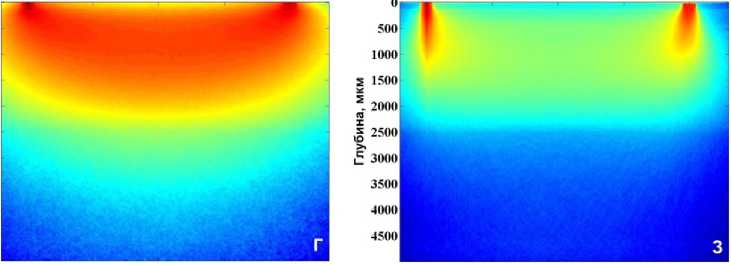
Для каждого из положений приемных волокон, т.е. на расстояниях 1, 2, 3 и 4 мм от освещающего волокна методом Монте Карло [7] сделаны расчёты пространственной локализации ЛДФ-сигнала в тканях кожи, позволяющих оценить объем зондируемой ткани и эффективную глубину детектирования. Результаты расчётов представлены на рис. 4.
Зондирующее излучение с длиной волны λ = 0,65 мкм характеризуется значительным поглощением гемоглобина и относительной прозрачностью оксигемоглобина (см. рис. 4). Легко видеть, что при увеличении расстояния от освещающего волокна до приемного волокна с 1 мм до 4 мм позволяет увеличить эффективную глубину зондирования в 3-4 раза и тем самым увеличить объём измеряемой области в 6-10 раз (см. рис. 4, А-Г). Результаты моделирования показывают, что, несмотря на сложный неоднородный характер распределения различных элемен-товсосудистого русла в зондируемом объеме ткани [3, 5, 6, 8], пространственное распределение детектируемого сигнала оказывается довольно равномерным с ярко выраженным максимумом в верхних дермальных слоях. При этом для 0,805 мкм, начиная с глубины 300 мкм, эффективная область измерений практически равномерно распределена вплоть до глубинных дермальных кровеносных слоев (см. рис. 4, Д-З). Наиболее сильно рассеивающие свет поверхностные слои кожи, в сочетании с разницей в показателях преломления слоев, оказывают своего рода экранирующий эффект при вводе / выводе зондирующего излучения, что является крайне нежелательным. Увеличение расстояния значительно уменьшает френелевское отражение на границе раздела «воздух –кожа», что, в свою очередь, приводит к уменьшению вклада рогового слоя и эпидермиса в детектируемый сигнал.
Результаты проведённого моделирования наглядно показывают, что увеличение расстояния на поверхности кожи между освещающим и принимающим волокнами и изменение длины волны падающего излучения фактически позволяют осуществлять сканирование тканей кожи по глубине (рис. 4), захватывая различные элементы сосудистого русла. Таким об-
Глубина, мкм Глубина, мкм Глубина, мкм Глубина, мкм
Положение оптических волокон на поверхности кожи 0
-1000
О 1000 Длина, мкм
Положение оптических волокон на поверхности кожи 0
-1000
0 1000 2000
Длина, мкм
Положение оптических волокон на поверхности кожи 0
Длина, мкм
S
S
Положение оптических волокон на поверхности кожи ri' 201111
I 2500
-1000
0 1000
Длина, мкм
Положение оптических волокон на поверхности кожи 0
5 зооо
= 2000
! 2500
-1000
ПИЮ 2<Ю0
Длина, мкм
Положение оптических волокон на поверхности кожи 0
- 2000
in 2500
Длина, мкм
Положение оптических волокон на поверхности кожи
Положение оптических волокон на поверхности кожи
о
1000 2000 3000
Длина, мкм
1000 2000 3000
Длина, мкм
,10°
Ю1
1О2
1О'3
Ю5
I1Q-6
О
to
О
СО
ь
О
О
О
ГО
ГО
го
Рис. 4. Пространственная локализация ЛДФ-сигнала в тканях кожи, рассчитанная методом Монте Карло [7]: А-Г — на длине волны 650±30 нм и Д-З — на длине волны 805±50 нм на расстояниях 1, 2, 3, и 4 мм от освещающего волокна соответственно разом, на базе полученных результатов становится возможным оценить распределение эритроцитов в зондируемом объеме ткани и изменение перфузии, которая характеризует кровоток в микрососудах.
Сравнение основных показателей микроциркуляции, зарегистрированных в коже центральной области щеки справа и слева методом ЛДФ, не выявило достоверных статистических различий между ними. ПМ справа составил 12,39±0,21 перф. ед., а слева — 12,38±0,16 перф. ед. (p>0,05). Коэффициент асимметрии для ПМ составил 0,009, что свидетельствует об отсутствии различий. На основании комплексного морфофункционального изучения состояния кожной микроциркуляции показано, что вариабельность показателей микроциркуляции в различных топографо-анатомических областях кожи лица находится в прямой зависимости от структурных особенностей строения микроциркуляторного русла этих областей, глубины залегания микрососудов и плотности функционирующих капилляров. Нормированный первый спектральный момент, представляющий собой отношение первого момента к нулевому, имел прямую пропорциональную зависимость от канала регистрации отраженного излучения на длинах волн 650 нм и 805 нм.
Значения основных параметров микроциркуляции крови кожи лица варьировали в довольно широких пределах. Значения показателя микроциркуляции (ПМ) в коже лба колебались от 7,68 пф. ед. до 12,16 пф. ед., составляя в среднем 9,92±0,54 пф. ед., в области центра правой щеки — от 9,5 до 15,29 пф. ед., в среднем 12,39±0,21 пф. ед., в области центра левой щеки — от 8,97 до 15,80пф. ед., в среднем 12,38±0,16 пф. ед., а в области подбородка — от 4,63 до 9,22 пф. ед. в среднем 6,93±0,54 пф. ед. Показатель микроциркуляции (ПМ) может быть высоким, как при увеличении перфузии тканей кровью, так и при венозном застое [8]. Среднее квадратичное отклонение (σ) при увеличении своего численного значения указывает на активность функции регуляторных механизмов. А коэффициент вариации (К) — соотношение о/ПМ *100%, характеризует активность сосудов микроциркуляторного русла и определяет в основном процентный вклад вазомоторного компонента в общую модуляцию тканевого кровотока. Чем он выше, тем больше вазомоторная активность сосудов. Средние значения основных показателей микроциркуляции в различных участках кожи лица представлены в таблице.
Средние значения основных показателей микроциркуляции в различных участках кожи лица
|
Участок кожи лица |
Показатель микроциркуляции (перф. ед.) |
Среднее квадратическое отклонение (перф. ед.) |
Коэффициент вариации (%) |
|
Лоб |
9,92 ±0,54 |
1,4±0,35 |
14 |
|
Правая щека |
12,39±0,21 |
1,8±0,49 |
14,5 |
|
Левая щека |
12,38±0,16 |
1,9±0,41 |
15,9 |
|
Подбородок |
6,93±0,54 |
0,8±0,46 |
11,5 |
Обсуждение. Для измерений кровотока различных топографо-анатомических областей кожи существенное значение имеет пространственная ориентация направления потоков крови по отношению к поверхности кожного покрова, где расположены принимающее и освещающее волокна. Проведенные исследования архитектоники микрососудов в коже разных топографических зон лица показали, что микрососуды, а соответственно и потоки форменных элементов крови ориентированы преимущественно перпендикулярно поверхности кожи. Эритроциты движутся с разными линейными скоростями: от 0,6 до 5 мм/с в артериолах, от 0,01 до 0,3 мм/с в капиллярах и от 0,32 до 1,2 мм/с в венулах [5].
Наибольшей проникающей способностью через кожу обладают волны длиной 650-1200 нм, так называемый диапазон «оптической прозрачности ткани». Глубже всего, до 70 мм, проникают инфракрасные лучи, лучи с длиной волны 0,8-1,0 мкм (805 нм) — 40 мм, 650 нм -15-25 мм, причем 40% их рассеивается и отражается.
Частота излучения, рассеянного движущейся частицей, отличается от частоты зондирующего сигнала (эффект Допплера). Для частицы, движущейся со скоростью v r = 1 мм/с, облученной лазерным излучением с длиной волны 650 нм, допплеровская частота равна 4.4 кГц. Эффект Допплера позволяет исследовать большие ансамбли эритроцитов, движущихся в микрососудах. Их скорости различны в артериолах, капиллярах и венулах, что позволяет методами частотной селекции производить анализ физиологических процессов, идущих в различных отделах системы микроциркуляции [9, 10].В частности, для анализа транспорта кислорода удобно использовать 4-канальный аппарат с лазерами, излучающими на длинах волн λ 1 = 0,65 мкм и λ 2 = 0,805 мкм. Первая длина волны характеризуется высоким поглощением света в гемоглобине и низким поглощением в окисленном гемоглобине. Вторая длина волны называется изобестической, так как поглощение оптического излучения в этих двух веществах одинаково. Эффективная поверхность рассеяния эритроцита в значительной степени определяется химическим составом внутриклеточного вещества. Оно представляет собой насыщенный, 32%-ный раствор гемоглобина в плазме крови. Большинство тканей организма для рассматриваемых длин волн имеют низкие омические потери (исключение составляет гемоглобин), что позволяло бы ожидать высокую прозрачность и большую глубину проникновения оптического излучения. В то же время большое количество микровключений веществ с различными показателями преломления приводит к интенсивному рассеянию и ограничивает глубину проникновения света. Размеры этих неоднородностей на порядок меньше длины волны видимого излучения. Это приводит к тому, что глубина проникновения излучения на длине волны λ 2 больше, чем на λ 1 . Зондирующее излучение с длиной волны λ = 0,65 мкм характеризуется значительным поглощением гемоглобина и метагемоглобина и относительной прозрачностью оксигемоглобина.Рас-стояние от освещающего волокна до первого приемного волокна в данном ЛДФ составило 1±0,2 мм, а до четвертого приемного волокна 4±0,8 мм, что позволило увеличить глубину проникновения излучения измеряемой области.
Заключение. В результате проведенных исследований были изучены особенности микроциркуляции в различных топографо-анатомических областях кожи лица и выявлены наиболее высокие показатели кожного кровообращения в области щек, ниже в области лба и самые низкие в области подбородка. Данные показатели находятся в прямой зависимости от структурных особенностей строения микроцирку- ляторного русла этих областей, глубины залегания и плотности функционирующих капилляров.
Глубина детектирования и пространственная локализация области, с которой осуществляется детектирование рассеянного излучения, зависят от оптических характеристик ткани, размеров и взаимного расположения источника и приемника, мощности зондирующего излучения. Объем зондируемой ткани, пространственная локализация ЛДФ-сигнала в тканях кожи и эффективной глубины детектирования определялись методом Монте Карло. Впервые сделаны оценки объема зондируемой ткани.
Метод ЛДФ как неинвазивный и высокочувствительный метод дает возможность подробнее понять, как влияют на циркуляцию крови те или иные методы лечения, а также подобрать подходящие методы терапии под контролем исследования показателей микроциркуляции, так как позволяет не только оценить перфузию ткани в целом, но и проанализировать транскапиллярный обмен в разных слоях кожи по глубине. Временной интервал проведения процедуры сравнительно незначительный, что может обеспечить его применение в ежедневной медицинской практике. Предложенный метод может быть использован для диагностики состояния биологического объекта в норме и при патологии, а также при оценке эффективности лечения различных дерматозов.
Список литературы Оценка состояния микроциркуляторного русла кожи лица методом лазерной допплеровской флоуметрии
- Тучин В. В. Оптическая биомедицинская диагностика. М.: Физматлит, 2007
- Меглинский И. В., Кoрoлевич А. Н., Тучин В. В. Исследование микроциркуляций кровотока методом диффузионно волновой спектроскопии//Биомедицинская радиоэлектроника. 2000. № 10. С. 37 -45
- Young A. R. Chromophores in human skin//Phys. Med. Biol. 1997. Vol. 42. P. 789 -802
- Крупаткин А. И., Сидорова В. В. Лазерная допплеров-ская флоуметрия микроциркуляции крови. М.: Медицина, 2005. 254 с.
- Козлов В. И., Кореи Л. В., Соколов В. Г. Лазерная допле-ровская флоуметрия и анализ коллективных процессов в системе микроциркуляции//Физиология человека. 1998. Т. 24. № 6. С. 112 -121
- Донец М. В., Кучерик А. О., Сорокин С. А. Математическая модель формирования сигнала лазерного анализатора капиллярного кровотока//Биомедицинские технологии и радиоэлектроника. 2004. № 3. С. 51
- Doronin A.,I. Meglinski I. Online Object Oriented Monte Carlo computational tool for the needs of biomedical optics//Biomedical Optics Express. 2011. Vol. 2. P. 2461 -2469
- Мчедлашвили Г. И. Микроциркуляция крови: общие закономерности регулирования и нарушений. Л.: Наука, 1989
- Светцов В. И., Смирнов С. А. Корпускулярно-фотонные процессы и технологии: учеб. пособие/Иван. гос. хим.-технол. ун-т. Иваново, 2002
- Ansari M. A., Massudi R. Study of short pulse laser in biological tissue by meansofboundary element method//Lasers. Med. Sci. 2011. № 26 (4). P. 503 -508.


