Оценка влияния изменений внутригрудного давления на церебральную гемодинамику (математическая модель)
Автор: Семенов Ю.С., Дьяченко А.И.
Журнал: Труды Московского физико-технического института @trudy-mipt
Рубрика: Молекулярная физика и физика живых систем
Статья в выпуске: 3 (23) т.6, 2014 года.
Бесплатный доступ
Данное исследование проводилось в рамках разработки метода коррекции гемодинамических сдвигов, происходящих в условиях микрогравитации. C первых минут пребывания в невесомости отсутствие гравитации приводит к перераспределению жидкости в организме космонавтов, в первую очередь крови, по направлению к голове, что приводит ко множеству негативных явлений. Суть разрабатываемого метода заключается в снижении внутригрудного давления путем создания дозированного разрежения в ротовой полости на вдохе. В данной работе представлена математическая модель кардиореспираторной системы человека, описывающая влияние изменений внутригрудного давления на церебральную гемодинамику. Впервые теоретически показано, что снижение внутригрудного давления должно приводить к снижению внутричерепного давления у человека. Полученные результаты согласуются с имеющимися экспериментальными данными и являются теоретическим обоснованием возможности применения ДОД в качестве профилактического средства при повышении внутричерепного давления.
Кардиореспираторная система, математическая модель, церебральная гемодинамика, внутригрудное давление, профилактика гемодинамических расстройств, дыхание под отрицательным инспираторным давлением
Короткий адрес: https://sciup.org/142186007
IDR: 142186007 | УДК: 612.213,
Текст научной статьи Оценка влияния изменений внутригрудного давления на церебральную гемодинамику (математическая модель)
Данное исследование проводилось в рамках разработки метода коррекции гемодинамических сдвигов, происходящих в условиях микрогравитации. С первых минут пребывания в невесомости отсутствие гравитации приводит к перераспределению жидкости в организме, в первую очередь крови. При длительном (более нескольких часов) отсутствии гравитации заметная часть крови перераспределяется в направлении головы, вызывая различные отечные явления. Снижается работоспособность космонавтов, ухудшается самочувствие, появляется ощущение заложенности носа. Адаптация к условиям невесомости вызывает послеполетную ортостатическую неустойчивость. Необходима, простая и удобная методика, позволяющая хотя бы временно устранить негативные эффекты, связанные с перераспределением крови в период острой адаптации. В последние годы появился новый подход к этой проблеме: дыхание под отрицательным (относительно атмосферного) давлением (ДОД) [1, 2, 3]. Отрицательное давление можно создавать как во время всего цикла, дыхания, так и на. отдельных его фазах.
Цель данного исследования - построить математическую модель кардиореспираторной системы человека, описывающую влияние изменений внутригрудного давления на церебральную гемодинамику.
При разработке модели мы использовали подход Ф. Гродинза к описанию работы сердца. [4], а. также модель церебральной гемодинамики [5]. Предлагаемая нами модель состоит из пяти компартментов: голова, левое сердце, правое сердце, малый круг кровообращения, большой круг кровообращения (исключая голову). Модель описывает изменение средних значений давлений и потоков в системе кровообращения за времена порядка 10 с, пульсовые колебания не рассматриваются. Модель включает регуляцию сердечной деятельно- сти по механизму Франка-Старлинга. При описании церебральной гемодинамики учитываются процессы капиллярной фильтрации и ауторегуляция тонуса артериол. Так как не учитываются регуляторные реакции со стороны нервной системы, такие как барорефлекс, модель применима для описания только малых изменений внутригрудного давления (не более 15 см вод. ст.). Также модель не учитывает гуморальную регуляцию (например, рефлекс Генри-Гауэра), поэтому модель можно использовать лишь для описания процессов, длительность которых не превосходит одного часа.
2. Модель сосудов
Для описания сосудов мы использовали модель Франка [6]. Рассмотрим участок сосудистого русла, состоящий из упругих резервуаров а, b и находящегося между резервуарами резистивного элемента Ra b (рис. 1).
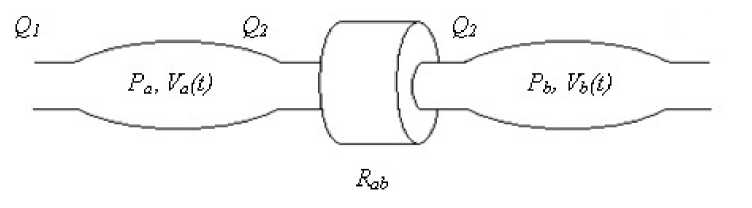
Рис. 1. Схема, модели упругого резервуара.
Для описания этого участка, используются три уравнения:
Q1 — Q2 = , Pa = (Va - Va0) , Q2Rab = Pa - Pb, at Ca где Pa, Va — давление и объем крови в первом резервуаре, Pb, Vb — давление и объем крови во втором резервуаре, Q — величина кровотока, Ca — величина растяжимости резервуара, Vao — объем первого резервуара, при котором давления внутри и снаружи резервуара одинаковы.
Три уравнения могут быть объединены в одно:
C-^P (t) + ^P (t) = Q (t).
at r
Для всех сосудов мы предполагали Vao равным нулю.
3. Модель сердца
Согласно модели Гродинза [4] наполнение расслабленного желудочка во время диастолы аналогично наполнению эластичного сосуда. Мы модифицировали модель, введя внутриг-рудное давление Pi.
Уравнение, описывающее диастолу, в этом случае записывается так:
RVd + Cc^Vd = PV - Pi, где R — полное вязкостное сопротивление желудочка, C — растяжимость расслабленного желудочка. Pv — давление в полой вене. Pi — впутрпгрулпос давление. Vd — текущий объем желудочка.
Решая данное уравнение и проводя арифметические преобразования аналогично процедуре, описанной в работе Гродинза. [4], в предположении, что систола, имеет постоянную продолжительность, равную 0,2 с, а. продолжительность диастолы равна.
/
- 0,2,
где J — частота сердечных сокращений в уд\мин, получаем
V ja = ( V r - С ( Р у - Рі)) е-^ + С ( Р у - Рі) = С ( Р у - Рі ) (1 - к ) + V r к, (1)
где введено обозначение к = e-td/RC, V ja — конечнодиастолический объем, V- — конечносистолический объем.
Рассмотрим систолу. Согласно эмпирическому «закону сердца» Франка-Старлинга [7], предположим, что полезная работа желудочка (И) прямо пропорциональна конечнодиастолическому объему: И = ко Vja- С другой стороны, И = (Рд - Р1) Vs, где Рд — артериальное давление, Vs — ударный объем. Таким образом, получим v _ к0^а
s ( Р д -Р1 ) ‘
Ударный объем равен разности конечно-диастолического и конечно-систолического объемов:
Vs = Vja - /. (3)
Решив систему уравнений (1), (2) и (3) относительно Vs, получим
= коС ( Р у -Р1 )(1 - к )
s ( Р д -Р1 )(1 - к ) + кко .
Тогда минутный объем кровотока (Q) равен
УкоС ( Р у -Р1 )(1 -к)
4 У s ( Р д -Р1)(1 - к ) + кко .
Данным уравнением описывается работа как левых, так и правых камер сердца, разница только в численном значении коэффициентов. Ниже индекс L используется для параметров левых камер сердца, R — для правых.
Численные значения параметров модели взяты в основном из [7]. Величины Rl, Rr, Gl, Or, ко ь и ko R можно оценить из экспериментальных данных, описанных в литературе по кардиологии, следующим способом.
Для краткости опустим индексы L и R. Из определения растяжимости ( С ) следует
Vfd
С = —^—, где Р у а - максимальное давление в желудочке в конце диастолы.
Руа
Вязкостное сопротивление (R) есть отношение разности давлений (АР), создающей по ток жидкости (q), к величине этого потока. Для грубой оценки предположим, что во время диастолы АР постоянна и равна максимальному давлению в предсердии во время систолы предсердий, q равен средней объемной скорости кровотока.
Величину ко легко определить, зная конечно-систолический и конечно-диастолический объемы и среднее артериальное давление, Рі для оценки можно принять равным атмосферному давлению.
4. Модель мозгового кровообращения
Для описания мозгового кровообращения использовалась модель, описанная в работе [5], с небольшими модификациями.
На рис. 2 приведено схематическое изображение модели мозгового кровообращения. Здесь Ра и, Рс и, Р ^и ~ давления в церебральных артериях, капиллярах и крупных венах соответствешю. Ra h- R pv ~ сопротивление церебральных артерий и мелких вен. Ру — давление на границе между мелкими и крупными венами (на уровне, где трансмуральное давление приближается к нулю). От сопротивления последних R a v кровоток не зависит. Сопротивления R y, R q отражают процессы фильтрации, qa h, q ^h ~ мгновенные артериальный и венозный кровотоки, qj, qo — фильтрационные потоки. Переменные емкости С аи,
С гс отражают нелинейные упругие свойства церебральных артерий и цереброспинального компартмента.
Согласно [8] соотношение объем-давление для краниоспинального компартмента может быть представлено в следующем виде:
Р іс — Р2 = Р гсп екЕ ' ^ , (4)
где Р іс, V h — текущие внутричерепное давление и суммарный объем жидкости краниоспинального компартмента, Р і сп, V h n — числовые постоянные: внутричерепное давление и суммарный объем жидкости краниоспинального компартмента для здорового человека. Эластичность компартмента характеризуется постоянной кв, Р2 ~ внешнее давление (так как череп предполагается абсолютно твердым телом, давление Р2 — давление, оказываемое внешней средой на туловище, т.е. спинномозговую часть краниоспинального компартмента).
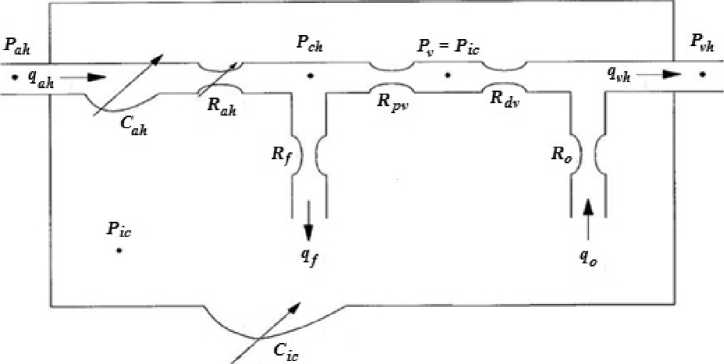
Рис. 2. Схематическое изображение модели краниоспинального компартмента. (по [5] с изменениями)
Уравнение (4) удобно преобразовать к виду
Vh = Дт + -^ln ( Р іс~ Р ) . к Е \ Рісп /
Артериальный бассейн рассматривается как совокупность большого числа, одинаковых сосудов, соединенных параллельно. В этом случае совокупность сосудов будет описываться теми же уравнениями, что и один сосуд. Различными будут только величины коэффициентов.
При рассмотрении мозгового кровообращения крайне важно учесть регуляторные реакции. В качестве первого приближения учитывается реакция артериального бассейна, только на. изменения кровотока. Уравнение ауторегуляции артериол [5]:
С.,, = Т (-С«» + ° (5ддһ)), где Саһ — растяжимость артерий, т — характерное время реакции. Qah — кровоток в артериях мозга, ° (ж) — сигмоидная функция (подробно описана в приложении к работе [5]), qn — постоянный коэффициент, равен величине церебрального кровотока для здорового человека.
При изменении упругих свойств сосуда, при постоянном трансмуральном давлении изменяются и его объем (Vah) и гидродинамическое сопротивление (Нан) Сопротивление сосуда, описываемое законом Хагена-Пуазейля, обратно пропорционально четвертой степени радиуса, т.е. при постоянной длине обратно пропорционально квадрату объема:
Rah =
kRR
(W ’
гДе Vah = Cah (Pah - Pic) ~ объем артериального бассейна, крр — постоянный множитель (его величину легко оценить, зная церебральный кровоток, давления в магистральных артериях, капиллярах, а также внутричерепное давление и объем артериального бассейна, все эти параметры неоднократно измерялись и описаны в литературе).
Вены в данной модели описываются резистором Старлинга (спадающийся сосуд): кровоток через данный сосуд пропорционален разности входного и внешнего давлений и не зависит от выходного давления. Причем емкостью вен пренебрегаем, так как регуляторные эффекты вен мозга пренебрежимо малы, а давление в частично спавшемся сосуде с пассивной стенкой равно внешнему внутричерепному давлению. В силу чего, с точки зрения механики, учет емкости вен не дает никакого вклада в динамику внутричерепного давления.
Процессы секреции\резорбции ликвора описываются с помощью резистивных элементов и идеального вентиля.
Методика оценки численных значений параметров описана в [5] и здесь не приводится.
5. Модель системы кровообращения Рис. 3. Электрический аналог системы кровообращения
Электрический аналог модели системы кровообращения приведен на рис. 3. Сопротивления Rab, Ryb и емкости Саь, С^ь соответственно отражают механические свойства артерий и вен большого круга кровообращения. Аналогично, Rai, R^i, Cai, C^i служат для описания малого круга.
Отдельно стоит упомянуть, что для повышения точности расчета и устойчивости алгоритма одно из уравнений модели было заменено на условие постоянства объема жидкости в системе. Отдельно контролировалось условие применимости приближения резистора Старлинга: системное венозное давление не должно быть больше внутричерепного.
6. Результаты моделирования
Ниже приведены (рис. 4, 5, б, 7) рассчитанные зависимости. Стоит отметить, что при снижении и небольшом повышении внутригрудного давления (P1) поведение модели совпадает с характерным для кардиореспираторной системы человека. В частности, модель воспроизводит «присасывающее» действие грудной клетки, т.е. рост системного кровотока (Q) при снижении внутригрудного давления. Причем системное артериальное давление ( Pas ) ПРИ этом несколько увеличивается, а системное венозное давление ( Pus ) снижается. Данные изменения сопровождаются увеличением объема крови в системных артериях ( Vib) и его снижением в системных венах ( Vu bY
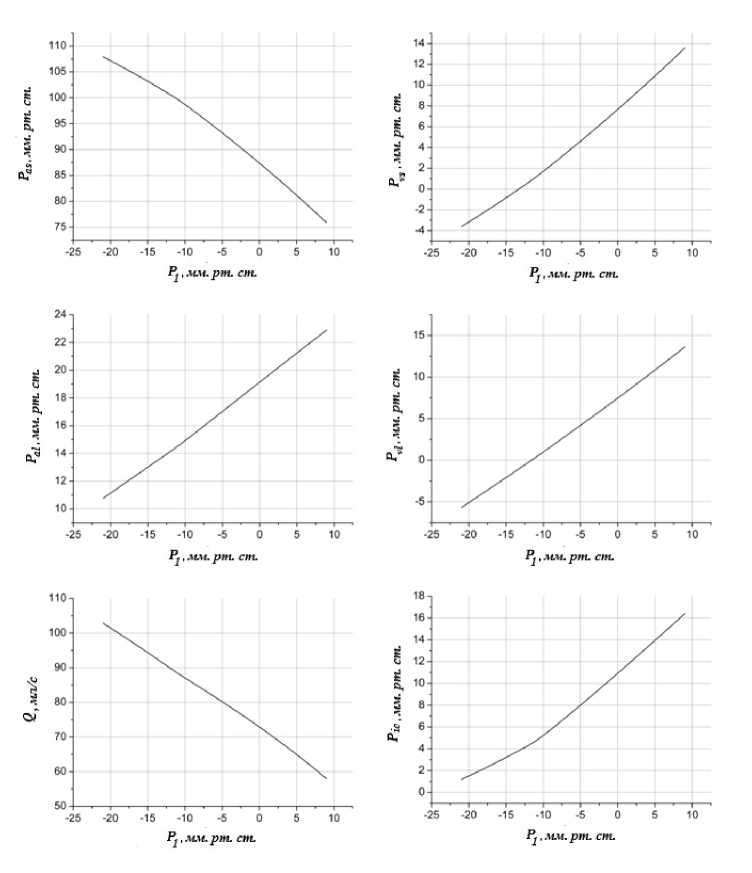
Рис. 4. Результаты моделирования действия изменений внутригрудного давления на. систему кровообращения (положение равновесия системы), пояснения в тексте
Артериальное ( Ра / ) и венозное ( Pu / ) давления в малом круге кровообращения уменьшаются при уменьшении внутригрудного давления, но, несмотря на данное уменьшение давлений, происходит увеличение объема крови в артериях (Vi/) и венах ( Vu / ) малого круга.
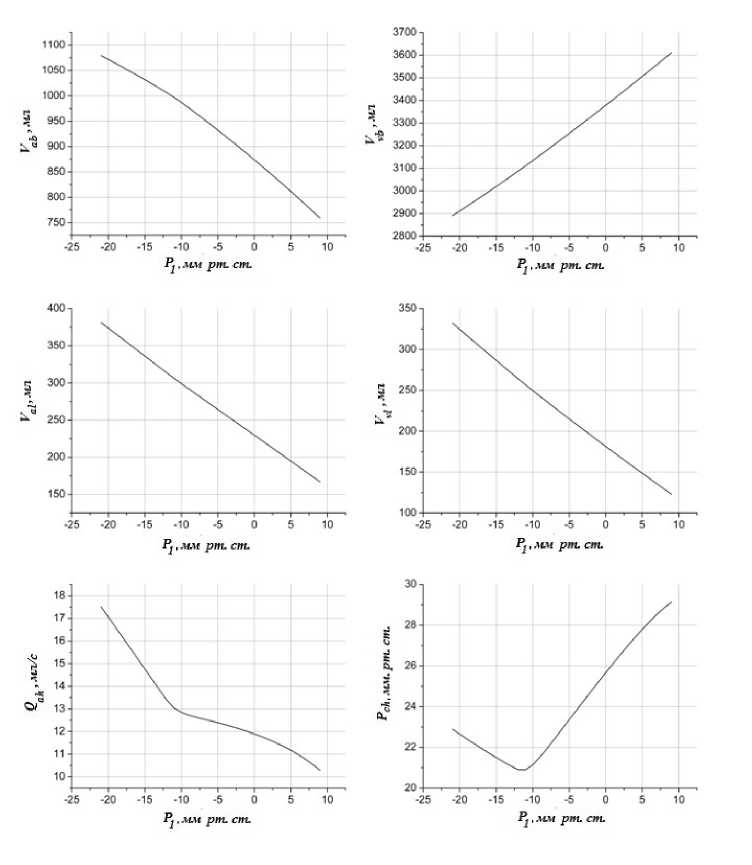
Рис. 5. Результаты моделирования действия изменений виутригрудиого давления на. систему кровообращения (положение равновесия системы, продолжение), пояснения в тексте
Предсказания модели соответствуют имеющимся экспериментальным данным [1, 2, 3, 9, 10, 11, 12, 13]. Но стоит обратить внимание на довольно заметное увеличение артериального системного давления (и соответствующее увеличение кровотока). Данные экспериментов свидетельствуют о повышении давления и кровотока, но величина эффекта заметно меньше расчетной. Данное несоответствие, вероятно, связано с отсутствием в модели барорефлекса. Без учета барорефлекса также невозможно моделирование ортопробы. Вопрос введения в модель барорефлекса заслуживает более детального рассмотрения.
Таким образом, представленная модель верно отражает процессы, происходящие в кар-диореспираторной системе, но, возможно, несколько завышает величины эффектов.
Наиболее интересно оценить с помощью модели изменения церебральной гемодинамики при ДОД. Как можно видеть из рис. 4 и 5, ДОД приводит к уменьшению внутричерепного давления ( Pic ) и небольшому увеличению церебрального кровотока ( Qah), причем при снижении внутригрудного давления ниже -11 мм рт. ст. ауторегуляции артериол становится недостаточно для поддержания неизменного кровотока. Давление в капиллярах краниоспинального компартмента (Рд) при снижении внутригрудного давления изменяется немонотонно.
Следующим шагом было моделирование процесса свободного дыхания и дыхания с дополнительным отрицательным давлением на вдохе (ДОДвд).
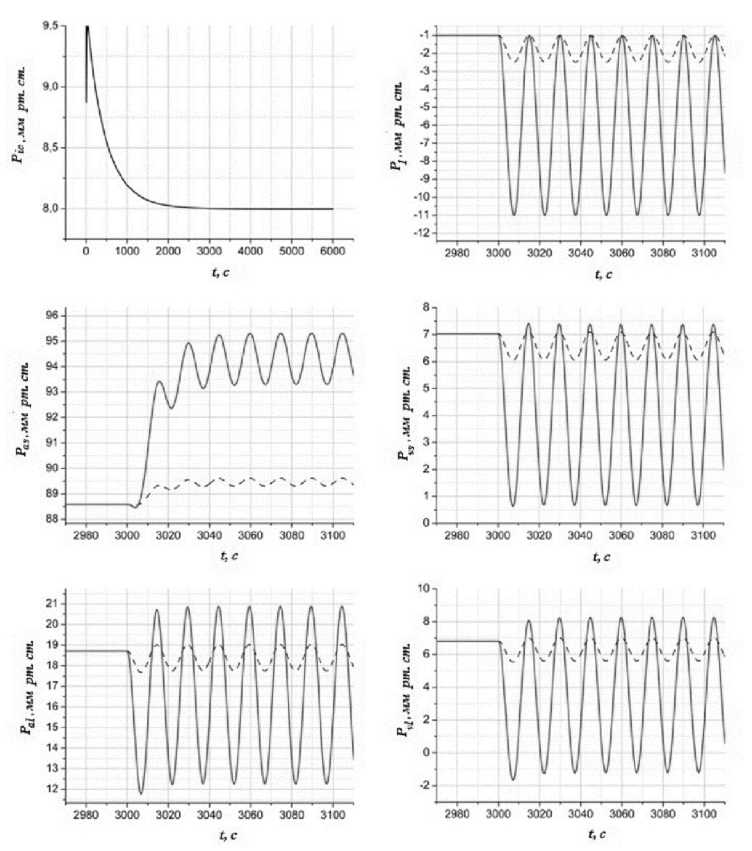
Рис. 6. Результаты моделирования действия УДОД на систему кровообращения, пояснения в тексте
Как отмечалось в работе [10], дыхание через устройство, создающее дополнительное отрицательное давление на вдохе (УДОД), приводит к снижению частоты дыхания вплоть до четырех раз в минуту. Поэтому для удобства сравнения при моделировании свободного дыхания была выбрана именно эта частота.
В работе [1] определили, что изменения внутригрудного давления примерно в два раза меньше изменений давления в подмасочном пространстве. Поэтому для моделирования ДОДвд была выбрана величина снижения внутригрудного давления -10 мм рт. ст., что примерно соответствует максимальному разрежению, использовавшемуся в работах [1, 2, 3, 10].
Свободное дыхание моделировалось колебаниями внутригрудного давления (Pi) от —2,5 мм рт. ст. до — 1 мм рт. ст.. ДОДвд — от -11 мм рт. ст. до — 1 мм рт. ст. (рис. 6). В течение первых 3000 с система релаксировала от произвольного начального состояния к равновесию, затем «включалось» дыхание. На рис. 6 и 7 кривые, полученные при свободном дыхании, изображены пунктирной линией, при ДОДвд - сплошной. Если какая-либо переменная изменялась в течение длительного времени, приводился установившийся режим.
Наиболее медленно изменяющейся переменной оказалось внутричерепное давление (Pic), именно поэтому период до начала «дыхания» составлял 3000 с (пример релаксации данного параметра приведен на первом графике рис. 6, для данного графика внутригруд- ное давление постоянно и равно
—5 мм рт. ст.).
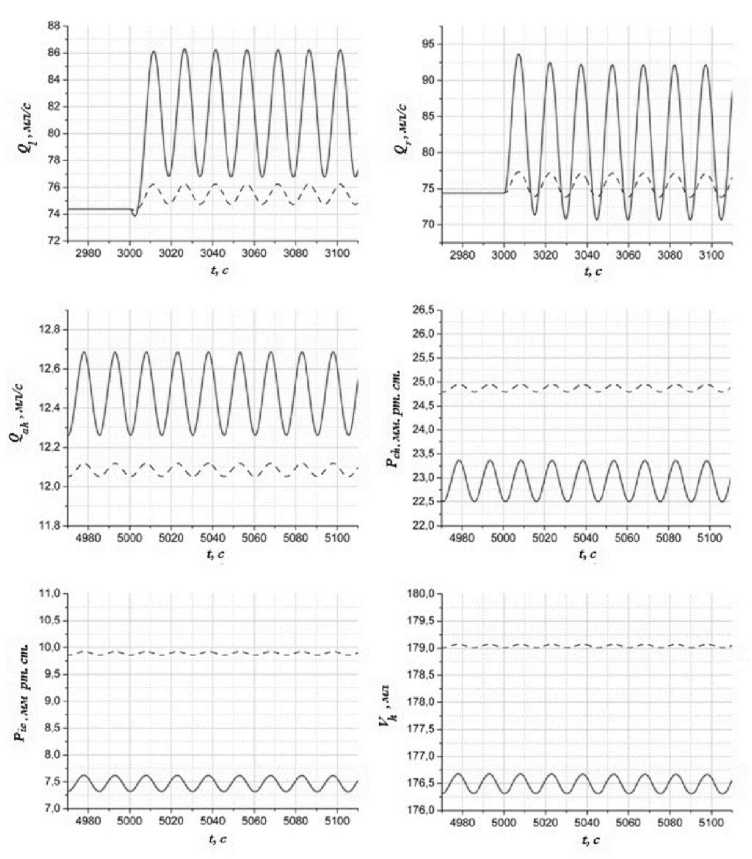
Рис. 7. Результаты моделирования действия УДОД на систему кровообращения (продолжение), пояснения в тексте
Оказалось, что поведение данной нелинейной модели похоже на поведение линейных систем: частота изменений внутригрудного давления совпала с частотой изменения переменных, существенного вклада кратных частот не наблюдалось.
Все переменные «чувствовали» влияние дыхания: проявились колебания с частотой, равной частоте «дыхания». Причем с увеличением амплитуды изменений внутригрудного давления (Pi) увеличивалась и амплитуда колебаний переменных. Любопытно, что при этом мгновенный кровоток левого сердца (Q/) не равен кровотоку правого сердца ( QT ), отличаются также и амплитуды колебаний данных переменных в установившемся режиме. Однако при этом средние за период кровотоки равны.
Также в ответ на изменение режима дыхания смещались средние значения переменных в соответствии с графиками рис. 4 и 5.
В данной модели системы кровообращения объем вен мозга предполагается неизменным, уменьшение кровенаполнения возможно лишь за счет изменения объема артерий (VahY При снижении внутригрудного давления (Pi) объем артерий мозга изменяется немонотонно, есть локальный минимум вблизи величины внутригрудного давления —10 мм рт. ст. (рис. 8), причем объем артерий при —15 мм рт. ст. примерно равен объему при —5 мм рт. ст., что с учетом разницы в подмасочном и внутригрудном давлениях и индивидуальных различий в параметрах сосудов согласуется с результатами измерения концентрации гемоглобина в тканях головы, проведенных с помощью методов инфракрасной спектроскопии [3]. При наибольшем и наименьшем разрежениях в подмасочном пространстве концентрации почти не отличаются от фоновых, а при среднем разрежении наблюдается максимальный эффект.
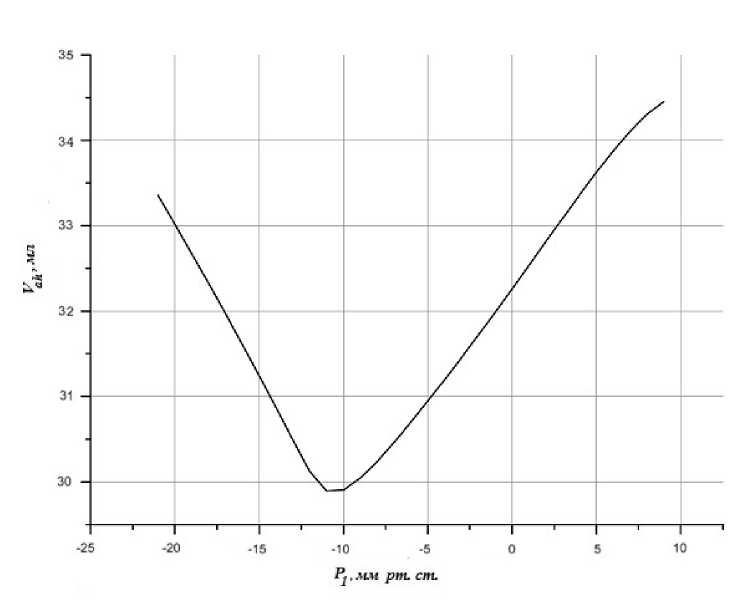
Рис. 8. Предсказанная моделью зависимость объема, артериальной крови в тканях мозга, от внутригрудного давления
7. Обсуждение
Качество модели невозможно оценить без сравнения с экспериментальными данными. К сожалению, большинство переменных модели невозможно измерить неинвазивно в абсолютных единицах или же, как в случае с дыхательными колебаниями артериального давления, точность неинвазивных измерений недостаточна, в силу несовершенства, измерительных методов. Инвазивных же измерений в исследованиях ДОДвд с участием добровольцев не проводилось. Несколько лучше ситуация обстоит с данными, полученными на. животных. Подавляющее большинство данных было получено при использовании постоянного ДОД (и на. вдохе, и на. выдохе).
Несмотря на. примитивность модели, она. отражает поведение кардиореспираторной системы, наблюдавшееся экспериментально. Так, в работах [11, 12] отмечается снижение давления в венах при ДОД. Кроме того, авторы работы [12] также наблюдали увеличение минутного кровотока. Некоторое увеличение артериального давления наблюдали авторы работы [9] при ДОДвд, давление измеряли с помощью методики Пеньяза, позволяющей получать данные об артериальном давлении с временным разрешением около 1 с. Также об увеличении артериального давления и минутного кровотока, в ряде случаев говорят авторы работы [13], применявшие ДОД на. протяжении всего дыхательного цикла. Помимо изменений артериальных и венозных давлений и кровотока, в работе [9] отмечалось снижение внутричерепного давления и увеличение церебрального кровотока, сразу же после начала. ДОДвд. Авторы затруднились предложить механизм, позволяющий объяснить данный эффект. В рамках предложенной нами модели столь быстрые изменения внутричерепного давления также не удается описать, наиболее вероятной причиной является изменение объема крови, депонированной в церебральных венах, вследствие оттока в грудную клетку при снижении внтригрудного давления. Изменение же церебрального кровотока, помимо механических причин, может быть вызвано даже небольшим увеличением количества углекислого газа, растворенного в плазме крови вследствие увеличения мертвого пространства, связанного с наличием дыхательной маски.
Следует отметить противоречивость некоторых экспериментальных данных, касающихся ДОД. В частности, различные косвенные данные указывают как на снижение, так и на увеличение церебрального кровотока под действием ДОД в антиортостатическом положении [1].
Одним из наиболее слабых мест предлагаемой модели является отсутствие различных механизмов регуляции. Наша модель включает только два механизма регуляции: закон саморегуляции сердца Франка-Старлинга и регуляцию растяжимости церебральных артерий в соответствии с величиной кровотока в артериях мозга. Для более адекватного описания гемодинамических реакций на ДОД необходимо учесть и другие механизмы регуляции кровообращения, предположительно играющие большую роль при ДОД, в первую очередь механизмы симпатической и парасимпатической регуляции, барорефлекса и хеморефлекса, количественно описанные в работе [14] и ряде других работ.
8. Заключение
Впервые теоретически показано, что ДОД должен снижать интракраниальное давление у человека. Ранее снижение интракраниального давления было продемонстрировано только в отдельных экспериментах, проведенных на животных. Также мы оценили предполагаемое увеличение мозгового кровотока. В ранее проведенных экспериментах наблюдалось увеличение индексов, характеризующих мозговой кровоток, однако абсолютное значение роста кровотока оставалось неизвестным.
Таким образом, полученные результаты являются теоретическим обоснованием возможности применения ДОД в качестве профилактического средства при повышении внутричерепного давления.
Список литературы Оценка влияния изменений внутригрудного давления на церебральную гемодинамику (математическая модель)
- Тихонов М.А., Котов А.Н., Реушкин В.Н., Реушкина Г.Д., Ушаков Б.Б., Фомина Г.А., Донина Ж.А., Лаврова И.Н., Баранов В.М. Респираторные и сердечно-сосудистые механизмы гипобарической коррекции антиортостатического перераспределения региональных объемов крови//Авиакосм. и эколог. мед. -2003. -Т. 37, вып. 2. -С. 51-59
- Семенов Ю.С., Попова Ю.А., Дьяченко А.И., Реушкина Г.Д., Колесников В.И., Суворов А.В. Особенности влияния дыхания под отрицательным давлением на вдохе на кардиореспираторную систему человека в условиях 5-суточной иммерсии//Авиакосм. и эколог. мед. -2011. -Т. 45, вып. 6. -С. 37-40
- Сафонова Л.П., Дьяченко А.И., Семенов Ю.С. Изменения в церебральной гемодинамике под влиянием отрицательного инспираторного давления//Биомедицинская радиоэлектроника. -2011. -№ 10. -С. 65-72
- Гродинз Ф. Теория регулирования и биологические системы. -М.: Мир, 1966
- Ursino M., Lodi C.A. A simple mathematical model of the interaction between intracranial pressure and cerebral hemodynamics//J. Appl. Physiol. -1997. -V. 82, N 4. -P. 1256-1269
- Шумаков В.И., Новосельцев В.Н., Сахаров М.П., Штенгольд Е.Ш. Моделирование физиологических систем организма. -М.: Медицина, 1971
- Шмидт Р., Тевс Г. Физиология человека. Т. 2. -М.: Мир, 2005
- Marmarou A., Shulman K., Rosende R.M. A nonlinear analysis of the cerebrospinal fluid system and intracranial pressure dynamics//J. Neurosurg. -1978. -V. 48, N 3. -P. 332-344
- Convertino V.A., Cooke W.H., Lurie K.G. Restoration of central blood volume: application of a simple concept and simple device to counteract cardiovascular instability in syncope and hemorrhage//J. Gravit. Physiol. -2005. -V. 12, N 1. -P. 55-60
- Гусева Е.А., Дьяченко А.И., Суворов А.В., Черногоров Р.В., Шулагин Ю.А. Влияние дыхания с дополнительным сопротивлением на вдохе на кардиореспираторную систему в условиях водной иммерсии//Альманах клинической медицины. -2008. -Т. 17, вып. 2. -С. 51-53
- Holt J.P. The effect of positive and negative intrathoracic pressure on peripheral venous pressure in man//Am. J. Physiol. -1943. -V. 139, N 2. -P. 208-211
- Gauer O.H., Henry J.P., Sieker H.O., Wendt W.E. The effect of negative pressure breathing on urine flow//J. Clin. Invest. -1954. -V. 33, N 2. -P. 287-296
- Kaye H., Kilburn H., Sieker H.O. Hemodynamic effects of continuous positive and negative pressure breathing in normal man//Circulation Research. -1960. -V. 8, N 3. -P. 660-669
- Cheng L., Ivanova O., Fan H.-H., Khoo M.C.K. An integrative model of respiratory and cardiovascular control in sleep-disordered breathing//Resp. Physiol. and Neurobiology. -2010. -V. 174. -P. 4-28


