Оценка влияния коагуляции на степень очистки воды от ионов металлов
Автор: Шестаков И.Я., Раева О.В.
Журнал: Сибирский аэрокосмический журнал @vestnik-sibsau
Рубрика: Технологические процессы и материалы
Статья в выпуске: 1 (47), 2013 года.
Бесплатный доступ
Представлены результаты экспериментальных исследований очистки воды, заключающейся в пропускании через нее переменного асимметричного тока с использованием нерастворимых разнородных электродов, введении коагулянта и отстаивании.
Вода, электрохимический способ, переменный ток, коагулянт, отстаивание
Короткий адрес: https://sciup.org/148177007
IDR: 148177007 | УДК: 628.16.087
Assessment of coagulation influence on index of purification of water from metal ions
The article presents the results of experimental studies of water purification, consisting of passing through it asymmetric alternating current with application of insoluble heterogeneous electrodes, introducing coagulating agent and settling.
Текст научной статьи Оценка влияния коагуляции на степень очистки воды от ионов металлов
Загрязнение воды является одной из острейших экологических проблем в мире. Более 90 % сточных вод сбрасываются в открытые водоемы без предварительной очистки. Загрязнены реки, озера, подземные источники. В большой мере причиной тому являются сточные воды гальванических производств, содержащие целый ряд ионов металлов, пагубно воздействующих на здоровье людей и окружающую среду.
Технологические процессы и материалы
Попытки создания установок для нейтрализации сточных вод гальванических производств не дают положительных результатов, потому что на нейтрализацию направляют смешанные стоки, содержащие целый «букет» особо опасных тяжелых металлов. Из-за повышенного загрязнения природных водоисточников традиционно применяемые технологии обработки воды стали недостаточно эффективными [1–3].
К одному из наиболее перспективных направлений очистки воды следует отнести электрохимические методы, и в частности, электрохимические методы очистки воды на переменном токе промышленной частоты.
Однако большое потребление электроэнергии и использование растворимых электродов ограничивают применение электрохимических процессов на практике.
В Сибирском государственном аэрокосмическом университете разработан способ очистки воды от анионов и катионов электрохимическим методом с применением нерастворимых электродов и переменного асимметричного тока [4–9].
Для реализации предлагаемого способа процесс очистки проводят в электролизере из чередующихся электродов, выполненных в виде пластин. Материал электродов: нержавеющая сталь 12Х18Н10Т, титановый сплав ОТ 4-0. Расстояние между электродами 12 мм. Объем заливаемой воды 1 л. Электроды подключались параллельно к источнику переменного тока частотой 50 Гц; боковые стенки при использовании электролизера являлись рабочими. Температура очищаемой воды 20–25 оС. Переменный электрический ток пропускался через воду в течение 10 мин при силе тока 0,5 А и напряжении на клеммах электродов 4,1 В.
Обработке подвергалась вода, содержащая ионы кадмия (II), меди (II), никеля (II) и хрома (VI). Начальная концентрация каждого иона в воде 0,5 мг/л.
После пропускания переменного электрического тока в воду вводился коагулянт – сульфат закиси железа FeSO4·7H2O (железный купорос), далее вода отстаивалась. Экспериментальные данные подтверждают, что сульфат закиси железа по сравнению с другими коагулянтами (например, железо (III) хлористое FeCl 3 ·6H 2 O, железо (III) сернокислое Fe 2 (SO 4 ) 3 ·9H 2 O) обладает хорошей растворимостью в воде, поэтому нашло широкое практическое применение в очистке воды.
При добавлении железного купороса в воду происходит его гидролиз, с образованием хорошо растворимого в воде гидроксида железа (II):
Fe 2+ + 2H 2 O ^ Fe(OH)2 + 2H+
Образующийся гидроксид железа (II) под действием кислорода, растворенного в воде, окисляется до гидроксида железа (III), выпадающего в осадок в виде хлопьев:
4Fe(OH) 2 + O 2 + 2H 2 O = 4Fe(OH) 3
Именно образующийся гидроксид железа (III) и является истинным коагулянтом (комплексообразова-телем).
Соотношение начальных концентраций иона ком-плексообразователя и удаляемого иона (С 2+ / Со ) оFe оi изменялось от 1:1 до 2,5:1. Время отстаивания воды (тотс) изменялось от 1 до 10 суток.
Количественный анализ ионов, содержащихся в воде после очистки, проводился на масс-спектрометре Agilent 7500 ICP-MS.
Принципиальная схема экспериментальной установки представлена на рис. 1.
Степень очистки определялась по формуле, % (г„-С ^ Y = 1 -0----к 1 100,
V С0 )
где С0 , Ск – начальная и конечная концентрации удаляемого иона металла, мг/л.
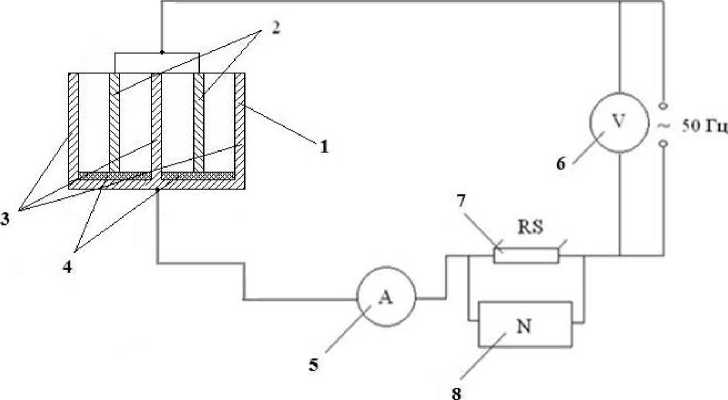
Рис. 1. Принципиальная схема экспериментальной установки:
1 – корпус; 2 – титановые электроды ОТ4-0; 3 – стальные электроды 12Х18Н10Т;
4 – пластины диэлектрические (оргстекло); 5 – амперметр; 6 – вольтметр;
7 – шунт измерительный; 8 – осциллограф С1-83
Удельные энергозатраты W определялись по формуле, (кВт·ч)/м3:
W = —10-3, V где I – сила тока, А; U – напряжение на клеммах электродов, В; т - время пропускания электрического тока, ч; V – объем заливаемой воды, м3; 10--3 – переводной коэффициент из Вт в кВт.
Исследование влияния соотношения начальных концентраций иона комплексообразователя и удаляемого иона на степень очистки воды проводилось при постоянном времени отстаивания (10 сут).
Результаты экспериментальных исследований представлены на рис. 2.
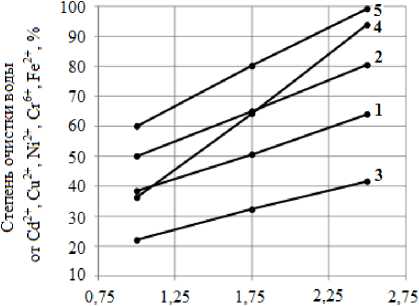
Соотношение начальных концентраций иона комплексообразователя и удаляемого иона
Рис. 2. Зависимость степени очистки воды от соотношения начальных концентраций иона комплексообразователя и удаляемого иона: 1 – кадмия; 2 – меди; 3 – никеля; 4 – хрома; 5 – железа
Исследование влияния времени отстаивания воды на степень очистки проводилось при постоянном соотношении начальных концентраций иона комплексооб-разователя и удаляемого иона (2,5:1). Результаты экспериментальных исследований представлены на рис. 3.
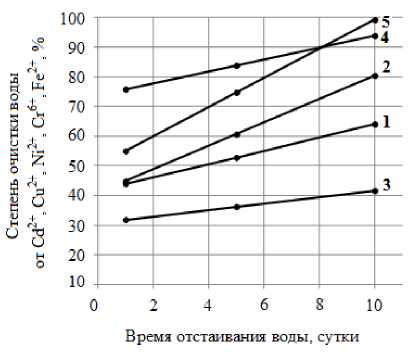
Рис. 3. Зависимость степени очистки воды от времени отстаивания воды. Удаляемые ионы: 1 – кадмий; 2 – медь; 3 – никель; 4 – хром; 5 – железо
Из графиков видно, что увеличение соотношения начальных концентраций иона комплексообразовате-ля и удаляемого иона и времени отстаивания приводит к значительному увеличению степени очистки воды от рассматриваемых ионов при малых удельных энергозатратах (0,34 кВт·ч/м3).
При увеличении соотношения начальных концентраций от 1:1 до 2,5:1 степень очистки увеличивается для кадмия в 1,7 раза, меди – 1,6, никеля – 1,9, хрома – 2,6 и железа – 1,7.
При увеличении времени отстаивания воды от 1 до 10 суток степень очистки увеличивается для кадмиям в 1,5 раза, меди – 1,8, никеля – 1,3, хрома – 1,2 и железа – 1,8.
Экспериментальные исследования показали, что наибольшая степень очистки воды от всех рассматриваемых ионов металлов достигается при пропускании через очищаемую воду переменного асимметричного тока с использованием нерастворимых электродов (нержавеющая сталь 12Х18Н10Т, титановый сплав ОТ 4-0), введением коагулянта – сульфата закиси железа FeSO 4 ·7H 2 O в соотношении начальных концентраций иона комплексо-образователя и удаляемого иона 2,5:1 и отстаиванием воды в течение 10 суток. При этом степень очистки воды равна: от кадмия 64 %, меди – 80,4 %, никеля – 41,6 %, хрома – 93,8 % и железа – 99,2 %. Удельные энергозатраты составляют W = 0,34 (кВт·ч)/м3.


