Очистка товарного электролита от примесей цветных металлов после десорбции золота с активированного угля
Автор: Лескив М.В., Белоусова Н.В., Дроздов С.В.
Журнал: Журнал Сибирского федерального университета. Серия: Техника и технологии @technologies-sfu
Статья в выпуске: 7 т.5, 2012 года.
Бесплатный доступ
В результате процесса десорбции золота с различных сорбентов получаются насыщенные растворы, в которые совместно с золотом элюируются цветные металлы. В процессе электролитического выделения золота последние переходят в катодный осадок, загрязняя его. В данной работе очистка электролита от примесей цветных металлов осуществляется добавлением перекиси водорода в раствор, в результате чего цветные металлы переходят в осадок в виде малорастворимых соединений, а золото остается в растворе, который отправляется на электролитическое получение металла. Установлено, что извлечение металлов примесей из раствора электролита повышается с увеличением температуры и расхода реагента-окислителя.
Очистка электролита, медь, никель, цинк, перекись водорода
Короткий адрес: https://sciup.org/146114701
IDR: 146114701 | УДК: 669.21
Finished electrolyte purification from impurities of non-ferrous metals after desorption of gold from activated carbon
After desorption of gold from different sorbents, saturated solutions in which non-ferrous metals eluate simultaneously with gold are obtained. During the electrolytic reduction of gold these metals pass into a cathode deposit and contaminate it. In the present work the electrolyte purification from impurities of non-ferrous metals is performed by the addition of hydrogen peroxide in the solution. As a result, non-ferrous metals precipitate in the form of slightly soluble compounds while gold remains in the solution which is transmitted for the electrolytic production of the metal. It was established that the extraction of the impurities of non-ferrous metals from the electrolyte solution increases as the temperature and the oxidizing agent consumption increase.
Текст научной статьи Очистка товарного электролита от примесей цветных металлов после десорбции золота с активированного угля
В настоящее время одной из наиболее важных задач цветной металлургии является оптимизация извлечения благородных металлов из упорных руд и концентратов. С изменением качества перерабатываемого золоторудного сырья, а также возросшими в последние годы требованиями к комплексности его использования необходимость решения данной задачи становится еще более актуальной.
Сейчас в процессах сорбционного выщелачивания золота в качестве сорбента широкое распространение получил активированный уголь. Одна из фабрик Олимпиадинского ГОКа работает по CIP-технологии [1] (уголь в пульпе), при этом в фазу сорбента переходит не только золото, но и ряд металлов-примесей, таких как никель, медь, цинк. В процессе десорбции цветные металлы десорбируются в раствор элюата вместе с золотом и, как следствие, при электролитическом выделении металла соосаждаются в катодный осадок, снижая его качество.
Попытки снизить содержание цветных металлов в электролите предварительной отмывкой насыщенного угля соляной кислотой приводили к удалению, в лучшем случае, до 50 % суммы примесей [2].
При проведении десорбции с активированного угля комплексы золота и металлов-примесей элюируются раствором щелочи [2]. Введение в раствор электролита перекиси водорода позволяет разрушить цианистые комплексы цветных металлов с образованием цианатов и нерастворимых соединений – гидроксидов [3]. Цианаты в конечном счете образуют аммоний и карбонат [4]:
[Cu(CNM2- + 4H2O2 + 2OH- = 4CNO- + Cu(OHM + 4H2O,(1)
[Ni(CNM2- + 4H2O2 + 2OH- = 4CNO- + Ni(OHM + 4H2O,(2)
Zn(CN)4]2- + 4H2O2 + 2OH- = 4CNO- + Zn(( )1 D_ + 4H2O,(3)
CNO- + 2H2O = NH4+ + CO32-.(4)
Цианистый комплекс золота (К у = 5-1039) не разрушается под воздействием перекиси водорода и полностью остается в растворе. Изменение устойчивости цианистых комплексов повышается в ряду [5]:
Ni(CN) 4 2- (1,84014) < Zn(CN) 4 2- (1,3^1017) < Cu(CN) 4 3- (54031) < Au(CN) 2 - (5D39).
К преимуществам данного способа относится и то, что он не предполагает введения каких-либо веществ, оказывающих негативное влияние на качество катодного золота.
Цель данной статьи – изучение условий очистки товарного электролита от металлов-примесей при введении в систему окислителя (перекиси водорода).
Методика эксперимента
Исследования проводились на промышленном электролите ЗИФ, отобранном на выходе из десорбера при температуре процесса 100 ° С. Состав электролита представлен в табл. 1.
В ходе экспериментов варьировались следующие показатели:
-
- температура процесса (60, 80 и 100 ° С);
-
- расход реагента окислителя (4, 5, 6 и 8 л/м3), где расход окислителя 4 л/м3 соответствует стехиометрически необходимому количеству на окисление комплексов цветных металлов и свободного цианид-иона, содержащихся в растворе электролита.
В качестве реагента-окислителя использовалась перекись водорода с концентрацией активного вещества 35-40 %.
Проба раствора электролита объемом 100 мл помещалась в колбу и нагревалась до заданной температуры. После чего добавлялся окислитель и включалось перемешивание. Пробы
Таблица 1. Состав электролита
Результаты
Изменения степени осаждения никеля, меди и цинка при расходе перекиси водорода 4 л/м3 представлены на рис. 1–3.
Как видно из зависимостей на рис. 1, увеличение температуры процесса оказывает влияние на полноту и начальную скорость осаждения никеля из раствора электролита. Изменение температуры с 60 до 100 ° С при расходе окислителя 4 л/м3 позволяет вдвое повысить степень осаждения никеля – с 40 до 80 %. Значение энергии активации процесса осаждения никеля,
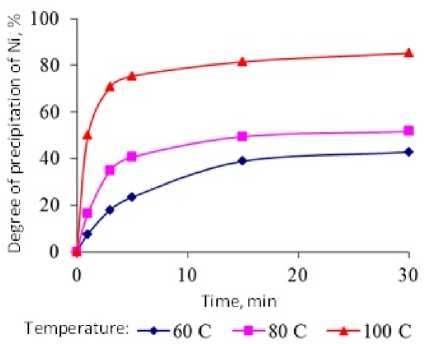
Рис. 1. Изменение степени осаждения никеля при обработке электролита перекисью водорода (4 л/м3) при температурах 60, 80, 100 ° С
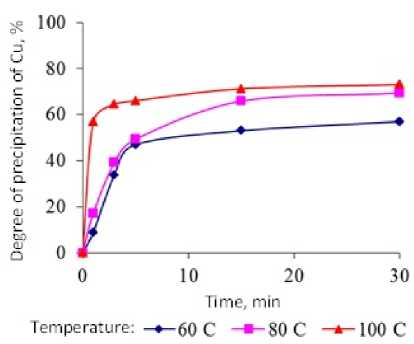
Рис. 2. Изменение степени осаждения меди при обработке электролита перекисью водорода (4 л/м3) при температурах 60, 80, 100 ° С
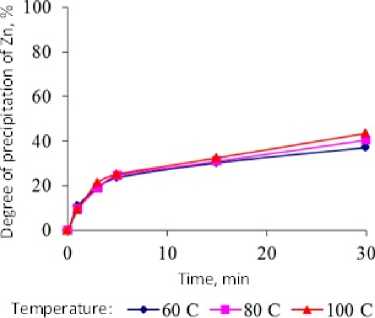
Рис. 3. Изменение степени осаждения цинка при обработке электролита перекисью водорода (4 л/м3) при температурах 60, 80, 100 ° С
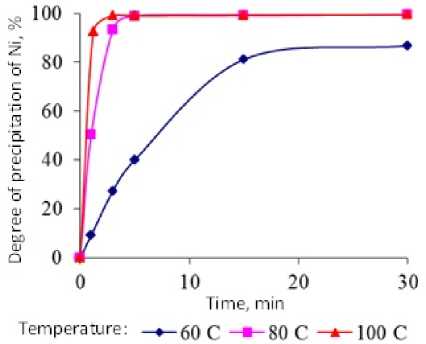
Рис. 4. Изменение степени осаждения никеля при обработке электролита перекисью водорода (8 л/м3) при температурах 60, 80, 100 °С определенное по начальным участкам кинетических кривых, составляет 52,1 кДж/моль, что говорит о том, что процесс протекает в кинетической области.
Степень осаждения меди из элюата в меньшей степени зависит от температуры, находится на уровне 50-65 % (рис. 2). Низкая степень осаждения меди связана с низкой концентрацией меди в исходном растворе электролита (40-50 мг/л) и с большей устойчивостью цианистого комплекса меди по сравнению с комплексом никеля.
Степень осаждения цинка, как видно из кинетических кривых рис. 3, не зависит от температуры процесса и остается на уровне 40 %.
Концентрация золота в растворе неизменна в течение всего процесса осаждения примесей.
При повышении расхода перекиси водорода до 8 л/м3 установленные закономерности сохраняются (рис. 4–6).
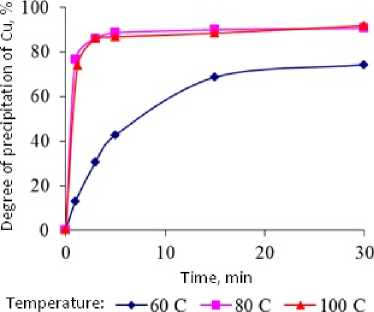
Рис. 5. Изменение степени осаждения меди при обработке электролита перекисью водорода (8 л/м3) при температурах 60, 80, 100 ° С
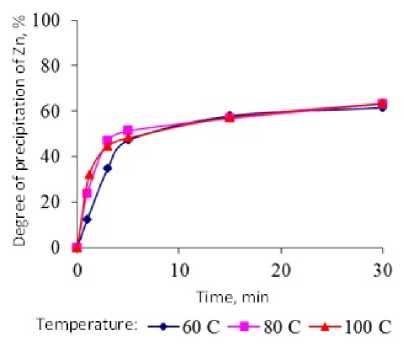
Рис. 6. Изменение степени осаждения цинка при обработке электролита перекисью водорода (8 л/м3) при температурах 60, 80, 100 ° С
При этом расходе при температурах 80-100 ° С степень осаждения меди и никеля достигает максимальных значений – 99 и 90 % соответственно (рис. 4 и 5). Анализ кинетических кривых свидетельствует, что окисление цианистых комплексов металлов полностью протекает за 2–4 мин после добавления перекиси водорода в систему. Образование осадка гидроксидов цветных металлов в этих условиях начинается сразу после введения Н2О2. Скорость фильтрации взвеси, полученной в результате осаждения примесей, достаточно высока. Цвет осадка зеленый, что свидетельствует о преобладании соединения никеля в осадке, что подтверждает химический анализ (табл. 2). Золото в осадке не обнаружено.
Степень осаждения цинка из элюата при увеличении расхода окислителя в два раза увеличивается на 20 % и также не зависит от температуры (рис. 6).
Сопоставление вышеприведенных данных позволяет сделать вывод: при минимальном расходе окислителя (4 л/м3) увеличение температуры способствует повышению степени – 748 –
Таблица 2. Состав осадка гидроксидов
|
Ni, % масс. |
Cu, % масс. |
Zn, % масс. |
|
27,95 |
0,58 |
1,10 |
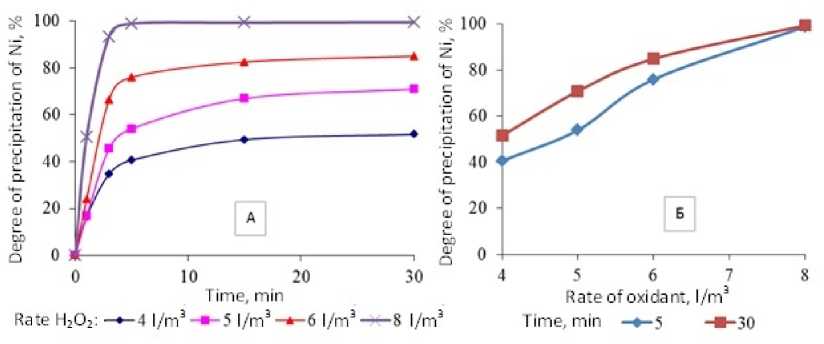
а
б
Рис. 7. Изменение степени осаждения никеля при температуре 80 °C: а - в зависимости от времени при различных расходах перекиси водорода; б – в зависимости от расхода перекиси водорода через 5 и 30 мин ведения процесса осаждения примесей, а при увеличении расхода до 8 л/м3 – скорости осаждения, тогда как полнота осаждения при достаточной продолжительности процесса остается на прежнем уровне.
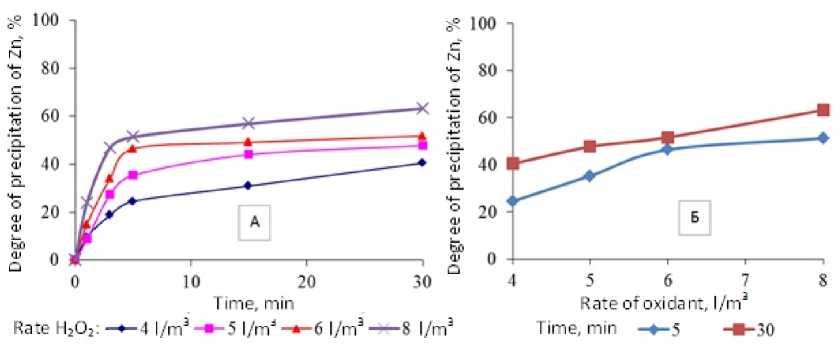
Изменения степени осаждения цветных металлов в зависимости от расхода перекиси водорода и продолжительности эксперимента показаны на рис. 7–9. Видно, что степень осаждения никеля, меди и цинка существенно зависит от расхода перекиси водорода. Основное количество цветных металлов осаждается в первые 5 мин после введения в систему Н2О2 (рис. 7-9 б ). Так, при расходе окислителя 4 л/м3 и температуре 80 ° C за первые 5 мин Ni осаждается на 79 % относительно значения, полученного через 30 мин, медь - на 82 %, цинк - на 60 %, а при расходе 8 л/м3 к тому же моменту времени степень осаждения Ni изменяется до 99 % относительно значения, полученного через 30 мин, медь – до 98 %, цинк – до 81 %.
Так как основной примесью, влияющей на качество катодного осадка при электролитическом получении золота, служит никель, то оптимальным расходом перекиси водорода, позволяющим наиболее быстро и полно осадить примеси цветных металлов, является расход 8 л/м3. При этом расходе степень очистки от никеля достигает 99%, от меди – 90%, от цинка – 65-70%. Эти показатели достигаются при температуре 80 ° C.
Рассмотренный способ предварительной очистки товарного электролита от металлов-примесей позволяет на стадии электролиза получать металл более высокого качества, при этом цветные металлы доизвлекаются из промпродукта, образующегося на стадии очистки, что позволяет решить вопрос комплексного использования сырья.
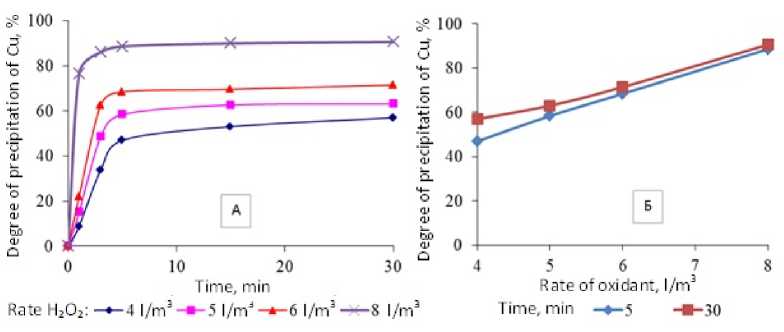
а
б
Рис. 8. Изменение степени осаждения меди при температуре 80 ° С: а - в зависимости от времени при различных расходах перекиси водорода; б – в зависимости от расхода перекиси водорода через 5 и 30 мин ведения процесса
а
б
Рис. 9. Изменение степени осаждения цинка при температуре 80 ° С: а - в зависимости от времени при различных расходах перекиси водорода; б – в зависимости от расхода перекиси водорода через 5 и 30 мин ведения процесса
Выводы
-
1. Установлено, что извлечение металлов-примесей из раствора электролита повышается с увеличением расхода реагента-окислителя, при этом оптимальное количество H2O2 (8 л/м3) соответствует двукратному избытку от стехиометрии.
-
2. Показано, что при минимальном расходе окислителя (4 л/м3) увеличение температуры способствует повышению степени осаждения примесей, а при увеличении расхода до 8 л/м3 – скорости осаждения, тогда как полнота осаждения, при достаточной продолжительности процесса, остается на прежнем уровне.
-
3. Независимо от условий обработки электролита содержание золота в растворе остается постоянным.
-
4. Установлено, что основное количество примесей осаждается в течение 3–5 мин после добавления окислителя в систему.
-
5. При оптимальных параметрах ведения процесса осаждения в лабораторных условиях содержание никеля в растворе снижается на 99, меди – на 90, цинка – на 70 %.


