Одномоментное стентирование ствола левой коронарной артерии и резекция мочевого пузыряпо поводу рака у больного с острым коронарным синдромом без подъема сегмента ST очень высокого риска (клинический случай)
Автор: Сукманова И.А., Пономаренко И.В., Гордеева Д.С.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические случаи
Статья в выпуске: 3 т.40, 2025 года.
Бесплатный доступ
Пациенты с новообразованиями имеют более высокий риск развития сердечно-сосудистых заболеваний (ССЗ). У 90% пациентов острая коронарная катастрофа возникает при прогрессировании рака. Сложность ведения таких больных связана с повышенным риском кровотечений, тромботических осложнений и необходимостью хирургического лечения рака в ближайшее время. В данном сообщении анализируется случай одномоментного стентирования ствола левой коронарной артерии (ЛКА) и резекции мочевого пузыря по поводу распадающейся аденокарциномы у пациента с острым коронарным синдромом без подъема сегмента ST (ОКСбпST) высокого риска. Основным принципом ведения таких пациентов на сегодняшний день остается совместная работа мультидисциплинарной команды и индивидуальный подход.
Острый коронарный синдром, ствол левой коронарной артерии, онкологические заболевания, мультидисциплинарная команда
Короткий адрес: https://sciup.org/149149308
IDR: 149149308 | УДК: 616.132.2-007.272-006.6:[616.62-089.87+616.132.2:615.472.5] | DOI: 10.29001/2073-8552-2025-40-3-188-193
Simultaneous stenting of the trunk of the left coronary artery and resection of the bladder for cancer in a patient with very high risk non-ST elevation acute coronary syndrome (clinical case)
Patients with neoplasms have a higher risk of developing cardiovascular diseases. In 90% of patients, acute coronary catastrophe occurs with the progression of cancer. The complexity of managing such patients is associated with an increased risk of bleeding, thrombotic complications and the need for surgical treatment of cancer in the near future. We analyze a case of simultaneous stenting of the trunk of the left coronary artery and resection of the bladder for decaying adenocarcinoma in a patient with acute coronary syndrome without high-risk ST segment elevation. The main principle of managing such patients today remains the joint work of a multidisciplinary team and an individual approach.
Текст научной статьи Одномоментное стентирование ствола левой коронарной артерии и резекция мочевого пузыряпо поводу рака у больного с острым коронарным синдромом без подъема сегмента ST очень высокого риска (клинический случай)
В настоящее время заболевания системы кровообращения, главным образом ишемическая болезнь сердца (ИБС), и новообразования являются ведущими в структуре основных причин смерти населения Российской Федерации – 43,8 и 13,8% соответственно1. Все больше данных свидетельствует о том, что рак и ИБС связаны общими факторами риска, патологическими механизмами и генетической предрасположенностью [1–6]. Онкологические больные имеют более высокий риск развития сердечно-сосудистых заболеваний (ССЗ), при этом факторы риска повышают риск возникновения нового рака. Данные проспективных исследований Framingham Heart Study и PREVEND подтверждают, что традиционные факторы риска ССЗ, 10-летняя оценка риска развития атеросклеротических ССЗ связаны с повышенным риском развития рака в будущем [4]. Стоит отметить, что преждевременный атеросклероз у молодых людей связан с более высоким риском развития рака. Таким образом, хроническое воспаление, связанное с атеросклерозом, является одним из механизмов канцерогенеза [1, 3].
Доля пациентов с острым коронарным синдромом
(ОКС) и диагнозом рака растет и по последним данным составляет около 3% [2, 6]. У пациентов с онкологическими заболеваниями значительно чаще встречается ОКС без подъема сегмента ST (ОКСбпST), составляя около 85% [7]. Стоит отметить, что почти у 90% пациентов ОКС возникает при прогрессировании онкологического заболевания. По литературным данным, первые 6 мес. после выявления онкологического заболевания сопровождаются максимальным риском развития, прогрессирования ИБС и смертности от ССЗ ввиду рак-индуцированного провоспалительного и протромботического состояния [1, 2, 4, 5, 8]. Согласно большинству научных работ, риск развития тромбоэмболических осложнений, включая инфаркт миокарда, может возникнуть за несколько месяцев до верификации онкологического заболевания и достигает максимума примерно в первые 1–2 года после постановки диагноза злокачественного новообразования [1, 2, 6]. Повышенный риск инфаркта миокарда особенно высок у пациентов с запущенными злокачественными новообразованиями, недифференцированным раком, аденокарциномами и связан с рак-индуцированным провос-палительным и протромботическим состоянием [8].
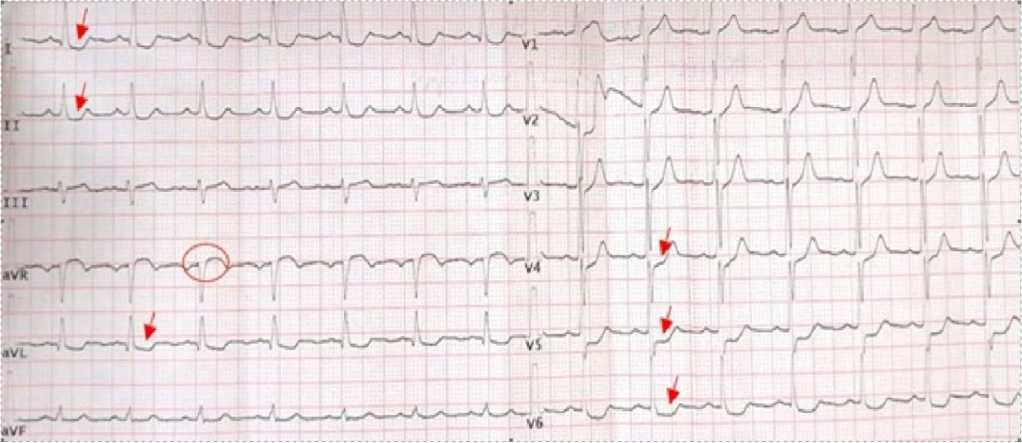
Рис. 1. Электрокардиограмма пациента Х
Fig. 1. ECG of the patient Х
Онкологические пациенты имеют высокий риск тромботических и ишемических осложнений, а также кровотечений после чрескожных коронарных вмешательств (ЧКВ) [2, 8, 9]. В действующих российских рекомендациях по ОКС с подъемом и без подъема сегмента ST отсутствуют данные по тактике ведения больных с ОКС с онкологическими заболеваниями [10]. В связи с ограничением исследований и недостаточной доказательной базой по ведению пациентов с ОКСбпST, высоким ишемическим риском и высоким риском кровотечения мультидисципли-нарный подход остается основополагающим при принятии клинических решений [11–14].
Описание клинического случая
Пациент Х, мужчина 42 лет, поступил в КГБУЗ «Алтайский краевой кардиологический диспансер» 24.11.2022 г. по скорой помощи с жалобами на интенсивные давящие боли за грудиной с иррадиацией в левую руку, нижнюю челюсть.
Из анамнеза. В течение 5 лет страдает гипертонической болезнью с подъемами артериального давления (АД) до 210/120 мм рт. ст. Регулярно принимает лозартан 100 мг, аторвастатин 20 мг, амлодипин 10 мг. Вредные привычки отрицает. Наследственность по ССЗ не отягощена. В течение последних 6 мес. эпизоды макрогематурии, дизурии. Обследовался амбулаторно, патологии не выявлено. Последние 1,5 мес. стал отмечать эпизоды давящих болей, жжения за грудиной на фоне умеренной физической нагрузки с иррадиацией в левую руку, нижнюю челюсть длительностью до 10 мин, самостоятельно купировались в покое. В течение последних 3 дней отмечалось прогрессирование клиники стенокардии.
Внезапное ухудшение 23.11.2022 г. в 21:00 – типичный ангинозный статус, вызвал скорую помощь. По ЭКГ до-госпитально – синусовый ритм, горизонтальная депрессия сегмента ST в I, II, aVL, V4–V6 отведениях до 2 мм, с реципрокной элевацией сегмента ST в aVR до 1,5 мм (рис. 1). На догоспитальном этапе получил аспирин 250 мг, клопидогрел 300 мг, гепарин 5000 МЕ в/в болюсом, морфин дробно в/в с целью обезболивания.
При поступлении состояние средней степени тяже- сти. Индекс массы тела – 35,8 кг/м2, АД – 120/80 мм рт. ст., частота сердечных сокращений – 88 уд/мин, ритм правильный, частота дыхания – 18 в мин, дыхание везикулярное, хрипов нет. Учитывая высокий риск осложнений, выполнена экстренная коронарография, выявлен стеноз терминального отдела ствола левой коронарной артерии (СтЛКА) до 80% с переходом на устье передней межжелудочковой артерии (ПМЖА) и огибающей артерии (ОА); ПМЖА – стеноз устья 80%, ОА – стеноз устья 80%, субокклюзия собственно ОА, диаметр менее 2 мм; правая коронарная артерия (ПКА) – протяженный стеноз в/3 до 60% (рис. 2). Риск по шкале SYNTAX – 25 баллов.
Лабораторно – достоверный прирост маркеров некроза миокарда, микроцитарная анемия средней степени тяжести (гемоглобин 78–72 г/л), умеренный лейкоцитоз (11,2 × 109/л), макрогематурия, в остальном – в пределах референтных значений. По эхокардиографии – фракция выброса левого желудочка (ЛЖ) 64%, гипертрофия стенок ЛЖ, зоны гипо- и акинеза не обнаружены, нарушение диастолической функции ЛЖ по обструктивному типу.
В динамике на фоне рецидивирования ангинозных болей течение заболевания осложнилось острой левожелудочковой недостаточностью. Проводилась в/в инфузия нитратов, морфина, диуретическая терапия, статины, ингибиторы ангиотензин-превращающего фермента, блокаторы кальциевых каналов, препараты железа, монотерапия клопидогрелем, заместительная гемотрансфузия эритроцитарной массой.
Учитывая явления макрогематурии неясного генеза, умеренный риск кровотечения по CRUSADE – 32 б, ARC-HBR (4 больших критерия), антикоагулянты и ацетилсалициловая кислота не назначались. С целью определения источника кровотечения проведена компьютерная томография с контрастированием почек и мочевыводящих путей, диагностировано образование передней стенки мочевого пузыря с признаками распада, прорастанием стенки.
25.11.2022 г. состояние пациента обсуждено мульти-дисциплинарной командой в составе кардиолога, кардиохирурга, рентгенэндоваскулярного хирурга и онкоуролога, принято решение о проведении ЧКВ в объеме стентиро-
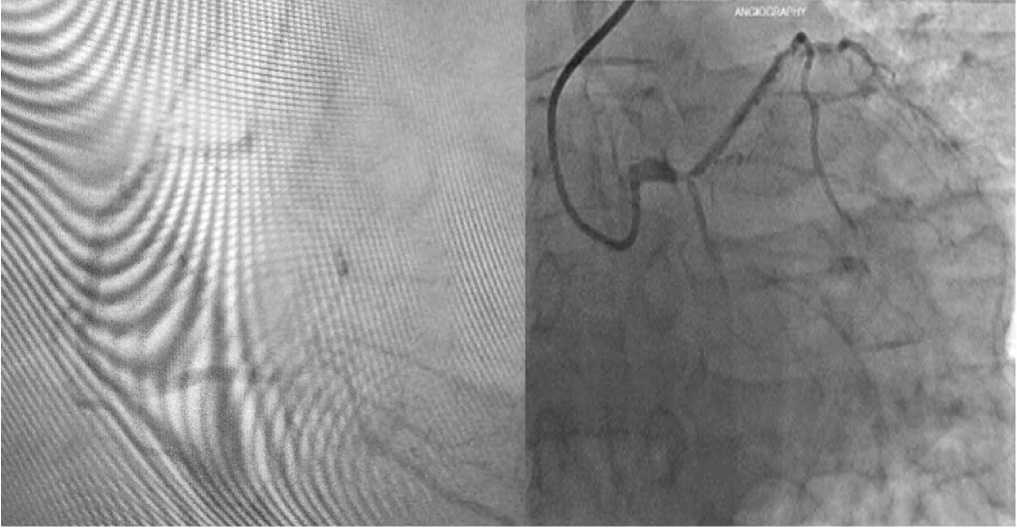
Рис. 2. Ангиографическая картина пациента Х
Fig. 2. Angiographic picture of the patient Х
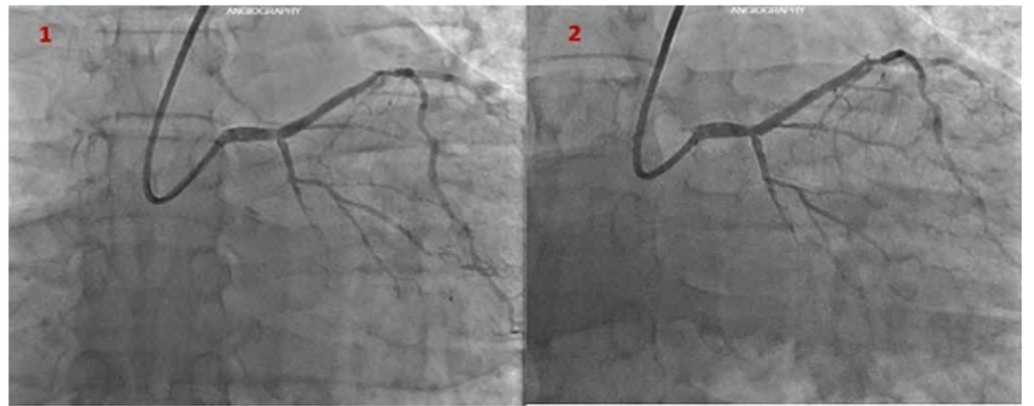
Рис. 3. Коронарография пациента Х: 1 – стентирование ствола левой коронарной артерии – передней межжелудочковой артерии; 2 – итоговый результат после постдилатации стента баллоном и постдилатация через ячейку стента в огибающей артерии
Fig. 3. Coronary angiography of the patient Х: 1 –stenting of the left coronary artery trunk - the anterior interventricular artery; 2 – the final result after postdilation of the stent with a balloon and postdilation through the stent cell in circumflex accent
вания СтЛКА и ПМЖА по неотложным показаниям с последующим оперативным лечением на мочевом пузыре в условиях Алтайского краевого кардиологического диспансера бригадой онкоурологов.
26.11.2022 г. в 06:50 проведено стентирование СтЛКА – ПМЖА стентом с лекарственным покрытием, постдилатация стента баллоном, постдилатация через ячейку стента в ОА (рис. 3). После ЧКВ в связи со снижением гемоглобина до 75 г/л проводилась гемотрансфузия. По ЭКГ после ЧКВ – синусовый ритм, ST на изолинии.
26.11.2022 г. в 10:40 под общей анестезией проведена операция – резекция мочевого пузыря с опухолью. По результатам биопсии верифицирована умеренно дифференцированная аденокарцинома.
27.11.2022 г. пациент переведен с клопидогреля на тикагрелор в дозе 90 мг 2 раза в день (учитывая имеющиеся факторы высокого риска тромбоза стентов).
Послеоперационный период протекал без осложнений, боли ангинозного характера не рецидивировали. В динамике макрогематурия купировалась.
09.12.2022 г. выписан на амбулаторный этап с рекомендациями, направлен на лечение к онкологам.
При выписке: гемоглобин – 95 г/л, тромбоциты – 428 × 109/л, лейкоциты – 9,0 × 109/л, СОЭ – 108 мм/ч, в остальном – без значимых отклонений от референтных значений.
На амбулаторный этап рекомендовано: тикагрелор – 90 мг 2 раза в сутки в течение 12 мес. после стентирования (под контролем гемоглобина, с перерасчетом рисков в динамике через 1 мес.), ацетилсалициловая кислота – 100 мг после обеда постоянно, периндоприл – 5 мг/сут, аторвастатин – 80 мг после ужина, бисопролол – 5 мг/ сут, омепразол – 20 мг утром за 30 мин до еды, железа (III) гидроксид полимальтозат – 100 мг 2 раза в день под контролем гемоглобина. По шкале PRECISE-DAPT – 43 балла, в связи с чем длительность двойной антитромбо-цитарной терапии (ДААТ) будет сокращена до 1–3 мес.
Обсуждение
Согласно рекомендациям ESC по кардиоонкологии (2022), ведение пациентов с ОКС и онкозаболеваниями отличается сложностью из-за хрупкости пациента, повышенного риска кровотечений, тромбоцитопении, тром-бообразования и возможной необходимости выполнения операций в ближайшее время. Из-за потенциально более высокого риска кровотечения предпочтительная антитромботическая стратегия после стентирования коронарных артерий состоит из ДААТ с аспирином и клопи-догрелем. Продолжительность ДААТ должна составлять 1–3 мес. для снижения риска кровотечений [2].
На сегодняшний день ЧКВ является альтернативой операции коронарного шунтирования (КШ) при поражении ЛКА / многососудистом поражении у пациентов с низкой категорией анатомической сложности по SYNTAX (менее 22 баллов) и при отсутствии сахарного диабета. Выбор же стратегии и способ реваскуляризации при многососудистом поражении / вовлечении ствола ЛКА требует специального обсуждения Heart-team-командой и основывается на оценке клиники заболевания, сопутствующей патологии, анатомической тяжести поражения коронарных артерий, риске реваскуляризации, ожидаемой продолжительности жизни [14–18].
В представленном клиническом случае, учитывая наличие у пациента ОКСбпST рефрактерной стенокардии, риск по шкале GRACE – 146 баллов, бифуркационный стеноз СтЛКА, индекс SYNTAX – 25 баллов и активное кровотечение (вследствие распада злокачественного новообразования), мультидисциплинарной командой принято решение о проведении двухэтапного хирургического вмешательства: реваскуляризации миокарда в объеме стентирования СтЛКА и ПМЖА с последующим оперативным лечением на мочевом пузыре в условиях кардиологического стационара по неотложным показаниям.
Представленный пациент имел факторы высокого тромботического риска, характерные для онкологических больных, и геморрагическое осложнение – активное кровотечение из распадающегося онкообразования, потребовавшее проведения гемотрансфузии. После оценки рисков по шкалам CRUSADE (32 балла), PRECISE-DAPT (43 балла), ARC-HBR (4 больших критерия), BARC выявлено, что геморрагические и ишемические (развитие инфаркта миокарда с подъемом или без подъема сегмента ST) риски сопоставимы. В связи с этим после выполнения ЧКВ основных симптомсвязанных артерий (ствол ЛКА и ПМЖА-бифуркационный стеноз) и проведения резекции мочевого пузыря продолжена антиагрегантная монотерапия тикагрелором в дозе 90 мг 2 раза в день без предшествующей нагрузочной дозы. В дальнейшем после полноценного гемостаза возобновлен прием ацетилсалициловой кислоты в дозе 100 мг с рекомендацией минимального периода приема ДААТ (1 мес.).
Кроме того, в настоящее время альтернативой общеизвестным шкалам оценки риска кровотечения у пациентов с ОКСбпST, таким как CRUSADE, PRECISE-DAPT, становится недавно разработанный алгоритм Academic Research Consortium for High Bleeding Risk (ARC-HBR) для определения пациентов с высоким риском кровотечений. Более детализированный подход, включая ана- лиз сопутствующих заболеваний пациента, в том числе активное злокачественное новообразование, позволяет оценить безопасность и эффективность схем лечения пациентов, перенесших ЧКВ. В клинических рекомендациях ESC по ведению пациентов с ОКСбпST (2020) отмечено, что алгоритм ARC-HBR следует использовать в клинической практике, наряду с общеизвестными валидированными шкалами [13, 19].
В связи с ежегодно увеличивающейся распространенностью онкологический заболеваний, широким использованием кардиотоксичных химиопрепаратов и часто встречающимся ОКС у этой категории больных актуальной задачей для профилактики осложнений остается разработка прогностических шкал.
Заключение
Таким образом, важной составляющей при ведении пациентов с ОКС и онкозаболеваниями на сегодняшний день остается совместная работа мультидисциплинар-ной команды врачей и индивидуальный подход, основанный на использовании рискометров.


