Офтальмосканирование в диагностике вторичных опухолей орбиты
Автор: Трухачва Н.Г., Фролова И.Г., Новиков В.А., Величко С.А., Штин В.И.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 4 (24), 2007 года.
Бесплатный доступ
В работе проведено изучение возможностей офтальмосонографии в диагностике вторичных опухолей орбиты. Обследовано 32 пациента с вторичным опухолевым поражением орбиты. Проанализировав ультразвуковые семиотические признаки вторичных новообразований орбиты, были отмечены следующие особенности: преобладала неправильная форма новообразования, низкая эхогенность опухолевой ткани, эхоструктура была неоднородной за счет наличия гиперэхогенных включений (участков патологического костеобразования) и гипоэхогенных участков, обусловленных наличием кистозного компонента и полостей распада. При локализации первичного очага в верхнечелюстных пазухах и в клетках решётчатого лабиринта офтальмосканирование является одним из наиболее информативных методов диагностики, так как объёмные образования при прорастании медиальной и латеральной стенок орбиты хорошо визуализируются, тогда, как при первичной локализации опухоли в лобных пазухах сонография не позволяет достоверно оценить степень прорастания. Высокая информативность с учетом безопасности, доступности позволяет рекомендовать офтальмосканирование в качестве одного из основных методов диагностики опухолей орбиты.
Офтальмосканирование, опухоль орбиты, придаточные пазухи носа
Короткий адрес: https://sciup.org/14054603
IDR: 14054603 | УДК: 617.76-006-071
Ophtalmoscanning in diagnosis of secondary orbital tumors
The present study was undertaken to evaluate the role of ophtalmosonography in diagnosis of secondary orbital tumors. Thirty-two patients with secondary orbital cancer were examined. Ultrasound examination revealed anomalous shaped tumors, tumor tissue low echogenicity, uneven echostructure due to the evidence of hyperechogenous sites of pathologic osteogenesis and hypoechogenous sites with cystic component and decomposition cavities. Ophtalmoscanning has the most informative value when primary tumor is located in maxillary sinuses and ethmoidal labyrinth cells because large lesions with involved medial and lateral orbital walls can be well visualized, whereas sonography fails to assess the tumor involvement extent when primary tumor is located in frontal sinuses. Due to high informative value and safety, ophtalmoscanning is recommended as one of the main diagnostic methods for orbital tumor detection.
Текст научной статьи Офтальмосканирование в диагностике вторичных опухолей орбиты
В структуре онкологической заболеваемости новообразования орбиты составляют от 1 до 2 % [2, 3]. Опухоль в орбите может быть первичной, прорастать из прилежащих анатомических зон или быть метастатической. Поражение орбиты возможно и при лимфопролиферативных процессах. Вторичные опухоли орбиты чаще всего обусловлены прорастанием новообразования из придаточных полостей носа. Метастазы в орбиту могут быть проявлением опухолей различной локализации [1, 2, 13]. Опухоли полиморфны по своему гистогенезу и степени дифференцировки. Частота поражения орбиты в результате прорастания опухолей из смежных областей колеблется от 12 до 50 % и зависит от характера роста и гистологического строения новообразования. При злокачественном процессе распро- странение в орбиту чаще всего наблюдается у больных с опухолями верхнечелюстных пазух, клеток решётчатого лабиринта, реже носоглотки, твёрдого и мягкого нёба [4, 8].
Диагностика новообразований орбиты трудна в силу сходства клинической симптоматики различных процессов, приводящих к увеличению объёма содержимого орбиты [9]. Клиническое исследование не располагает достоверными признаками, позволяющими проводить дифференциальный диагноз, определять зону и характер распространения патологического процесса. Традиционные рентгенологические методы исследования являются малоинформативными при небольших опухолях орбиты. Рентгенологические изменения орбиты и прилежащих околоносовых пазух в большинстве случаев диагностируются уже при выраженных клинических проявлениях. Применение компьютерной и магнитно-резонансной томографии позволяет выявить опухоль и оценить степень распространения опухолевого процесса, однако экономические причины, малая доступность, небезопасность при повторных исследованиях не позволяют их широко использовать [6, 8, 10]. С появлением ультразвукового исследования возможности диагностики расширились, что нашло своё отражение в ряде работ [7, 11, 12]. Изучение возможностей офтальмосонографии в диагностике вторичных опухолей орбиты с точки зрения повышения эффективности последней определяет актуальность и целесообразность работы. Вместе с тем остаются недостаточно освещёнными вопросы эхосемиотики патологии орбиты, особенно вторичного их поражения, что и явилось целью нашего исследования.
Материалы и методы
Обследовано 32 пациента с вторичным опухолевым поражением орбиты. Ультразвуковое исследование (УЗИ) проводилось на аппарате «Aloka SSD 5500» с использованием линейного датчика с постоянной частотой 10 МГц и конвексного датчика с постоянной частотой 3,5 МГц в режиме серошкального сканирования (В-режим) и цветового допплеровского картирования (ЦДК).
Сканирование проводилось транспальпебраль-но через верхние и нижние веки закрытого глаза в стандартном горизонтальном положении пациента лёжа или в вертикальном положении сидя без специальных приспособлений. При исследовании оценивалось состояние глазных яблок, их расположение, ретробульбарное пространство, мышцы, зрительный нерв, стенки орбиты и сосудистые структуры, ретроорбитальная клетчатка, наличие опухоли в полости глазницы.
В процессе исследования при выявлении опухоли анализировались ее размеры, форма, эхогенность, структура, контуры, связь с окружающими тканями и сосудистым пучком, васкуляризация (характер кровотока) и кровоснабжение окружающих тканей при цветовом допплеровском картировании (ЦДК). В режиме ЦДК оценивали следующие признаки: наличие собственных сосудов в массиве опухоли, тип кровотока, а также степень васкуляризации, распределение сосудов в плоскости акустического среза, характер их деления.
При планировании органосохраняющего лечения ультразвуковым методом уточнялась локализация и топометрия патологического очага (размеры, площадь, объем), рассчитывалось расстояние очага от внешнего края костной стенки орбиты, определялось его соотношение с мягкотканными структурами орбиты – зрительным нервом, сосудами, глазодвигательными мышцами и костными структурами.
Спиральная компьютерная томография выполнялась на мультиспиральном томографе «Somatom sensation-4» с применением внутривенного контрастирования омнипаком в аксиальной, сагиттальной и фронтальной проекциях по программе спирального сканирования (срезы 1/1 мм, pitch равный 1–1,5), с последующими мультипланарными реформациями и построением объемного изображения.
Результаты и обсуждение
Пациенты с вторичными опухолевыми поражениями орбиты имели характерные для данной патологии клинические проявления. Основными жалобами являлись: экзофтальм, выявляемый в 60 % случаев, в 32 % случаев больные обращали внимание на наличие объёмного образования в проекции век, в единичных наблюдениях опухоль сопровождалась отёком мягких тканей лица и выявлялось затруднение носового дыхания.
При проведении УЗИ орбиты было установлено, что в 84 % случаев опухоль прилежала к какой-либо из стенок орбиты. Опухоли чаще локализовались у медиальной и верхней стенок орбиты – 43,7 % и 31,2 % соответственно, реже нижней и латеральной – 18,7 % и 6,2 % соответственно.
При поражении клеток решётчатого лабиринта вторичная опухоль в 62,3 % локализовалась у медиальной стенки, в 21,2 % у верхней. Опухоль, прорастающая из верхнечелюстных пазух, чаще локализовалась у нижней стенки – 44,7 %, реже медиальной – 22,6 % и латеральной – 8,6 % случаев.
Смещение глазного яблока было выявлено в 85 % случаев. При локализации вторичной опу-
Таблица 1
Частота встречаемости ультразвуковых признаков вторичных злокачественныхопухолей орбиты по данным офтальмосонографии (n – 32)
Размеры опухолей в максимальном измерении варьировали от 12 до 46 мм. Форма опухоли была различной, в большинстве случаев она приближалась к овальной (72 %), практически во всех наблюдениях располагалась по стенке, повторяя её контур и выступая в полость орбиты на 3–5 мм.
Анализ данных офтальмосонографии позволил выявить характерные ультразвуковые признаки опухолей орбиты (табл. 1). Проанализировав семиотические признаки вторичных новообразований орбиты в целом, мы отметили следующие особенности: строение опухоли
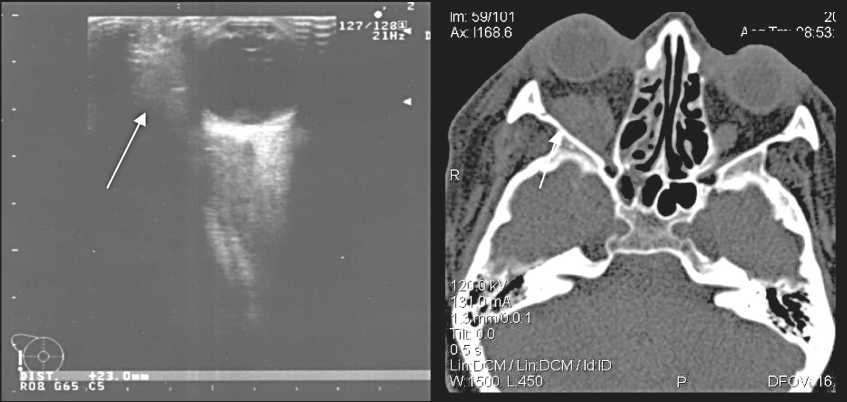
Рис. 1 (а,б). Низкодифференцированная аденокарцинома слизистой оболочки правой верхнечелюстной пазухи (вторичная опухоль занимает задне-латеральные отделы орбиты)
в 78,1 % было солитарным, однако в 21,9 % выявлялось многоузловое их строение. Преобладала неправильная форма новообразования (78,1 %), низкая эхогенность опухолевой ткани (75 %). Контуры новообразований были нечёткими в 65,6 % случаев, чаще определялись как бугристые (78,1 %), Эхогенность окружающих опухоль тканей орбиты была повышенной в 65,6 % случаев. Эхоструктура была неоднородной в 59,3 % случаев. Неоднородность была обусловлена наличием гиперэхогенных включений за счет участков патологического костеобразования, а в 25 % случаев встречались гипоэхогенные включения, морфологически обусловленные наличием кистозного компонента и (или) полостей распада. В 49 % случаев имело место разрушение костной стенки орбиты.
Определение достоверных дифференциальных отличий в эхографических признаках при сравнении вторичных злокачественных опухолей орбиты различного генеза не представлялось возможным в связи с малым количеством больных в группах. Однако, анализируя в сравнительном аспекте ультразвуковую семиотику опухолей и их морфологическое строение, мы получили следующие данные. Чаще всего наблюдалось солитарное строение опухоли, форма опухоли в большинстве случаев была неправильной.
Но при хондросаркоме полости носа и придаточных пазух преобладала низкая эхогенность опухоли (86,6 %) и неоднородная ее эхоструктура, гиперэхогенные включения встречались в 80 % случаев, при этом эхогенность окружающих тканей была повышена. Анализ сонографических данных при низкодифференцированной аденокарциноме слизистой оболочки верхнечелюстной пазухи показал, что низкая эхогенность регистрировалась в 62,5 % случаев, неоднородность эхоструктуры опухоли встречалась реже. При анализе ультразвуковых признаков прочих вторичных новообразований орбиты также отмечено солитарное их строение, неоднородность структуры. При использование ЦДК в опухолевом узле в 59,3 % случаев определялись собственные сосуды, имеющие извитой, разнонаправленный ход, в остальных случаях собственный кровоток в опухоли был представлен единичными сосудистыми структурами.
Всем пациентам, кроме УЗИ орбиты, в сравнительном аспекте была выполнена компьютерная томография (КТ). Выявление опухолей, в зависимости от локализации первичного очага, по данным лучевых методов исследования и оперативного вмешательства показано в табл. 2.
При первичном расположении опухоли в верхнечелюстных пазухах (рис. 1) и прорастании её в орбиту у 15 из 20 больных прорастание было обнаружено методом сонографии, во всех этих случаях интраорбитальный компонент опухоли располагался в области медиальной или латеральной стенок орбиты. У 5 больных прорастание в орбиту было выявлено только по результатам КТ и оперативного вмешательства, так как опухолевый компонент определялся
Таблица 2
Выявление вторичных опухолей орбиты в зависимости от локализации первичного процесса по данным лучевых методов исследования и операций (n- 44)
При прорастании злокачественного новообразования из полости носа (рис. 2) ультразвуковым методом интраорбитальный компонент был обнаружен у 10 из 14 пациентов, при этом у 4 пациентов с ложноотрицательным результатом при помощи КТ интраорбитальный компонент был обнаружен в проекции нижнезадних отделов орбиты и эхоскопически не визуализировался. При первичной локализации опухоли в клетках решётчатого лабиринта прорастание (рис. 3) в орбиту было выявлено у 7 из 10 пациентов по данным офтальмосонографии. У 3 больных интраорбитальный компонент опухоли располагался у верхнемедиальной стенки орбиты, и при расположении датчика параллельно сканируемой плоскости визуализация опухоли была затруднена.
Таким образом, во всех ложноотрицательных случаях при ультразвуковом исследовании глаз- ниц высота интраорбитального опухолевого компонента не превышала 3–5 мм, а костная стенка орбиты была разрушена на небольшом (5–7 мм) протяжении. Следовательно, эффективность офтальмосонографии в выявлении вторичных опухолей орбиты зависела от локализации первичной опухоли Так, при прорастании опухоли из верхнечелюстной пазухи чувствительность сонографии в выявлении вторичного поражения орбиты составила 75 %, а специфичность и точность – 66 % и 72 % соответственно. При первичной локализации опухоли в полости носа чувствительность ультразвука в определении интраорбитального компонента опухоли была выше и составила 85 %, специфичность – 66 %, а точность – 80 %. При расположении первичной опухоли в клетках решётчатого лабиринта чувствительность офтальмосонографии в диагностике поражения орбиты составила 83 %, а специфичность и точность 66 % и 77 % соответственно.
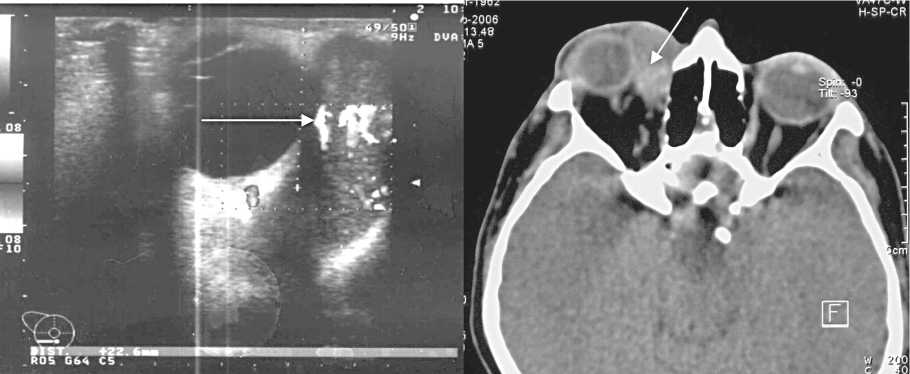
Рис. 2 (а,б). Хондросаркома полости носа (объемное образование располагается в медиальных отделах правой орбиты, тесно прилежит к глазному яблоку)
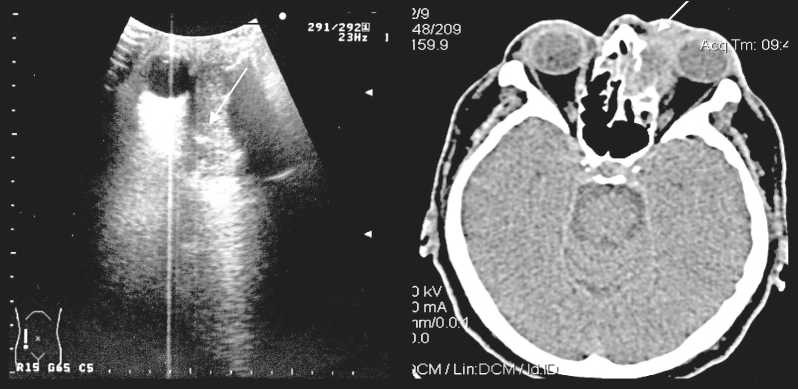
Рис. 3 (а, б). Переходно-клеточная папилома полости носа (опухоль распространяется на клетки решетчатого лабиринта и медиальные отделы орбиты с разрушением костных структур)
Заключение
Таким образом, наш опыт свидетельствует о весьма высоких диагностических возможностях офтальмосонографии в выявлении вторичных опухолей орбиты. При вторичных новообразованиях орбиты имеет значение локализация первичного очага – при локализации первичного очага в верхнечелюстных пазухах и в клетках решётчатого лабиринта офтальмосканирование является одним из наиболее информативных методов диагностики, так как объёмные образования при прорастании медиальной и латеральной стенок орбиты хорошо визуализируются, тогда как при первичной локализации опухоли в лобных пазухах сонография не позволяет достоверно оценить степень прорастания в силу особенностей расположения (датчик располагается параллельно сканируемой плоскости, за счет чего визуализация опухоли затруднена). Высокая информативность с учетом безопасности, доступности позволяет рекомендовать офтальмосканирование в качестве одного из основных методов диагностики опухолей орбиты, что даст возможность исключить из алгоритма обследования дорогостоящие методы визуализации (КТ, МРТ и другие). Своевременное выявление признаков местного распространения опухолевого процесса способствует правильному выбору тактики планируемого лечения в современной орбитальной хирургии (органосохраняющее лечение и эндопротезирование).


