Окислительно-восстановительные процессы при экстракции кобальта в системах с бис(2,4,4-триметилпентил)дитиофосфиновой кислотой
Автор: Флейтлих И.Ю., Григорьева Н.А., Кузьмин В.И., Пашков Г.Л.
Журнал: Журнал Сибирского федерального университета. Серия: Техника и технологии @technologies-sfu
Статья в выпуске: 3 т.6, 2013 года.
Бесплатный доступ
В статье приведены данные по экстракции кобальта из сернокислых растворов бис(2,4,4 триметилпентил)дитиофосфиновой кислотой (НR, Цианекс 301) в нонане и толуоле. Установлено, что экстракция кобальта характеризуется быстрой реакцией с образованием комплекса СоR 2 тетраэдрического строения с последующим окислением Со(II) кислородом воздуха и образованием октаэдрического комплекса СоR 3. Спектрофотометрически показано, что реакция окисления кобальта по металлу и по бис(2,4,4-триметилпентил) дитиофосфиновой кислоте имеет первый порядок. Изучен процесс окисления дитиофосфината кобальта (II) до дитиофосфината кобальта (III) дисульфидом дитиофосфиновой кислоты (R R). Реакция окисления кобальта имеет второй порядок по металлу и первый – по дисульфиду. Показано, что этот окислительно-восстановительный процесс обратим. Изучено влияние электронодонорных добавок (ЭДД, L) на окислительно-восстановительные процессы при экстракции кобальта Цианекс 301. В качестве добавок использовали: триоктиламин (ТОА), триалкиламин фракции С 7 -С 9 (ТАА), октиламин (ОА), трибутилфосфат (ТБФ), n-октанол (ОС). По степени подавления окисления кобальта в системах с Цианекс 301 – добавки можно расположить в следующий ряд: ТОА > ТБФ >> n-октанол ≈ НR без добавок. Экстракция Со в зависимости от типа добавки изменяется в ряду: HR+октиламин > HR ≈ HR+октанол >> HR+ ТОА.
Жидкостная экстракция, бис(2, 4-триметилпентил)дитиофосфиновая кислота, кобальт, окислительно-восстановительный процесс
Короткий адрес: https://sciup.org/146114743
IDR: 146114743 | УДК: 542.61:546.742
Redox processes during cobalt extraction to the systems with bis(2,4,4-trimethylpentyl)dithiophosphinic acid
The paper presents data on cobalt extraction from sulfate solutions with bis(2,4,4-trimethylpentyl) dithiophosphinic acid (HR, trade mark Cyanex 301) diluted with nonane and toluene. It was concluded that cobalt extraction with bis(2,4,4-trimethylpentyl)dithiophosphinic acid is characterized by a fast reaction resulting in the formation of the tetrahedral СоR 2 complex in the organic phase followed by Co(II) oxidation with air oxygen and the formation of the octahedral СоR 3 complex. The cobalt oxidation reaction is first order with regard to both the metal and bis(2,4,4-trimethylpentyl)dithiophosphinic acid concentrations. Oxidation of cobalt(II) dithiophosphinate to cobalt(III) dithiophosphinate by the disulfide of dithiophosphinic acid (RR) has been studied. The cobalt oxidation reaction is second order with regard to the metal concentration and first order with regard to the disulfide concentration. The redox process was shown to be reversible. Cobalt extraction in the presence of various electron donor additives (L) has been studied. Trioctyl amine (TOA), octylamin (OA), n-octanol, tributylphosphate (TBP) were used as additives. On degree of suppression of oxidation of cobalt in systems with Cyanex 301 + additives it is possible to arrange in following seriesr ТОА> ТБФ>> n-oktanol ≈ НR without additives. A decrease in cobalt extraction is observed in the series: HR+ octylamin > HR ≈ HR+ n-octanol>> HR +TOA.
Текст научной статьи Окислительно-восстановительные процессы при экстракции кобальта в системах с бис(2,4,4-триметилпентил)дитиофосфиновой кислотой
Цианекс 301, активным компонентом которого является бис(2,4,4-триметилпентил)дити-офосфиновая кислота (HR), представляет большой интерес для гидрометаллургии кобальта [1]. Исследования по химии экстракции кобальта Цианекс 301 немногочисленны; по мнению авторов, комплексы имеют тетраэдрическую конфигурацию [2–5]. Необходимо отметить, что в большинстве работ при изучении экстракции кобальта бис(2,4,4-триметилпентил)дитиофос-
Ранее была изучена экстракция кобальта ди(2-этилгексил)дитиофосфорной кислотой (Д2ЭГДТФК), химические свойства которой во многом аналогичны с дитиофосфиновой кислотой [6]. Показано, что в инертных растворителях Со(II) быстро извлекается в органическую фазу с образованием комплекса CoR2 тетраэдрической конфигурации. В открытых системах кобальт медленно окисляется кислородом воздуха до Co(III) с образованием комплекса CoR3 октаэдрической конфигурации. В [7, 8] показано, что образующийся дитиофосфат Co(III) в дальнейшем медленно диспропорционирует на дитиофосфат Co(II) и дисульфид дитиофосфор-ной кислоты. Именно этим процессом объясняется протекание обратного процесса - восстановление Со (III).
В настоящей работе приведены результаты исследований по экстракции кобальта из сернокислых растворов бис(2,4,4-триметилпентил)дитиофосфиновой кислотой в отсутствии и присутствии электронодонорных добавок, а также по изучению Red-Ox процессов, протекающих при его экстракции.
Экспериментальная часть
В работе использовали бис(2,4,4-триметилпентил)дитиофосфиновую кислоту (HR), очищенную по методике [9]. Очищенный продукт содержал 98 % основного вещества. Дисульфид бис(2,4,4-триметилпентил)дитиофосфиновой кислоты R2P(S)-S-S-(S)PR2, (R-R) получали по методике [8]. В качестве электронодонорных добавок использовали триоктиламин (ТОА), триалкиламин фракции С 7 -С 9 (ТАА), октиламин (ОА), трибутилфосфат (ТБФ), n-октанол (ОС).
Методика проведения экспериментов по экстракции кобальта и по изучению Red-Ox-процессов в органических растворах описана в [10].
Определение кобальта проводили в водной фазе (рафинатах), общее содержание кобальта в органической фазе устанавливали по разности между его исходным и конечным содержанием в водном растворе после экстракции. Кроме того, концентрацию Co (III) в экстрактах определяли спектрофотометрически, по величине оптической плотности (λ = 455 нм; l = 1 см), в этом случае концентрацию Со(II) находили по разности между общей концентрацией кобальта и Co (III).
Результаты и обсуждение
Экстракция кобальта. В электронных спектрах поглощения (ЭСП) свежеполученного экстракта кобальта (II) имеются полосы с максимумами в области 620, 675 и 790 нм, относящиеся к комплексам CoR2 тетраэдрической конфигурации. В присутствии избытка экстрагента, по мере выдержки экстрактов на воздухе, в спектре поглощения появляется полоса в области 455 нм, относящаяся к комплексам кобальта (III) октаэдрической конфигурации C0R 3 [6].
Окисление кобальта с образованием более прочных соединений приводит к постепенному увеличению коэффициентов распределения металла (табл.).
Билогарифмические зависимости коэффициентов распределения кобальта от кислотности (lgDCo = f(-lgCH+) и концентрации мономерной формы дитиофосфиновой кислоты (lgDCo = f( 1дСмон . )
Таблица. Кинетика экстракции кобальта 0,4 М раствором бис(2,4,4-триметилпентил)дитиофосфиновой кислоты в нонане 0,5 М H 2 SO 4 + 2,0 М Li 2 SO 4 ; C Со = 5,17 . 10-2 М; О:В = 1:1
Окисление кобальта (II) в органической фазе кислородом воздуха. Одним из наиболее значимых факторов, влияющих на скорость окисления кобальта, является концентрация HR. В отсутствие избытка экстрагента существенного окисления кобальта кислородом воздуха не наблюдается (рис. 1, кривая 1). (По оси ординат отложены значения оптической плотности при λ = 455 нм, которые прямо пропорциональны концентрациям окисленного кобальта.) Скорость окисления существенно возрастает при добавлении дитиофосфиновой кислоты (рис. 1, кривые 2-4). Начальные скорости окисления кобальта линейно растут в зависимости от концентрации экстрагента, т.е. реакция имеет первый порядок по экстрагенту.
Данные по окислению кобальта от времени, представленные в координатах lnСоR2(исх)/ СоR 2 (τ) = f(τ), показывают, что зависимость линейна, это свидетельствует о первом порядке реакции по металлу.
Red-Ox-процессы в системе СоR2 – дисульфид. Red-Ox-процессы в изучаемой системе не ограничиваются процессом окисления кобальта (II) кислородом воздуха. В частности, возможен и обратный процесс – восстановление кобальта (III) до кобальта (II). В нормальных условиях этот процесс характеризуется крайне низкой скоростью, однако при повышении температуры он проявляется достаточно отчетливо (рис. 2, кривая 2).
Концентрация Со (III) в органической фазе во времени уменьшается, что, очевидно, связано с восстановлением Со (III) дитиофосфинат-ионом до Со(II) с образованием дисульфида дитиофосфиновой кислоты (R-R). Процесс восстановления Со(III) тоже обратим; так, при смешении растворов дитиофосфината кобальта (II) с дисульфидом имеет место возрастание
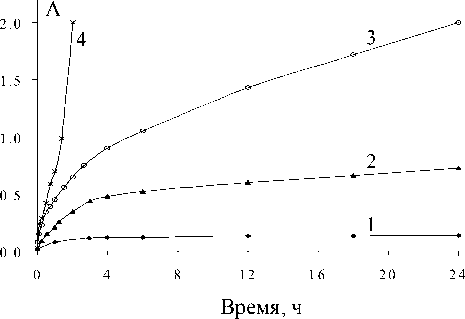
Рис. 1. Влияние дитиофосфиновой кислоты и времени выдержки экстрактов в воздушной атмосфере на окисление кобальта в нонане: 1 – 0,001 М СоR 2 (I); 2 – (I) + 0,02 М HR; 3 – (I) + 0,1 М HR; 4 – (I) + 0,2 М HR
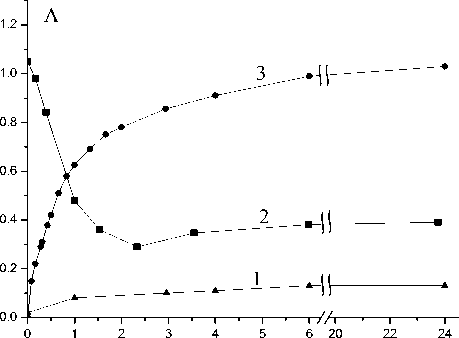
Время, ч
Рис. 2. Изменение оптической плотности от времени при восстановлении и окислении кобальта в экстрактах интенсивности поглощения полосы Со(III) во времени, что свидетельствует об обратной реакции – окислении Со(II) дисульфидом до Со(III) (рис. 2, кривая 3), при этом окраска экстрактов меняется от голубого до коричневого.
-
1. Изменение оптической плотности растворов СоR 2 в отсутствии дисульфида. СоR 2 – 0,001 М; Т = 22 °С.
-
2. Восстановление СоR 3 ; СоR 3 (исх.) = 0,0005 М в толуоле; Т = 60 °С.
-
3. Окисление СоR 2 дисульфидом; СоR 2 (исх.) = 0,0005 М; R-R(исх.) = 0,02 М в толуоле; Т = 22 °С.
Исследовано влияние концентрации кобальта(II) и дисульфида на скорость окисления кобальта. Показано, что скорость окисления кобальта линейно возрастает с увеличением концен- трации дисульфида в смеси, что свидетельствует о первом порядке реакции по этому реагенту. Зависимость окисления CoR2 дисульфидом от времени в координатах CоR2(исх.)/CоR2(т) = f(T) линейна, это свидетельствует о втором порядке реакции по металлу.
Методом изомолярных серий показано, что соотношение CoR2 : R-R достаточно близко к 2 (1,7:1). Это дает основание записать уравнение обратимой Red-Ox-реакции в системе «CoR2 -дисульфид» в следующем виде:
2CoR2 + R-R ^ 2CoR3.(1)
Таким образом, в целом экстракционное извлечение кобальта Цианекс 301 можно описать следующими процессами:
– экстракция кобальта (II)
Со2+ (в) + 2HR(0) ~ C°r2(0) + 2Н+(В);
-
– дальнейшее окисление кобальта кислородом воздуха в присутствии дитиофосфиновой кислоты по схеме:
O 2
C0R2 -----► СоК2^О2 -----► C0R3 + H2O -(3)
Образующийся комплекс CoR3 диспропорционирует, в свою очередь, на CoR2 и дисульфид – R-R (1).
Кроме того, изучено влияние электронодонорных добавок (ЭДД, L) на окислительновосстановительные процессы при экстракции кобальта бис(2,4,4-триметилпентил)дитиофос-финовой кислотой.
Насыщенный кобальтом экстракт в отсутствие добавок достаточно устойчив к окислению в течение длительного времени (рис. 3, кривая 1). При наличии в органической фазе свободной
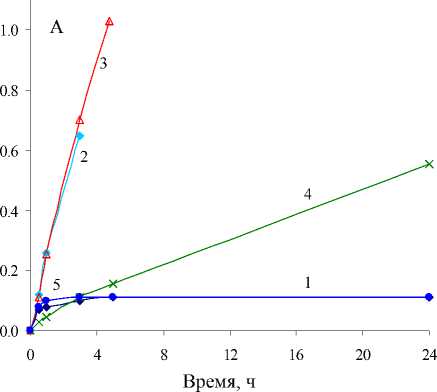
Рис. 3. Зависимость оптической плотности кобальтовых экстрактов в системах c бис(2,4,4-триметилпентил)дитиофосфиновой кислотой (HR) в нонане в присутствии добавок от времени выдержки экстрактов на воздухе. Состав экстрактов: концентрация кобальта 0,001 М; концентрация HR 0,02 М.
1 - C0R 2 ; 2 - CoR 2 + HR (I); 3 - I + 0,3 M n-октанола; 4 - I +0,15 M ТБФ; 5 - I + 0,04 М ТОА
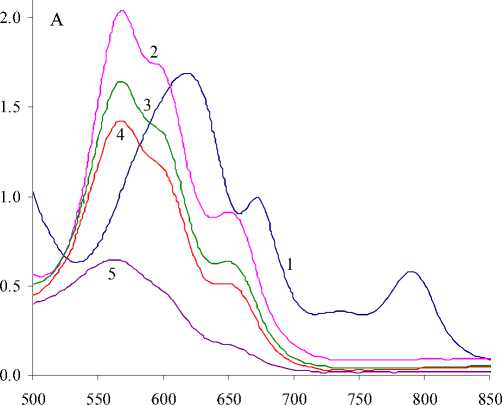
Длина волны, нм
Рис. 4. Электронные спектры поглощения кобальтовых экстрактов с бис(2,4,4-триметилпентил) дитиофосфиновой кислотой в нонане в присутствии октиламина (ОА) Состав экстрактов: 1 – Со -0,02 М (I); 2 – (I) + 0,1 М ОА; 3 – (I) + 0,3 М ОА; 4 – (I) + 0,5 М ОА; 5 – (I) + 0,8 М ОА дитиофосфиновой кислоты при контакте с воздухом наблюдается заметное окисление Со(II) в органической фазе с образованием дитиофосфината кобальта CoR3 октаэдрической конфигурации (рис. 3, кривая 2).
Введение n-октанола в органическую фазу заметно не сказывается на скорости окисления кобальта – кривые 2 и 3 практически совпали. В отличие от октанола ТБФ существенно предотвращает окисление кобальта (рис. 3, кривая 4). В присутствии ТОА (рис. 3, кривая 5) окисление кобальта практически полностью предотвращается. Как можно видеть, введение ЭДД в кобальтовые экстракты, содержащие дитиофосфиновую кислоту, подавляет окисление кобальта. Это связано как с уменьшением активности дитиофосфиновой кислоты в присутствии добавок, так и с взаимодействием добавок с исходным комплексом кобальта (II), препятствующим оксигенации экстрагированного комплекса. Свежеполученный экстракт кобальта (II) в отсутствие электронодонорных добавок имеет голубую окраску, которая в электронных спектрах поглощения обусловлена полосами с максимумами в области 620, 675 и 790 нм, относящимися к тетраэдрической конфигурации CoR2. Введение добавок во всех случаях приводит к появлению новых полос поглощения в спектрах экстрактов и уменьшению интенсивности полос исходного тетраэдрического комплекса CoR2. В качестве примера приведены ЭСП кобальтовых экстрактов в системе CoR2 + октиламин в нонане (рис. 4).
Изменения в ЭСП экстрактов кобальта однозначно свидетельствуют о взаимодействии исходного CoR2 с добавками и образовании смешанно-лигандных комплексов типа CoR/nL, где n = 1,2, октаэдрической или тетрагонально-пирамидальной конфигурации.
Экстракция Со носит сложный характер в зависимости от типа добавки и изменяется в ряду: HR+октиламин > HR = HR+октанол >> HR+ ТОА. Такое поведение Со находит удовлет-– 304 – ворительное объяснение с точки зрения известных представлений о наложении синергетического и антагонистического эффектов.
Как видно, экстракция кобальта с Цианекс 301 носит сложный характер; наряду с собственно экстракцией протекают Red-Ox-процессы в органической фазе; присутствие электронодонорных добавок в органической фазе оказывает существенное влияние на протекание этих процессов.


