Онкомаркеры СА 125, НЕ 4 как предикторные факторы прогноза у больных с пограничными опухолями яичников
Автор: Васильев А.Н., Красильников С.Э., Войцицкий В.Е., Герасимов А.В., Кулиджанян А.П., Бабаянц Е.В., Сисакян В.Г., Крылышкин М.И., Афанасьева Н.А., Мансурова А.С.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 4 (70), 2015 года.
Бесплатный доступ
Целью исследования являлось выявление уровня онкомаркеров СА 125 и НЕ 4 в сыворотке крови у больных пограничными опухолями яичников в зависимости от стадии заболевания, гистологического типа пограничной опухоли, а также проводимого лечения. Материал и методы. Исследование основано на ретроспективном анализе историй болезни 30 больных пограничными опухолями яичников. Группой контроля являлись 70 пациенток с диагнозом рак яичников и 30 клинически здоровых женщин. Результаты исследования. Показатели экспрессии онкомаркеров СА 125 и НЕ 4 при пограничных опухолях превышают показатели у здоровых женщин. При пограничных опухолях яичников I-II стадий значения онкомаркеров СА 125 и НЕ 4 сопоставимы с аналогичными показателями при раке яичников. Однако при III стадии заболевания наблюдаются рост значений уровня онкомаркеров СА 125 и НЕ 4, которые при раке яичников в несколько раз превышает значения у пациенток с пограничными опухолями яичников. После окончания лечения происходит значимое снижение экспрессии онкомаркеров СА 125 и НЕ 4. Заключение. Онкомаркеры HE 4 в комбинации с CA 125 могут являться предикторными факторами оценки эффективности лечения, инструментом для выявления пациенток, относящихся к группе онкологического риска.
Онкомаркеры са 124, не 4, пограничные опухоли яичников, эффективность лечения
Короткий адрес: https://sciup.org/14056558
IDR: 14056558 | УДК: 618.11-006-036-076
Tumor markers СА 125 and НЕ 4 as prognostic and predictive factors in borderline ovarian tumors
The aim of the study was to evaluate the relationship between serum levels of tumor markers СА 125 and НЕ 4 and disease stage, histological type as well as treatment in patients with borderline ovarian tumors. Materials and methods. Thirty patients with borderline ovarian tumors were retrospectively studied. The control group consisted of 70 patients with ovarian cancer and 30 healthy women. Results. Expression levels of СА 125 and НЕ were higher in patients with borderline tumors than in healthy women. In patients with stage I-II borderline ovarian tumors, СА 125 and НЕ 4 levels were similar to those observed in patients with ovarian cancer. However, in patients with stage III borderline ovarian tumors. After completing treatment, a significant reduction in the expression of СА 125 and НЕ 4 markers occurred. Conclusion. Tumor markersHE4 and CA 125 can be predictive factors for tumor response to therapy and the tool for detecting patients at high risk for ovarian cancer.
Текст научной статьи Онкомаркеры СА 125, НЕ 4 как предикторные факторы прогноза у больных с пограничными опухолями яичников
Диагностика пограничных опухолей яичников, называемых еще карциномами с низкой степенью злокачественности, является одной из актуальных проблем современной онкогинекологии. Среди злокачественных опухолей яичников их доля составляет 15–23 % [2, 7]. Несмотря на тот факт, что данные новообразования, в отличие от рака яичников (РЯ), отличаются менее агрессивным течением, их своевременное выявление определяет более благоприятный прогноз. Обычно эти новообразования выявляются на ранней стадии у женщин репродуктивного возраста, что позволяет провести органосохраняющее лечение и сохранить репродуктивную функцию пациенток.
На дооперационном этапе клиническая и инструментальная (УЗИ, МРТ, КТ) диагностика пограничных опухолей, как и рака яичников, затруднена из-за отсутствия патогномоничных симптомов. По этой причине диагноз пограничной опухоли может быть достоверно установлен только по итогам послеоперационного морфологического исследования. В связи с этим большинство операций по поводу новообразований с низким потенциалом злокачественности выполняется в неспециализированных учреждениях, где нет возможности для экспресс-диагностики, от результата которой зависит адекватный объем оперативного вмешательства [1, 2].
С начала 2000-х годов отечественными и зарубежными исследователями для мониторинга эффективности лечения, выявления ранних рецидивов опухолей и выделения пациенток группы повышенного онкологического риска стали применяться методы молекулярно-биологической диагностики с использованием онкомаркеров [3, 4]. Одним из них является опухольассоциированный антиген СА 125, представляющий собой высокомолекулярный гликопротеин, активно секретируемый железистыми клетками эпителия яичников, кишечника и некоторых других клеток. Высокая концентрация данного гликопротеина в крови чаще всего свидетельствует об онкологической патологии яичников. Выявлена прямая корреляция уровня СА 125 в зависимости от возраста пациенток, стадии и гистологического строения опухоли. Так, у здоровых женщин этот показатель составляет 8,9 ± 2,2 Ед/ мл, у больных РЯ I–II стадий – 88 ± 22,1 Ед/мл, при РЯ III–IV стадий уровень СА 125 возрастает до 409 ± 30,1 Ед/мл, при пограничных опухолях – до 68,7 ± 19,7 ед/мл.
При этом содержание онкомаркера было повышено в 90,9 % случаях при серозных пограничных опухолях и в 61,0 % при муцинозных пограничных опухолях [2, 8, 9]. У больных, радикально оперированных по поводу РЯ, уровень СА 125 снижается до 5–15 Ед/мл (эффект удаления опухоли) [3, 4].
Перспективным является также применение нового онкомаркера – эпидидимального белка НЕ 4, принадлежащего к семейству ингибиторов протеиназ [8, 9]. По данным рандомизированных исследований, определение СА 125 в качестве единственного маркера рака яичников обеспечивает чувствительность диагностики, равную 78,3 %, специфичность – 59,4 %, тогда как дополнительное тестирование HE 4 позволяет значительно повысить диагностическую значимость исследования: чувствительность возрастает до 95,1 %, специфичность – до 86,5 % [6, 8, 9]. Применение такого комплексного подхода было осуществлено и для диагностики пограничных опухолей яичников. При этом средние показатели уровня онкомаркера НЕ 4 составили 69 пкмоль/л при колебаниях от 35–202 пмоль/л в зависимости от стадии и гистологического типа опухоли, медиана СА 125 – 53 Ед/мл при колебаниях от 8 до 1225 Ед/мл [8]. Однако данных, позволяющих оценить прогностическое значение комплекса тестов HE 4 и CA 125 для выявления пограничных опухолей, пока недостаточно.
Целью исследования являлось выявление зависимости уровня онкомаркеров СА 125 и НЕ 4 в сыворотке крови у больных пограничными опухолями яичников от стадии заболевания, гистологического типа пограничной опухоли, а также проводимого лечения.
Материал и методы
Исследование основано на ретроспективном анализе историй болезни 30 женщин, больных пограничными опухолями яичников, получавших лечение с января 2012 г. по сентябрь 2013 г. в он-когинекологическом отделении Новосибирского областного онкологического диспансера. Возраст больных колебался от 23 до 62 лет. Из них 50 % составили женщины фертильного возраста – от 23 до 36 лет (n=15). Группой контроля являлись 70 пациенток с диагнозом рак яичника, в возрасте от 35 до 78 лет. Среди них возрастная группа от 30 до 40 лет составила 14 % (n=10). Большая часть наблюдений – 56 % (n=39) – пришлась на пациенток в возрасте 40–60 лет. Женщины старше 60 лет составляли 30 % (n=21). Кроме того, уровень СА 125 и НЕ 4 оценивался у 30 здоровых женщин, проходивших профилактические осмотры.
Из 30 пациенток с пограничными опухолями яичников 9 (30 %) женщин первоначально получили хирургическое лечение в учреждениях гинекологического профиля в нерадикальном объеме, что было обусловлено стертой клинической картиной заболевания и недооценкой факторов онкологи- ческого риска. Двум пациенткам оперативное лечение выполнено по экстренным показаниям, что в последующем потребовало релапаротомии с проведением радикального объема операции.
Стадирование проводилось согласно классификации FIGO 2009 г., в большинстве случаев выявлены Iа и Ib стадии заболевания – 19 (63,3 %) пациенток; IIа, IIб, IIс стадии диагностированы в 8 (26,6 %), III и IIIа стадии – в 3 (10,1 %) случаях. Для морфологической характеристики пограничных опухолей использовалась «Международная гистологическая классификация опухолей женской половой сферы ВОЗ (1996)». Серозные пограничные опухоли (ПОЯ) выявлены в 27 (89,3 %), муцинозные – в 3 (11 %) случаях, что несколько меньше данных зарубежных авторов [6, 8].
Первая стадия рака яичников была выявлена у 10 (14 %), II стадия – у 4 (6 %), III стадия – у 40 (58 %), IV стадия – у 15 (22 %) женщин. Серозный РЯ наблюдался у 65 (93 %), муцинозный РЯ – у 5 (7 %) пациенток. При этом высокодифференцированная аденокарцинома диагностирована в 21 (32 %), умереннодифференцированная – в 28 (44 %), низкодифференцированная – в 7 (10 %), папиллярный рак – в 9 (14 %) случаях. Морфологическая верификация получена по данным гистологического исследования операционных препаратов.
Всем пациенткам проводилось общеклиническое обследование, УЗИ органов малого таза c вагинальным датчиком, УЗИ брюшной полости, обследование ЖКТ. Сравнивались показатели концентрации онкомаркеров СА 125 и НЕ 4 в сыворотке крови до начала и в процессе лечения, а также после его окончания. Определение онкомаркеров проводилось иммунологическими методами в лаборатории «ИНВИТРО».
Пациенткам с Ia стадией пограничных опухолей яичников с благоприятными факторами прогноза (отсутствие нарушения целостности капсулы опухоли до операции, размеры опухоли менее 10 см, высокая дифференцировка опухоли G1, возраст больных моложе 40 лет) проводилась только органосохраняющая операция, в объеме односторонней аднексэктомии, с биопсией контралатерального яичника и мультифокальной биопсией брюшины, резекцией большого сальника. При ПОЯ Ia стадии с неблагоприятными факторами прогноза (нарушение целостности капсулы опухоли до операции, размеры опухоли более 10 см, массивные сращения и спайки опухоли с окружающими тканями, низкая дифференцировка опухоли G3, возраст больных старше 40 лет) в послеоперационном периоде проводилось 3 курса химиотерапии карбоплатином в монорежиме. При ПОЯ Ib стадии выполнялось комбинированное лечение: операция в объеме гистерэктомии с придатками с резекцией большого сальника дополнялась курсами химиотерапии, количество которых варьировало в зависимости от стадии заболевания согласно «Стандартам по оказанию медицинской помощи онкологическим больным».
Эффективность проводимого лечения оценивалась по данным УЗИ, МРТ и гинекологического осмотра. За время наблюдения данных за рецидив заболевания не выявлено.
Статистическая обработка полученных данных проводилась с использованием программы «Sta-tistica 6.0» с использованием общепринятых параметрических и непараметрических статистических методов. Вычислялась средняя величина (M), среднеквадратичное отклонение (δ), стандартная ошибка средней. При сравнении двух независимых групп по количественному признаку использовался t-критерий Стьюдента для независимых ошибок. Критический уровень достоверности принимали равным 0,05(p≤0,05).
Результаты исследования
В среднем уровень онкомаркера СА 125 в сыворотке здоровых женщин составил 8 Ед/мл (6–29 Ед/мл), НЕ 4 – 49 пмоль/л (36–98 пмоль/л), что соответствует данным других авторов [2, 5, 6, 8, 9]. Значения уровня онкомаркера СА 125 в сыворотке крови у пациенток с пограничными опухолями яичников I стадии составили 10,3 ± ± 1,9 ЕД/мл (n=19), II стадии –15,2 ± 3,2 Ед/мл (n=8), что сопоставимо с показателями уровня онкомаркера у больных РЯ I стадии – 12,5 ± 2,5 Ед/ мл (n=10) и II стадии –18 ± 2,4 Ед/мл (n=4). Тогда как у больных РЯ III стадии отмечается значительный рост показателей СА 125 – 564 ± 78 Ед/мл (n=40), что практически в 2 раза превышает аналогичные значения у пациенток с пограничными опухолями яичников III стадии – 275 ± 95 ЕД/мл (n=3) (рис. 1, 2).
Аналогичные изменения выявлены при анализе уровня онкомаркера НЕ 4 (рис. 3). У пациенток с пограничными опухолями и раком яичников I–II стадий его значения до лечения не различаются: ПОЯ I стадии – 38 ± 2,3 пмоль/л, РЯ I стадии – 41 ± ± 4,1 пмоль/л, ПОЯ II стадии – 42 ± 4,4 пмоль/л, РЯ II стадии – 43 ± 4,9 пмоль/л. Начиная с III стадии заболевания, наблюдается превышение значений уровня онкомаркера НЕ 4 у больных раком яичников, по сравнению с группой пациенток с пограничными опухолями – 310 ± 31,4 пмоль/л и 228 ± ± 54 пмоль/л соответственно (p<0,05).
После лечения при РЯ I–II стадий не отмечено статистически значимого уменьшения значений НЕ 4, что, вероятно, связано с гетерогенностью опухолей, хотя прослеживается тенденция к их снижению. Однако при ПОЯ и РЯ III–IV стадий наблюдалось значимое снижение концентрации онкомаркера НЕ 4 (p<0,05). При этом уровень опухолевых маркеров при раке яичников в 1,5–2 раза (p<0,05) превышает аналогичные показатели у больных с пограничными опухолями яичника. Вероятнее всего, это обусловлено изначально более высокими значениями уровня онкомаркеров у больных раком яичников (рис. 1, 2).
Следует отметить, что уровень онкомаркеров зависит не только от стадии, но и от гистотипа опухоли. В нашем исследовании выявлено снижение среднего уровня маркера СА 125 у женщин с серозными ПОЯ в репродуктивном возрасте (n=15) – 95 ± 5,4 ЕД/мл по сравнению с группой пациенток с муцинозными пограничными опухолями (n=3) – 65,3 ± 3,4 Ед/мл, что согласуется с данными литературы [2, 5, 6, 8, 9]. Обратная тенденция выявлена для онкомаркера НЕ 4, его среднестатистические значения у пациенток в репродук-
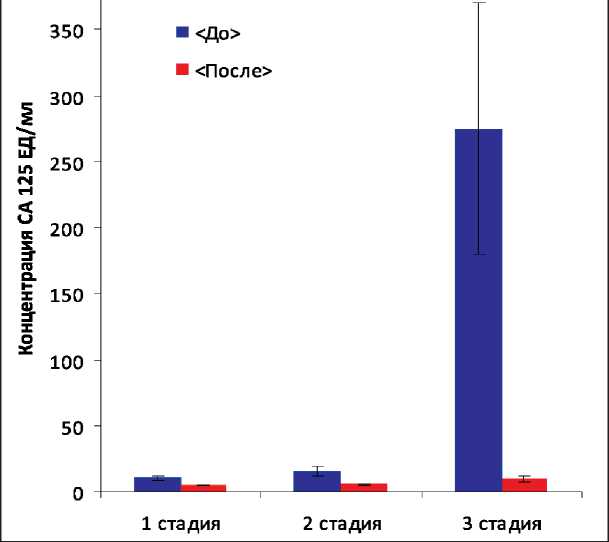
Рис. 1. Уровень онкомаркера СА 125 в сыворотке крови больных с пограничными опухолями яичников до и после лечения (p<0,05)
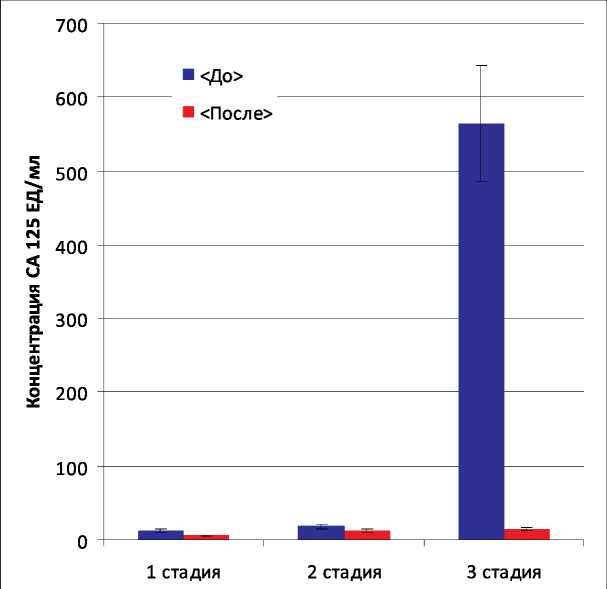
Рис. 2. Уровень онкомаркера СА 125 в сыворотке крови больных раком яичников до и после лечения (p<0,05)
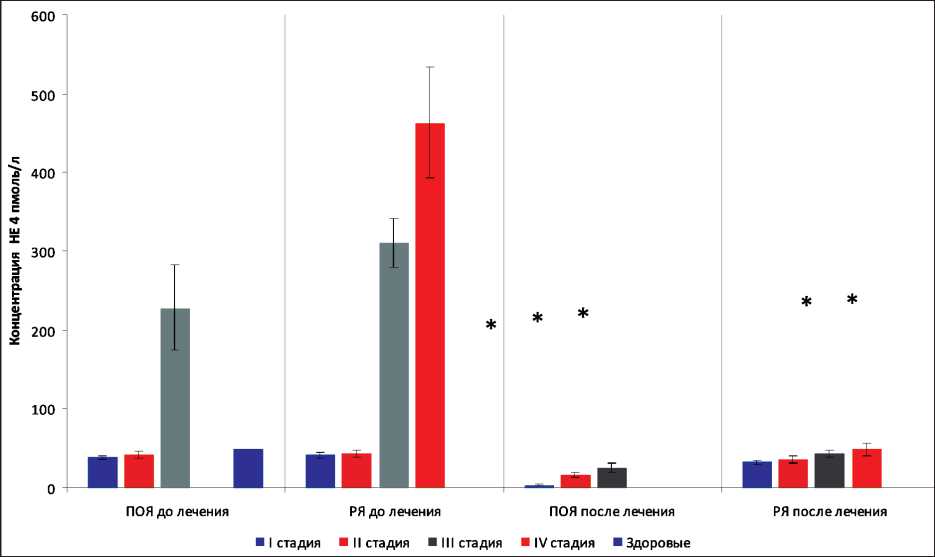
Рис. 3. Уровень онкомаркера Не 4 в сыворотке крови больных с ПОЯ и РЯ до и после лечения (p<0,05)
тивном возрасте составляют 76,5 ± 3,2 пмоль/л, что ниже, чем у больных с муцинозными ПОЯ, – 85,5 ± 3,6 пмоль/л.
Заключение
Результаты проведенного исследования позволяют утверждать, что показатели уровня онкомаркеров СА 125 и НЕ 4 при пограничных опухолях до лечения значительно превышают таковые у здоровых женщин. При пограничных опухолях яичников I–II стадий значения онкомаркеров СА 125 и НЕ 4 сопоставимы с аналогичными показателями при раке яичников. Однако при III стадии заболевания наблюдается рост значений уровня онкомаркеров СА 125 и НЕ 4, которые при раке яичников в не- сколько раз превышают значения у пациенток с пограничными опухолями яичников.
Список литературы Онкомаркеры СА 125, НЕ 4 как предикторные факторы прогноза у больных с пограничными опухолями яичников
- Бохман Я.В. Лекции по онкогинекологии. М., 2007. 167 с.
- Новикова Е.Г., Батталова Г.Ю. Пограничные опухоли яичников. М., 2007. 151 с.
- Сергеева Н.С., Маршрутина Н.В. Общие представления о серологических биомаркерах и их месте в онкологии//Практическая онкология. 2011. Т. 12, № 4. С. 147-154.
- Тюляндин С.А., Моисеенко В.М. Практическая онкология: избранные лекции. СПб., 2004. 784 с.
- Чернышова А.Л., Чуруксаева О.Н. Роль опухолевого маркера СА-125 в выявлении рецидива рака яичников и определении тактики лечения//Сибирский онкологический журнал. 2010. № 3. С. 34-37.
- Bast R.C. Jr., Skates S., Lokshin A., Moore R.G. Differential diagnosis of pelvic mass: improved algorithms and novel biomarkers//Int. J. Gynecol. Cancer 2012. Vol. 22. P. 5-8. doi: 10.1097/IGC.0b013e318251c97d.
- Tropé С.G., Kaern J., Davidson B. Boderline ovarian tumours//Best Pract. Res. Clin. Obstet. Gynaecol. 2012. Vol. 26 (3). P. 325-336 DOI: 10.1016/j.bpobgyn.2011.12.006
- Kalapotharakos G., Asciutto C., Henic E., Casslen B., Borgfeldt C. High preoperative blood ievels of HE 4 predicts poor prognosis in patients with ovarian cancer//J. Ovarian Res. 2012. Vol. 5 (1). P. 20 DOI: 10.1186/1757-2215-5-20
- Moore R.G., McMeekin D.S., Brown A.K., DiSilvestro P., Miller M.C., Allard W.Jeffery, Gajewski W., Kurman R., C.Bast Jr. R., Skates S.J. A novel multiple marker bioassay utilizing HE 4 and CA 125 for the prediction of ovarian cancer in patients with a pelvic mass//Gynecol. Oncol. 2009. Vol. 112 (1). P. 40-46 DOI: 10.1016/j.ygyno.2008.08.031


