Определение антиоксидантной активности молочно-растительного экстракта методом жидкостной хроматографии
Автор: Рудниченко Елена Сергеевна, Коренман Яков Израильевич
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Фундаментальная и прикладная химия, химическая технология
Статья в выпуске: 2 (52), 2012 года.
Бесплатный доступ
Установлена антиоксидантная активность молочно-растительного экстракта природного подсластителя якона. Для извлечения якона из твердых клубней впервые в качестве экстрагента применен ультрафильтрат творожной сыворотки - продукт экстракционного разделения молочной сыворотки. Антиоксидантную активность экстракта якона измеряли амперометрически на жидкостном хроматографе «ЦветЯуза-01-АА». Разработана методика выполнения измерений содержания актиоксидантов. Приведены уравнения для расчета антиоксидантной активности якона. Суммарное содержание природных антиоксидантов позволяет рекомендовать экстракт якона для создания новых пищевых продуктов с повышенной антиоксидантной активностью.
Ванилины, ванилиновая кислота, экстракция, полиэтиленгликоль, уф-спектрофотометрия
Короткий адрес: https://sciup.org/14039823
IDR: 14039823 | УДК: 543.544.05.068.7
Determination of antioxidant activity of milk - vegetable extracts by liquid chromatography
Antioxidant activity of milk-plant extract of natural sweetener yakon has been established. To extract yakon solid tubers for the first time as an extractant used ultrafiltrate of cheese whey - a product of the extraction separation of whey. Antioxidant activity of extracts was measured amperometrically yakon on the liquid chromatograph "Colour-Yauza-01-AA."A technique for measuring the content of antioxidant. The equations for calculating antioxidant activityyakon. The total content of natural antioxidants can be recommended extract yakon to create new foods with high antioxidant activity.
Текст научной статьи Определение антиоксидантной активности молочно-растительного экстракта методом жидкостной хроматографии
Антиоксидантной активностью характеризуются токоферолы ( а-, в-, Y—, 8 -изомеры), аскорбиновая кислота, аскорбаты натрия, кальция и калия, изоаскорбиновая кислота, лактат калия, кверцетин, дигидрокверцетин (производные флавонов), лимонная и винная кислоты, фермент глюкозооксидаза.
Применение природных антиоксидантов, которые являются полезными добавками, представляется наиболее перспективным для ингибирования окислительных процессов по сравнению с их синтетическими аналогами.
В настоящее время все большее внимание привлекает подсластитель натурального происхождения – якон [1]. Корнеплоды якона содержат большой спектр олигофруктанов, а также моносахариды (в основном глюкозу и фруктозу), сахарозу, 60-70 % сухого вещества представлено инулином. Из минеральных веществ корнеплоды якона содержат азот и фосфор, магний, натрий, кальций, железо, цинк,
медь, калий. Основными азотсодержащими компонентами являются амиды и аминокислоты как в свободном состоянии, так и в составе белка. Кроме того, корнеплоды якона содержат соединения, характеризующиеся антиоксидантной активностью, а также способны накапливать селен до 1,1 мг/кг.
Экстрагирование – один из перспективных способов извлечения компонентов, характеризующихся антиоксидантными свойствами, которые тормозят процессы окисления, протекающие в клетках. В качестве экстрагента применен ультрафильтрат творожной сыворотки.
Цель работы – определить антиоксидантную активность полученного молочнорастительного экстракта якона.
Нами предлагается в качестве экстрагента ультрафильтрат творожной сыворотки – продукт фракционного разделения молочной сыворотки, полученный нами на ультрафильтрационной установке с мембранами типа ОПМ-450С. Он содержит значительное количество лактозы (около 90 % от общего содержания сухих веществ), аминокислоты, низкомолекулярные белковые вещества, молочную кислоту, макро- и микроэлементы, жиро- и водорастворимые витамины. По органолептическим показателям ультрафильтрат творожной сыворотки представляет собой прозрачную желтую жидкость с более высокой биологической и коллоидной стабильностью, чем творожная сыворотка.
Молочно-растительный экстракт получали по следующей методике. Клубни якона измельчали до 2 мм и сушили при 60 °С до содержания сухих веществ на уровне 6 – 7 мас. %, добавляли экстрагент – ультрафильтрат творожной сыворотки (соотношение объемов твердой и жидкой фаз 1 : 6 и подкисляли раствором гидрокарбоната натрия или лимонной кислоты до рН 4,4, кислотность экстрагента контролировали потенциометрически. Экстрагировали на вибросмесителе при 60 °С. В течение 60 мин достигалось максимальное содержание сухих веществ в экстракте. Затем проводили двухступенчатую очистку экстракта путем его пропускания через колонку, заполненную активированным углем.
Определение антиоксидантной активности выполняли в окислительном режиме амперометрическим методом на жидкостном хроматографе «ЦветЯуза-01-АА».
Амперометрический метод – единственный непосредственно измеряющий содержание всех антиоксидантов в пробе. Метод отличается высокой селективностью определения только в отношении антиоксидантов [24]. Другие методы – непрямые, предназначены для измерения ингибирования реакционных смесей, генерируемых определенными реакциями. Методом восстановления Fe3+ до Fe2+ (FRAP) также можно определять суммарное содержание антиоксидантов, однако он не предназначен для детектирования всех антиоксидантов, в частности, тиолов, так как их восстановительный потенциал значительно ниже потенциала превращения Fe3+ до Fe2+ [5].
Настоящая методика выполнения измерений предназначена для измерения содержания антиоксидантов (СА) в водорастворимых БАДах, напитках (соках, чае, винах, пиве, квасах, бальзамах, коньяках), экстрактах растений в диапазоне 0,2 – 4,0 мг кверцетина (стандарта)/дм3. В случае, если измеренная величина СА превышает 4,0 мг/дм3, предусматривается разбавление пробы бидистилла-том до 1000 раз.
Величина СА образцов определяется содержанием в них природных флавоноидов, в частности, катехинов (вещества группы флавана); кверцетина, рутина, дигидрокверцетина (вещества группы флавона); а также витаминов и других соединений, способных связывать свободные радикалы.
Для определения антиоксидантов в экстракте измеряли величину тока, возникающего при окислении антиоксиданта на поверхности стеклоуглеродного электрода. Полученный сигнал сопоставляли со стандартом (дигидрокверцетин), измеренным в тех же условиях. Величина тока зависит от природы анализируемого объекта и приложенного потенциала.
Условия измерений: температура (25 + 10) оС, напряжение переменного тока 220 В, частота тока (50 ± 1) Гц.
Предварительно готовили элюент (2,2 мМ раствор ортофосфорной кислоты) и стандартные растворы дегидрокверцетина с концентрациями 0,5; 1,0; 1.5; 2,0; 3,0
и 3,5 мг/дм3.
Высокая чувствительность определения, низкий остаточный ток и хорошая воспроизводимость аналитического сигнала наблюдаются на стеклоуглеродном электроде, выбранном в качестве рабочего [6]. Для построения градуировочного графика устанавливали потенциал +1,3 В. Скорость потока элюента 1,2 см3/мин. Применяли дегидрокверцетин квалификации ч.д.а. Серию растворов готовили по навеске и с последующим разведением дистиллированной водой. Построение градуировочной функции проводили по 6 водным растворам дегидрокверцетина, величину тока которых измеряли по 3 раза.
Строили градуировочную функцию методом наименьших квадратов (рис. 1). Полученный график описывается уравнением прямой, достоверность аппроксимации 0, 9938:
Y = 0,00037405· X + 0,1861 , где Х – сигнал кверцетина (площадь выходной кривой), нА·с; Y – концентрация раствора дегидрокверцетина, мг/дм3.
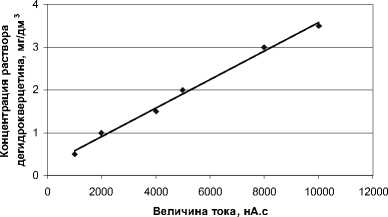
Рис. 1. Градуировочный график для определения антиоксидантной активности
Окисление антиоксиданта происходит на поверхности стеклоуглеродного электрода, потенциал которого при этом возрастает.
Вольтамперометрическое окисление молочно-растительного экстракта представлено на рис. 2: τ – продолжительность анализа (время выхода) экстракта, полученного из клубней якона, с; I – величина аналитического
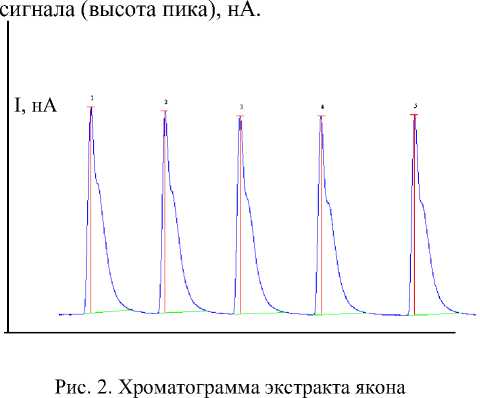
Т а б л и ц а
Показания анализатора «ЦветЯуза-01-АА» при анализе экстракта якона
|
Номер пика |
Время выхода пробы, c |
Полуширина пика, c |
Высота пика, нА |
Площадь пика, нА∙c |
|
1 |
23,61 |
10,74 |
589,82 |
6333,55 |
|
2 |
77,31 |
10,46 |
578,47 |
6049,58 |
|
3 |
132,08 |
10,54 |
567,10 |
5974,53 |
|
4 |
191,04 |
10,35 |
568,40 |
5882,67 |
|
5 |
258,89 |
10,32 |
573,76 |
5921,23 |
|
Среднее результатов измерений |
6032,31 |
|||
По результатам измерений вычисляли среднее арифметическое площади пиков (таблица). Из полученных значений высот пиков следует, что относительная погрешность измерений не превышает 5 %.
Антиоксидантную активность экстракта (СА) вычисляли по уравнению:
СА = Саг ∙ N, где Саг – содержание антиоксидантов, найденное по градуировочному графику, мг/дм3 (рис. 1) ; N – кратность разбавления экстракта.
Y = 0,00037405·6032,31 + 0,1861 = 2,44 мг/дм3, с учетом 50-кратного разбавления получаем концентрацию раствора дегидрокверцетина Y = 2,44·50 = 122 мг/дм3.
Метод жидкостной хроматографии с амперометрическим детектированием – универсальный метод определения антиоксидантной активности [7-9]. Анализ легко выполним, высокочувствителен, требует минимального расхода реактивов. Относительная погрешность – не более 5 % при доверительной вероятности 0,95.
Из полученных результатов можно сделать вывод о том, что молочно-растительный экстракт проявляет антиоксидантную активность по отношению к процессу электровосстановления кислорода. Значение суммарного содержания природных антиоксидантов позволяет рекомендовать экстракт для антиоксидантной терапии, а также для создания новых продуктов с повышенной антиоксидантной активностью.


