Определение содержания йода в скорлупе ореха методом пиролиза в интервале температур 100-550°C
Автор: Токторбаева Гулсун Болотовна, Ташполотов Ысламидин Ташполотович
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Технические науки
Статья в выпуске: 7 т.6, 2020 года.
Бесплатный доступ
В статье изложены результаты научных исследований по переработке ореховой скорлупы методом пиролиза. Изучен процесс пиролиза скорлупы грецких орехов в интервале температур 100-550 °C с образованием древесного угля без доступа воздуха. Неорганическая составляющая в скорлупе составляет порядка 25%, в тоже время органическая часть - 75%. Установлено, что выход древесного угля из скорлупы грецких орехов составляет при 550 °C 31,3% веса, а концентрация йода - 0,105 мкг/дм3.
Скорлупа грецкого ореха, древесный уголь, йод
Короткий адрес: https://sciup.org/14117791
IDR: 14117791 | УДК: 662 | DOI: 10.33619/2414-2948/56/26
Determination of the content of iodine in a nut corner by pyrolysis in the temperature range 100-550°C
The article presents the results of scientific research on the processing of nutshells by the pyrolysis method. The process of pyrolysis of walnut shells in the temperature range of 100-550 °C with the formation of charcoal without air was studied. The inorganic component in the shell is about 25%, while the organic part is 75%. It was found that the yield of charcoal from the walnut shell is 31.3% by weight at 550 °C, and the iodine concentration is 0.105 μg/dm3.
Текст научной статьи Определение содержания йода в скорлупе ореха методом пиролиза в интервале температур 100-550°C
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 662
В работе представлены результаты научных исследований по переработке ореховой скорлупы методом пиролиза. Установлено, что в интервале температур от 250°C до 550°C выход древесного угля из скорлупы грецких орехов составляет при 550°C 31,3% веса [1].
Как известно, при переработке грецкого ореха на ядро или высококачественное масло в качестве отхода образуется скорлупа грецкого ореха, составляющая в среднем 51-59% от веса самого ореха, в процессе пиролиза можно получить ценные и полезные продукты, например йод [2].
Йод
широко распространeн в природе. В незначительных количествах он находятся
повсюду в морской воде, земной коре в растительном и животном организмах. Соединение йода содержится в некоторых сточных водах химической и фармацевтической промышленности. В природе йод содержится преимущественно в виде иодидов и он относится к важнейшим биогенным элементам, необходимой для нормального функционирования организма человека, в то же время повышенная концентрация йода представляют определенную опасность для здоровья человека [1; 2].
Измерение концентрации йода основано на окисление йодидов до йодатов в кислой среде в бромированой воде путем восстановления последних до свободного йода согласно формул:
J+3Br2+3H2O→JO3+6H++6Br
KClO3+5KJ+H2SO4=3J2+3K2SO4+3H2O
J+2Na2S2O4= Na2S4O6+2 Na J
Количественное определение йода проводятся иодометрическим титрованием.
Экспериментальная часть
Химический состав ореховой скорлупы исследовали с помощью спектроскопического и фотометрического методов, полученные результаты представлены в Таблице.
Таблица.
ХИМИЧЕСКИЙ СОСТАВ ОРЕХОВОЙ СКОРЛУПЫ
Наименование соединение металлов в, % о О О О О О О О О О О О О Q о о
■^ ^ Z О £ 3 Й m £ б й £ 3 ^ Z
Зола ореховой косточки
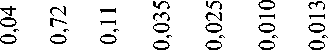

со о
На основании экспериментальных исследований методом пиролиза ореховой скорлупы установлено, что неорганическая составляющая в скорлупе составляет порядка 25%, в тоже время органическая часть — 75%. Неорганическая часть скорлупы содержит 23,8% оксид кремния.
Для определения содержания йода в ореховой скорлупе, сначала отобранные пробы просушили в сушильном шкафу до постоянного их веса [3; 4; 5; 6]. Для эксперимента отобрали 100 грамм исследуемого образца. Измельчали их в шековой дробильке и пропускали полученный порошок через сито с размером ячейки 0,076 мм.
Далее исследуемый образец с определенной дисперсностью загружали в химический стакан емкостью 250 см3, в который добавили 150 мл 95%-ного этилового спирта. Полученную спиртовую суспензию перемешивали электромензильной установке в течении 45 мин. После этого в исследуемые пробы добавляли 1000см3 дистлированной воды и потом раствор фильтровали через бумажный фильтр.
Пробы с более низким содержанием йодидов предварительно концентрировали методом выпаривания. После этого пробы помешали в термостойкий стакан с водой, прибавляли 10 капель 1%-ного раствора фенольфталейна. После этого далее в раствор ввели 10 см3 спирта, тщательно перемешивали и добавили 2-3 капли концентрированного раствора K 2 SO 3 . Сухой остаток в чашке должен быть бесцветным, в противном случае нужно повторяют весь процесс.
|(сс ) О |
Раствор К 2 СО 3 доводили до ярко красного окрашивания не изчезающего при перемешивании. После этого раствор помешали в форфорувую чашку и выпаривали в водяной бане до сухого остатка, просушили в сушильном шкафу и далее прокаливали в электропечи при температуре до 4500С до объема 300-400 см3. Прокаливание продолжали до полного обучливания (термического ожога) органического вещества. Проколенный остаток увлажняли водой и растирали со стеклянной палочкой до однородной массы.
Для перевода иодида калия с йодами для выделения свободного йода осуществляли последовательно следующие процессы: бесцветный остаток растворяли в 1,5 см3 дистиллированной воды, фильтровали через воронку конической колбы емкостью около 25 см3.
Объем исследуемого раствора должен составлять около 4 см3. К фильтрату добавили 2 капли раствора метилового оранжевого и также вводили 2 см3 5%-го раствора H 2 SO 4 . Затем порциями по 20-25 капли приливают бромированную воду до окрашивания раствора в желтый цвет. Для восстановления брома в смесь добавили 2-3 капли муравьиной кислоты, взбалтывали, содержимое брома испытывали по запаху через 2 минуты.
На бледно-розовый раствор прибавляли несколько крупинки йодистого калия, 2 капли 1%-го раствора крахмали и спустя через 5 минут исследуемый раствор титровали 0,001Н раствором тиосульфата до слабо-розового окрашивания.
Вычисление результатов измерений.
Концентрации йода в воде (мкг/дм3) определяли по формуле:
С=1/6* V*T*дмкг/дм3.
где: V-объем 0,001 Н раствора тиосульфата натрия, см3;
T-титр 0,001 Н раствора йодата, выраженный мкг равный 127:
1/6-количество йода из KClO 3 при титровании (уравнение реакции во введении данной статьи); g — объем исследуемой пробы, дм3 для пробы объемом 1 дм3 концентрация йода вычисляют по формуле:
С=V*21,15 мкг/дм3
Подставляя все данные окончательно получим:
С=0,005*21,15=0,105 мкг/дм3
Таким образом, концентрация йода в ореховой скорлупе составляет 0,105 мкг/дм3.
Выводы
-
1. Основной температурный интервал термического разложения скорлупы грецкого ореха южного региона Кыргызстана в атмосфере воздуха составляет в среднем в интервале температуры 100–350°С. Изучение процессов пиролиза скорлупы грецких орехов в интервале температур 100–550°С показало, что активное формирование структуры происходит при температурах от 300 до 400°С. Выход древесного угля при 550°С составляет 31,4%.
-
2. Максимальная температура скорости разложения скорлупы грецкого ореха находится в интервале температуры от 3540C до 4820C в атмосфере воздуха.
-
3. Зольность получаемого древесного угля из скорлупы грецкого ореха с повышением температуры пиролиза возрастает от 0,53% в исходной скорлупе при 100°С до 1,92% при температуре пиролиза 550°С.
-
4. Концентрация йода в ореховой скорлупе составляет 0,105 мкг/дм3.
Список литературы Определение содержания йода в скорлупе ореха методом пиролиза в интервале температур 100-550°C
- Токторбаева Г. П., Ташполотов Ы. Процессы пиролиза скорлупы Juglans regia L. в интервале температур 250-550°С с получением древесного угля // Бюллетень науки и практики. 2019. Т. 5. №7. С. 135-140. DOI: 10.33619/2414-2948/44/17
- Оболенская А. В., Ельницкая З. П., Леонович А. А. Лабораторные работы по химии древесины и целлюлозы. М.: Экология, 1991. 320 с.
- Определение концентрации химических в воде централизованных систем питьевого водоснабжения. Сборник методических указаний. МУС 4.1.737-99-4.1757-99.
- Унифицированный методы исследования качество вод. методы химического анализы вод-Ч.1-М; 1977- С424.
- ГОСТ 8.513-96. ГСИ. "Методики выполнения измерении".
- Методические указания МУК 4.1.1090-92 "Определение йода в воде".


