Определение термодинамических характеристик реакции получения N-метил-D-глюкозимина
Автор: Михайлов Степан Петрович, Бровко Роман Викторович, Мушинский Лев Сергеевич, Сульман Михаил Геннадьевич
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Химические науки
Статья в выпуске: 11 т.6, 2020 года.
Бесплатный доступ
Представленная статья посвящена термодинамическим расчетам обратимой реакции образования N-метил-D-глюкозимина, промежуточного продукта получения N-метил-D-глюкозамина, широко используемого в фармацевтической практике в качестве балластного вещества или противоиона, улучшающего биодоступность основного лекарственного средства. N-метил-D-глюкозимин синтезируется в результате взаимодействия D-глюкозы с метиламином в среде органических растворителей, реакция является обратимой, а выход целевого продукта всецело зависит от условий проведения реакции. Применение термодинамических расчетов позволяет оценить влияния условий проведения химических процессов на выход целевых продуктов, что в свою очередь способствует более глубокому пониманию механизмов протекания химических реакций. При химическом равновесии прямая и обратная реакции протекают с равными скоростями, а концентрации продуктов и реагентов остаются постоянными. При протекании реакции в замкнутой системе, через определенное время наступает состояние равновесия, при этом реакция не протекает с полной трансформацией реагентов. В представленной статье приводятся результаты термодинамических расчетов реакции синтеза N-метил-D-глюкозимина методом Ван-Кравлена-Черемнова. Рассчитаны энергия Гиббса, константы равновесия и конверсия глюкозы при единичной активности реагирующих веществ. Показано что рост температуры реакционной массы с 20 до 160 °С способствует увеличению конверсии глюкозы с 3 до 32%, в связи с чем можно рекомендовать проведение этой реакции при повышенных температурах.
D-глюкоза, n-метил-d-глюкозимин, основание шиффа, термодинамические расчеты, равновесие, энергия гиббса
Короткий адрес: https://sciup.org/14117692
IDR: 14117692 | УДК: 544.47 | DOI: 10.33619/2414-2948/60/04
N-methyl-D-glucoseimine synthesis reaction thermodynamic properties calculation
The presented article is devoted to thermodynamic calculations of the N-methyl-D-glucosimine reversible formation reaction, an intermediate product for N-methyl-D-glucosamine synthesis, which is widely used in pharmaceutical practice as a ballast or counterion that improves the bioavailability of the main active substance. N-methyl-D-glucosimine is synthesized as a result of the interaction of D-glucose with methylamine in organic solvents, the reaction is reversible, and the yield of the target product depends entirely on the reaction conditions. The use of thermodynamic calculations makes it possible to evaluate the influence of the chemical process conditions on the yield of target products, which in turn contributes to a deeper understanding of the chemical reactions mechanisms. In chemical equilibrium, direct and reverse reactions proceed at equal rates, while the concentrations of products and reagents remain constant. When the reaction proceeds in a closed system, after a certain time, a state of equilibrium occurs, while the reaction does not proceed with a complete transformation of the reagents. This article presents the results of thermodynamic calculations of the reaction for the synthesis of N-methyl-D-glucosimine by the Van Kravlen - Cheremnov method. The Gibbs energy, equilibrium constants, and D-glucose conversion were calculated as activity function of reacting substances. It was shown that an increase in the temperature of the reaction mixture from 20 to 160 °C promotes an increase in the conversion of D-glucose from 3 to 32%, and therefore it is possible to recommend carrying out this reaction at elevated temperatures.
Текст научной статьи Определение термодинамических характеристик реакции получения N-метил-D-глюкозимина
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 544.47
Применение термодинамических расчетов позволяет оценить влияния условий проведения химических процессов на выход целевых продуктов, что в свою очередь способствует более глубокому пониманию механизмов протекания химических реакций. Термодинамика — это наука о физических и химических системах, находящихся в стационарном, нестационарном состояниях при их взаимодействии с окружающей средой [1– 2]. Взаимодействия могут включать обмен теплотой [3], работой и массы между системой и окружающей средой, определяемый граничными условиями [4]. Типичная работа включает в себя воздействие внешних механических [5], электрических и магнитных полей [6]. Первый закон термодинамики описывает эти взаимодействия, утверждая, что чистое изменение энергии окружающей среды должно уравновешиваться противоположным изменением внутренней энергии системы. В то время как второй закон термодинамики управляет эволюцией состояния внутри системы при заданных взаимодействиях между системой и окружающей средой. Второй закон термодинамики заявляет, что любые внутренние процессы, если они происходят спонтанно, то есть необратимо, должны приводить к положительным значениям энтропии. Комбинация первого и второго законов термодинамики была впервые получена Гиббсом и названа им фундаментальным термодинамическим уравнением, которое вдохновило Максвелла на построение модели ее поверхности [1]. Комбинированный закон термодинамики представляет собой интеграцию внешних и внутренних переменных системы и, очевидно, включает как равновесные, так и неравновесные состояния системы [2], хотя Гиббс сосредоточился на применении комбинированного закона к состояниям равновесия в своей работе [1]. Через серию основополагающих публикаций Гиббс [1] разработал основу для равновесия гетерогенных веществ посредством геометрического представления термодинамических свойств, включая связующие линии, треугольники, определение химических потенциалов, а также критерии равновесия и стабильности.
Получение N-метил-D-глюкозимина является первым этапом синтеза N-метил-D-глюкозамина, который широко используется фармацевтической практике в качестве балластного вещества и противоиона, улучшающего биодоступность основного лекарственного средства. N-метил-D-глюкозимин синтезируется в результате взаимодействия D-глюкозы с метиламином в среде органических растворителей, реакция является обратимой, а выход целевого продукта всецело зависит от условий проведения реакции. В представленной статье приводятся результаты термодинамических расчетов реакции синтеза N-метил-D-глюкозимина методом Ван-Кравлена–Черемнова.
Методы исследования
Расчет Δ G т о обр методом Ван-Кравлена–Черемнова
Эмпирический метод расчета ΔGто обр Ван-Кравлена–Черемнова основан на использовании Формулы 1 [7–8],
Δ G т о обр = Σ А+ Σ BT (1)
где Σ А, Σ В — суммы эмпирических коэффициентов групповых составляющих, на которые разбивается данное соединение.
Эмпирические коэффициенты являются справочными и/или вычисляются методами статистической термодинамики.
Для расчета константы равновесия использовался третий закон термодинамики в приложении к обратимым химическим реакциям (2):
Δ G т о обр =-RT×ln(K a ) (2)
где Δ G т о обр — энергия Гиббса для соответствующей реакции, Дж/(моль×К); R — газовая постоянная, 8,314 Дж/(моль×К); T — температура, K; K a — константа равновесия реакции.
В свою очередь константа равновесия реакции может быть использована для вычисления конверсии целевых веществ или продуктов реакции, в соответствии с Формулой 3.
_ а г лю (а)а м еАм (а)
a а г лю (1-а)(а м еАм -а г лю (а))
где а 0лю
—
активность исходного раствора глюкозы, моль/л; а МеАм
—
активность
исходного раствора метиламина, моль/л.
Результаты и обсуждение
Для реакции синтеза N-метил-D-глюкозимина (4) групповые составляющие уравнения Ван-Кравлена–Черемнова приведены в Таблице.
OH C
H COH
HO C H + CH NH
H COH
H COH
CH OH
CH 3
NH C
H COH
HO CH
H COH
H COH
CH OH
+ H 2 O
D-глюкоза метиламин
N-метил-D-глюкозимин
Таблица.
РЕЗУЛЬТАТЫ ВЫЧИСЛЕНИЯ ГРУППОВЫХ КОЭФФИЦИЕНТОВ СОЕДИНЕНИЙ ПО МЕТОДУ ВАН-КРАВЛЕНА–ЧЕРЕМНОВА
|
Группа |
Групповая составляющая |
Рассматриваемое соединение |
||
|
A, ккал/моль |
В×10-2, ккал/моль |
A, ккал/моль |
В×10-2, ккал/моль |
|
|
H 2 O |
||||
|
H 2 O |
-58,076 |
1,154 |
-58,076 |
1,154 |
|
Глюкоза (С 6 H 12 O 6 ) |
||||
|
–CH 2 – |
-5,283 |
2,443 |
-5,283 |
2,443 |
|
–CH– |
-0,756 |
2,942 |
-3,024 |
11,768 |
|
–C=OH |
-29,16 |
0,663 |
-29,16 |
0,663 |
|
–ОН |
-42,959 |
1,134 |
-42,959 |
1,134 |
|
(первичная) |
||||
|
–ОН |
-44,538 |
1,18 |
-178,152 |
4,72 |
|
(вторичная) |
||||
|
ИТОГО |
-258,578 |
20,728 |
||
|
Метиламин (СН 3 NH 2 ) |
||||
|
–CH 3 |
-10,833 |
2,176 |
-10,833 |
2,176 |
|
–NH 2 |
2,82 |
2,71 |
2,82 |
2,71 |
|
ИТОГО |
-8,013 |
4,886 |
||
|
N-метил-D-глюкозимин (С 7 Н 15 N) |
||||
|
–CH 2 – |
-5,283 |
2,443 |
-5,283 |
2,443 |
|
–CH– | |
-0,756 |
2,942 |
-3,024 |
11,768 |
|
–N=C– | |
46,32 |
-0,89 |
46,32 |
-0,89 |
|
–ОН |
-42,959 |
1,134 |
-42,959 |
1,134 |
|
(первичная) |
||||
|
–ОН |
-44,538 |
1,18 |
-178,152 |
4,72 |
|
(вторичная) |
||||
|
–CH 3 |
-10,833 |
2,176 |
-10,833 |
2,176 |
|
ИТОГО |
-193,931 |
21,351 |
||
С учетом общего вида уравнения Ван-Кравлена–Черемнова (1) и реакции получения N-метил-D-глюкозимина (2), Δ G т о реакции может быть выражено Формулой 5.
о реакции= 2А Сп°Родр — = 2А С И'сХбр- = 14,585—3,109х10 -2 Т
Графическая зависимость Δ G т о реакции от температуры в диапазоне температур 20– 150 °С приведены на Рисунке 1.
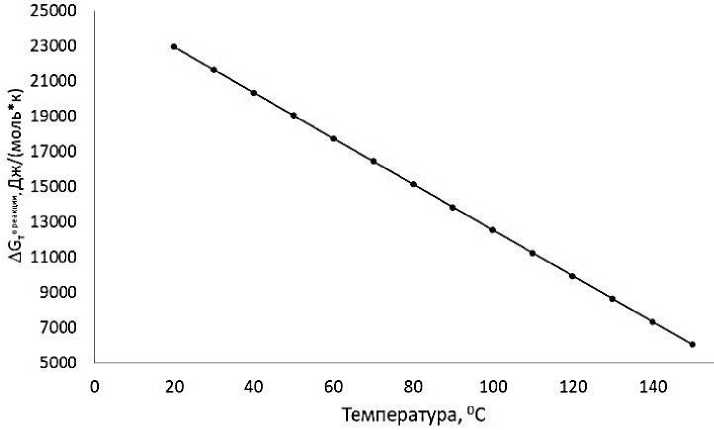
Рисунок 1. Зависимость энергии Гиббса от температуры для реакции получения N-метил-D-глюкозимина.
Необходимо отметить, что энергия Гиббса реакции находится в положительной области, что позволяет судить о смещении равновесия процесса влево. Однако, тенденция уменьшения энергии Гиббса при увеличении температуры с 20 до 160 °С, с 23 кДж/(моль×к) до 6 кДж/(моль×л) показывает на возможность смещения равновесия реакции вправо при более высокой температуре. Рассчитанные по Формуле 2 константы равновесия были сведены график (Рисунок 2) зависимости константы равновесия от температуры. При этом увеличение реакционной температуры от 20 до 160 °С способствует увеличению константы равновесия реакции образования N-метил-D-глюкозимина с 0,001 до 0,18.
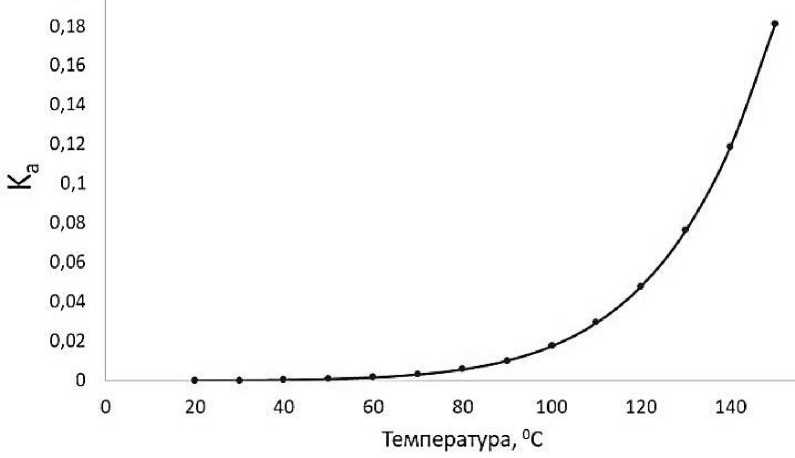
Рисунок 2. Зависимость константы равновесия от температуры для реакции получения N-метил-D-глюкозимина.
В случае единичных значений начальных активностей D-глюкозы и метиламина возможно провести оценку конверсии реагентов (Рисунок 3). При этом рост температуры реакционной массы с 20 до 160 °С способствует увеличению конверсии глюкозы с 3 до 32%, в связи с чем можно рекомендовать проведение этой реакции при повышенных температурах.
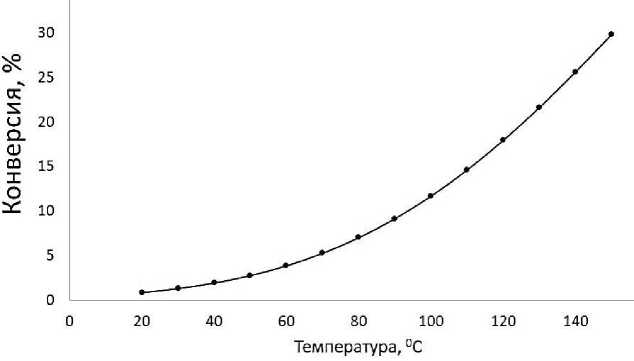
Рисунок 3. Зависимость равновесной конверсии от температуры для реакции получения N-метил-D-глюкозимина при единичных начальных активностях реагирующих веществ.
Заключение
N-метил-D-глюкозимин является промежуточным продуктом получения N-метил-D-глюкозамина, широко используемого химического соединения в фармацевтической практике в качестве балластного вещества или противоиона, улучшающего биодоступность основного лекарственного средства. Проведенные термодинамические расчеты реакции синтеза N-метил-D-глюкозимина методом Ван-Кравлена–Черемнова позволили получить значения энергии Гиббса, константы равновесия и конверсии исходных соединений при единичной активности реагирующих веществ. Показано что рост температуры реакционной массы с 20 до 160 °С способствует увеличению конверсии глюкозы с 3% до 32%, в связи с чем можно рекомендовать проведение этой реакции при повышенных температурах.
Исследование выполнено в рамках проекта РФФИ 18-08-00489.
Список литературы Определение термодинамических характеристик реакции получения N-метил-D-глюкозимина
- Gibbs J. W. The collected works of J. Willard Gibbs (№536.7092). Yale Univ. Press, 1948.
- Hillert M. Phase equilibria, phase diagrams and phase transformations: their thermodynamic basis. Cambridge University Press, 2007. DOI: 10.1017/cbo9780511812781
- Prigogine I. Introduction to Thermodynamics of Irreversible Processes. New York, London: Interscience Publ. Inc., 1961.
- De Groot S. R., De Groot S. R. Thermodynamics of irreversible processes. Amsterdam: North-Holland, 1951. V. 336.
- Müller I., Ruggeri T. Rational extended thermodynamics. Springer Science & Business Media, 2013. V. 37.
- Jou D., Casas-Vázquez J., Lebon G. Extended Irreversible Thermodynamics. New York: Springer, 2010.
- Liu Z. K., Wang Y. Computational thermodynamics of materials. Cambridge University Press, 2016.
- Liu Z. K., Li B., Lin H. Multiscale entropy and its implications to critical phenomena, emergent behaviors, and information // Journal of Phase Equilibria and Diffusion. 2019. V. 40. №4. P. 508-521. DOI: 10.1007/s11669-019-00736-w


