Определение типа фазового перехода раствора полупроводника при переходе из жидкого состояния в парообразное
Автор: Ярижева М.А.
Журнал: Теория и практика современной науки @modern-j
Рубрика: Физика и астрономия
Статья в выпуске: 6 (108), 2024 года.
Бесплатный доступ
В данной работе говорится о фазовом переходе раствора полупроводника при переходе их жидкого состояние в парообразное
Фазовый переход, фреон-13, жидкость, полупроводник
Короткий адрес: https://sciup.org/140306487
IDR: 140306487
Determination of the type of phase transition of a semiconductor solution during the transition from a liquid state to a vapor state
This paper discusses the phase transition of a semiconductor solution during the transition of their liquid state to a vaporous one
Текст научной статьи Определение типа фазового перехода раствора полупроводника при переходе из жидкого состояния в парообразное
При уменьшении температуры и увеличении давления вещества испытывают скачкообразные изменения агрегатного состояния, переходя из газообразного состояния в жидкое, а затем из жидкого в твердое. При изменении температуры и давления в противоположном направлении происходит обратный переход: из твердого состояния в жидкое и газообразное. С этими переходами связано поглощение или выделение определенного количества теплоты – скрытой теплоты перехода.
Фазовые переходы с поглощением и выделением теплоты и изменением объема называются переходами первого рода. Помимо этих превращений в природе встречаются переходы, при которых теплота не поглощается и не выделяется и не изменяется объем. Такие переходы проявляются в скачкообразном изменении теплоемкостей и других производных термодинамических параметров. К ним относится изменение симметрии кристаллической решетки, происходящее без изменения плотности и энергии решетки.
Примером фазового перехода второго рода может служить превращение железа, никеля и других металлов и магнитных сплавов из ферромагнитного состояния в парамагнитное.
С точки зрения термодинамики системой (термодинамической системой) называется любое макроскопическое тело, т. е. тело, состоящее из огромного количества микрочастиц (молекул, атомов и т. п.) и находящееся в равновесном или близком к равновесному состоянии. Термодинамическая система, в свою очередь, может состоять из одной, двух или нескольких фаз. Фазой называется физически однородная часть системы, отличающаяся от других ее частей физическими свойствами и отделенная от них четко выраженными границами. Примерами двухфазных систем могут служить жидкость и ее насыщенный пар, жидкость и кристалл, находящиеся в соприкосновении друг с другом.
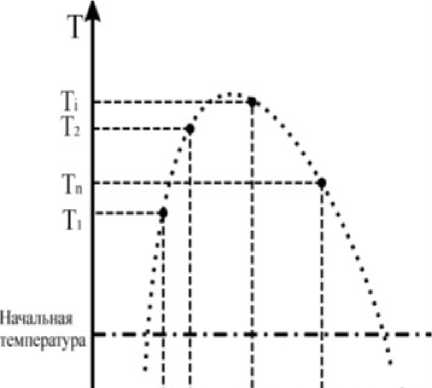
Метод определения линии равновесия «жидкость – пар» в TV-плоскости по исчезновению мениска поясняет рис. 1.
Имеется набор герметичных ампул с исследуемым веществом. Количества вещества в ампулах различные, однако, во всех случаях средний удельный объем v i = V i /M i (M i – масса вещества в i-й ампуле, V i – объем i-й ампулы) таков, что при начальной температуре опыта вещество находится в двухфазном состоянии: в ампуле находятся в равновесии жидкость и ее насыщенный пар, отделенные друг от друга резкой видимой границей, называемой мениском.
При нагреве, как видно на рис. 1 и исходя правила рычага, количество жидкой фазы в ампулах, где средний удельный объем меньше критического удельного объема, будет увеличиваться (мениск будет двигаться вверх). В тех ампулах, где средний удельный объем больше критического, будет увеличиваться количество газообразной фазы (мениск будет двигаться вниз). Удельный объем v i (заранее заданный) и температура, при которой мениск достигнет верха или низа i-й ампулы, т. е. вещество перейдет в однофазное (жидкое или газообразное) состояние, определяют, очевидно, координаты одной точки (v i , T i ) на линии фазового равновесия в TV-плоскости. Если нанести эти точки на TV-диаграмму и провести через них аппроксимирующую кривую, то мы восстановим линию равновесия «жидкость – пар». По координатам купола кривой определяются критическая температура и критический удельный объем.
Экспериментальная установка для определения кривой равновесия «жидкость – пар» методом исчезновения мениска изображена на рис. 9. Установка состоит из сосуда, помещенного в защитный кожух с прозрачными стенками, в котором подвешены ампулы с исследуемым веществом (Фреон-13). В сосуд подается из термостата вода определенной температуры. Температура воды меняется от комнатной до 29,5 oC. При достижении температуры 29,5 oC нагреватель термостата автоматически отключается.
J—I►
Рис. 1. Определение кривой равновесия «жидкость – пар» в Tv-плоскости методом
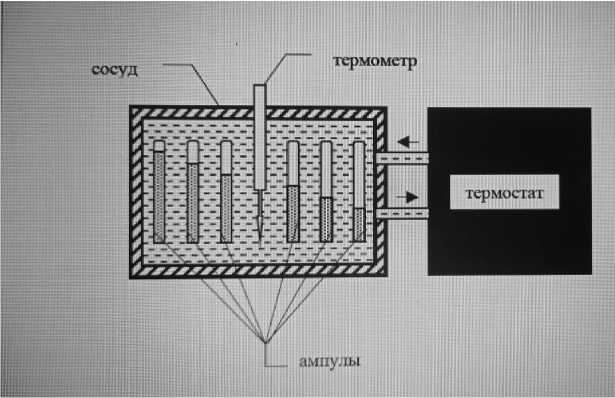
Рис. 9. Схема установки
Для определения кривой равновесия «жидкость – пар» методом исчезновения мениска, провели нагрев ампул от комнатной температуры до 29,5 oС. Нагрев в диапазоне температур 27,5 oС – 29,5 oС проводили со скоростью не выше 0,1 К/мин. Для этой цели нагреватель термостата должен быть включен на минимальную мощность, при необходимости скорость нагрева может быть дополнительно замедлена путем подачи воды из водопровода (с небольшим расходом) в систему охлаждения термостата. В процессе нагрева зафиксировали, в какую сторону перемещается мениск в каждой из ампул. Обратить внимание, не происходит ли в некоторых ампулах размытия мениска и помутнения вещества (критическая опалесценция!). Определили температуры исчезновения менисков. Измерили скорость нагрева.
После выключения нагревателя термостата в процессе остывания зафиксировали температуры, при которых появляются мениски в ампулах. Скорость остывания также не должна превышать 0,1 К/мин. (она регулируется изменением расхода водопроводной воды в системе охлаждения термостата). Измерили скорость охлаждения.
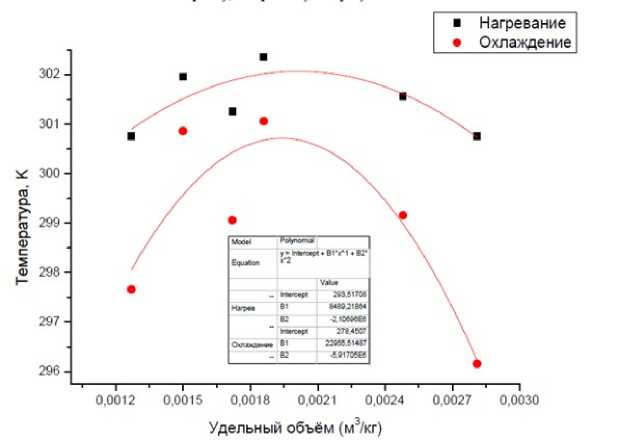
В результате измерений были получены данные, представленные в таблице 1 .
Поданным таблицы 1 построили TV-диаграмму (рисунок ). Провели через них аппроксимирующие кривые (линия равновесия «жидкость – пар») отдельно для нагрева и охлаждения. Определили координаты критической точки (V С и T С ).
Список литературы Определение типа фазового перехода раствора полупроводника при переходе из жидкого состояния в парообразное
- Румер Ю. Б., Рывкин М. Ш. Термодинамика, статистическая физика и кинетика. М.: Наука, 1972.
- Ландау Л. Д., Лифшиц Е. М. Статистическая физика. М.: Наука, 1964.
- Федотов Я.А. Основы физики полупроводниковых конструирования и технологии РЭА и ЭВА. - М.: Советское радио, 2009.
- Глазов В.М., Павлова Л.М. Химическая термодинамика и фазовые превращения. М.: Металлургия, 1981, - 336 с.


