Оптимизация диализа гуминовых кислот
Автор: Аввакумова Н.П., Глубокова М.Н., Жданова А.В., Кривопалова М.А., Катунина Е.Е., Кириллова В.Я.
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Средства коррекции экологического неблагополучия
Статья в выпуске: 1-6 т.11, 2009 года.
Бесплатный доступ
Разработка новых лекарственных препаратов на основе гуминовых кислот, выделенных из низкоминерализованных иловых сульфидных грязей, обуславливает необходимость биохимического изучения субстанции, и, в том числе, определения биологической доступности. В модельных системах определены оптимальные условия диализа гуминовых кислот через биологическую мембрану. Коэффициент проницаемости гуминовых кислот возрастает с уменьшением кислотности и концентрации растворов, а также с введением трансагентов типа диметилсульфоксида и некоторых катионов металлов.
Гуминовые кислоты, биологическая мембрана, биологическая доступность
Короткий адрес: https://sciup.org/148198483
IDR: 148198483 | УДК: 577.171.54:615.243.3
Optimization of humic acids dialysis
Development of new medical products on the basis of humic acids allocated from low mineralized sludge sulphidic dirts, causes necessity of biochemical studying the substance, and, also, definitions of biological availability. In modelling systems optimum conditions of humic acids dialysis through biological mem-brane are certain. The factor of humic acids permeability increases with reduction of acidity and concen-tration of solutions, and also with introduction transagents of dimethylsulfoxide type and some metal cations.
Текст научной статьи Оптимизация диализа гуминовых кислот
К гуминовым веществам относятся специфические темноокрашенные, азотсодержащие высокомолекулярные соединения кислотной природы, содержание которых в биосистемах составляет 45-90% [1]. Они характеризуются неоднородностью, полидисперсностью и представлены большим набором сходных по строению, но неидентичных молекул. В зависимости о условий формирования гуминовые вещества биосферы подразделяются на почвенные и донные. Общепринятая классификация компонентов гуминовых веществ основана на различной растворимости в кислотах и щелочах [2].
Гуминовые кислоты - наиболее обширная, термодинамически устойчивая группа гуминовых веществ. Они извлекаются щелочами. Образуя растворы темно-бурого цвета, и выпадают в осадок при подкислении до рН=1-2. Гуминовые кислоты по своей химической структуре являются нерегулярными сополимерами ароматических гидрооксиполикарбоновых кислот с включениями азотсодержащих и углеводных фрагментов. Ароматический углеродный скелет содержит фенольные гидроксогруппы, хиноидные структуры, бензольные кольца, связанные мостиками через азот и кислород, карбоксильные группы. Для гуминовых кислот характерна нестехиометрич-ность состава, нерегулярность строения, гетерогенность структурных фрагментов и полидисперсность. Для них неприменимо понятие молекулы и более адекватно употребление понятия молекулярный ансамбль, в котором шестичленные кольца представлены в основном трех- и
Кириллова Валентина Яковлевна, кандидат биологических наук, старший преподаватель четырехзамещенными структурами и соединены мостиками с кратными связями. Построенная из таких фрагментов молекула должна иметь вытянутую форму и обладать определенной гибкостью. Предпочтительной в настоящее время является модель так называемого стохастического клубка. Считается, что такая конформация характерна для молекул, имеющих неупорядоченность в структуре, не обладающих большим числом внутримолекулярных связей и не способных принимать жесткие формы. Для стохастического клубка характерно непостоянство формы, он все время изгибается и закручивается, в определенных условиях принимая то приближающуюся к сферической, то более вытянутую конформацию. Последняя зависит от многих факторов, среди которых важнейшими являются рН, ионная сила, тип противоиона, концентрация гуминовых веществ [5]. С увеличением рН молекулы стремятся принять вытянутую конформацию, так как возрастает степень ионизации кислотных групп гуминовых веществ и их взаимное отталкивание. Ионная сила раствора определяет условный размер молекулы, которая с увеличением числа ионов в растворе сжимается. Определяющее значение для формы макромолекулы имеет также тип противоионов. Если они представлены легкодис-социирующими катионами (Li+, Na+, K+), то молекула все еще может быть сильно вытянута. Если присутствуют двухвалентные ионы или водород, то макромолекула будет вытянута в меньшей степени [3, 4]. Гуминовые кислоты являются преобладающим биологически активным компонентом низкоминерализованных иловых сульфидных грязей и перспективны для получения новых высокоэффективных пелоидопрепара-тов [5, 6].
Вышеизложенные особенности строения гуминовых кислот, с одной стороны, и актуализация таких проблем природопользования, как уменьшение запасов нативных лечебных грязей, сложность их утилизации и регенерации определили цель данного исследования: изучение способности гуминовых кислот диализировать через биологическую мембрану животного происхождения (фрагмент кишечной стенки быка). Выяснение биологической доступности препаратов гуминовых кислот, осуществлялось по следую- щей методике: растворы гуминовых кислот одинакового объема (2 мл) и различной концентрации помещали в диализатор, который погружали в стаканчик для диализата, содержащий 10 мл воды очищенной (оптимальные объемы определили опытным путем). Через 1 час определяли оптическую плотность диализата на приборе ФЭК-56М при длине волны 400 нм, в кюветах толщиной 5 мм. Содержание гуминовых кислот определяли по предварительно полученному калибровочному графику. В результате проделанного эксперимента была установлена линейная зависимость проницаемости гуминовых кислот от исходной концентрации раствора в интервале концентраций от 0,01 до 1%(масс.) (рис. 1).
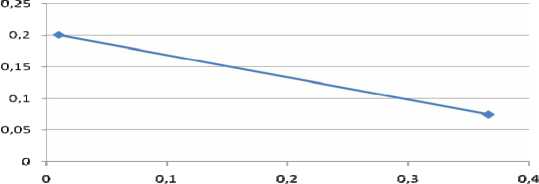
w,%
Рис. 1. Зависимость оптической плотности растворов диализата от концентрации гуминовых кислот
По полученным результатам был рассчитан коэффициент проницаемости е гуминовых кислот по формуле:
6=W(диал.) 100%. W (исх.) • где W(диал.)- концентрация гуминовых кислот в диализате (%масс.); W(исх.)- концентрация исходного раствора гуминовых кислот (%масс.). При физиологическом значении рН раствора коэффициент проницаемости составил около 20%.
С целью определения влияния уровня рН на значение коэффициента проницаемости нами по приведенной выше методике исследовались растворы гуминовых кислот с кислотностью растворов 6,0; 7,4; 8,0.
Таблица. Зависимость оптической плотности (Д) раствора гуминовых кислот от рН раствора
|
рН |
Д |
£ |
|
6 |
0,27 |
19,5 |
|
7,4 |
0,3 |
20,5 |
|
8 |
0,38 |
20,8 |
Как видно из представленных данных, кислотность растворов незначительно влияет на проницаемость гуминовых кислот через биологическую мембрану, хотя прослеживается тенденция увеличения коэффициента проницаемости с ростом значений рН.
Влияние катионов на диализ гуминовых кислот осуществляли на примере ионов серебра. Для этого 0,1%(масс.) раствор субстанции модифицировали добавлением 0,5 мл 0,02моль-экв/л раствора нитрата серебра. Как видно (рис. 2), диализ гумата серебра интенсивнее диализа гуминовых кислот в 1,25 раза. Диализ осуществляли в присутствии трансагента диметилсульфоксида (ДМСО) в концентрациях 1,0; 5,0; и 10%масс. Как свидетельствуют результаты фото- метрирования диметилсульфоксид увеличивает проницаемость пелоидопрепаратов через биологические мембраны. Для гуминовых кислот и гумата серебра оптимальной является 10%-ная концентрация ДМСО, при которой наблюдается максимальный выход пелоидопрепаратов и увеличение проницаемости в 1.5 раза (рис. 2).
В результате эксперимента нами был установлен характер зависимости прохождения гуминовых кислот и их комплексов с ионами серебра через биомембрану в водную среду в зависимости от различных факторов. Слабощелочная среда способствует увеличению ионногенных групп с отрицательным зарядом на поверхности макромолекул гуминовых кислот, что, по-видимому, сопровождается усилением электростатического отталкивания отдельных фрагментов молекулы. Возможно, происходит нарушение надструктур стохастического клубка, приводящее к изменению пространственной формы молекул. Катионы серебра, являясь мягкими кислотами Льюиса, увеличивают способность гуминовых кислот к диализу через животную мембрану в 1,3 раза (на 29%). Диметилсульфоксид обладает способностью проникать через биологические мембраны, в том числе, через кожные барьеры и слизистые оболочки, без повреждения последних, способствуя переносу лекарственных веществ. Добавление в раствор гуминовых кислот диметилсульфоксида усиливает диализационную способность субстанции прямо пропорционально. В 10%-ом растворе диметилсульфоксида проницаемость гуминовых кислот возрастает в 1,6 раза. Диализационная способность гумата серебра в таком же растворе диметилсульфоксида увеличивается в 2 раза.
Выводы: полученные результаты свидетельствуют как о принципиальной возможности проникновения гуминовых кислот и их комплексов с ионами серебра через биологические мембраны, так и о зависимости биологической доступности указанных веществ от кислотности, ионной силы раствора и присутствия трансагентов.
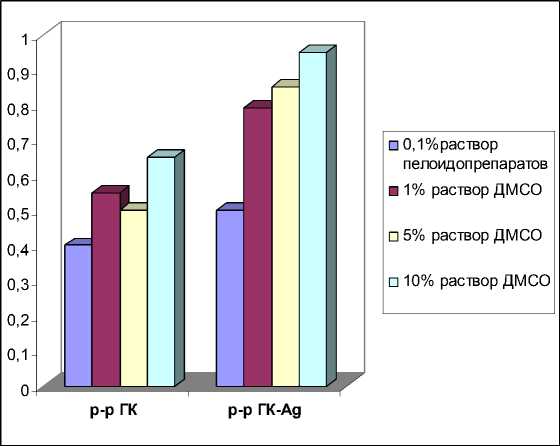
Рис. 2. Зависимость оптической плотности диализатов растворов гуминовых кислот и гумата серебра от концентрации диметилсульфоксида.
Список литературы Оптимизация диализа гуминовых кислот
- Орлов, Д.С. Гуминовые вещества в биосфере/Д.С.Орлов. -М.,1993. -238 с.
- Орлов, Д.С. Гуминовые вещества в биосфере/Д.С. Орлов//Соросовский образовательный журнал. -М., 1997. -№ 2. -С. 56-63.
- Лодыгин, Е.Д. Изучение молекулярной структуры гумусовых кислот подзолистых и болотно-подзолистых почв методом 13 С-ЯМР спектроскопии/Е.Д. Лодыгин, В.А. Безносиков//Почвоведение. -2003.-№ 9. -С. 1085-1094.
- Лодыгин, Е.Д. Изучение молекулярно-массового распределения гумусовых веществ подзолистых почв методом гель-хроматографии/Е.Д. Лодыгин, В.А. Безносиков//Гуминовые вещества в биосфере: тезисы III Всероссийской конференции. -СПб., 2005. -С. 73-74.
- Аввакумова, Н.П. Биохимические аспекты терапевтической эффективности гумусовых кислот лечебных грязей/Н.П. Аввакумова. -Самара: ГП «Перспектива»; СамГМУ, 2002. -124 с.
- Аввакумова, Н.П. Противовоспалительная активность препаратов в ряду гумусовых кислот низкоминерализованных иловых сульфидных грязей/Н.П. Аввакумова и др.//International journal on immunorehabilitation. -2002. -V. 4, № 1. -P. 190-191.


