Опыт гастропанкреатодуоденальной резекции с циркулярной резекцией магистральных венозных сосудов
Автор: Орелкин В.И., Тонеев Е.А., Жинов А.В., Городнов С.В., Аброськин Б.В., Орлкина Ю.Д.
Журнал: Хирургическая практика @spractice
Рубрика: Статьи
Статья в выпуске: 4 (44), 2020 года.
Бесплатный доступ
Цель работы - представить результаты лечения пациентов с злокачественными заболеванием поджелудочной железы.Материал и методы исследования. Представлено собственное клиническое наблюдение хирургического лечения злокачественных новообразований головки поджелудочной железы с инвазией в магистральные венозные сосуды. За 2019 год на базе 1 хирургического отделения ГУЗ Областного клинического онкологического диспансера 2 пациентам были выполнены гастропанкреатодуоденальные резекции с циркулярной резекцией воротной вены и ангиопластикой по типу «конец в конец».Результаты исследования и их обсуждение. Инвазия опухоли в магистральные венозные сосуды не является противопоказанием к выполнению радикального оперативного вмешательства и достижима при выполнении гастропанкреатодуоденальной резекции, за счет резекций магистральных венозных сосудов вместе с инвазирующей в ее стенку опухолью.Выводы. Резекция воротной вены вместе с инвазирующей в ее стенку опухолью головки поджелудочной железы способствует достижению радикальности операции при выполнении гастропанкреатодуоденальной резекции.
Рак головки поджелудочной железы, воротная вена, резекция магистральных венозных сосудов, гастропанкреатодуоденальная резекция, хирургическое лечение
Короткий адрес: https://sciup.org/142229642
IDR: 142229642 | УДК: 617-089.844 | DOI: 10.38181/2223-2427-2020-4-40-47
Experience of gastropancreatoduodenal resection with circular resection of major venous vessels
Purpose of work. Improve patient outcomes in patients with pancreatic cancer.Material and methods of research. We present our own clinical observation of surgical treatment of malignant neoplasms of the head of the pancreas with invasion of the main venous vessels. In 2019, on the basis of 1 surgical Department of the GUZ Regional clinical oncological dispensary, 2 patients underwent gastropancreatoduodenal resections with circular portal vein resection and end-to-end angioplasty.The results of the study and their discussion. Tumor invasion into the main venous vessels is not a contraindication to performing radical surgery and is achievable when performing gastropancreatoduodenal resection, due to resections of the main venous vessels together with the tumor invading its wall.Conclusions. Resection of the portal vein together with the pancreatic head tumor invading its wall contributes to the achievement of radical surgery when performing gastropancreatoduodenal resection.
Текст научной статьи Опыт гастропанкреатодуоденальной резекции с циркулярной резекцией магистральных венозных сосудов
Рак поджелудочной железы представляет в настоящее время серьезную медико-социальную проблему. По данным GLOBOCAN 2018 года 70-80% пациентов встречаются с запущенными стадиями,при которых проведение радикального хирургического вмешательство невозможно [1]. Наиболее частой гистологической структурой является протоковая аденокарцинома, характеризующаяся агрессивным ростом и склонностью к раннему метастазированию [2]. Классическим видом хирургии при злокачественных новообразованиях в области головки и перешейка поджелудочной железы является выполнение гастропанкреатодуоденальной резекции (ГПДР ,операция Wiplle) [3]. Значимым направлением в хирургии поджелудочной железы является совершенствование методов лечения рака поджелудочной железы и расширение показаний для хирургического вмешательства. Непосредственный контакт поджелудочной железы с портальной веной и ее прито-ками,а также с нижней полой веной предрасполагают к изначальной распространенности процесса, даже при незначительных размерах опухоли [4]. Одной из главных проблем при выполнении гастропанкреатодуоде-нальной резекции является инвазия опухоли, чаще всего, в магистральные венозные сосуды. После инструментальной и интраоперационной констатации инвазии опухоли в магистральные венозные сосуды (чаще всего портальную и верхнюю брыжеечную вены) принимается решение о резекции данных кровеносных сосудов. Исходя из протяженности инвазии, каждый хирург может воспользоваться несколькими способами: циркулярная резекция венозных сосудов с пересечением их в нескомпрометированной части,краевая резекция пораженного кровеносного сосуда. Восстановление резецированного участка определяется возможностями сосудистой стенки, опять же имеются несколько способов: ангиопластика «конец в конец» или протезирование сосуда в функциональном отношении.
Материалы и методы
С целью исключения отдаленного распространенного процесса пациентам в качестве первого этапа было выполнено оперативное вмешательство в объеме: диагностическая лапароскопия,с биопсией париетальной брюшины. В последующем, исходя из визуального осмотра в ходе оперативного вмешательства, данных цитологического и гистологического анализа биоптатов и лабораторно-инструментальных исследований исключалось отдаленное распространение опухоли.На мультидисциплинарном консилиуме врачей ГУЗ ОКОД с участием химиотерапевта, радиолога и хирурга определилась тактика лечения в пользу хирургического вмешательства на первом этапе: ГПДР головки поджелудочной железы с циркулярной резекцией воротной вены и ангиопластикой по типу «конец в конец».
Результаты
и кассеты 60 мм. Затем произведена холецистэктомия с лигированием питающих кровеносных сосудов. Выделен и пересечен общий печеночный проток выше впадения пузырного протока. На расстоянии 20-25 сантиметров от связки Трейтца пересечена тощая кишки с помощью линейного двухрядного аппарата УО, использованы 2 кас-
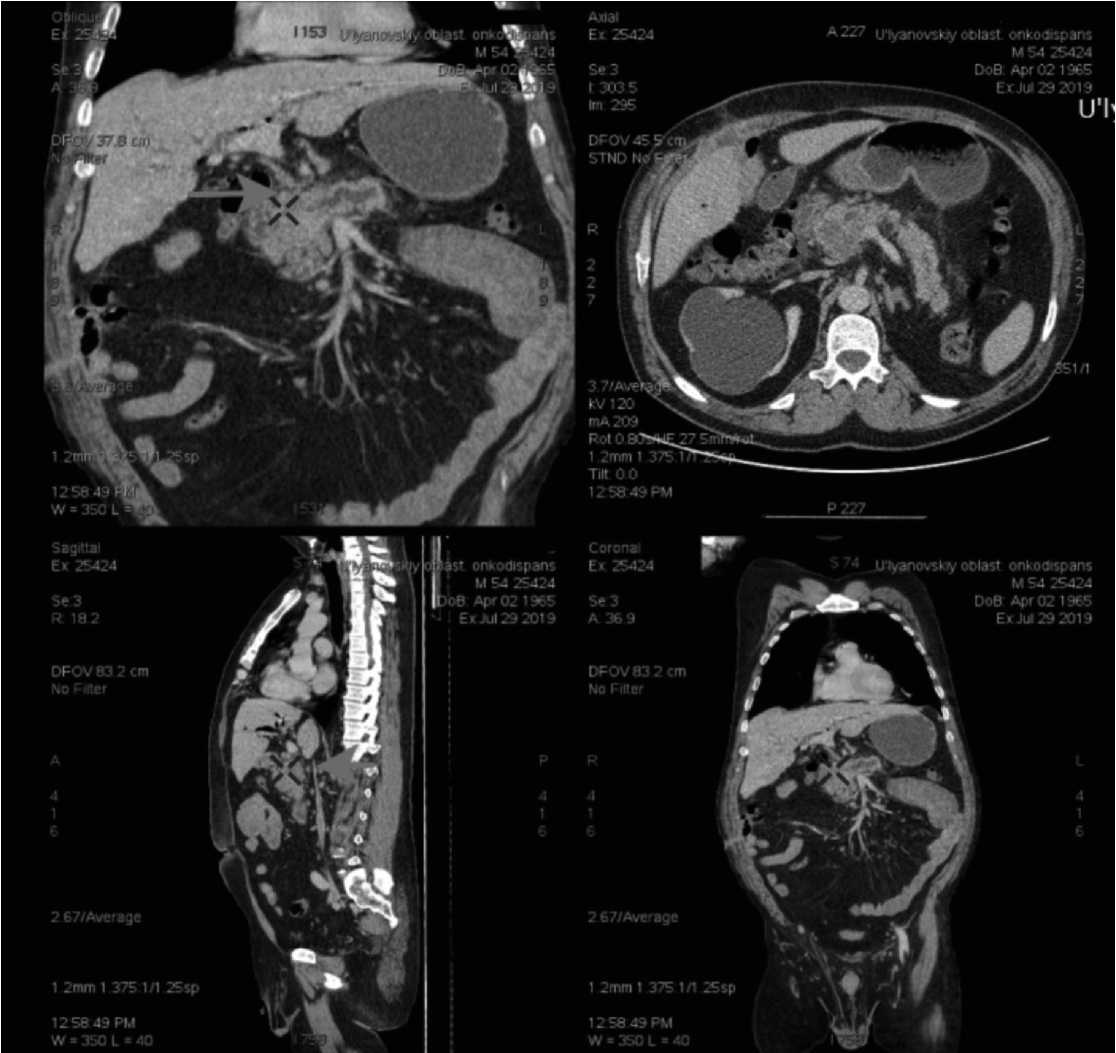
Рис.1. МСКТ-грамма гепатобилиарной системы: 1 – опухоль головки поджелудочной железы; 2 – место инвазии опухоли в магистральные сосудистые структуры (воротная вена).
Fig. 1. MSCT gram of the hepatobiliary system: 1 - pancreatic head tumor; 2 - the site of tumor invasion into the main vascular structures (portal vein).
сеты 40 милиметров. Брыжейка проксимальной части тощей кишки и дуоденоеюнального изгиба лигирована и пересечена. Выполнена перевязка верхней и нижней панкреатодуоденальных артерий и вен. После мобилизации головки поджелудочной железы констатирована инвазия опухоли в портальную вену на протяжении 1 см. Ворот- ная вена взята на сосудистые зажимы дистальнее и про-ксимальннее места инвазии. (рис. 2).
Осуществлена циркулярная резекция участка воротной вены, в просвет кровеносного сосуда для предупреждения свертывания крови введен разведенный раствор гепарина с физиологическим раствором 0,9 %
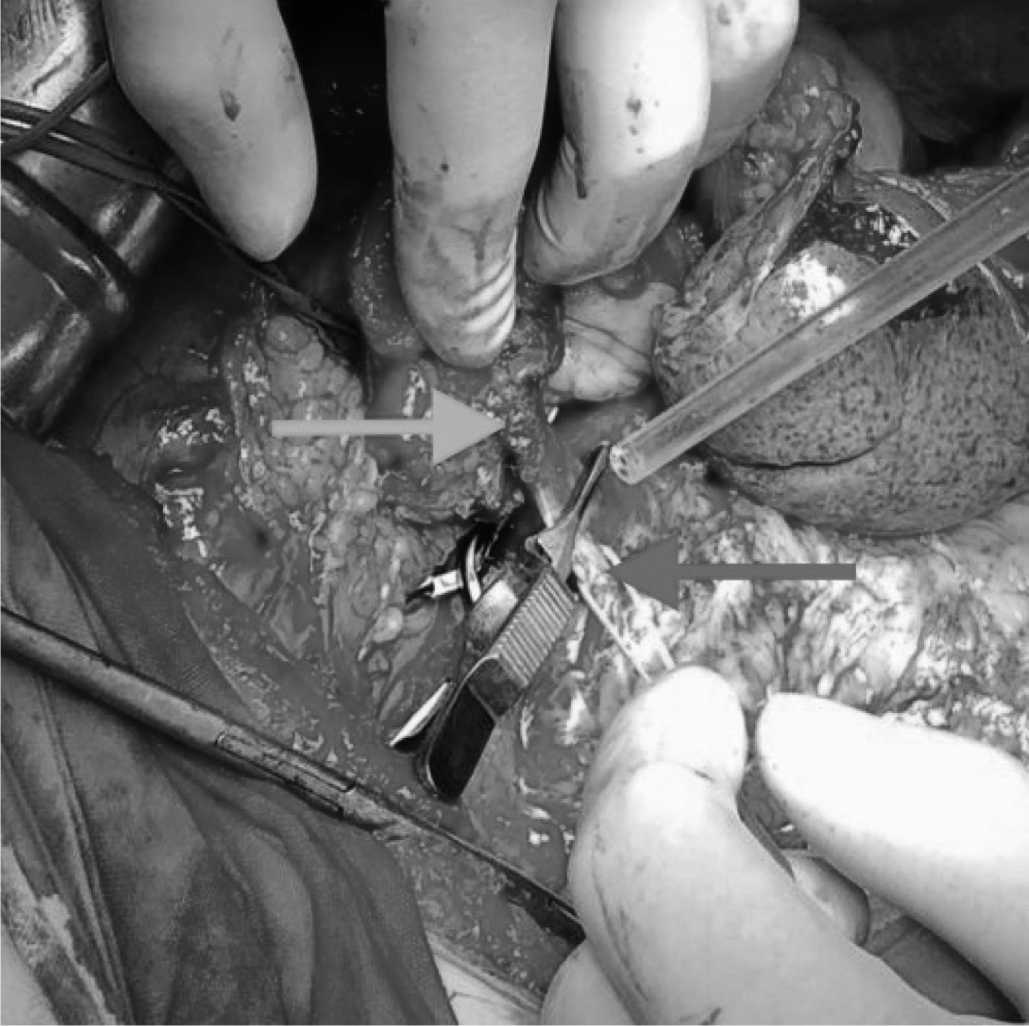
Рис. 2. Наложение сосудистых зажимом на воротную вену проксимальннее и дистальнее места инвазии опухоли: зеленная стрелка – место инвазии опухоли в воротную вену, синяя стрелка – воротная вена
Fig. 2. TApplying a vascular clamp to the portal vein proximal and distal to the site of tumor invasion: green arrow - site of tumor invasion into the portal vein, blue arrow - portal vein
Наложен циркулярный сосудистый шов, соединяющий проксимальный и дистальный участок портальной вены по типу «конец в конец». Среднее время пережатия портальной вены в обоих случаях составляло 13 минут. (рис. 4).
В последующем констатирован удовлетворительный кровоток по вене и диаметр наложенного анастомоза. В двух проведенных операциях были сформированы пан-креатоеюноаностомозы, двухрядным инвагинацион-
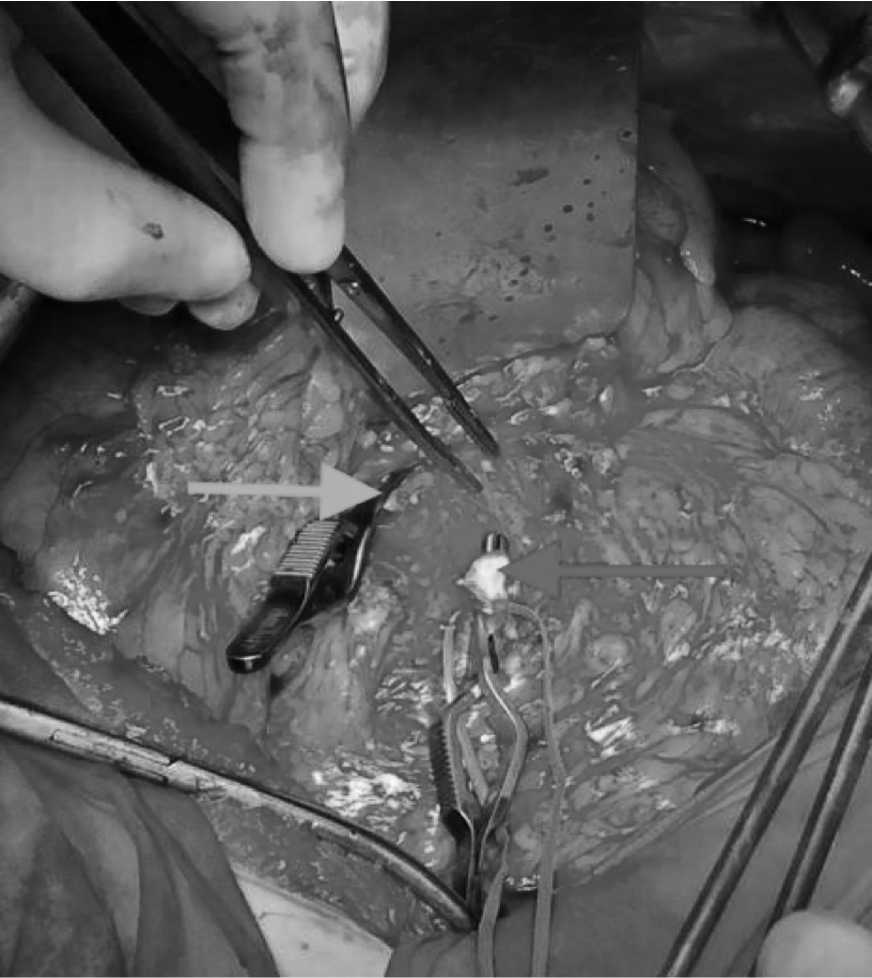
Рис. 3. Циркулярное пересечение воротной вены: зеленная стрелка – дистальный конец, синяя стрелка – проксимальный конец.
Fig. 3. Circular transection of the portal vein: green arrow, distal end, blue arrow, proximal end.
ным швом (дуктомукозанастомоз) "конец в бок". Также наложены гепатикоеюноаностомозы в среднем на расстоянии 8 см дистальнее. Гастроэнтероаностомоз сформирован у обоих пациентов в среднем на расстоянии 40 сантиметров дистальнее гепатикоеюноаностомоза с использованием линейного аппаратного шва GIA (Medtronic) 60 мм. Время ГПДР резекций составило 310 и 340 минут соответственно, что превышало время стандартных ГПДР резекций (среднее время выполнения стандартной ГПДР 240-260 минут). Увеличение времени операции объяснялось выполнением циркулярной резекции воротной вены с наложением сосудистого шва.
В результате планового гистологического заключения в обоих случаях выявлена высокодифференцированная (протоковая) аденокарцинома поджелудочной железы, в лимфоузлах (16 шт.) без метастазов. При микроскопическом исследовании выявлена инфильтрация опухолью стенки воротной вены.Линия резек-
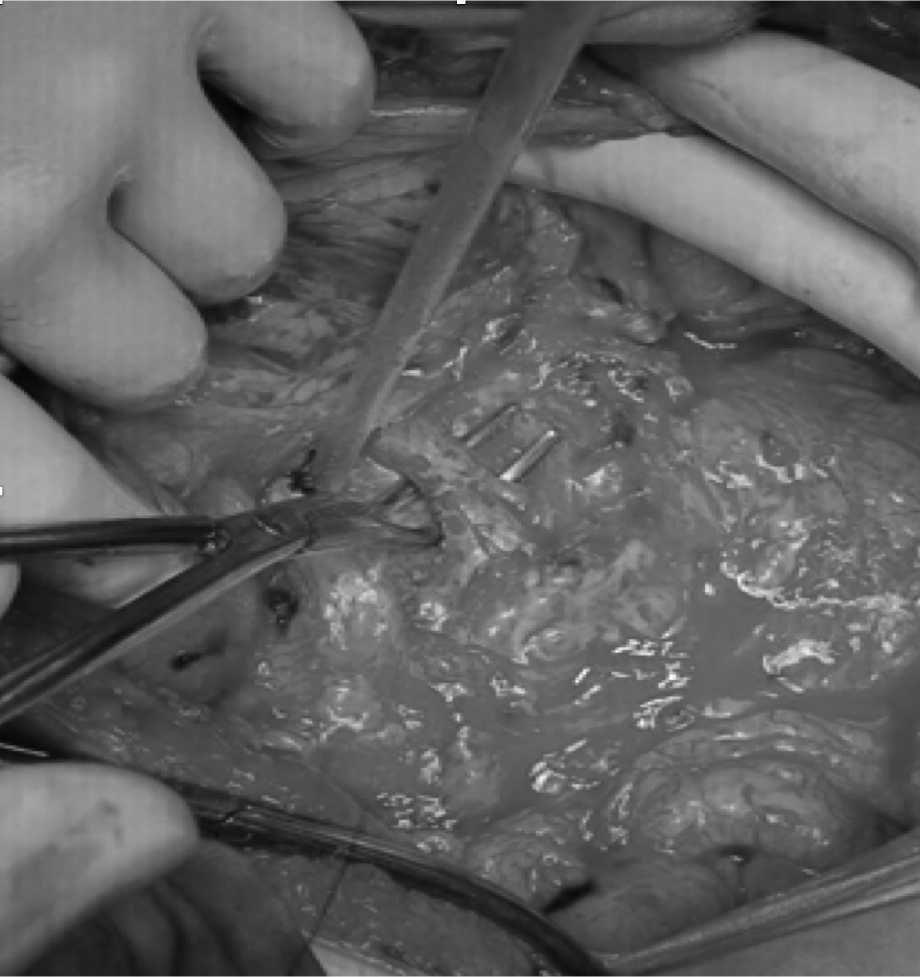
Рис. 4. Циркулярный сосудистый шов, соединяющий проксимальный и дистальный участок портальной вены по типу «конец в конец».
Fig. 4. A circular vascular suture that connects the proximal and distal portion of the portal vein in an end-to-end manner.
ции без опухолевого роста. Послеоперационный период протекал без осложнений,клинически и лабораторноинструментально признаков печеночной недостаточности не было выявлено.Среднее пребывание пациентов, в круглосуточном стационаре, составляло 18 койкодней.
Обсуждение
Основными осложнениями при ГПДР, приводящими к летальным исходам и инвалидизации больных, являются несостоятельность панкреатоеюноанастомоза (ПЕА). Она определяется на основании критериев Международной группы по изучению недостаточности панкреатических анастомозов (International Study Group on Pancreatic Fistula). В послеоперационном периоде наших пациентов несостоятельности ПЕА не было констати-ровано.У обоих пациентов панкреатоеюноанастомоз был сформирован прямым вшиванием панкреатического протока в отверстие стенки тонкой кишки.По данным литературы определение тактики выполнения панкреатоеюноанастомоза весьма противоречивы. Так, Patrick Pessaux с соавт. [5] сообщили, что при диаметре вирсунгова протока до 3 мм., панкреатоеюноанастомоз формировался ими на вирсунгостомическом дренаже. Частота несостоятельности анастомоза составила 26%, тогда как при прямом панкреатоеюноанастомозе она была диагностирована в 42%. Кроме того, не подтвердились преимущества панкреатогастроанастомозов перед ПЕА в плане развития недостаточности (частота несостоятельности 12,3 и 11,1% соответственно) [6–8]. При выполнении ГПДР описаны такие осложнения, как лимфорея и секреторная диарея, которые связаны с большим объемом лимфодиссекции [19]. У наших пациентов в послеоперационном периоде данных осложнений не было выявлено. В работе S. Pedrazzoli с соавт. [9] не отмечено статистически значимых различий в продолжительности жизни больных обеих групп,что, по-видимому, объяснялось незначительной разницей в количестве удаляемых лимфатических узлов. В исследовании C.J. Yeo с соавт. [10] годичная и пятилетняя выживаемость после стандартной операции составили 75 и 13%, а после расширенной — 73 и 29%. Одногодичная выживаемость после гастропанкреатодуоденальной резекции составила 71,2% с медианой выживаемости 13 мес. В нашем случае не выполнено ни одной релапаротомии. Полученные результаты свидетельствуют о том, что увеличение объема ГПДР за счет расширения объема лимфаденэктомии и возможности резекции магистральных венозных сосудов, в нашем случае ворот- ной вены,не приводит к увеличению периоперационной летальности и частоты послеоперационных осложнений. При этом отдаленные результаты ГПДР резекций внушают оптимизм. В дальнейшем оба пациента которым был выполнен данный объем оперативного вмешательства, от дальнейшего проведения адъювантного лечения категорически отказались, о возможных осложнениях и последствиях предупреждены. При контрольном осмотре через 6 месяцев по данным МСКТ органов грудной клетки и брюшной полости без признаков рецидива заболевания,данные онкомаркеров (РЭА, СА19-9) в пределах референсных значений. Таким образом основным фактором, влияющим на продолжительность жизни пациентов после ГПДР, является радиальное удаление всей опухолевой ткани.
Заключение
Резекция воротной вены вместе с инвазирующей в ее стенку опухолью головки поджелудочной железы способствует достижению раикальности операции при выполнении гастропанкреатодуоденальной резекции.
Рак поджелудочной железы является заболеванием с высокой смертностью и выявляется, как правило, в запущенных случаях. Хирургическая резекция поджелудочной железы позволяет добиться удовлетворительных ближайших и отдаленных результатов. Инвазия опухоли в воротную вену некоторых клинических случаях не должна являться причиной отказа пациенту в радикальном хирургическом лечении.
Список литературы Опыт гастропанкреатодуоденальной резекции с циркулярной резекцией магистральных венозных сосудов
- Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2018;68(6):394-424. DOI: 10.3322/caac.21492
- Oh SY, Edwards A, Mandelson MT, Lin B, Dorer R, Helton WS, Kozarek RA. et al. Rare long-term survivors of pancreatic adenocarcinoma without curative resection. World J Gastroenterol. 2015;21(48):13574-13581. DOI: 10.3748/wjg.v21.i48.13574
- De La Cruz MS, Young AP, Ruffin MT. Diagnosis and management of pancreatic cancer. Am Fam Physician. 2014;89(8):626-632
- Патютко Ю.И., Котельников А.Г. Резекция магистральных сосудов при операциях по поводу рака органов билиопанкреато-дуоденальной зоны//Хирургия рака органов билиопанкреато-дуоденальной зоны. М.: Медицина, 2007. С. 244-272.
- Smoot RL, Donohue JH. Modified Appleby procedure for resection of tumors of the pancreatic body and tail with celiac axis involvement. J Gastrointest Surg. 2012;16:2167-2169
- Yamamoto Y, Sakamoto Y, Ban D, et al. Is celiac axis resection justified for T4 pancreatic body cancer? Surgery. 2012;151:61-69
- Ryan DP, Hong TS, Bardeesy N. Pancreatic adenocarcinoma. N Engl J Med. 2014;371:1039-1049
- Yadav D, Lowenfels AB. The epidemiology of pancreatitis and pancreatic cancer. Gastroenterology. 2013;144(6):1252-1261. DOI: 10.1053/j.gastro.2013.01.068
- Ilic M, Ilic I. Epidemiology of pancreatic cancer. World J Gastroenterol. 2016;22(44):9694-9705. DOI: 10.3748/wjg.v22.i44.9694


