Опыт хирургического лечения осложненных форм грыж пищеводнoго отверстия диафрагмы с учетом конституциональных особенностей пациентов
Автор: Черкасов Д.М., Черкасов М.Ф., Старцев Ю.М., Меликова С.Г., Галашокян К.М.
Журнал: Московский хирургический журнал @mossj
Рубрика: Общие вопросы
Статья в выпуске: 1 (71), 2020 года.
Бесплатный доступ
Грыжи пищеводного отверстия диафрагмы являются распространенными заболеваниями в хирургической и гастроэнтерологической практике и выявляются почти у 30% взрослого населения России. Цель исследования: улучшение результатов лечения пациентов с осложненными формами грыж пищеводного отверстия диафрагмы путем разработки индивидуального комплексного подхода с учетом типа телосложения, анатомических и возрастных особенностей. Материалы и методы. В данной работе на 40 препаратах от трупов людей изучены возрастные и конституциональные особенности биомеханических свойств фасциальных структур, а также кровоснабжение диафрагмы. Клиническая часть работы включает опыт лечения 163 пациентов с осложненными грыжами пищеводного отверстия диафрагмы. Результаты. На основании данных анатомических исследований выполнена пластика пищеводного отверстия диафрагмы, с использованием собственных тканей (n=124) и с применением сетчатых имплантатов (n=39). Поздние послеоперационные осложнения изучены в сроки до 5 лет у 117 из 124 больных (94,4%) с пластикой собственными тканями и у всех 39 больных, которым применялись сетчатые имплантаты...
Грыжа пищеводного отверстия диафрагмы, гастроэзофагеальная рефлюксная болезнь, диафрагма, тип телосложения
Короткий адрес: https://sciup.org/142224478
IDR: 142224478 | УДК: 616.329-089 | DOI: 10.17238/issn2072-3180.2020.1.88-94
Текст научной статьи Опыт хирургического лечения осложненных форм грыж пищеводнoго отверстия диафрагмы с учетом конституциональных особенностей пациентов
Актуальность.
Грыжи пищеводного отверстия диафрагмы являются распространенными заболеваниями в хирургической и гастроэнтерологической практике и выявляются почти у 30% взрослого населения России [1].
Такие осложнения заболевания, как гастроэзофагеальная рефлюксная болезнь, пищевод Барретта, эрозии, язвы, стенозы, ущемления являются показаниями к оперативному лечению [1, 2]. Самое частое осложнение грыж пищеводного отверстия диафрагмы – гастроэзофагеальная рефлюксная болезнь, которая занимает четвертое место в гастроэнтерологической патологии после хронического холецистита, хронического панкреатита и гастродуоденальных язв.
При желудочной и кишечной (пищевод Барретта) метаплазии эпителия слизистой оболочки пищевода увеличивается риск развития злокачественных опухолей. Частота встречаемости пищевода Барретта составляет в популяции 1,5 – 4%, а риск развития аденокарциномы на его фоне увеличивается в 20 – 60 раз [1,3].
Хирургическое вмешательство, заключающееся в выполнении крурорафии и создании антирефлюксного механизма (фундопликации по одному из способов), является в настоящее время основным методом лечения осложненных форм грыж пищеводного отверстия диафрагмы [6-8]. В ряде случаев используются пластические материалы [4-6].
Лечение грыж пищеводного отверстия диафрагмы, осложненных метаплазией слизистой оболочки пищевода является комплексным и заключается в консервативной терапии в сочетании с антирефлюксным оперативным лечением, после выполнения которого проводится элиминация метапластически измененных участков эпителия пищевода, чаще всего с использованием внутрипросветных эндоскопических методик [2]. Аргон-плазменная коагуляция является одним из таких методов и в последние годы широко используется для этих целей в связи со своей эффективностью и безопасностью [3].
Цель исследования. Улучшение результатов лечения пациентов с осложненными формами грыж пищеводного отверстия диафрагмы путем разработки индивидуального комплексного подхода с учетом типа телосложения, анатомических и возрастных особенностей.
Материалы и методы. Возрастные и конституциональные особенности биомеханических свойств фасциальных структур, а также кровоснабжение диафрагмы, изучены на 40 препаратах от трупов людей в возрасте от 19 до 75 лет, умерших от причин, не связанных с заболеваниями органов пищеварения и сердечно-сосудистой системы.
В клинической части исследования проведен анализ результатов лечения 163 больных осложненными формами грыж пищеводного отверстия диафрагмы в возрасте от 17 до 76 лет (мужчин – 71 (43,6%), женщин – 92 (56,4%)). В возрасте от 17 до 21 года было 5 пациентов, от 22 до 35 – 18, от 36 до
60 – 85 и старше 60 лет – 55 больных. По типу телосложения 51 больной был брахиморфного типа, 85 – мезоморфного и 27 – долихоморфного.
Аксиальная грыжа пищеводного отверстия диафрагмы отмечена у 125 больных (76,7%), параэзофагеальная – у 38 (23,3%). Среди пациентов с аксиальными грыжами, используя формулу Granderath, у 43 грыжа классифицирована как малая, у 71 – как большая, у 11 – как гигантская, с параэзофагеальными грыжами у 25 больных имела место большая грыж, у 13 – гигантская.
Все 163 пациента страдали гастроэзофагеальной рефлюксной болезнью, у 23 выявлен эрозивно-язвенный эзофагит, у 9 имела место желудочная метаплазия, у 21 – кишечная метаплазия слизистой оболочки пищевода, у 6 – пептическая стриктура, у 1 – ущемленная параэзофагеальная грыжа.
Показаниями к оперативному лечению явились: неэффективность многократных курсов медикаментозного лечения – у 66 пациентов; метапластические изменения слизистой оболочки пищевода – у 30 (кишечная метаплазия – 21, желудочная – 9); параэзофагеальная грыжа – 37; эрозии и язвы пищевода – 23; пептическая стриктура пищевода – 6; ущемленная параэзо-фагеальная грыжа – 1.
Симультанные оперативные вмешательства произведены у 23 пациентов: у 16 в связи с желчнокаменной болезнью, хроническим калькулезным холециститом выполнена лапароскопическая холецистэктомия, у 6 при грыжах передней брюшной стенки антирефлюксная операция дополнена лапароскопической герниотомией с герниопластикой, еще у одной пациентки с лейомиомой желудка выполнена энуклеация доброкачественной опухоли.
У 39 (23,9%) пациентов с осложненными формами грыж пищеводного отверстия диафрагмы при хирургическом лечении нами использованы сетчатые имплантаты. У 24 (14,7%) больных показанием к их установке служили гигантские грыжи пищеводного отверстия диафрагмы (у 13 – параэзофагеальные, у 11 – аксиальные). У 15 (9,2%) пациентов сетчатые имплантаты были использованы у пациентов брахиморфного типа телосложения II зрелого и пожилого возраста с большими грыжами, в тех случаях, когда имелись атрофические изменения мышечного каркаса диафрагмы.
У 30 пациентов (18,4%) проведено комплексное лечение грыж пищеводного отверстия диафрагмы, осложненных метаплазией слизистой оболочки пищевода, включающее в себя антирефлюксное оперативное вмешательство и проведение аргон-плазменной коагуляции Возраст больных данной группы колебался от 29 до 76 лет (средний возраст – 53,4 года). Женщин было 14 (46,7%) мужчин – 16 (53,3%).
При метаплазии слизистой оболочки пищевода преобладали тяжелые степени эзофагита (стадии C и D) (по Лос-Анджелесской классификации). Согласно Пражским критериям, у 11 (36,7%) больных имел место короткий сегмент метаплазии эпителия, у 19 (63,3%) – длинный сегмент. У 6 из 30 (20,0%) пациентов выявлена дисплазия низкой степени выраженности (у 4 – на фоне кишечной метаплазии, у 2 – на фоне желудочной). Дисплазии высокой степени в нашем исследовании не отмечено.
Сеансы аргон-плазменной коагуляции слизистой начинались через 1 – 1,5 месяца после крурорафии с фундопликацией и выполнялись амбулаторно.
Для выполнения аргон-плазменной коагуляции применяли следующие параметры: мощность – 30 – 40 Вт., расход аргона 2 – 2,2 л/мин., режим – FORCED APC.
Расчет статистических данных производился на персональном компьютере с использованием программного обеспечения «Microsoft Excel 2016» и статистической программы «R» (версия 3.2, R Foundation for Statistical Computing, Vienna, Austria).
Результаты
Анатомическими исследованиями установлено, что с возрастом происходят дегенеративные изменения эластической ткани фасциальных структур диафрагмальных ножек на фоне рубцовых изменений коллагеновых пучков. В пожилом возрасте фасциальный футляр этих структур теряет свою прочность и упругость.
Кроме того, начиная со II зрелого возраста, особенно у лиц брахиморфного типа телосложения, количество жировой клетчатки около пищеводного отверстия диафрагмы значительно уменьшается и в пожилом возрасте ее, по сравнению с юношеским периодом, примерно в 2 раза меньше. Это является предрасполагающим фактором к развитию грыж пищеводного отверстия диафрагмы. Во II зрелом и особенно в пожилом возрасте также ухудшается и кровоснабжение мышечных структур зоны пищеводного отверстия диафрагмы, уменьшается диаметр основных питающих сосудов и, особенно их ветвей I – IV порядков, снижается и количество ветвей III – IV порядков, отходящих от основных сосудов, они становятся извитыми, в области ножек диафрагмы и в реберно-диафрагмальном ее отделе появляются малососудистые участки. С возрастом происходит уменьшение емкости артериального русла, которая в пожилом возрасте снижается в 1,5 – 2 раза по сравнению с I возрастным периодом.
Проанализированы результаты лечения больных осложненными формами грыж пищеводного отверстия диафрагмы, оперированных с использованием собственных тканей (n=124) и с применением сетчатых имплантатов (n=39).
В группе больных, которым пластика ножек диафрагмы выполнялась местными тканями, наблюдались следующие неспецифические послеоперационные осложнения: серома одной из послеоперационных ран – 5 (4,0%); малый гидроторакс – 3 (2,4%); послеоперационная пневмония – 2 (1,6%).
Наиболее частыми ранними специфическим послеоперационными осложнениями во время нахождения в стационаре в этой группе были синдром gas-bloat (18 больных), дисфагия (7), икота (2), диспепсические явления (метеоризм, диарея, запор, аэрофагия) (13). Всего отмечено 40 ранних осложне- ний у 29 пациентов (23,4%) (у ряда больных отмечено более 1 осложнения).
Через 1 месяц в данной группе больных (обследованы 120 из 124 пациентов) большинство ранних осложнений купировались, только у одного пациента сохранялась дисфагия и у трех – диспепсические расстройства.
Из 39 больных, которым по показаниям применялись сетчатые имплантаты, у 11 больных (28,4%) отмечено во время нахождения в стационаре 15 ранних осложнений: синдром gasbloat – 7, дисфагия – 3, икота – 1, диспепсические явления – 4.
Через 1 месяц при обследовании всех 39 больных данной группы ранние послеоперационные осложнения сохранялись только у 4 пациентов (10,3%): синдром gas-bloat – 2, дисфагия – 1, диспепсические расстройства – 2. У одного пациента отмечено сочетание gas-bloat синдрома и диспептических расстройств.
Все ранние послеоперационные осложнения относились к I степени по классификации Clavien-Dindo. Следует отметить, что ранние послеоперационные осложнения как в период пребывания больных в стационаре, так и после выписки через один месяц после оперативного вмешательства чаще встречались в группе пациентов, у которых при укреплении ножек диафрагмы были использованы сетчатые имплантаты. Все ранние послеоперационные осложнения были купированы консервативными мероприятиями
Поздние послеоперационные осложнения изучены в сроки до 5 лет после операции у 117 из 124 больных (94,4%) с пластикой диафрагмальных ножек собственными тканями и у всех 39 больных, которым применялись сетчатые имплантаты.
После пластики местными тканями выявлено 11 (9,4%) поздних осложнений: миграция фундопликационной манжетки отмечена у 3 больных, феномен телескопа – у 2, гиперфункция манжетки – у 1 и гастроэзофагеальный рефлюкс – у 5 пациентов.
У 3 пациентов с миграцией фундопликационной манжеты в средостение и у 2 с феноменом соскальзывания манжетки, клинических проявлений не было. У одного больного с периодически возникающей дисфагией клинические проявления купировались спазмолитиками. При явлениях гастроэзофагеального рефлюкса проводились курсы лечения ингибиторами протонной помпы с положительным эффектом.
В группе больных осложненными формами грыж пищеводного отверстия диафрагмы, у которых применялись сетчатые имплантаты, только у одного пациента (2,6%) выявлен гастроэзофагеальный рефлюкс, эффект был достигнут консервативными методами лечения. Таким образом, поздние специфические послеоперационные осложнения в группе пациентов, которым по показаниям были применены в качестве пластического материал сетчатые имплантаты, встречались достоверно реже, чем при пластике ножек диафрагмы местными тканями.
Оценка качества жизни пациентов проводилась при помощи опросника качества жизни пациентов с гастроэзофагеальной рефлюксной болезнью (GERD-HRQL) (рисунок 1), опросника GSRS, в котором оценивались шкалы синдрома абдоминальной боли (AP), рефлюксного синдрома (RS), а также суммарный балл и определения индекса SF-36 по шкалам физического функционирования (PF), ролевого функционирования (RP), боли (P), общего здоровья (GH), жизнеспособности (VT), социального функционирования (SF) через 6, 12 месяцев, 3 года и 5 лет.
В группе больных, которым пластика диафрагмальных ножек выполнялась местными тканями, через 3 месяца обследовано 119 из 124 больных, через 6 и 12 месяцев – по 117, через 3 года – 78 и спустя 5 лет – 44. При применении сетчатых имплантатов через 3, 6 и 12 месяцев обследованы все 39 пациентов, через 3 года – 21, через 5 лет – 9.
|
1 |
Как сильно выражена изжога? |
0 |
1 |
2 |
3 |
4 |
5 |
|
2 |
Бывает ли изжога, когда ложитесь? |
0 |
1 |
2 |
3 |
4 |
5 |
|
3 |
Бывает ли изжога, когда встаете утром? |
0 |
1 |
2 |
3 |
4 |
5 |
|
4 |
Есть ли изжога после еды? |
0 |
1 |
2 |
3 |
4 |
5 |
|
5 |
Влияет ли изжога на Ваш выбор питания? |
0 |
1 |
2 |
3 |
4 |
5 |
|
6 |
Вызывает ли изжога нарушение сна? |
0 |
1 |
2 |
3 |
4 |
5 |
|
7 |
Бывает ли у Вас нарушение глотания? |
0 |
1 |
2 |
3 |
4 |
5 |
|
8 |
Бывают ли у Вас боли при глотании? |
0 |
1 |
2 |
3 |
4 |
5 |
|
9 |
Чувствует ли Вы вздутие или распирание вверху живота? |
0 |
1 |
2 |
3 |
4 |
5 |
|
10 |
Если Вы принимаете лекарства, то эффективны ли они на весь день? |
0 |
1 |
2 |
3 |
4 |
5 |
|
11 |
Как Вы оцениваете удовлетворенность вашим самочувствием? |
Удовлетворен |
Нейтрально |
Не удовлетворен |
|||
Рис.1 Опросник для расчета индекса качества жизни при ГЭРБ (GERD-HRQL)
Субъективные симптомы гастроэзофагеальной рефлюксной болезни уменьшаются резко после операции (через 3 месяца), продолжают снижаться и до 12 месяцев послеоперационного периода, после чего приобретают постоянный характер. Показатели индекса GERD-HRQL у пациентов с пластикой сетчатым имплантатом до операции и через 3 месяца после операции выше, чем у пациентов, пластика которым выполнялась местными тканями (рисунок 2). Это связано с большими размерами грыжевых ворот и изначально более выраженными клиническими проявлениями у пациентов данной группы.
Изучая качество жизни пациентов, выявлено, что в обеих группах показатели опросника GSRS по шкалам «абдоминальная боль» и «рефлюксный синдром» и шкале суммарного измерения значительно снижаются к третьему месяцу и продолжают уменьшаться к 6 месяцу, и с 12 месяцев приобретают значения, сравнимые со здоровыми людьми. Наиболее выраженно происходит снижение данных показателей уже к 3 месяцу по шкале «рефлюксный синдром». У пациентов, пластика ножек
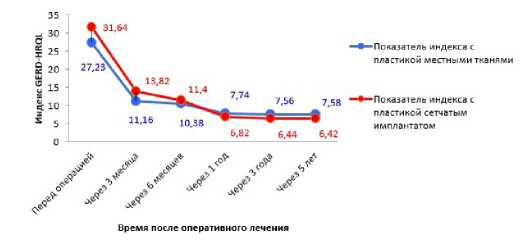
Рис.2 Сравнение динамики индекса качества жизни при ГЭРБ (GERD-HRQL) после оперативного лечения с пластикой местными тканями и с использованием сетчатых имплантатов диафрагмы которым выполнялась с использованием сетчатых имплантатов, снижение данных показателей происходит более медленно. Показатели по шкале «диспептический синдром» у пациентов с пластикой местными тканями к третьему месяцу не отличаются от предоперационных, а при пластике сетчатыми имплантатами даже несколько повышаются, что связано с ранними послеоперационными диспептическими расстройствами, и начинают снижаться к 6 месяцу, а с 12 месяцев также приобретая постоянные значения, сопоставимые со значениями у здоровых лиц.
Показатели индекса SF-36 по шкалам физического, ролевого функционирования, общего здоровья, жизнеспособности, социального функционирования у больных обеих групп постепенно повышаются к 3 и 6 месяцам послеоперационного периода, а к 12 месяцу становятся такими же, как и у здоровых людей, а уровень выраженности боли резко снижается уже к 3 месяцу и к 6 месяцу не отличается от нормальных величин. Уровень выраженности боли в послеоперационном периоде у пациентов, пластика которым выполнялась с использованием сетчатого имплантата, достоверно выше, чем у больных, которым пластика диафрагмальных ножек производилась местными тканями.
Рецидивов заболевания в обеих группах клинических наблюдений отмечено не было.
При грыжах пищеводного отверстия диафрагмы, осложненных метаплазией слизистой оболочки пищевода антиреф-люксная операция, не влияя на метапластические процессы, снижает выраженность воспалительных изменений слизистой оболочки пищевода и позволяет проводить аргон-плазменную коагуляцию в более благоприятных условиях.
Для элиминации участков метаплазии слизистой оболочки пищевода у 9 пациентов достаточным явилось проведение 2 сеансов аргоноплазменной коагуляции, у 2 – трех воздействий, у 14 больных (при МДЦСМ, превышающей 3,0 см) необходимым явилось выполнение 4 сеансов и у 5 (также при МДЦСМ превышающей 3,0 см) – 5 сеансов. Перфораций пищевода и кровотечений во время аргон-плазменной коагуляции отмечено не было.
Среднее время завершения сеансов аргон-плазменной коагуляции после антирефлюксной операции у пациентов с метаплазией слизистой оболочки пищевода при МДЦСМ менее 1,5 см составило 72,5 дней, от 1,5 до 3,0 см – 85,4, более 3,0 см – 170,7 суток.
После окончания курсов аргон-плазменной коагуляции во всех клинических наблюдениях отмечена полная регрессия метапластически измененного эпителия, замещавшегося характерным для пищевода многослойным плоским эпителием. В сроки наблюдений до пяти лет рецидивов метаплазии в нашем исследовании отмечено не было.
Обсуждение
В условиях локальной ишемии фасциально-мышечных структур в области пищеводного отверстия диафрагмы, начиная со II зрелого возрастного периода, особенно у лиц брахиморфного типа телосложения, использование только собственных тканей в качестве пластического материала анатомо-физиологически мало обосновано. У данной категории пациентов необходимо ставит вопрос о дополнительном укреплении зоны диафрагмальных ножек сетчатыми имплантатами [2, 9].
Одним из анатомически обоснованных вариантов является установка сетчатого имплантата в заднее средостение над диафрагмой таким образом, чтобы его поверхность перекрывала пищеводное отверстие и диафрагмальные ножки, дополненная затем задней крурорафией. При ушивании диафрагмальных ножек исключается контакт сетчатого имплантата с органами брюшной полости, препятствуя возможным осложнениям [9]. При этом последний шов на диафрагмальные ножки накладывается выше имплантата, тем самым обеспечивая полное укрытие имплантата и исключает возможность его контакта со стенкой пищевода («Способ хирургического лечения грыж пищеводного отверстия диафрагмы», Патент на изобретение РФ №2611912/01.03.2017).
Нами разработан алгоритм пластики диафрагмальных ножек у пациентов II зрелого и пожилого возраста в зависимости от размеров грыжи и типа телосложения (рисунок 3).
У всех больных независимо от типа телосложения при малых грыжах пластика диафрагмальных ножек выполняется местными тканями, при гигантских грыжах обязательно применяются сетчатые имплантаты. При больших грыжах у пациентов брахиморфного типа телосложения перед крурорафией устанавливается сетчатый имплантат, у лиц долихоморфного типа – сшивание ножек диафрагмы нитью V-loc дополняется одиночными швами нитью Викрил, а у пациентов мезоморфного типа телосложения применяются обе методики с учетом оценки состояния ножек диафрагмы.
Беря за основу определение максимальной длины циркулярного сегмента метаплазии (МДЦСМ), нами разработана и внедрена в практику методика выполнения аргоноплазменной коагуляции («Способ эндохирургического лечения пищевода Барретта», Патент на изобретение РФ № 2625592/17.07.2017.).
При МДЦСМ не более 1,5 см выполняется аргоноплаз- менная коагуляция двух соседних стенок пищевода (например, задней и левой), при втором сеансе коагулируются изменения двух оставшихся стенок. Если максимальная длина циркулярного сегмента метаплазии составляет от 1,5 до 3 см, то сначала производится аргоноплазменная коагуляция двух противоположных стенок пищевода, а следующим сеансом – двух оставшихся стенок. При МДЦСМ, превышающей 3 см, во время первого сеанса воздействуют только на одну стенку пищевода, вторым сеансом осуществляют аргоноплазменную коагуляцию расположенной напротив стенки пищевода, во время следующего сеанса – третьей стенки пищевода, и затем – оставшейся четвертой стенки [3].
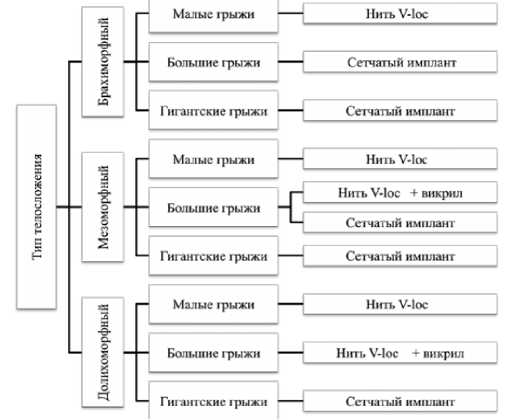
Рис.3 Алгоритм применения пластического материала у больных грыжами пищеводного отверстия диафрагмы II зрелого и пожилого возраста.
Данная схема является условной, в ряде наблюдений, особенно при МДЦСМ более 3,0 см, после проведения контрольной эндоскопии потребовались 1 или 2 дополнительных сеанса аргоноплазменной коагуляции. За один сеанс площадь поверхности коагуляционного воздействия для снижения риска развития стриктуры пищевода не должна быть более 4 см².
У пациентов с осложненными формами грыж пищеводного отверстия диафрагмы, получивших комплексное лечение, наблюдается резкое улучшение качества жизни в течение первого года после операции с последующей стабилизацией эффекта в сроки наблюдения до 5 лет.
При этапном лечении метаплазии слизистой оболочки пищевода, включающем в себя выполнение крурорафии с фундопликацией и агоноплазменной коагуляции по предложенному методу, удалось добиться регрессии у всех пациентов [3]. Интраоперационных осложнений не было. В отдаленные сроки от 1 до 5 лет рецидива метаплазии не отмечено.
Заключение
Анатомическими исследованиями выявлено, что во втором зрелом периоде и в пожилом возрасте, особенно у лиц брахиморфного типа телосложения, в связочных структурах и параэзофагеальной клетчатке происходят дистрофические изменения, ухудшается кровоснабжение мышечных структур, окружающих пищеводное отверстие диафрагмы, уменьшается диаметр питающих сосудов. У этой группы больных при больших грыжах пищеводного отверстия диафрагмы для укрепления диафрагмальных ножек следует применять сетчатые имплантаты.
Предложенный алгоритм хирургического лечения позволяет дифференцированно подходить к выбору метода пластики в зависимости от размеров грыжевых ворот, типа телосложения, возраста, состояния мышечных структур ножек диафрагмы.
Разработанный нами новый способ пластики пищеводного отверстия диафрагмы с применением сетчатого имплантата, позволяет уменьшить риск повреждения расположенных рядом органов и структур.
При грыжах пищеводного отверстия диафрагмы, осложненных метаплазией слизистой оболочки пищевода, предложенный дифференцированный подход к элиминации очагов метаплазии в зависимости от МДЦСМ, позволяет минимизировать число интра- и послеоперационных осложнений, хорошо переносится больными, может проводиться амбулаторно.
Видеоэндохирургическое лечение осложненных форм грыж пищеводного отверстия диафрагмы при соблюдении предложенного алгоритма является высокоэффективным, дает низкое число послеоперационных осложнений, улучшает качество жизни пациентов. В сроки наблюдения до 5 лет, как при использовании по показаниям сетчатых имплантатов, так и при пластике местными тканями рецидивов грыж пищеводного отверстия не отмечено.
Авторы заявляю об отсутствии конфликтов интересов.
Грекова. 2018. Т.177. № 6. С. 16-19. DOI: 10.24884/0042-4625-2018-1776-16-19
Сведдения об авторах:
Список литературы Опыт хирургического лечения осложненных форм грыж пищеводнoго отверстия диафрагмы с учетом конституциональных особенностей пациентов
- Аллахвердян А.С., Праздников Э.Н. Пищевод Барретта как осложнение гастроэзофагеальной рефлюксной болезни: диагностика и современные методы лечения (взгляд хирурга) // Consilium Medicum. 2015. № 8. С. 55-61.
- Inoue H., Sumi K., Onimaru M. History of surgical therapy and recent advancement of endoscopic therapy for GERD. Nihon Shokakibyo Gakkai Zasshi. 2017, No. 114(10), pp. 1797-1803. DOI: 10.11405/nisshoshi.114.1797
- Преимущества оригинального способа эндохирургического лечения пищевода Барретта / М.Ф. Черкасов, А.В. Скуратов, Д.М. Черкасов, Ю.М. Старцев, С.Г. Меликова // Эндоскопическая хирургия. 2018. Т. 24. № 2. С. 30-33. DOI: 10.17116/endoskop201824230
- Пути повышения эффективности хирургического лечения грыж пищеводного отверстия диафрагмы / Д.И. Василевский, С.Ю. Дворецкий, И.С. Тарбаев, А.М. Ахматов // Вестник хирургии им. И.И. Грекова. 2018. Т.177. № 6. С. 16-19. 10.24884/0042-4625-2018-177- 6-16-19 DOI: 10.24884/0042-4625-2018-177-6-16-19
- Креативная хирургия грыжи пищеводного отверстия диафрагмы / О.В. Галимов, В.О. Ханов, Д.З. Мамадалиев, Р.Р. Сайфуллин, Р.Р. Сагитдинов // Хирургия. Журнал им. Н.И. Пирогова. 2017. № 7. С. 30-32. DOI: 10.17116/hirurgia2017730-32
- Subjective outcome after laparoscopic hiatal hernia repair for intrathoracic stomach / P.S.S. Castelijns, J.E.H. Ponten, M.C.G. Van de Poll, S.W. Nienhuijs, J.F. Smulders. Langenbecks Arch Surg, 2017, No. 402, pp. 521-530. DOI: 10.1007/s00423-016-1504-2
- Long-Term Patient-Reported Outcomes of Paraesophageal Hernia Repair / DJ. Lazar, D.H. Birkett, D.M. Brams, H.A. Ford, C. Williamson, D. Nepomnayshy. Sсientific paper JSLS, 2017, No. 4(21). 10.4293/ JSLS.2017.00052 DOI: 10.4293/JSLS.2017.00052
- Durability of giant hiatus hernia repair in 455 patients over 20 years / P.A. Le Page, R. Furtado, M. Hayward, S. Law, A. Tan, S.J. Vivian, H. Van der Wall, G.L. Falk. Ann R Coll Surg Engl, 2015, No. 97(3), pp. 188-193. DOI: 10.1308/003588414X14055925060839
- Antonakis F., Köckerling F., Kallinowski F. Functional Results after Repair of Large Hiatal Hernia by Use of a Biologic Mesh. Front Surg, 2016, No. 3, pp. 3-16. DOI: 10.3389/fsurg.2016.00016


