Опыт хирургического лечения рецидивов рака желудка
Автор: Чайка А.В., Хомяков В.М., Вашакмадзе Л.А., Черемисов В.В., Рябов А.Б.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 4 (70), 2015 года.
Бесплатный доступ
Лечение больных раком желудка (РЖ) по-прежнему остается актуальной проблемой современной онкологии. Рецидив заболевания является одной из основных причин смертности при этой патологии. Цель исследования - изучить возможности хирургического лечения рецидивов РЖ. Методы. Проанализирован опыт хирургического лечения 35 больных с рецидивами РЖ в период 2000-2013 гг. (торако-абдоминальное отделение МНИОИ им. П.А. Герцена). По поводу первичного рака 8 больных были оперированы в торако-абдоминальном отделении МНИОИ им. П.А. Герцена, 27 больных - в других лечебных, в том числе онкологических, учреждениях страны. У 6 больных рецидивы РЖ развились после ПСРЖ, у 17 - после ДСРЖ, у 12 пациентов - после ГЭ. Средний безрецидивный период в группе составил 22,9 ± 3,4 мес. Изолированные локо-регионарные рецидивы были у 29 больных; у 6 пациентов при оперативном вмешательстве диагностирована диссеминация и нерезектабельность процесса. Результаты. Локо-регионарные рецидивы в анастомозе выявлены у 22 больных; в резецированном желудке - у 3; локо-регионарный экстраорганный рецидив диагностирован у 7 больных; солитарные метахронные отдаленные метастазы - у 3 пациентов. Всего выполнено 33 операции: ЭОЖ - у 12 больных; ререзекция желудка после ДСРЖ - у 2; резекция пищеводно-кишечного анастомоза (после ГЭ) - у 8; удаление экстраорганного рецидива - у 8 больных; трем пациентам выполнено удаление солитарных метастазов. Частота осложнений составила 45,5 % (15 больных). Осложнения I класса по Clavien-Dindo диагностированы у 3 больных, II - у 5 больных, IIIA - у 2, IIIB - у 2; IV - у 2 больных; V класса (смерть от послеоперационных осложнений) - у 1 больной. Несостоятельность швов анастомоза отмечена у 4 больных (у двух из них - поздняя), у одного - привела к летальному исходу. Послеоперационная летальность - 3 %. Отдаленные результаты лечения прослежены у 32 больных. Одногодичная выживаемость в группе оперированных больных составила 44 %, трехлетняя - 25 %; выживаемость 5 лет и более отмечена у 1 больной (2,8 %), р=0,08. Выводы. Хирургический метод имеет ограниченное применение при лечении рецидивов РЖ, он оправдан при изолированном локо-регионарном рецидиве и улучшает результаты лечения больных РЖ. Результаты хирургического лечения при локо-регионарном экстраорганном рецидиве не хуже таковых при лечении рецидивов в анастомозе или желудке.
Рак желудка, рецидив, результаты хирургического лечения
Короткий адрес: https://sciup.org/14056775
IDR: 14056775 | УДК: 616.33-006.6-036.65-089
Experience of surgical treatment at recurrent gastric cancer
Introduction. Currently, the only potentially curative treatment for gastric cancer is radical gastrectomy. Even after curative resection, death from gastric cancer is primarily due to recurrence. The purpose of the study was to analyze feasibilities of surgical treatment for recurrent gastric cancer. Methods. From 2000 to 2013, the experience in surgical treatment of 35 patients with recurrent gastric cancer was analyzed. Eight patients underwent surgery for primary gastric cancer in the Thoracic and Abdominal Department of Moscow P.A. Hertsen Cancer Research Institute and 27 patients were operated on in other hospitals including cancer centers. Recurrence from gastric cancer was observed in 6 patients after proximal subtotal gastric resection (PSGR), in 17 patients after distal subtotal gastric resection (DSGR) and in 12 patients after gastrectomy (GE). The median time to recurrence was 22.9 ± 3.4 months. Isolated locoregional recurrence of gastric cancer was detected in 29 patients. Cancer dissemination was diagnosed in 6 patients. Results. Anastomotic recurrence was detected in 22 patients, recurrence within the remnant stomach, in 3 patients, locoregional extra-gastric recurrence in 7 patients and solitary metachronous distant metastases were diagnosed in 3 patients. A total of 33 operations were performed: extirpation of the operated stomach in 12 patients, re-resection of the stomach after DSGR in 2 patients, resection of the esophageal-intestinal anastomosis (after GE) in 8 patients, removal of extra-gastric recurrence in 8 patients and removal of solitary metastases in 2 patients. The complication rate was 45.5 % (15 patients). Grade I complications according to Clavien-Dindo classification were diagnosed in 3 patients, grade II complications in 5 patients, grade IIIA in 2 patients, grade IIIB in 2 patients, grade IV in 2 patients and grade V complications (death from postoperative complications) in 1 patient. The failure of anastomosis sutures was observed in 4 patients, 1 of them died of this complication. Postoperative death rate was 3%. Long-term treatment outcomes were observed in 32 patients. In patients who underwent surgery, the 1-, 3- and 5-year survival rates were 44 %, 25 % and 2.8 %, respectively (р = 0.08). Conclusion. Surgical intervention has been limited to locoregional recurrent gastric cancer. Results of surgical treatment for locoregional extra-gastric recurrence were no worse than those in the treatment for recurrence in the anastomosis or within the remnant stomach.
Текст научной статьи Опыт хирургического лечения рецидивов рака желудка
семинация; отдаленные (гематогенные и лимфогенные) метастазы, выявляемые метахронно после хирургического лечения изначально диагностированного РЖ I–III стадий [15, 25, 30]. Общая частота локо-регионарных рецидивов составляет 6–50 %, изолированных – 6–46 % [15].
Прогностически неблагоприятными факторами являются увеличение стадии РЖ, глубина инвазии опухоли, наличие регионарных метастазов, низкая степень дифференцировки рака, диффузноинфильтративная форма роста, проксимальная локализация и распространение на пищевод [25], а также наличие признаков высокой биологической агрессивности опухоли [1, 9, 24]. Предлагаются различные алгоритмы и формулы расчета риска возникновения, локализации и срока рецидива на основании ряда прогностических факторов, с использованием моно- и мультивариантного статистического анализа данных [25, 27, 30].
Основными методами выявления и уточняющей диагностики рецидивов РЖ являются эндоскопические [14, 15, 16], в том числе с применением высокого разрешения, узкоспектральной (NBI), хромоэндоскопии, различных видов эндомикроскопии, эндосонографии, а также лучевые методы визуализации: рентгенологическое исследование с барием, комплексное ультразвуковое исследование (УЗИ), мультиспиральная компьютерная томография (МСКТ) [10, 14, 15, 17, 27]. Основным методом выявления перитонеальной диссеминации является диагностическая лапароскопия [10, 23].
Возможности хирургического лечения рецидивов РЖ ограничены [7, 18, 22, 29, 30]. Удаление опухоли в радикальном объеме возможно при наличии локо-регионарного рецидива без отдаленных метастазов. Солитарные отдаленные метастазы, выявленные метахронно после хирургического лечения первичного РЖ, также подвергаются хирургическому удалению в сочетании с консервативными методами противоопухолевого воздействия [18, 30].
Частота послеоперационных осложнений составляет 20–45 %, послеоперационная летальность – от 9,5 до 25,5 % [14, 15, 18, 30]. В структуре послеоперационных осложнений наибольшее значение имеет частота несостоятельности швов пищеводных анастомозов – от 2,5 до 17 % [14, 15, 30].
После хирургического лечения рецидивов РЖ большинство больных умирает в течение
2 лет после операции [11, 15, 29, 30]. По данным отдельных авторов, двухлетняя выживаемость достигает 20–40 % [7, 2, 26]. Пятилетняя выживаемость отмечена в единичных наблюдениях [2, 7]. Большинство авторов склоняются к выводу, что хирургический компонент лечения рецидивов РЖ имеет ограниченное применение и используется в случае изолированного локо-регионарного рецидива либо солитарного метастаза в печени, у функционально операбельных больных и в условиях специализированных онкологических центров [15, 20, 22]. Использование различных сочетаний противоопухолевого воздействия (хирургический, лучевой и химиотерапевтический) – «multimodal therapy» – представляется наиболее оптимальным для лечения больных с рецидивами РЖ при приемлемом качестве жизни [15, 20, 22, 26]. Наиболее универсальным является химиотерапевтическое лечение с применением схем с препаратами платины, иринотекана, S1, как самостоятельное, так и в неоадъювантном и адъювантном режимах. Исследуется эффективность сочетания хирургического и лучевого методов лечения [21, 26].
Цель исследования – определить роль хирургического компонента в лечении больных с рецидивами РЖ. Поставлены задачи проанализировать опыт хирургического лечения больных этой категории, выявить особенности оперативных вмешательств, оценить непосредственные и отдаленные результаты лечения.
Материал и методы
Для стадирования первичных опухолей была использована Международная TNM-классификация злокачественных новообразований 7-го пересмотра [28]. Более чем у 50 % пациентов первичный
Таблица 1
Распределение по стадиям первичного РЖ
|
Стадии |
IA |
IB |
IIA |
IIB |
IIIA |
IV |
Всего |
|
Число |
2 |
2 |
1 |
12 |
16 |
2 |
35 |
|
больных |
(5,7 %) |
(5,7 %) |
(2,9 %) |
(34,3 %) |
(45,7 %) |
(5,7 %) |
(100 %) |
РЖ диагностирован на стадии IIIA–B и IV стадии (IV стадия установлена у 1 больного при выявлении метастатически измененного лимфоузла брыжейки тонкой кишки; у другого – в лимфоузле основания a. colica media). Метастатическое поражение регионарных лимфоузлов зафиксировано у 19 больных (табл. 1).
Диагностический алгоритм включал эзофагогастродуоденоскопию с биопсией; рентгенологическое контрастное исследование с применением суспензии сульфата бария per os; УЗИ органов брюшной полости, забрюшинного пространства, малого таза, шейных, над- и подключичных лимфоузлов; МСКТ органов брюшной полости и грудной клетки в нативном варианте либо с болюсным контрастным внутривенным усилением (по показаниям). Экстраорганные рецидивы и отдаленные метастазы верифицировались путем трепанобиопсии под контролем УЗИ.
Хирургическое лечение рецидивов РЖ было проведено 29 больным, выполнено 33 операции (трем больным проводились повторные оперативные вмешательства в связи с новым рецидивом). Еще у 6 пациентов вмешательство было ограничено эксплоративной лапаротомией в связи с выявленными диссеминацией и/или нерезекта-бельностью процесса.
У больных с экстраорганными рецидивами выполнялись вмешательства в объеме удаления рецидивной опухоли (8 операций). Эти рецидивы локализовались преимущественно в лимфатических узлах вокруг головки поджелудочной железы, печеночно-двенадцатиперстной связки, в забрюшинном пространстве у чревного ствола, а также в оставленных лимфатических узлах по ходу левой желудочной и общей печеночной артерий.
Хирургическое лечение в объеме R0 проведено 22 больным, в объеме R1 – 7, R2 – одному больному. Все операции сопровождались расширенной лимфаденэктомией. Комбинированные операции (с резекцией вовлеченных органов: поджелудочной железы, надпочечника, поперечно-ободочной кишки и ее брыжейки, спленэктомией) выполнены 9 больным.
Комбинированный доступ применен у 10 больных: у 8 – лапаротомия с правосторонней торакотомией; у 1 – левосторонняя комбинированная лапароторакотомия; у 1 – абдомино-цервикальный доступ с трансхиатальным удалением пищевода. Торакотомии выполнялись при высоком расположении пищеводного анастомоза и при распространении опухоли на пищевод. Пластическое замещение удаленного пищевода тонкой кишкой произведено у 9 больных, сегментом толстой кишки – у 2 пациентов.
Пациентам с метахронными солитарными метастазами (4 наблюдения) выполнялись циторедуктивные операции: левосторонняя адреналэктомия, брюшно-промежностная экстирпация прямой кишки, радиочастотная аблация метастаза в печени (2 вмешательства).
Результаты и обсуждение
Анализируемая группа характеризовалась преобладанием прогностически неблагоприятных вариантов РЖ и изначально большой распространенностью опухолевого процесса. Появление рецидива РЖ при небольшой стадии первичного РЖ отражает неадекватный объем операции. Развитие экстраорганных локо-регионарных рецидивов обусловлено недостаточным объемом лимфаденэктомии и резекции вовлеченных в опухолевый процесс структур и органов при операции по поводу первичного РЖ. При этом выполнение стандартной лимфаденэктомии D2 не гарантировало отсутствие рецидива в лимфоузлах при преобладании лимфогенного пути метастазирования. При диффузных формах РЖ метастазы в лимфоузлы диагностировались относительно редко, преобладающим путем метастазирования был перитонеальный канцероматоз.
Вариант реконструкции пищеварительного тракта после ЭОЖ либо резекции пищеводнокишечного анастомоза зависит от объема операции и варианта анастомозов при первичном раке, а также местной распространенности рецидивной опухоли (вовлечение пищеводно-желудочного анастомоза, высокий переход на пищевод, распространение на желудочно-кишечный анастомоз с вовлечением отводящей кишки) [4, 5, 6, 11]. При высоком переходе опухоли на пищевод реконструкция выполняется с помощью тонко- или толстокишечных пищеводных трансплантатов [5, 6]. Предпринимаются попытки выполнения операций лапароскопическим доступом [20].
Частота осложнений после хирургического лечения в нашем исследовании оставалась в пределах, представленных в литературе, и составила 45,5 % (15 больных), что сопоставимо с таковой при операциях при первичном РЖ. По классификации Clavien-Dindo осложнения I класса диагностированы у 3 больных; II – у 5 больных, IIIA – у 2, IIIB – у 2; IV –у 2 больных; V класса (смерть от послеоперационных осложнений) – 1 больной. Несостоятельность швов анастомоза отмечена у 4 больных (у двух из них – поздняя), у одного привела к летальному исходу. Послеоперационная летальность – 3 %, также в пределах общемировых показателей. Таким образом, операции по поводу рецидивов РЖ не сопровождаются значительным увеличением числа осложнений.
Консервативные методы лечения применялись в адъювантном режиме при большой распространенности рецидива РЖ после операции либо при неоперабельном процессе, выживаемость не превышала 1 года.
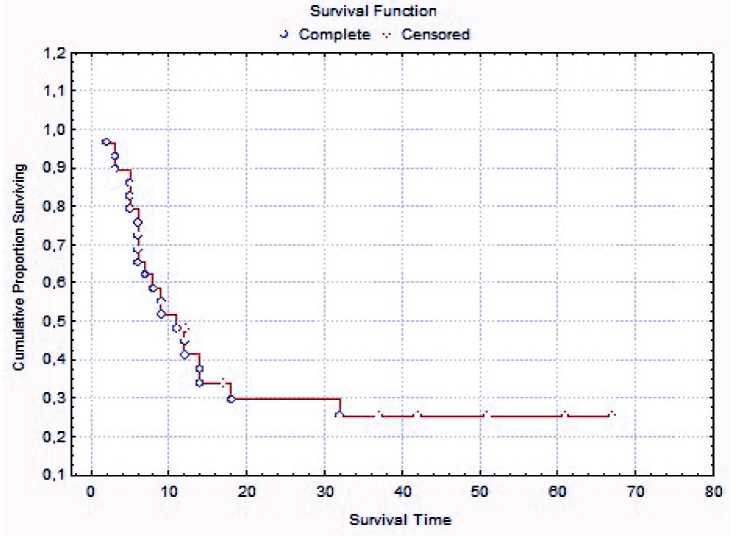
Cumulative Proportion Surviving (Kaplan-Meier) о Complete ■:■ Censored
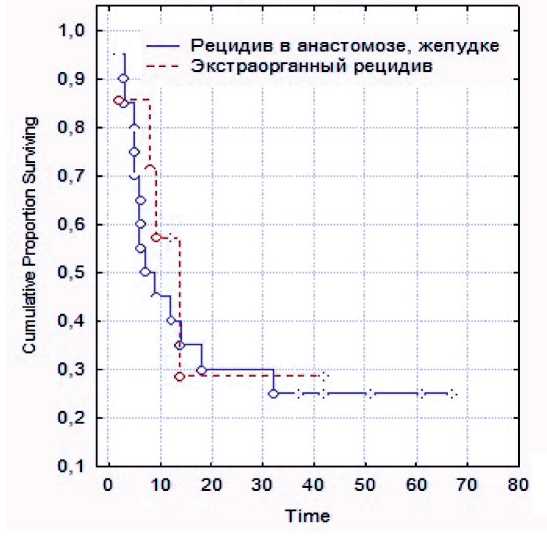
Отдаленные результаты лечения прослежены у 32 больных, трое выбыли из-под наблюдения. Одногодичная выживаемость в группе оперированных больных составила 44 %; трехлетняя – 25 %; выживаемость 5 и более лет отмечена у 1 (2,8 %) больной, р=0,08 (рис. 1). Средняя продолжительность жизни в группе составила 18,0 ± 3,4 мес, медиана выживаемости – 10 мес. При сравнении группы больных, оперированных по поводу реци- дивов в анастомозе и экстраорганных рецидивов, статистически значимых отличий не выявлено; результаты хирургического лечения в группе экс-траорганных рецидивов не хуже, чем при органном рецидиве (рис. 2).
Список литературы Опыт хирургического лечения рецидивов рака желудка
- Барышев А.Г. Отдаленные результаты лечения больных раком желудка в свете биомолекулярных особенностей опухоли//Российский биотерапевтический журнал. 2011. № 2 (10). С. 85-88.
- Вашакмадзе Л.А., Алешкина Т.Н., Чайка А.В. Хирургическая тактика при рецидивах рака желудка//Российский онкологический журнал. 2001. № 1. С. 9-12.
- Вашакмадзе Л.А., Бутенко А.В., Савинов В.А. Возможность выполнения мультивисцеральных резекций при регионарном рецидиве рака желудка//Российский онкологический журнал. 1998. № 4. С. 53-54.
- Вашакмадзе Л.А., Чайка А.В., Сидоров Д.В., Белоус Т.А., Алешкина Т.Н. Хирургическое лечение больных с рецидивами рака желудка. М., 2008. 40 с.
- Вашакмадзе Л.А., Черемисов В.В., Хомяков В.М. Реконструкция верхних отделов пищеварительного тракта при одномоментных или последовательных хирургических вмешательствах на пищеводе и желудке//Онкология. 2013. № 2. С. 16-22.
- Давыдов М.И., Стилиди И.С., Бохян В.Ю. Внутриплевральная толстокишечная пластика у больных раком желудка с высоким поражением пищевода//Российский онкологический журнал. 2002. № 3. С. 27-29.
- Джураев М.Д., Худайбердиева М.Ш., Эгамбердиев Д.М. Рецидив рака желудка: современное состояние проблемы//Сибирский онкологический журнал. 2009. № 3 (33). С. 60-63.
- Ена И.И., Шаназаров Н.А. Современные подходы к хирургическому лечению рака желудка//Фундаментальные исследования. 2011. № 10. С. 204-211.
- Жарков В.В., Михайлов И.В. Факторы прогноза при раке желудка//Медицинские новости. 2005. № 9. С. 17-21.
- Китаев В.М., Дмитращенко А.А., Маршенина Т.Б. Значение компьютерной томографии в комплексной диагностике рецидивов рака желудка//Материалы III симпозиума «Клинико-инструментальная диагностика в хирургии». М., 1994. С. 110-111.
- Клименков А.А., Неред С.Н., Губина Г.И. Современные возможности хирургического лечения рецидива рака желудка//Материалы VIII Российского онкологического конгресса. М., 2004. С. 13-16.
- Петрова Г.В., Грецова О.П., Простов Ю.И., Простов М.Ю. Заболеваемость населения России злокачественными новообразованиями//Злокачественные новообразования в России в 2012 году (заболеваемость и смертность)/Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М., 2014. С. 4-44.
- Писарева Л.Ф., Одинцова И.Н., Ананина О.А., Афанасьев С.Г., Волков М.Ю., Давыдов И.М. Рак желудка в Томской области: эпидемиологические аспекты//Сибирский онкологический журнал. 2013. № 6. С. 40-43.
- Bohner H., Zimmer T., Hopfenmuller W., Berger G., Buhr H.J. Detection and prognosis of recurrent gastric cancer. Is routine follow-up after gastrectomy worthwile?//Hepato-gastrol. 2000. Vol. 47. P. 1489-1494.
- Carboni F., Lepaine P., Santoro R., Lorusso R., Manchini P., Carlini M., Santoro E. Treatment for isolated loco-regional recurrence of gastric adenocarcinoma: Does surgery play a role?//World J. Gastroenterol. 2005. Vol. 11 (44). P. 7014-7017.
- Hosokawa O., Kaizaki Y., Watanabe K., Hattori M., Duoden K., Hayashi H., Maeda S. Endoscopic surveillance for gastric remnant cancer after early cancer surgery//Endoscopy. 2002. Vol. 34. P. 469-473.
- Kim K.A., Park C.M., Cha S.H., Seol N.Y., Cha I.H., Lee K.Y. CT finding in the abdomen and pelvis after gastric carcinoma resection//AJR. 2002. Vol. 179. P. 1037-1041.
- Lehnert T., Rudek B., Buhl K., Golling M. Surgical therapy for loco-regional recurrence and distant metastasis of gastric cancer//Eur. J. Surg. Oncol. 2002. Vol. 28 (4). P. 455-461.
- Mansfield P.F. Surgical management of invasive gastric cancer. URL: http://www.uptodate/com/surgical-management-of-invasive-gastriccancer (29.04.2014).
- Mayumi K., Terakura M., Hamano G., Ikebe T., Takemura M., Hori T. A case of repeated postoperative recurrence of gastric cancer treated via laparoscopic approach//Gan To Kagaku Ryoho. 2013. Vol. 40 (12). P. 2176-2178.
- Miller R.C., Haddock M.G., Gunderson L.L., Donohue J.H. Intraoperative radiotherapy for treatment of locally advanced and recurrent esophageal and gastric adenocarcinoma//Dis Esophagus. 2006. Vol. 19 (6). P. 487-495.
- Nashimoto A., Yabusaki H., Matsuki A., Aizawa M. Surgical treatment for curable and incurable recurrent gastric cancer//Gan To Kagaku Ryoho. 2013. № 40 (8). P. 971-975.
- Okugawa Y., Toiama Y., Inoue Y., Saigusa S., Kobayashi M., Tanaka K., Mohri Y., Miki C., Kusunoki M. Late-onset peritoneal recurrence of advanced gastric cancer 20 years after partial gastrectomy//Nihon Shokakibyo Gakki Zasshi. 2011. Vol. 108. P. 238-244 DOI: 10.1186/1477-7819-8-104
- Panani A.D. Cytogenic and molecular aspects of gastric cancer: clinical implications//Cancer let. 2008. Vol. 266. P. 99-115.
- Schwarz R., Zagala-Nevarez K. Recurrent patterns after radical gasntrectomy for gastric cancer: prognostic factors and implications for postoperative adjuvant therapy//Ann. Surg. Oncol. 2002. Vol. 9. P. 394-400.
- Shchepotin I., Evans S.R., Shabahang M., Cherny V., Buras R.R., Zadorozhny A., Nauta R.J. Radical treatment of locally recurrent gastric cancer//Am. Surg. 1995. Vol. 61 (4). P. 371.
- Shiraishi N., Inomata M., Osawa N., Yasuda K., Adachi Y., Kitano S. Early and late recurrence after gastrectomy for gastric carcinoma. Univariate and multivariate analyses//Cancer. 2000. Vol. 89. P. 255-261.
- Sobin L.N., Gospodarowicz M.K., Wittekind Ch. TNM-classification of malignant tumours. 7th ed. Wiley-Blackwell, 2009.
- Takeoshi I., Ohwada S., Ogawa T., Kawashima Y., Ohya T., Kawate S., Nakasone Y., Aria K., Ikeya T., Morishita Y. The resection of non-hepatic intraabdominal recurrence of gastric cancer//Hepatogastroenterology. 2000. № 47. P. 1479-1481.
- Yoo C.H., Hoh S.H., Shin D.W., Choi S.H., Min J.S. Recurrence following curative resection of gastric cancer//Br. J. Surg. 2000. Vol. 87 (2). P. 236-242.


