Опыт использования хиксозида в терапии туберкулезного поражения бронхов
Автор: Морозова Т.Н., Баринбойм О.Н., Докторова Н.П., Данилов А.Н.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Фтизиатрия
Статья в выпуске: 2 т.10, 2014 года.
Бесплатный доступ
Цель: оценить эффективность и переносимость ингаляционного применения комбинированного противотуберкулезного препарата Хиксозид в лечении больных туберкулезом легких с наличием специфического бронхита. Материал и методы. Исследование проводилось больным с туберкулезом бронхов (впервые выявленным и с рецидивом) при отсутствии состояний, препятствующих назначению адекватной химиотерапии, ВИЧ-отрицательным. В 1 группе (п=30) в составе комплексной химиотерапии ингаляционно вводился Хиксозид (Диоксидин 100 мг + Изониазид 250 мг). Во 2 группе (п=21) стандартное лечение сочеталось с ингаляционным введением Изониазида. Курс 21 день. Результаты. После курса ингаляций сХиксозидом клиническое излечение туберкулеза бронхов через 2 месяца лечения наступало у 69,2% пациентов против 38,1 % в группе сравнения, р=0,039. Наблюдалась положительная динамика в течении неспецифического эндобронхита — 85,7% против 52,9%, р=0,017. сократились сроки лечения до достижения рубцевания полостей распада и прекращения бактериовыделения: 143±27 дней против 164±32, р=0,019. Нежелательные реакции на Хиксозид, потребовавшие его отмены, развились у 13,3% пациентов, быстро купировались и не повлияли на здоровье больных в дальнейшем. Заключение. Применение ингаляционного препарата Хиксозид в комплексном лечении больных туберкулезом позволяет ускорить клиническое излечение туберкулеза бронхов, заживление деструкции в легочной ткани и прекращение бактериовыделения.
Лечение туберкулеза, туберкулез бронха, хиксозид
Короткий адрес: https://sciup.org/14917950
IDR: 14917950
Текст научной статьи Опыт использования хиксозида в терапии туберкулезного поражения бронхов
-
1 В ведение. Несмотря на стабилизацию эпидемической ситуации по туберкулезу в Российской Федерации, эффективность лечения больных туберкулезом остается недостаточной, что может проявиться в будущем новой волной эпидемии. В структуре заболеваемости регистрируется высокий удельный вес деструктивного туберкулеза с большой частотой осложненных форм заболевания [1–3]. Одним из частых осложнений распространенного деструктивного специфического процесса является туберкулезный эндобронхит [4], который определяет высокую эпидемиологическую опасность заболевания и требует применения дополнительных процедур для его излечения.
Потенциальный путь решения проблемы — создание новых противотуберкулезных препаратов или усовершенствование известных этиотропных средств, отличающихся высокой противомикробной активностью и возможностью дифференцированных способов введения (интрабронхиально, парентерально и пр.). Российскими специалистами произведен новый комбинированный противотуберкулезный препарат Хиксозид [5], представляющий собой комбинацию двух веществ: антибактериального средства гидроксиметилхиноксалиндиоксид (Диок-
сидин) — 100 мг и противотуберкулезного препарата Изониазид — 250 мг. Выпускается в форме лиофилизата для приготовления раствора для ингаляций и внутриплевральных введений.
По данным Глушкова Р. Г. и Соколовой Г. Б. [6], комбинация изониазида с диоксидином обладает синергизмом, в результате чего противотуберкулезная активность изониазида повышается более чем в 5 раз. Основой синергического эффекта является разрыхление производными хиноксалин-1,4-диоксида бактериальной стенки микобактерий туберкулеза, обеспечивающее поступление противотуберкулезного препарата во внутриклеточное пространство. При доклиническом исследовании препарата сделано заключение о высокой активности Хиксозида в отношении устойчивых к изониазиду штаммов микобактерий туберкулеза (МБТ), а созданная растворимая форма может быть рекомендована к использованию в лечебной практике в виде ингаляций и внутриполост-ного применения.
Однако в научной литературе недостаточно данных об использовании Хиксозида в клинической практике и оценке его эффективности [7, 8].
Цель: оценить эффективность и переносимость ингаляционного применения комбинированного противотуберкулезного препарата Хиксозид в лечении больных туберкулезом легких с наличием специфического поражения бронхов.
Материал и методы. Для выполнения поставленной задачи проведено проспективное рандомизированное исследование с наблюдением за 51 пациентом, получавшим лечение в условиях стационара Саратовского областного клинического противотуберкулезного диспансера.
Критериями включения в исследование являлись: впервые выявленные больные и пациенты с рецидивом туберкулеза легких; специфическое поражение бронхов, подтвержденное при фибробронхоскопии; возраст больных от 18 до 60 лет.
Критериями исключения определены: гиперчувствительность к изониазиду и диоксидину по анамнестическим данным; лекарственная устойчивость к изониазиду; сопутствующая патология, препятствующая назначению адекватной противотуберкулезной терапии в соответствии с режимами лечения; ВИЧ-инфекция; беременность и кормление грудью; необходимость терапии глюкокортикостероидами; отказ от продолжения лечения до получения 21 дозы препарата Хиксозид.
Все исследования и методики лечения проведены в соответствии с международными этическими требованиями ВОЗ и принципами Хельсинкской декларации (Женева, 1983). Включение пациентов в группу наблюдения осуществлялось на основании их информированного добровольного согласия.
Всем пациентам при поступлении в стационар проводилось стандартное клиническое, микробиологическое и рентгенологическое обследование, включающее: сбор анамнеза и жалоб; физикальное исследование; общий клинический анализ крови; общий клинический анализ мочи; биохимический анализ крови (билирубин, трансаминазы, креатинин, мочевина); рентгенологическое исследование органов грудной клетки с определением объема и локализации поражения; фибробронхоскопическое исследование (ФБС); спирография; микроскопия и посев мокроты на жидкие и плотные питательные среды для выявления микобактерий туберкулеза; посев мокроты на вторичную флору и грибы; исследование крови на антитела к ВИЧ; осмотр гинеколога для исключения беременности (для женщин детородного возраста).
Лечение в основной схеме химиотерапии назначалось в соответствии с приказом МЗ РФ № 109 [9]. Все пациенты были разделены на 2 группы. В 1 группе, n=30, комплексная терапия туберкулеза дополнялась ингаляционным введением Хиксозида ежедневно, 1 раз в сутки, после приема пищи, в дозе, соответствующей инструкции по применению: 2 мл при массе тела до 40 кг, 8 мл при массе тела 40–50 кг, 10 мл при массе тела 60 кг и более. Продолжительность курса составила 21 день. Пациентам 2 группы (группа сравнения), n=21, стандартная химиотерапия проводилась в сочетании с ингаляционным введением 10% Изониазида 3 мл 1 раз в сутки в течение 21 дня. Ингаляции пациентам проводились через компрессорный небулайзер. Пациентам обеих групп общая суточная доза введения Изониазида всеми методами составляла 10 мг/кг в сутки. С целью предупреждения нежелательных явлений Изониазида назначался витамин В6 парентерально в дозе 0,1 г/сут.
В ходе ежедневного мониторинга оценивалось клиническое состояние больного (жалобы, объективный осмотр). Контрольными точками исследования пациентов обеих групп определены: 1) окончание курса ингаляций с Хиксозидом в 1 группе и Изониазидом во 2 группе — не менее 21 дня; 2) 60 доз интенсивной фазы химиотерапии; 3) завершение стационарного этапа лечения. Третья контрольная точка по временному параметру была индивидуальной для каждого пациента: показанием к окончанию интенсивной фазы лечения в стационаре было достижение рубцевания полостей распада и/или прекращение бактериовыделения при стабилизации клинической и рентгенологической картины.
В качестве динамического лабораторного обследования выполнялись общий клинический и биохимический анализы крови; общий клинический анализ мочи. Микробиологическое обследование осуществлялось исследованием мокроты на МБТ методом микроскопии и абсолютных концентраций. Учитывая особенности развития туберкулезного воспаления, контрольную фибробронхоскопию проводили во 2-й и 3-й контрольной точке. Наблюдение за пациентами вне контрольных точек, рентгенологическое обследование органов грудной клетки в динамике осуществлялись на сроках, определенных нормативными актами [9, 10].
Статистическая обработка данных проводилась с помощью унифицированной компьютерной программы Statistica ´99 Edition (StatSoft, Inc). Проведен анализ качественных бинарных данных с построением таблиц сопряженности. Учитывая, что некоторые значения абсолютных частот были равны или меньше 5, сравнение групп по качественным бинарным признакам проводилось с использованием критерия Фишера. Критическое значение уровня значимости для величины принималось равным 0,05.
Результаты. Проведенный анализ возрастно-половых характеристик пациентов показал отсутствие статистически значимых различий в группах. Среди больных преобладали мужчины: 60,0% (n=18) в 1 группе и 66,7% (n=14) во 2 группе (p=0,590). Средний возраст пациентов составил 42±12 и 41±15 лет (p=0,793).
В структуре клинических форм в обеих группах преобладал инфильтративный туберкулез легких: 86,7% (n=26) в 1 группе и 85,7% (n=18) во 2 группе (p=0,918). Диссеминированный туберкулез легких встречался в 6,7% (n=2) и 9,5% (n=2) случаев, фиброзно-кавернозный туберкулез в 6,7% (n=2) и 4,8% (n=1) в 1 и 2 группах соответственно (p=0,703 и 0,772).
Проведенная на начальном этапе лечения фи-бробронхоскопия выявила у пациентов преимущественно одностороннее специфическое поражение бронхов: 93,3% (n=28) и 100,0% (n=21) в 1 и 2 группах соответственно (p=0,222), представленное главным образом инфильтративным поражением сегментарных бронхов. У 6,7% (n=2) лиц 1 группы кроме инфильтрации стенки бронха регистрировались ее рубцовые изменения. Сопутствующая неспецифическая патология проявилась диффузным трахеобронхитом разной степени выраженности у 76,7% (n=23) человек в 1 группе и у 81,0% (n=17) больных 2 группы (p=0,733) (табл. 1).
В клинической картине заболевания у пациентов обеих групп превалировали интоксикационный и бронхообструктивный синдромы. Симптомы интоксикации наблюдались у 76,7% (n=23) пациентов 1 группы и 81,0% (n=17) 2 группы (p=0,733), с умеренными и выраженными симптомами соответственно у 56,7% (n=17) и 61,9% (n=13) больных (p=0,722). Нарушение бронхиальной проходимости, проявляющееся продуктивным кашлем, сухими и влажными хрипами в легких, наблюдалось в 70,0% (n=21) случаев в 1
Исходные результаты фибробронхоскопии (ФБС) в группах
Таблица 1
|
Результаты ФБС |
1 группа, n=30 |
2 группа, n=21 |
p |
||
|
абс. |
% |
абс. |
% |
||
|
Одностороннее поражение сегментарных бронхов |
19 |
63,3 |
14 |
66,7 |
p=0,770 |
|
Одностороннее поражение долевых бронхов |
9 |
30,0 |
7 |
33,3 |
p=0,821 |
|
Двусторонний туберкулезный эндобронхит |
2 |
6,7 |
0 |
0 |
|
|
Рубцовые изменения в бронхах |
2 |
6,7 |
0 |
0 |
|
|
Диффузный трахеобронхит 1–2 ст. |
11 |
36,7 |
9 |
42,9 |
p=0,668 |
|
Диффузный трахеобронхит 2–3 ст. |
12 |
40,0 |
8 |
38,1 |
p=0,886 |
Таблица 2
Исходная клиническая и лабораторная характеристика туберкулезного процесса в группах сравнения
Следует отметить, что клинические проявления поражения бронхов были обусловлены не только специфическими изменениями. У значительной доли наблюдаемых пациентов при поступлении диагностировались хронические неспецифические заболевания легких в стадии обострения: 76,7% (n=23) в 1 группе и 81,0% (n=17) во 2 группе (p=0,733), преимущественно представленные хронической обструктивной болезнью легких (ХОБЛ) — 63,3% (n=l9) и 61,9% (n=13) (p=0,942). При исследовании вторичной флоры в мокроте наиболее часто (50,0%) регистрировалась ассоциация Streptococcus pyogenes и
Streptococcus pneumonie, в 23,3% обнаруживались грибы рода Candida.
Как видно из табл. 2, анализ лабораторных данных установил соответствие показателей периферической крови выраженности туберкулезных проявлений. У 76,7% (n=23) и 85,7% (n=18) больных 1 и 2 группы наблюдалось повышение СОЭ, в том числе более 30 мм/ч у 26,7% (n=8) и 23,8% (n=5) соответственно (p=0,811). Умеренный лейкоцитоз регистрировался у 70,0% (n=21) больных, снижение уровня лимфоцитов ниже 20% у 46,7% (n=14). Биохимический анализ крови до лечения у всех пациентов был в пределах физиологической нормы.
Рентгенологически у пациентов, включенных в исследование, преобладали обширные поражения легочной ткани (более доли): у 43,3% (n=13) пациентов 1 группы и 38,1% (n=8) 2 группы (p=0,722).
Таблица 3
Рентгенологические параметры туберкулезного процесса в группах сравнения при поступлении пациентов в стационар
|
Параметр |
1 группа, n=30 |
2 группа, n=21 |
p |
||
|
абс. |
% |
абс. |
% |
||
|
Поражение 1–2 сегментов |
9 |
30,0 |
8 |
38,1 |
p=0,554 |
|
Патология в пределах доли |
8 |
26,7 |
5 |
23,8 |
p=0,811 |
|
Распространенность: 2 доли и более |
13 |
43,3 |
8 |
38,1 |
p=0,722 |
|
Наличие полостей распада, всего |
30 |
100,0 |
21 |
100,0 |
p=1,0 |
|
Единичные полости распада |
10 |
33,3 |
8 |
38,1 |
p=0,714 |
|
Множественные деструкции |
20 |
66,6 |
13 |
61,9 |
p=0,714 |
|
Размеры полостей 4 см и более |
9 |
30,0 |
6 |
28,6 |
p=0,939 |
|
выраженный пневмофиброз |
15 |
50,0 |
9 |
42,9 |
p=0,624 |
Распространенность патологического процесса в пределах одной доли в одном легком либо двух сегментов в обоих легких встречалась в 1 и 2 группах соответственно в 26,7% (n=8) и 23,8% (n=5) случаев (p=0,811); у 30,0% (n=9) и 38,1 % (n=8) больных воспаление было ограничено 1–2 сегментами (p=0,554). Распад легочной ткани диагностирован у всех пациентов, включая множественные деструкции: 66,7% (n=20) и 61,9% (n=13) (p=0,714) и крупные размеры полостей распада: 30,0% (n=9) и 28,6% (n=6) в 1 и 2 группах соответственно (p=0,939) (табл. 3).
Микробиологические характеристики специфического процесса также были сопоставимы в обеих группах. Массивность бактериовыделения соответствовала тяжести туберкулезного процесса: обильное бактериовыделение регистрировалось у 30,0% (n=9) пациентов 1 группы и 28,6% (n=6) во 2 группе (p=0,939), умеренное бактериовыделение — у 43,3% (n=13) и 47,6% (n=10) (p=0,726) в 1 и 2 группах соответственно. Микобактерии туберкулеза методом микроскопии выявлены в 60,0% (n=18) и 81,0% (n=17) случаев (p=0,118). Культуральными методами бактериовыделение регистрировалось у 93,3% (n=28) больных 1 группы (в двух случаях МБТ, выявленные в мазке, не дали роста в посеве) и 100% (n=21) лиц 2 группы (p=0,222). У трети пациентов обеих групп определялась лекарственная устойчивость (ЛУ) к химиопрепаратам: 26,7% (n=8) в 1 группе и 33,3% (n=7) во 2 группе (p=0,646). При этом монорезистентная ЛУ выявлена в 16,7% (n=5) и 23,8% (n=5) случаев (p=0,518), полирезистентность в 10,0% (n=3) и 9,5% (n=2) (p=0,221) в 1 и 2 группах соответственно.
Для оценки переносимости препарата Хиксо-зид проводился ежедневный мониторинг состояния больных 1 группы при ингаляционном введении лекарственного средства. Побочные реакции на препарат отмечены у 16,6% (n=5) пациентов. В 13,3% (n=4) случаев развились нежелательные явления, потребовавшие отмены препарата: у одного больного в первый день применения возник отек, гиперемия лица и верхних конечностей, фебрильная температура; у второго пациента также после первой ингаляции повысилась температура до 38ºС, появился надсадный сухой кашель, тошнота, рвота; у двух пациентов приступообразный сухой кашель, тошнота и рвота возникли на четвертый и седьмой дни аэро-зольтерапии. Предположено, что реакция развилась на компонент препарата — Диоксидин, так как Изониазид перорально переносился удовлетворитель- но. Данные нежелательные реакции купировались в течение суток после отмены препарата и проведения симптоматической терапии. У одного человека (3,3%) побочная реакция в виде приступообразного кашля также развилась на первой неделе, была устранимой и отмены препарата не потребовала. У пациентов 2 группы побочных реакций на ингаляционное введение Изониазида не отмечалось.
Так как у 4 больных Хиксозид был отменен в первые дни использования, оценка результативности терапии в 1 группе проводилась у 26 пациентов.
Анализ клинических и микробиологических признаков в 1-й контрольной точке (сразу по окончании курса аэрозольтерапии) не выявил статистически значимых различий. У трети больных достигнута положительная клиническая динамика в виде нормализации температуры, прибавки массы тела на 1–1,5 кг, снижения СОЭ и лейкоцитоза, прекращения кашля. Катаральные явления в легких при этом у значительной части пациентов еще сохранялись. Негативация мазка мокроты через 21 день ингаляций была зарегистрирована у 33,3% (n=6) пациентов 1 группы и 23,5% (n=4) больных 2 группы (p=0,788). Ретроспективный анализ результатов культурального исследования показал прекращение бактериовыделения в 19,2% (n=5) случаев в 1 группе и 14,3% (n=3) во второй (p=0,180) (рис. 1).
Оценка динамических параметров туберкулезного процесса во 2-й контрольной точке показала сопоставимые результаты у пациентов обеих групп (рис. 2).
Отсутствие симптомов интоксикации, подтвержденное показателями периферической крови, наблюдалось у 61,5% (n=16) больных 1 группы и 52,4% (n=11) пациентов 2 группы (p=0,494); хрипов в легких — у 57,7% (n=15) больных в 1 группе и 47,6% (n=10) во второй (p=0,498). Прекращение бактериовыделения методом посева зарегистрировано у 46,2% (n=12) больных 1 группы и 38,1% (n=8) 2 группы (p=0,584); негативация мазка мокроты — у 57,7% (n=15) пациентов 1 группы и 42,9% (n=9) 2 группы (p=0,312). Первый рентгенологический контроль выявил достижение значительной и умеренной рентгенологической динамики, проявившейся рассасыванием инфильтрации у 42,3% (n=11) и 38,1% (n=8) пациентов в 1 и 2 группах соответственно (p=0,782), рубцеванием полостей распада у 23,1% (n=6) больных в 1 группе и 28,6% (n=6) во 2 группе (p=0,642), и еще у 19,2% (n=5) и 14,3 (n=3) лиц — уменьшением размеров и количества деструкций (p=0,650). Наи-
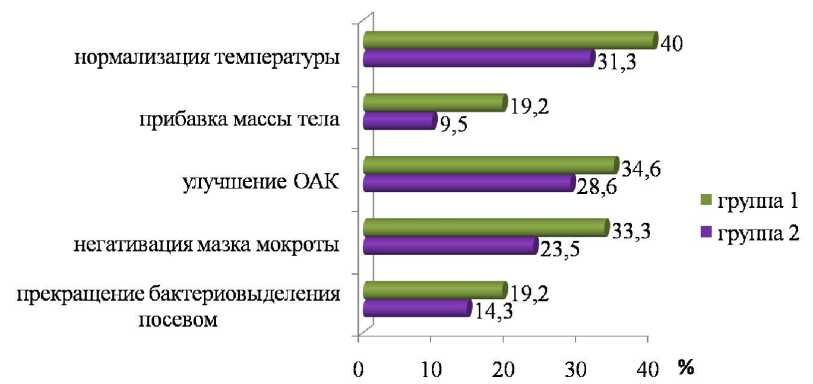
Рис. 1. Клинические и микробиологические показатели в сравниваемых группах в 1-й контрольной точке — после 21 дня ингаляций (различия статистически незначимы)
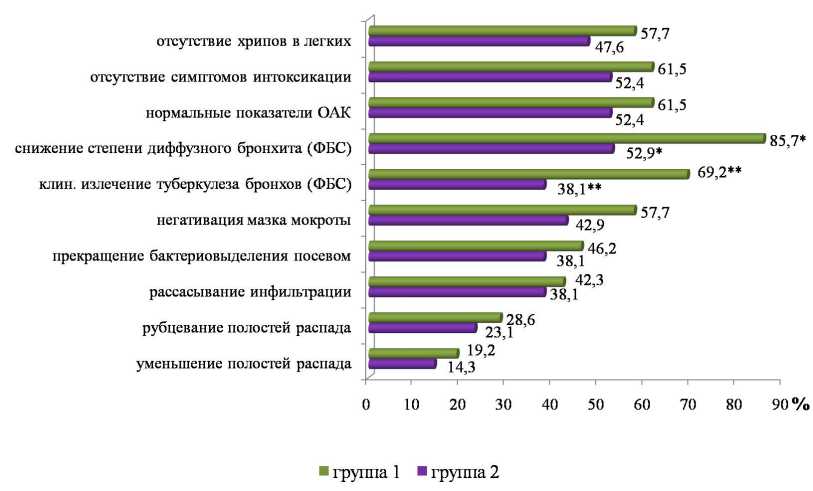
Рис. 2. Динамика клинических, микробиологических и рентгенологических характеристик туберкулезного процесса во 2-й контрольной точке — на 60 дозах химиотерапии (*, ** — различия статистически значимы, p<0,05)
лучшие показатели достигнуты у пациентов с ограниченными исходными поражениями легочной ткани без выраженного фиброза.
Сравнительный анализ результатов контрольной фибробронхоскопии через 2 месяца лечения выявил значительно больший удельный вес излечения туберкулеза бронхов в 1 группе: 69,2% (n=18) против 38,1 % (n=7) во 2 группе (p=0,039) и уменьшения степени диффузного неспецифического бронхита: 85,7% (n=18) в 1 группе против 52,9% (n=9) во 2 группе (p=0,017).
Анализ клинической, микробиологической, рентгенологической динамики туберкулезного процесса по окончании стационарного этапа химиотерапии (3-я контрольная точка) вновь показал отсутствие статистически значимых различий между пациентами 1 и 2 групп по клиническим, микробиологичексим и рентгенолоическим параметрам (рис. 3).
К окончанию интенсивной фазы лечения симптомы интоксикации отсутствовали у всех исследуемых больных; общий анализ крови соответствовал норме у 88,5% (n=23) пациентов 1 группы и 71,4% (n=15) больных 2 группы (p=0,125); прибавка массы тела более 1,5 кг зарегистрирована у 80,8% (n=21) лиц в 1 группе и у 66,7% (n=14) во 2 группе (p=0,310); не вы- слушивались хрипы в легких у 88,5% (n=23) и 76,2% (n=16) пациентов в 1 и 2 группах соответственно (p=0,242).
Негативация мазка мокроты достигнута у всех пациентов обеих групп, бактериовыделение методом посева прекратилось у 80,8% (n=21) больных 1 группы и 71,4% (n=15) лиц 2 группы (p=0,426) и соответствовало удельному весу рубцевания полостей распада.
В 1 группе заживление деструкций при рентгенологическом контроле достигнуто у 80,8% (n=21) пациентов и еще у 19,2% (n=5) отмечено уменьшение размеров и числа полостей распада более чем на ½; значительное рассасывание инфильтрации (на ½ и более). Во 2 группе рубцевание полостей распада зарегистрировано у 61,9% (n=13) больных (p=0,154), уменьшение деструкций у 23,8% (n=5) пациентов (p=0,679), рассасывание инфильтрации у 76,2% (n=16) (p=0,439).
К окончанию интенсивной фазы лечения нивелировались и различия в результатах фибробронхоско-пии, при этом зарегистрирован высокий удельный вес клинического излечения, как специфического — 100% в обеих группах, так и неспецифического брон-
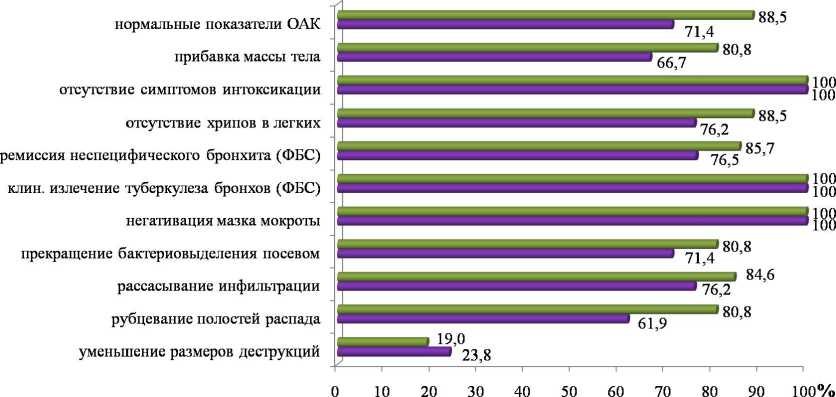
■ группа 1 ■ группа 2
Рис. 3. Динамика туберкулезного процесса в анализируемых группах в 3-й контрольной точке (по окончании интенсивной фазы лечения), p>0,05
хита — 85,7% (n=18) в 1 группе и 76,5% (n=13) во 2 группе (p=0,478).
Несмотря на отсутствие статистически значимых различий в результатах терапии, для достижения выраженной положительной динамики в виде рубцевания полостей распада и прекращения бактериовыделения пациентам наблюдаемых групп потребовались разные сроки лечения. В 1 группе число средних доз у больных с достигнутыми критериями эффективности длительность интенсивной фазы лечения составила 143±27 дней, во 2 группе 164±32 (p=0,019), что может свидетельствовать о лучшей эффективности лечения с применением комбинированного препарата Хиксозид.
Обсуждение. В лечении туберкулезного поражения бронхов немаловажным является не только назначение стандартной химиотерапии, но и использование местного воздействия противотуберкулезных и противовоспалительных средств. Наиболее часто используется ингаляционное введение основного противотуберкулезного препарата Изониазид. В случае выраженной воспалительной реакции слизистой бронхов практикуются дополнительные ингаляции с Диоксидином в качестве противовоспалительного средства. Изученные нами итоги применения комбинированного препарата Хиксозид выявили не только удобство его использования за счет одномоментной ингаляции двух лекарственных средств, но и его высокую эффективность. Оцененные нами результаты применения Хиксозида непосредственно после курса аэрозольтерапии, через 2 месяца от начала химиотерапии (60 доз) и по окончании интенсивной фазы лечения оказались сопоставимы с итогами ингаляционного введения Изониазида при прочих равных условиях. В связи с малочисленностью опубликованных исследований по этой теме, а также различными условиями трактовки результатов, полученных другими авторами, статистическое сравнениене представляется нам достаточно корректным. Так, в работе Барламова О. П. и соавт. [7] учитывалась любая положительная клиническая и рентгенологическая динамика, достигнутая через 60 доз химиотерапии: 86% и 86% соответственно. В нашей работе сделан акцент на значительных положительных сдвигах в клинической (61,5%) и рентгенологической (42,3%) симптоматике. Данные по прекращению бактерио- выделения методом бактериоскопии через 2 месяца лечения оказались сопоставимы: 57,7% в нашем исследовании и 65% по результатам Барламова О. П. и соавт., p=0,593. Так же как и в работе Тюльковой Т. Е. и соавт. [8], проводивших сравнительной изучение введения Хиксозида и комбинации Изониазида с Диоксидином, абациллирование в конце лечения было зарегистрировано нами с одинаковой частотой в изучаемых группах: 80,0% и 71,4%, p=0,426.
В отличие от других работ, в нашем исследовании впервые проведен сравнительный анализ ингаляционного применения Хиксозида и Изониазида, включая результаты контрольной фибробронхоскопии через 2 месяца и по окончании интенсивной фазы лечения, который показал лучшую эффективность Хиксозида на 60 дозах химиотерапии. Впервые были получены данные о сокращении сроков лечения пациентов, получивших Хиксозид, присопоставимости итоговой эффективности лечения.
Различной оказалась оценка переносимости Хиксозида. По данным Барламова О. П. и Тюлько-вой Т. Е., побочных реакций на Хиксозид зафиксировано не было, мы же получили 16,6% нежелательных реакций, развившихся в первые дни применения.
Заключение. Применение нового отечественного препарата Хиксозид в ингаляционной форме у больных с наличием специфического поражения бронхов показало его высокую эффективность при удовлетворительной переносимости. Удельный вес побочных реакций на Хиксозид составил 16,6% и по преимуществу был связан с его компонентом Диоксидином. У 13,3% пациентов нежелательные реакции потребовали отмены препарата, но не отразились на состоянии здоровья в дальнейшем и не сказались на изменении схемы химиотерапии. На 60 дозах химиотерапии у пациентов, получивших аэрозольтерапию Хиксозидом, по данным фибробронхоскопии, достоверно чаще достигалось клиническое излечение туберкулеза бронхов (69,2% против 38,1 %, p=0,039), а также значительные улучшения в течении неспецифического эндобронхита по сравнению с контрольной группой (85,7% против 52,9%, p=0,017). При достижении равных показателей результативности интенсивной фазы лечения в группах сравнения, у больных, получавших Хиксозид, сроки стационарного лечения были сокращены в среднем на 20 дней за счет более раннего достижения основных критериев эффективности: заживления деструкций и прекращения бактериовыделения.
Список литературы Опыт использования хиксозида в терапии туберкулезного поражения бронхов
- Киселева Ю.Ю., Васильева И.А., Казённый Б. Я. и др. Актуальные вопросы лечения больных туберкулезом в современных условиях и факторы, влияющие на эффективность химиотерапии. Туберкулез и болезни легких 2012; (9): 16-21
- Туберкулез в Российской Федерации, 2010 г.: аналитический обзор статистических показателей, используемых в Российской Федерации. М., 2011; 280 с.
- Смердин С. В., Богородсткая Е.М., Стерликов С. А. и др. Эффективность стандартных режимов химиотерапии при туберкулезе легких с бактериовыделением.Туберкулез и болезни легких 2012; (2): 24-32
- Кузиев А. А, Парпиева H.H., Иргашев А.А. Поражение бронхов при ограниченных и распространенных формах туберкулеза легких. Туберкулез и болезни легких 2011; (4): 220
- Хиксозид (HIKSOZID). Инструкция к применению. http://www.vidal.ru/poisk_preparatov/hixozid__28752.htm (дата обращения 20.03.2013)
- Глушков P. Г., Соколова Г. Б. Новый противотуберкулезный препарат Хиксозид. Антибиотики и химиотерапия 2008; 53 (5-6): 11-13
- Варламов О. П., Пеленёва И.М., Рей-хард В. В. Результаты применения Хиксозида в комплексной терапии больных распространенными формами туберкулеза легких. Фтизиатрия и пульмонология 2013; 1 (6). URLhttpV/ftiziopulmo.ru (дата обращения 18.06.2013)
- Тюлькова Т. E., Корначев А. О, Козлов Н. В. Опыт применения препарата Хиксозид. В кн.: Сборниктрудов конгресса: XXII Национальный конгресс по болезням органов дыхания; под. ред. акад. А. Г. Чучалина. М.: ДизайнПресс, 2012; с. 293
- Приказ Министерства здравоохранения РФ от 21 марта 2003 года № 109 «О совершенствовании противотуберкулезных мероприятий в Российской Федерации». http://law7.ru/legal2/se5/pravo510/index.htm (дата обращения 04.04.2013).
- Приказ Министерства здравоохранения РФ от 13 февраля 2004 года № 50 «О введении в действие учетной и отчетной документации мониторинга туберкулеза», http://www.garant.ru/products/ipo/prime/doc/6229299/(дата обращения 18.02.2014).


