Опыт локального воздействия на септический очаг при деструктивном коксите
Автор: Чернигов С.Ю., Чернигова С.В., Зубкова Н.В.
Журнал: Вестник Омского государственного аграрного университета @vestnik-omgau
Рубрика: Ветеринария и зоотехния
Статья в выпуске: 1 (49), 2023 года.
Бесплатный доступ
Представлен обзор современных экспериментальных исследований, посвященных проблеме лечения глубокой хирургической инфекции тазобедренного сустава, также проведен анализ существующих материалов, используемых для изготовления имплантатов (спейсеров) крупных суставов. У гнойного воспаления тазобедренного сустава (коксит) ведущее место в структуре ортопедических заболеваний. Это может быть результатом ятрогенного инфицирования, осложненных переломов, артритов. Существует несколько классификаций гнойного коксита, которые характеризуют степень и глубину развития гнойного воспаления. Анамнез и клинические проявления являются первичными критериями при подозрении на инфекцию в суставе, в дальнейшем диагноз должен быть подтвержден с помощью основных и вторичных диагностических показателей. Выделение возбудителя и получение развернутой антибиотикограммы вместе с хирургическим лечением (артротомия с имплантацией спейсера) имеют решающее значение для определения комплексной стратегии антибиотикотерапии больного животного. По мнению большинства авторов, успешным исходом коксита является установка временного имплантата с антибиотиком. Спейсер - это устройство на основе биосовместимых материалов, таких как металл, полиметилметакрилат, полиэтилен, с включением антимикробных средств, которое позволяет временно заполнить имеющиеся дефекты сустава. Спейсер с антибиотиком помогает заполнить образовавшееся после резекции пространство и обеспечивает высокую локальную концентрацию антимикробных средств. Преимущества спейсера - в более высокой элюции антибиотиков с поверхности имплантата, способности заместить фрагмент отсутствующей кости в проксимальном отделе бедра / вертлужной впадине. Применение спейсера рассматривается как этиотропное и патогенетическое лечение перед последующим эндопротезированием. В изученной литературе описаны лишь единичные случаи применения спейсеров тазобедренного сустава у животных с гнойным кокситом.
Гнойная хирургия, воспаление, коксит, тазобедренный сустав, антимикробная терапия, спейсер
Короткий адрес: https://sciup.org/142237263
IDR: 142237263 | УДК: 619:616.72-002.1-022 | DOI: 10.48136/2222-0364_2023_1_128
Experience of local exposure to septic foci in destructive coxitis
The article presents an overview of modern experimental studies devoted to the problem of the treatment of deep surgical infection of the hip joint, as well as an analysis of existing materials used for the manufacture of implants (spacers) of large joints. Purulent inflammation of the hip joint (coxitis) occupies a leading place in the structure of orthopedic diseases. Such inflammation may be the result of iatrogenic infection, complicated fractures, arthritis. There are several classifications of purulent coxitis, which characterize the degree and depth of development of purulent inflammation. Anamnesis and clinical manifestations are the primary criteria for suspected infection in the joint, further diagnosis should be confirmed with the help of basic and secondary diagnostic indicators. Isolation of the pathogen and obtaining a detailed antibiogram together with surgical treatment (arthrotomy with spacer implantation) are crucial for determining a comprehensive strategy for antibiotic therapy of a sick animal. According to most authors, the successful outcome of coxitis is the installation of a temporary implant with an antibiotic. Spacer is a device based on biocompatible materials, such as metal, polymethylmethacrylate, polyethylene, with the inclusion of antimicrobial agents, which is used to temporarily fill the joint cavity. A spacer with an antibiotic helps to fill the space formed after resection, and provides a high local concentration of antimicrobial agents. The advantages of the spacer are a higher elution of antibiotics from the implant surface, the ability to replace a fragment of missing bone in the proximal femur / acetabulum. The use of spacer is considered as an etiotropic and pathogenetic treatment before subsequent endoprosthetics. In the studied literature, only isolated cases of the use of hip joint spacers in animals with purulent coxitis are described.
Текст обзорной статьи Опыт локального воздействия на септический очаг при деструктивном коксите
Присоединение гнойного воспаления при повреждениях крупных суставов остается острой проблемой для травматологов ветеринарной и гуманитарной медицины на протяжении многих лет. Около 80% случаев хромоты животных – результат травматических артритов [1; 2]. Комплексный термин применяется для обозначения изменений в суставе, индуцированном механическим воздействием на него. Таким образом, воспаление тазобедренного сустава (ТС) – коксит – наиболее часто диагностируемое заболевание в ветеринарии, в то время как случаи гнойной инфекции тоже не редкость.
В литературе авторы предлагают подразделять заболевание в зависимости от этиологического фактора, при этом кокситы могут быть первичными и вторичными [3]. Первичный воспалительный процесс возникает чаще при открытых травматических повреждениях суставов с проникновением инфекции через раневой канал, реже в связи с хирургическим вмешательством на суставы. При вторичном коксите наиболее вероятным путем заражения является гематогенный, когда инфекция распространяется из различных гнойных очагов. Воспаление при септическом артрите может развиваться в суставной сумке и внутри синовиальной оболочки, впоследствии распространяться на окружающие мягкие ткани и внутрисуставные части костей. Такого рода анатомотопографическая градация позволяет выделить формы септического артрита тазобедренного сустава: синовит, панартрит, остеоартроз. Гнойный коксит сопровождается у животных хронической болью и обширным разрушением вертлужной впадины и головки бедренной кости. Различают поверхностные и глубокие местные инфекционные процессы [4]. К поверхностным относят подкожное гнойное воспаление, лигатурные свищи, инфицированные гематомы, краевой некроз раны и т.д. Глубокая хирургическая инфекция тазобедренного сустава возникает в виде флегмоны (параоссальной, межмышечной), перипротезной инфекции, послеоперационного остеомиелита [5; 6]. Гнойный коксит может протекать с проявлением эмпиемы сустава с накоплением гнойного экссудата в межмышечных пространствах. Септическое воспаление сустава сопровождается морфофункциональным изменением и разрушением вертлужной впадины и головки бедренной кости, как правило, это приводит к анкилозу, патологическим вывихам бедренной кости [7]. От начала заболевания до появления клинических симптомов деструкции суставного хряща может пройти несколько суток, поэтому септический артрит тазобедренного сустава следует рассматривать как острое хирургическое заболевание, при котором немедленно необходимы диагностические и лечебные мероприятия.
Цель обзора – проанализировать зарубежную и отечественную литературу, опубликованную за последние 15 лет, посвященную лечению септического артрита тазобедренного сустава.
Материалы исследования
Научная статья основана на поиске научной ветеринарной и медицинской литературы в отечественных и зарубежных рецензируемых базах данных за 2009–2022 гг.
Vestnik of Omsk SAU, 2023, no. 1(49)
VETERINARY AND ZOOTECHNY
(Elibrary, PubMed, Scopus), также использовали поисковую систему Google; в ней статьи ограничивались ключевыми словами: antibacterial spacer, hip spacer. Так, в результате поиска «antibacterial spacer» найдено 1181 работа на базе PubMed и 1553 ((Elibrarу), «hip spacer» – 521 работа (PubMed); 621 работа (Elibrarу) (рисунок). В системе Google найдены статьи, отражающие тематику существующих спейсерных систем, их структурных, антибактериальных и механических свойств. Для написания статьи отобрали 78 статей, 84% из них за последние 5 лет.
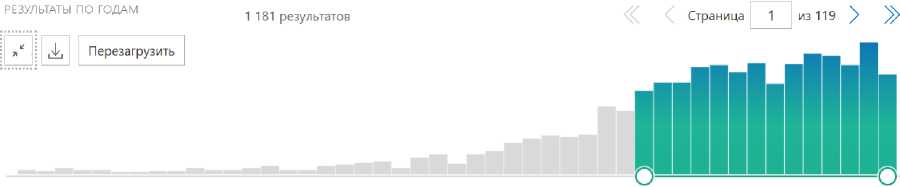
2009 2022
Результаты поиска на базе «PubMed»
Существующие методы лечения животных с гнойным кокситом . Тактика лечения гнойно-воспалительных заболеваний заключается в проведении комплекса хирургических мероприятий и послеоперационной реабилитации. Обязательным этапом всех хирургических методов лечения гнойного коксита является резекция некротизированных тканей как единственный способ удаления микробных конгломератов. Аналог указанного выше способа – хирургическое вмешательство в сустав, включающее артротомию, иссечение гнойного содержимого и нежизнеспособных тканей с последующим дренированием [8]. Пораженные суставные элементы удаляются, после проводят обязательную иммобилизацию оперированного сустава с помощью ортопедического ортеза. Недостатки этого способа: ограничение функциональных возможностей животного, образовавшийся дефицит костной и/или других тканей, развитие рубцов в области сустава. В случае глубокого гнойного процесса с распространением деструкции на головку бедренной кости проводят хирургическое вмешательство по резекции патологического участка с последующей стабилизацией конечности устройствами фиксации [9; 10].
Быстрое восстановление опорной способности конечности зависит от направленной антимикробной терапии патологической области, сохранения анатомических взаимоотношений в суставе (конгруэнтности) и обеспечения оптимальной функциональности. Фундаментальным направлением борьбы с инфекцией опорно-двигательного аппарата, несомненно, является антибактериальная терапия. Известны варианты консервативного лечения гнойного артрита, заключающиеся в медикаментозной системной терапии, а также доставке препарата непосредственно в очаг инфекции [11; 12]. Высокая концентрация антибиотика в пораженном очаге позволяет эффективно действовать на патогенную микрофлору, при этом побочные эффекты на органах и системах организма не возникают. Для борьбы с инфекцией в суставе было предложено множество вариантов локальной доставки антимикробного средства к очагу поражения – от инфильтрационной пропитки околосуставной сумки и инъекции в сустав до формирования источника химиотерапии с помощью различного рода «носителей» [6; 8; 9].
Применение спейсеров в лечении гнойных кокситов. Спейсер используется для временного заполнения полости сустава в период между удалением некротизиро-
Vestnik of Omsk SAU, 2023, no. 1(49) VETERINARY AND ZOOTECHNY ванных фрагментов тканей и последующей установкой постоянного эндопротеза [13]. Использование временного биокомпозиционного устройства с антибиотиками – достаточно распространенная операция для поддержания функции тазобедренного сустава и одновременного обеспечения локального воздействия антимикробных средств.
Первое упоминание об использовании спейсеров у людей при лечении глубокой перипротезной инфекции относится к 1988–1989 г. [14]. В 1992 г. компания «DePuy» (США) представила первое промышленное артикулирующее устройство для коленного сустава PROSTALAC.
Прогресс мировой науки в области биотехнологий позволил современные полимерные материалы использовать для депо антибиотиков при лечении гнойно-воспалительных заболеваний опорно-двигательной системы. Широкую известность получили такие материалы, как полиметилметакрилат, полиэтилен, металл, которые стали основой современных биокомпозиций (спейсеров), в их составе вещества, обладающие антимикробной активностью.
Сегодня существует несколько технологий создания антибактериальных спейсе-ров: производственные и интраоперационные. В период проведения операции хирург изготавливает имплантат с использованием метода литья в формы или формирует на стадии полимеризации. Отметим, что спейсер должен соответствовать ряду необходимых требований: простоте конструкции; антимикробной активности; созданию условий для восстановления опороспособности конечности; сохранению функции; подготовке к последующему ревизионному эндопротезированию [14; 15].
Промышленные имплантаты наиболее просты в использовании, имеют высокую однородность основного материала, равномерное распределение противомикробных химиотерапевтических средств по всему объему спейсера, точные пропорции компонентов, требуемый уровень стерильности. Производители, а это в основном зарубежные компании, предлагают также различные модификации спейсеров: с продольными каналами, отверстиями, с ножкообразными выступами, с увеличенной площадью поверхности самого имплантата и многое другое. Это значительно увеличивает скорость выполнения самой операции. Однако при использовании имплантатов возникает необходимость разнообразных спейсеров, в том числе с различными антибактериальными средствами и их комбинациями. У таких устройств высокая стоимость, а также «привязанность» к конкретным производителям (а их в мире не так много), специализирующимся на изготовлении лечебных имплантатов. «Привязанность» к этим имплантатам в настоящее время может стать серьезным вызовом для травматологов, т.к. в современных условиях, в связи с введением санкций, отечественное импортозамещение соответствующих изделий недостаточно (или полностью отсутствует); реалии значительно ограничивают или вообще делают невозможным выполнение таких операций. Использование же динамических спейсеров позволяет хирургу самостоятельно делать выбор в отношении тех или иных биокомпозиций с набором необходимых свойств (вязкость, наличие (отсутствие) антимикробного компонента в составе). Преимущество – в доступности приобретения необходимых компонентов и возможности добавлять в матрицу необходимое количество антибиотика, соответствующего типу возбудителя и его чувствительности.
Спейсеры условно можно разделить на две основные группы – неартикулирующие и артикулирующие. Изначально спейсеры TC изготавливали статичными однокомпонентными, то есть неартикулирующими, но вскоре после их широкого применения получены результаты, свидетельствующие о большом количестве послеоперационных осложнений (в виде частых вывихов, переломов костных структур, образования
Vestnik of Omsk SAU, 2023, no. 1(49) VETERINARY AND ZOOTECHNY контрактур, развития дистрофических процессов в мышцах бедра). Эти факторы значительно осложняли последующую ревизионную операцию и приводили к неудовлетворительным результатам реабилитации. Неартикулирующие имплантаты заменили на двух- и трехкомпонентные шарнирные (артикулирующие), в значительной степени повысив эффективность выполняемых операций. Многокомпонентность спейсера TC обеспечивала расширение показаний для выполнения операций, сохранения анатомических и функциональных взаимосвязей в суставе и конечности в целом. Одним из прототипов полезной модели артикулирующих имплантатов стал бедренный компонент, он выполнен в виде металлической ножки, покрытой биокомпозиционным материалом с антибиотиком широкого спектра действия, и тазовый компонент, изготовленный из того же материала [16].
Механизм терапевтического действия спейсеров заключается в периодическом высвобождении из поверхностного слоя биокомпозиционного материала антибиотика в окружающие ткани от 3 до 6 мес. Первичная установка спейсера обеспечивает высокую концентрацию антибиотика в полость сустава для подавления микрофлоры уже с первых часов после операции [17]. Подбор антибиотика осуществляют в соответствии с предварительным анализом чувствительности микрофлоры, а размер спейсера – в соответствии с индивидуальными параметрами дефекта костных элементов сустава. При подборе и установке имплантата происходит полное восстановление длины конечности с учетом напряжения параартикулярных мышц бедра, что позволяет максимально сохранить функциональность конечности и обеспечивает локальное подавление инфекционного процесса на протяжении всего постоперационного периода.
Эффективность этиотропной терапии обеспечивается предварительной верификацией возбудителя с определением его чувствительности к антибиотикам, давая возможность выбрать наиболее подходящий препарат для спейсера. Традиционно антимикробный препарат для добавления в биокомпозиционный материал определяется на основании микробиологического исследования по изучению чувствительности высеянных из инфекционного очага микроорганизмов. В различных исследованиях авторы научных статей сообщают о достаточно широком спектре химиотерапевтических препаратов, используемых при изготовлении спейсеров, но чаще всего описано применение гентамицина, ванкомицина и тобрамицина, реже – цефалоспоринов, аминогликозидов, пенициллина.
Имеются данные о применении некоторых антибиотиков, например, рифампицина, способствующих разрушению микробной биопленки, но при добавлении в биоком-позиционный материал значительно снижающих его механическую прочность. Другие авторы сообщают о попытке ввести в состав спейсеров антисептические вещества, такие как серебро, цинк, медь и другие, но такие работы носят единичный характер [18]. Эти исследования основываются на том, что в эксперименте на животных внутривенное введение наночастиц меди при генерализованной инфекции, вызванной синегнойной палочкой и золотистым стафилококком, показало большую эффективность по сравнению с цефтриаксоном. Это многообещающие исследования, открывающие новую страницу в лечении септических осложнений.
Наряду с этим имеются клинические исследования, показывающие, что не все антибиотики можно смешивать с биокомпозиционными материалами, т.к. теряется их биодоступность. Также не рекомендованы к применению антибиотики с термической нестабильностью. Имеются данные, что ряд антибиотиков при совместном использовании может способствовать усиленному вымыванию друг друга из матрицы спейсера, не обеспечивая выраженного противомикробного эффекта на всем этапе ле-
Vestnik of Omsk SAU, 2023, no. 1(49) VETERINARY AND ZOOTECHNY чения. Известны синергические эффекты от применения двух и более антибиотиков, когда происходит пиковое высвобождение отдельных компонентов. В литературе есть сведения о комбинации некоторых антибактериальных препаратов, а также о том, что повышение концентрации антибиотика более чем на 10% снижает механическую прочность самого имплантата [19].
Способы доставки антибактериальных препаратов в полость пораженного сустава до сих пор вызывают научную дискуссии, но большинство авторов склоняются к использованию смеси антибиотиков в биокомпозиционном материале. Противники двухэтапной методики лечения кокситов, предусматривающей установку антимикробного спейсера, высказываются о невозможности создания длительной эффективной концентрации антибиотика в очаге инфекции. По их мнению, в результате такого лечения сам спейсер может служить основой для адгезии и образования на нем микробной биопленки [20; 21]. Это значительно снижает эффективность купирования инфекции, особенно если последняя вызвана полирезистентными штаммами бактерий и/или микробными ассоциациями с их участием [22; 23].
Известно, что максимальный выход антибиотика происходит с поверхности спей-сера. Антибактериальные препараты из внутренних частей спейсера из-за высокой плотности структуры биокомпозиционного материала практически не выделяются во внутрисуставную среду. Таким образом, по мнению некоторых ученых, насыщение всего объема биокомпозиционного материала антибиотиками при изготовлении спей-сера неэффективно за счет снижения прочностных характеристик имплантата, не выраженного локального антимикробного воздействия, и считается экономически нецелесообразным.
Исходя из этих исследований, для повышения терапевтической эффективности спейсера необходимо увеличить площадь поверхности, содержащую антимикробакте-риальные вещества, способную к дозированному длительному выходу препарата, и одновременное обеспечить достаточно прочностные характеристики имплантата. В то же время в работах, посвященных изучению характеристик элюирования и антибактериальной активности биокомпозиционного материала, содержащего противотуберкулезные препараты, подтверждено: ряд препаратов сохраняют свое антимикобактериальное действие в составе биокомпозиционного материала после реакции полимеризации [24]. В исследовании in vitro, проведенном теми же авторами, такие свойства определяли в течение 30 дней в порошковой форме изониазида и стрептомицина, в течение недели в амоксициллине и клавуланате, в течение 30 дней в композициях изониазида и рифампицина с использованием высоких доз рифампицина (4 г на 40 г биокомпозиционного материала).
Другие ученые приводят результаты исследований, свидетельствующие о том, что нерассасывающийся биокомпозиционный материал может быть местом формирования устойчивости к антибиотикам, местом адгезии микроорганизмов и их роста [25]. Одни авторы предлагают дополнительно вводить антибиотики, к примеру ванкомицин, в композиционный материал с гентамицином, другие – наносить его на поверхность спейсера во время изготовления [26; 27]. В то же время авторы подобных изобретений не подтверждают долгосрочный антимикробный эффект спейсера.
Электростатическое поле, поверхностное натяжение, силы Ван-дер-Ваальса, гидрофобность и водородные связи приводят к неспецифическому взаимодействию бактерий и поверхности имплантата. Некоторая избирательность микроорганизмов к имплантатам зависит от материала, например, адгезия штаммов Staphylococcus epidermidis происходит лучше к полимерным частям эндопротеза, а S. штаммов aureus – к металлу
Vestnik of Omsk SAU, 2023, no. 1(49) VETERINARY AND ZOOTECHNY
-
[28] . В связи с этим в дальнейшем при оценке антимикробного действия предлагаемой антимикробной композиции в качестве тест-штамма используют Staphylococcus epidermidis. В качестве прототипа для наиболее близкой к технической сущности авторы выбрали антимикробную композицию для формирования спейсера на основе био-композиционного материала с гентамицином. Продолжительность антимикробного действия антимикробной композиции, выбранной в качестве прототипа, составляет 56 дней [29].
Наряду с этим в некоторых исследованиях зафиксировано: при использовании антибактериальных спейсеров может возникать ряд осложнений, таких как вывих, переломы имплантатов, бедренных и тазовых костей. Для профилактики таких механических повреждений авторы предполагают использование различных типов металлических каркасов: интрамедуллярных штифтов, ножек эндопротеза, стержней Штеймана, винтов. В случаях, когда инфекционный процесс распространяется в костномозговой канал бедренной кости, спейсеры изготавливают с более длинной «ножкой» для заполнения инфицированной полости биокомпозиционным материалом с антибиотиком или используют различные биоразлагаемые материалы с антимикробными химиотерапевтическими препаратами [30]. Но и эти авторы говорят, что одна из основных проблем при местном применении противомикробных препаратов в целом – появление резистентных микроорганизмов. Это происходит, если уровень антибиотиков падает ниже минимальной ингибирующей концентрации. К сожалению, даже после подавления воспалительного процесса функцию пораженного сустава не удается сохранить, поскольку значительно выражен дефект проксимального отдела бедренной кости, движения ограничены в суставе, происходит укорочение конечности, требуется эндопротезирование тазобедренного сустава [31; 32].
Заключение
Применение антибактериального спейсера тазобедренного сустава позволяет эффективно купировать гнойное воспаление, сохранить анатомические и функциональные взаимосвязи суставных поверхностей, создать депо антибиотика с постепенным его выделением в очаг инфекции. Успех операции зависит от многих факторов: мастерства хирурга, наличия сопутствующих заболеваний, наличия надлежащей реабилитации после операции. Сочетание комплекса факторов позволяет обеспечить оптимальные условия для эндопротезирования сустава, несомненно, при условии ремиссии воспаления.
Список литературы Опыт локального воздействия на септический очаг при деструктивном коксите
- Чернигова С.В., Чернигов С.Ю. Возможности лечения животных с гнойным кокситом // Актуальные проблемы ветеринарной науки и практики: материалы национальной науч.-практ. онлайн-конференции факультета ветеринарной медицины ИВМиБ ФГБОУ ВО Омский ГАУ, Омск, 13 ноября 2020 года. Омск: ФГБОУ ВО Омский ГАУ. 2020. С. 46–48.
- Дочилова Е.С., Чернигова С.В., Чернигов Ю.В. Нарушение функции опорно-двигательного аппарата у животных на примере ветеринарных клиник города Омска // Омский научный вестник. 2015. № 2(144). С. 207–209.
- Тимофеев С.В., Филиппов Ю.И., Концевая С.Ю. и др. Общая хирургия животных: учебник для студентов вузов, обучающихся по специальности 111201 «Ветеринария». М.: Зоомедлит. 2007. 687 с.
- Трояновская Л.П., Белогуров А.Н. Ветеринарная хирургия, ортопедия и офтальмология: учеб. пособие для студентов высших учебных заведений, обучающихся по направлению подготовки (специальности) 111801 – Ветеринария (квалификация (степень) «специалист»). Воронеж: Воронежский государственный аграрный университет им. Императора Петра I. 2011. 285 с.
- Чернигова С.В., Чернигов Ю.В. Современные принципы классификации сепсиса животных // Вестник ветеринарии. 2013. № 1(64). С. 47–49.
- Schrader S.C. Septic arthritis and osteomyelitis of the hip in six mature dogs. J Am Vet Med Assoc. 1982;181(9):894-8. PMID: 7141987.
- Савинцев А.М., Малько А.В. Выбор операции эндопротезирования тазобедренного сустава при анкилозах после гнойных заболеваний // Избранные вопросы хирургии тазобедренного сустава. СПб.: Российский ордена Трудового Красного Знамени научно-исследовательский институт травматологии и ортопедии им. Р.Р. Вредена. 2016. С. 207–212.
- Безрук Е.Л. Бактериологическая характеристика эффективности различных способов дренирования случайных ран // Вестник Ульяновской государственной сельскохозяйственной академии. 2020. № 2(50). С. 156–162.
- Ariza J., Euba G., Murillo O. Orthopedic device-related infections. Enferm Infecс Microbiol Clin. 2008;26(6):380-390.
- Чернигов Ю.В., Чернигова С.В., Чернигов С.Ю. Морфо-функциональное обоснование применения цементных спейсеров при лечении животных с остеомиелитом вертлужной впадины (экспериментальное исследование) // Биотехнология: состояние и перспективы развития: материалы IX Междунар. конгресса, Москва, 20–22 февраля 2017 года. М.: РЭД ГРУПП. 2017. С. 41–42.
- Regis D., Sandri A., Rizzo A., Bartolozzi P. A preformed temporary antibiotic-loaded cement spacer for the treatment of destructive septic hip arthritis: a case report. Int J Infect Dis. 2010 Mar; 14(3):e259-61. DOI 10.1016/j.ijid.2009.04.019. PMID: 19664951.
- Привольнев В.В., Родин А.В., Каракулина Е.В. Местное применение антибиотиков в лечении инфекций костной ткани // Клиническая микробиология и антимикробная химиотерапия. 2012. Т. 14. № 2. С. 118–131.
- Cho Y.J., Patel D., Chun Y.S., Shin W.J., Rhyu K.H. Novel Antibiotic-Loaded Cement Femoral Head Spacer for the Treatment of Advanced Pyogenic Arthritis in Adult Hip. J Arthroplasty. 2018;33(6): 1899-1903. DOI 10.1016/j.arth.2017.12.028. PMID: 29361346.
- Шпиняк С.П., Барабаш А.П., Лясникова А.В. Использование спейсеров при лечении инфекционных осложнений при полной замене коленного колеса // Современные проблемы науки и образования. 2015. № 5. С. 3.
- Pinsornsak P., Niruktisarn T., Surabotsopon P., Boontanapibul K. Novel molded antibiotic cement spacer: is it better than handmade cement spacer for treatment of chronically infected total hip arthroplasty? Int Orthop. 2022 Aug; 46(8):1693-1700. DOI 10.1007/s00264-022-05456-4. PMID: 35678842
- Jones C.W., Selemon N., Nocon A., Bostrom M., Westrich G., Sculco P.K. The Influence of Spacer Design on the Rate of Complications in Two-Stage Revision Hip Arthroplasty. J Arthroplasty. 2019;34(6):1201-1206. DOI 10.1016/j.arth.2019.02. 012. PMID: 30879874.
- William C.C.H., Simmrat S., Suhaeb A.M. Antibiotic-laden Arthroplasty with a Novel Design of Cement Mould and Metallic Endoskeleton for Treatment of Hip Infection, an Inexpensive Alternative: A Preliminary Report of Two Cases. Malays Orthop J. 2017; №11(2):78–81. DOI 10.5704/MOJ.1707.015.
- Бабушкина И.В., Мамонова И.А., Гладкова Е.В. Этиологическая роль возбудителей хронического остеомиелита и влияние наночастиц меди на клинические штаммы Staphylococcus aureus // Вестник Пермского университета. Серия «Биология». 2014. № 2. С. 52–56.
- Шевченко Ю.Л., Стойко Ю.М., Грицюк А.А. и др. Локальная антибиотикопрофилактика при эндопротезировании крупных суставов (литературный обзор) // Вестник французского медико-хирургического центра им. Н.И. Пирогова. 2010. № 3.
- Белов Б.С. Бактериальный (септический) артрит и инфекция протезированного сустава: современное состояние проблемы // Качество жизни. Медицина. 2008. № 5. С. 18–23.
- Faschingbauer M., Reichel H., Bieger R., Kappe T. Mechanical complications with one hundred and thirty eight (antibiotic-laden) cement spacers in the treatment of periprosthetic infection after total hip arthroplasty. Int. Orthop. 2015;5:989-994. DOI 10.1007/s00264-014-2636-z
- Чернигова С.В., Чернигов Ю.В. Роль провоспалительных медиаторов в развитии септических осложнений у животных // Ветеринарная патология. 2011. № 1–2(36). С. 92–96.
- Greig J.M., Wood M.J. Staphylococcus lugdunensis vertebral osteomyelitis. Clin. Microbiol. Infect. 2003;11:1139-1141.
- Патент на полезную модель № 201180 U1 Российская Федерация, МПК A61B 17/56, A61F 2/32. Спейсер тазобедренного сустава: № 2020121570: заявл. 29.06.2020: опубл. 01.12.2020 / Е.О. Перецманас, Т.Е. Тюлькова, В.С. Зубиков и др. ; заявитель Федеральное государственное бюджетное учреждение «Национальный медицинский исследовательский центр фтизиопульмонологии и инфекционных заболеваний» Министерства здравоохранения Российской Федерации (ФГБУ «НМИЦ ФПИ» Минздрава России).
- Виденин В.Н. Послеоперационные гнойно-воспалительные осложнения у животных (профилактика и лечение): учеб. пособие. СПб.: Лань. 2000. 160 с.
- Патент № 2707734 C1 Российская Федерация, МПК A61K 31/7036, A61F 2/28, A61L 27/54. Антимикробная композиция для формирования спейсера: № 2019109897: заявл. 03.04.2019: опубл. 29.11.2019 / А.Г. Афиногенова, Г.Е. Афиногенов, С.А. Линник [и др.] ; заявитель Федеральное бюджетное учреждение науки «Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Федеральное государственное бюджетное образовательное учреждение высшего образования «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Министерства здравоохранения Российской Федерации, Федеральное государственное бюджетное образовательное учреждение высшего образования «Санкт-Петербургский государственный университет». EDN ZCKQCJ.
- Патент № 2556622 C2 Российская Федерация, МПК A61B 17/56. Способ лечения гнойного артрита: № 2013142978/14: заявл. 20.09.2013: опубл. 10.07.2015 / И.Ф. Ахтямов, Х.Г. Исмаилов, Э.Б. Гатина и др. EDN THKCWD.
- Lin M., Chang F., Hua M., Wu Y., Liu S. Inhibitory Effects of 1,2,3,4,6-Penta-O-Galloyl-?-d-Glucopyranose on Biofilm Formation by Staphylococcus aureus. Antimicrob. Agents Chemother. 2011;55: 1021–1027.
- Luther J.F., Cook J.L., Stoll M.R. Arthroscopic exploration and biopsy for diagnosis of septic arthritis and osteomyelitis of the coxofemoral joint in a dog. Vet Comp Orthop Traumatol. 2005;18(1):47-51. PMID: 16594217
- Комаров Р.Н., Митрофанов В.Н., Новиков А.В., Королев С.Б. Тактика лечения инфекционных осложнений после эндопротезирования тазобедренного сустава // Травматология и ортопедия России. 2016. № 22(4). С. 25–34.
- Schwaller C.A., Elke R. Cement removal with ultrasound in revision or total hip prosthesis. German. Orthopade. 2001;30;5:310-306.
- Тихилов Р.М., Шаповалов В.М., Шубняков И.И. и др. Руководство по эндопротезированию тазобедренного сустава ; Российский научно-исследовательский институт травматологии и ортопедии им. Р.Р. Вредена. СПб. 2008. 324 с.


