Опыт применения ниволумаба в терапии предлеченных пациентов с метастатической меланомой кожи
Автор: Самойленко И.В., Жуликов Я.А., Харкевич Г.Ю., Петенко Н.Н., Демидов Л.В.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Профилактика, диагностика и лечение онкологических заболеваний
Статья в выпуске: 3 т.8, 2018 года.
Бесплатный доступ
Появление анти-PD-1-препаратов значительно улучшило прогноз пациентов с метастатической меланомой кожи. Однако в международной литературе накоплено мало данных по эффективности этих препаратов во второй и последующих линях терапии. Нами проанализирован собственный опыт применения ниволумаба в терапии метастатической меланомы кожи. В данное нерандомизированное неконтролируемое сплошное исследование были включены 53 пациента с метастатической или нерезектабельной меланомой, из которых 86,8 % (46) получили две и более линии системной терапии по поводу метастатической меланомы. Частота объективного ответа составила 22,6 % (95 % Доверительный интервал (ДИ) 53,3-64,4 %). Медиана выживаемости без прогрессирования - 4,37 мес. (95 % ДИ 2,27-6,47). Медиана общей выживаемости - 17,9 мес. (95 % ДИ 8,89-26,99). Одно-, двух-, трехлетняя общая выживаемость составила 66, 35 и 35 % соответственно. Эффективность ниволумаба во второй и последующих линиях терапии значительно ниже, чем показано в результатах рандомизированных исследований по применению анти-PD-1-препаратов в первой линии терапии.
Меланома, ниволумаб, анти-pd-1, иммунотерапия
Короткий адрес: https://sciup.org/140243799
IDR: 140243799 | DOI: 10.18027/2224-5057-2018-8-3-78-85
Nivolumab experience in the treatment of pre-treated patients with metastatic skin melanoma
The appearance of anti-PD-1 drugs significantly improved prognosis of patients with metastatic skin melanoma. However, little data on the effectiveness of these drugs in the second and subsequent lines of therapy has been accumulated in the international literature. We have analyzed our experience in the use of nivolumab in the treatment of metastatic melanoma. This non-randomized, uncontrolled, continuous study included 53 patients with metastatic or unresectable melanoma, of whom 86.8 % (46) received two or more lines of systemic therapy for metastatic melanoma. The rate of objective response was 22.6 % (95 % Confidence Interval (CI) 53.3-64.4 %). The median progression-free survival was 4.37 months (95 % CI 2.27-6.47). The median overall survival was 17.9 months (95 % CI 8.89-26.99). One-, two-, three-year overall survival contained 66, 35 and 35 %, respectively. The efficacy of nivolumab in the second and subsequent treatment lines is significantly lower than showed in the results of randomized trials of the use of anti-PD-1 drugs in the first line of therapy.
Текст научной статьи Опыт применения ниволумаба в терапии предлеченных пациентов с метастатической меланомой кожи
Меланома кожи – агрессивная злокачественная опухоль, характеризующаяся резистентностью к стандартной химио- и лучевой терапии. В эру химиотерапии медиана общей выживаемости (ОВ) пациентов с метастатической меланомой кожи составляла всего 6–10 мес. [1]. Появление ингибиторов иммунных контрольных точек – блокаторов CTLA-4 (cytotoxic T-lymphocyteassociated protein 4), PD-1 (programmed death 1) и его лиганда (PD-L1) значительно улучшило прогноз этих пациентов [2, 3]. Первый препарат из этого класса – ипилимумаб (разработан Bristol-Myers Squibb, США) в рандомизированном клиническом исследовании III фазы значительно улучшил медиану выживаемости без прогрессирования (ВБП) по сравнению с вакциной gp100 [4]. В объединенном анализе, включившем 12 исследований по применению ипилимумаба в лечении метастатической меланомы кожи, трехлетняя ОВ составила 26 % [5]. Применение ан-ти-PD-1-препаратов – ниволумаба (разработан Bristol-Myers Squibb, США) и пембролизумаба (Разработан Merck, США) в первой линии терапии связано с более высоким клиническим эффектом и благоприятным профилем безопасности по сравнению с монотерапией ипилимумабом. В исследовании III фазы Checkmate-067 трехлетняя ВБП составила 32 % в группе ниволумаба и 10 % в группе ипилимумаба [6]. Результаты применения анти-PD-1-препаратов у предлеченных пациентов намного скромнее. В исследовании Checkmate-037 изучалась эффективность ниволумаба у предлеченных пациентов по сравнению с химиотерапией дакарбазином или паклитакселом и карбоплатином [7]. Медианы ОВ составили 16 и 14 мес. соответственно, однако различия не достигли статистической значимости (отношение рисков 0,95; 95,54 % ДИ 0,73–1,24) [7].
Таким образом, на данный момент в международной литературе накоплено мало данных по эффективности анти-PD-1-препаратов во второй и последующих линиях терапии метастатической меланомы кожи.
В данной работе мы провели анализ эффективности и переносимости терапии ниволумабом пациентов с метастатической меланомой, принимавших участие в программе расширенного доступа к ниволумабу (CA209-097) в отделении биотерапии опухолей Национального медицинского исследовательского института им. Н. Н. Блохина Минздрава России.
Методы
Пациенты
В программу расширенного доступа включались пациенты: старше 18 лет; с IIIC–IV стадией меланомы (по 7th AJCC); гистологически подтвержденным
Опыт применения ниволумаба в терапии предлеченных пациентов с метастатической меланомой кожи диагнозом; ECOG-статусом 0–2; отсутствием или недоступностью эффективных терапевтических опций. Критерии исключения: прием системных глюкокортикоидов более 10 мг /сут. по преднизолону в связи с наличием метастазов в головной мозг или сопутствующих аутоиммунных заболеваний; беременность; наличие ВИЧ, гепатита B или C. Также в данное исследование было включено семь пациентов, получивших менее двух линий предшествующей терапии по поводу метастатической меланомы, принимавших ниволумаб вследствие недоступности ингибиторов BRAF и ипили-мумаба.
Дизайн исследования и режим терапии
В ретроспективное нерандомизированное неконтролируемое сплошное исследование по изучению эффективности ниволумаба во второй и последующих линиях были включены 53 пациента с метастатической или нере-зектабельной меланомой различных локализаций, которым было выполнено хотя бы одно введение ниволумаба. Ниволумаб вводился внутривенно в дозе 3 мг/кг каждые 2 нед. до прогрессирования заболевания или непереносимой токсичности. Максимальная длительность лечения составляла 24 мес. При прогрессировании заболевания после окончания курса терапии разрешалось возобновление лечения.
Нами не были запланированы конечные точки ввиду особенностей дизайна исследования. Однако мощность исследования позволила выделить достоверные благоприятные прогностические факторы в отношении ОВ.
Оценка эффективности и безопасности
ВБП определялась от времени первого введения препарата до первого подтвержденного прогрессирования заболевания или смерти (если ни одного контрольного исследования не было выполнено до этого). ОВ определялась от времени первого введения до смерти. Ответ на терапию оценивался по критериям Response Evaluation Criteria in Solid Tumors 1.1 (RECIST 1.1), первое контрольное обследование выполнялось на 12-й нед. с момента первого введения препарата, затем каждые 12 нед. Нежелательные явления (НЯ), связанные с приемом ниволумаба, оценивались по критерию National Cancer Institute Common Terminology Criteria for Adverse Events 4.03.
Статистический анализ
Перед началом исследования статистический анализ не был запланирован. Для описания характеристик пациентов были использованы методы описательной статистики, для оценки ОВ и ВБП – метод Каплана – Мейера. Статистические расчеты выполнены в программе IBM SPSS Statistics Professional 20.0.
Результаты
Пациенты и терапия
Включение пациентов происходило в период с марта 2015 г. по декабрь 2017 г. Основные характеристики пациентов (n=53) приведены в табл. 1.
База данных была закрыта в апреле 2018 г., медиана периода наблюдения составила 30,7 мес. Прогрессирование наступило у 41 (77,4 %) пациента, смерть – у 26 (49,1 %).
Последующую системную терапию получили 23 (43,4 %) пациента. Наиболее часто назначались следующие схемы терапии: ингибиторы BRAF в монотерапии (n=7, 13,2 %); комбинация ингибиторов BRAF и MEK (n=5, 9,4 %); химиотерапия (n=6, 11,4 %). Терапия ниволумабом после прогрессирования была продолжена у трех (5,4 %) пациентов. В связи с выраженным ухудшением соматического статуса или отсутствием доступных и эффективных лекарственных опций после прогрессирования заболевания на терапии ниволумабом последующее лечение не было назначено у 14 (26,4 %) пациентов.
Таблица 1
|
Характеристика |
NIVO (n=53) |
|
Средний возраст, годы Возраст, % |
52,8 (23–76) |
|
> 65 лет |
88,7 |
|
≥ 65 и > 75 лет |
9,4 |
|
≥ 75 лет |
1,9 |
|
Мужчины, % |
35,8 |
|
ECOG 0, % |
39,6 |
|
М-стадия, % M1c |
71,7 |
|
Уровень ЛДГ, % > ВГН |
37,7 |
|
Мтс в головной мозг, % |
20,8 |
|
Мтс в печень, % |
32,1 |
|
Мутация BRAF V600, % |
54,7 |
|
Локализация первичной опухоли на коже, % |
84,9 |
|
Число предшествующих линий терапии по поводу метастатической меланомы: |
|
|
0–1 |
13,2 |
|
2 |
39,6 |
|
3 и более |
47,2 |
|
Ипилимумаб в предшествующей терапии, % Сумма диаметров очагов до начала терапии, мм |
66 |
|
средняя (95 % ДИ) |
69,9 (55,7–84,1) |
|
медиана (мин – макс) |
66,0 (10–242) |
|
Сумма диаметров таргетных очагов более 100 мм, % |
34 |
Эффективность
Частота объективного ответа составила 22,6 % (95 % Доверительный интервал (ДИ) 53,3–64,4 %), у 5 (9,4 %) пациентов был достигнут частичный ответ и у 7 (13,2 %) – полный ответ. Стабилизация заболевания более 6 мес. наблюдалась у 8 (15,2 %) пациентов. Таким образом, контроль заболевания наблюдался у 20 (37,7 %) больных. Медиана длительности ответа не достигнута (НД) (95 % ДИ НД–НД). Прогрессирование заболевания наблюдалось у 31 (53,8 %) пациента. У двух (3,8 %) пациентов ответ не был оценен. Данные о лучшем ответе на лечение по раз-
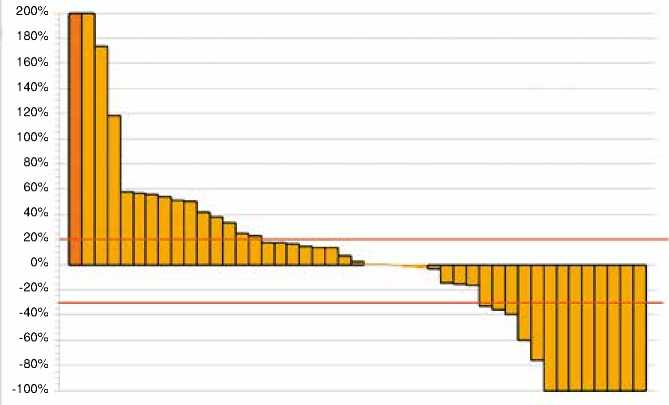
Рисунок 1
меру таргетных очагов у пациентов, прошедших первое контрольное обследование (n=45), приведены на рис. 1.
Медиана ВБП составила 4,37 мес. (95 % ДИ 2,27–6,47). Одно-, двух-, трехлетняя ВБП – 27, 24 и 21 % соответственно (рис. 2).
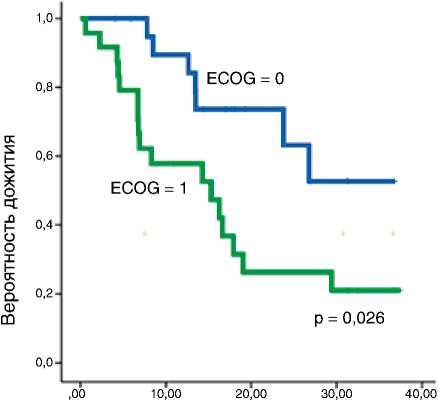
Медиана ОВ составила 17,9 мес. (95 % ДИ 8,89–26,99). Одно-, двух-, трехлетняя ОВ – 66, 35 и 35 % соответственно (рис. 2). Нами были выделены следующие благоприятные прогностические факторы в отношении ОВ: ЛДГ ниже верхней границы нормы (ВГН), ECOG-статус 0, суммарный диаметр таргетных очагов менее 100 мм (рис. 3).
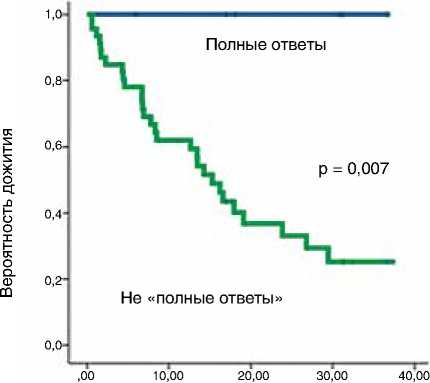
Наличие полного ответа на терапию было связано с высокой ОВ (рис. 4). Нами также проанализированы возможные различия в отношении ряда клинических и лабораторных признаков между пациентами с контролем заболевания и прогрессированием на терапии ниволума-бом. При статистическом анализе (критерий Хи-квадрат) были выявлены достоверные статистические различия в отношении следующих характеристик: наличие метастазов в печени (p<0,05), сумма диаметров таргетных очагов ≥ 100 (p<0,05), которые достоверно оказывали отрицательное влияние на объективный ответ (табл. 2).
Безопасность
В данном исследовании не было выявлено ранее не описанных НЯ. Возникновение иммуноопосредованных НЯ, предположительно связанных с приемом ниволумаба, наблюдалось у 31 (58,5 %) пациента. НЯ 3–4 степени возникли у 7 (13,2 %) пациентов. Большая часть НЯ купировались
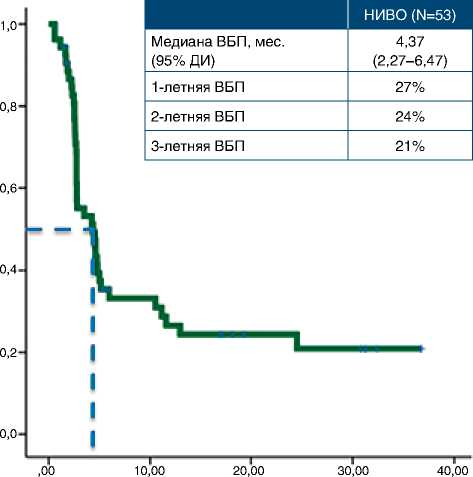
Рисунок 2
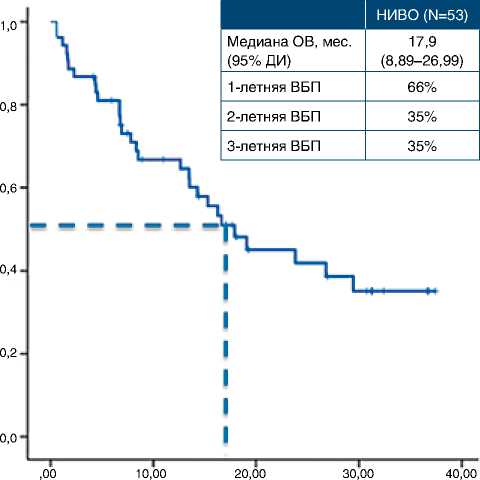
Опыт применения ниволумаба в терапии предлеченных пациентов с метастатической меланомой кожи
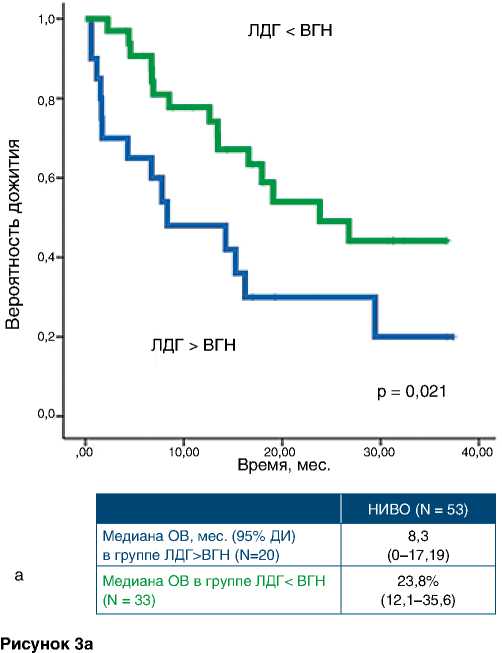
Время, мес.
НИВО (N = 53)
Медиана ОВ, мес. (95% ДИ)
в группе ECOG = 0 (N = 35)
Медиана ОВ в группе ECOG = 1 (N = 18)
HД (НД – НД)
15,27% (4,7–25,8)
HR (95% ДИ) 0,27 [0,08–0,85]
Рисунок 3б
Полный ответ vs не «полный ответ»
Время, мес.
Время, мес.
|
НИВО (N = 53) |
|
|
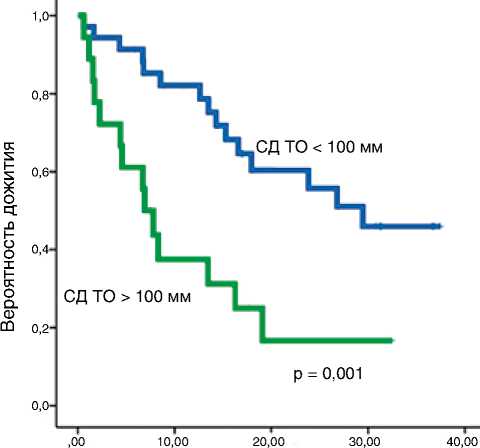
Медиана ОВ, мес. (95% ДИ) в группе CД < 100 мм (N = 35) |
29,43 (НД – НД) |
|
Медиана ОВ в группе СД > 100 мм (N = 18) |
6,89% (4,8–9,0) |
|
HR (95% ДИ) |
0,31 [0,15 – 0,65] |
|
НИВО (N = 53) |
|
|
Медиана ОВ, мес. (95% ДИ) в группе ПО (N = 7) |
НД (НД – НД) |
|
Медиана ОВ в группе Не – ПО (N = 46) |
15,4% (6,79 – 21,39) |
|
HR (95% ДИ) |
НД |
в
Рисунок 3в
Рисунок 4
|
Таблица 2 |
|||
|
Характеристика |
Пациенты с контролем над заболеванием (n=20) |
Пациенты с прогрессированием заболевания (n=33) |
Различия |
|
Средний возраст, годы (95 % ДИ) Возраст, % |
49 (43–55) |
53 (48–57) |
НД |
|
> 65 лет |
90 |
87,9 |
|
|
≥ 65 и > 75 лет |
10 |
91 |
НД |
|
≥ 75 лет |
0 |
3 |
|
|
Мужчин, % |
25 |
42,4 |
НД |
|
ECOG 0, % |
55 |
30,3 |
НД |
|
М-стадия, % |
|||
|
M1а |
30 |
18,2 |
|
|
M1b |
10 |
3 |
НД |
|
M1c |
60 |
78,8 |
|
|
Уровень ЛДГ, % |
|||
|
> ВГН |
25 |
45 |
НД |
|
Мтс в головной мозг, % |
15 |
24,2 |
НД |
|
Мтс в печень, % |
15 |
42,4 |
p<0,05 |
|
Мутация BRAF V600, % |
50 |
57,6 |
НД |
|
Локализация первичной опухоли на коже, % |
80 |
87,9 |
НД |
|
Предшествующая адъювантная терапия, % |
65 |
57,6 |
НД |
|
Число предшествующих линий терапии по поводу метастатической меланомы |
НД |
||
|
0–2 |
60 |
48,5 |
|
|
3 и более |
40 |
51,5 |
|
|
Ипилимумаб в предшествующей терапии, % |
65 |
66,7 |
НД |
|
Сумма диаметров очагов до начала терапии, мм |
p=0,035 |
||
|
Средняя (95 % ДИ) |
60,7 (45–76) |
91,2 (67–116) |
|
|
Медиана (мин – макс) |
54,5 (10–84) |
86,0 (0–242) |
|
|
Сумма диаметров таргетных очагов более 100 мм, % |
10 |
48,5 |
p<0,05 |
Таблица 3
|
Характеристика |
CheckMate 067 группа ниволумаба |
KEYNOTE 001 |
CheckMate 037 группа ниволумаба |
Данное исследование |
|
|
Получали ипилиму-маб до ниволумаба |
Никогда не получали ипилимумаб |
||||
|
Количество пациентов |
316 |
342 |
313 |
272 |
53 |
|
ECOG |
|||||
|
0 (%) |
75,3 |
63 |
73 |
60 |
39,6 |
|
1 (%) |
24,4 |
37 |
27 |
40 |
45,3 |
|
2 (%) |
0,3 |
0 |
0 |
0 |
15,1 |
|
Распространенность заболевания |
|||||
|
M1a и M1b (%) |
41,8 |
20 |
22 |
25 |
28,8 |
|
M1c (%) |
58,2 |
80 |
75 |
75 |
71,7 |
|
Наличие метастазов в головной мозг (%) |
2,5 |
11 |
5 |
19 |
20,8 |
|
ЛДГ |
|||||
|
Норма (%) |
62 |
58 |
62 |
49 |
54,7 |
|
Выше ВГН (%) |
35,4 |
41 |
35 |
51 |
37,7 |
|
Количество линий предшествующей терапии |
|||||
|
0 (%) |
100 |
0 |
51 |
0 |
7,5 |
|
1 (%) |
0 |
30 |
33 |
28 |
5,7 |
|
2 (%) |
0 |
37 |
15 |
51 |
39,6 |
|
≥3 (%) |
0 |
32 |
1 |
21 |
47,2 |
|
Результаты |
|||||
|
ЧОО (%) |
43,7 |
29 |
39 |
31,7 |
22,6 |
|
Медиана ВБП, мес. |
6,9 (95 % ДИ 4,3–9,5) |
4 (95 % ДИ 3–6) |
5 (95 % ДИ 3–7) |
3,1 |
4,37 (95 % ДИ 2,27–6,47) |
|
Медиана ОВ, мес. |
НД |
20 (95 % ДИ 18–25) |
29 (95 % ДИ 22–НД) |
16 |
17,9 (95 % ДИ 8,89–26,99) |
|
Все НЯ (%) |
86 |
82 |
85 |
59 |
58,5 |
|
НЯ 3–4 степени (%) |
21 |
14 |
14 |
8 |
13,2 |
Опыт применения ниволумаба в терапии предлеченных пациентов с метастатической меланомой кожи
Таблица 4
|
НЯ |
Число больных с НЯ, n (%) |
|
|
Любой степени |
3–4 степени |
|
|
Кожные |
17 (32) |
1 (2) |
|
Эндокринные Hypothyroidism |
7 (13) |
0 (0) |
|
ЖКТ Диарея |
6 (11) |
0 (0) |
|
Гастрит |
1 (2) |
1 (2) |
|
Печеночные |
4 (7,5) |
1 (2) |
|
Легочные |
2 (4) |
0 (0) |
в течение 3–4 нед. от момента возникновения. Отмена терапии в связи с непереносимостью произошла у трех (5,6 %) пациентов. Не зафиксировано ни одного смертельного случая, связанного с возникновением НЯ. Основные НЯ, зарегистрированные в исследовании, приведены в табл. 4.
Обсуждение
Данная статья описывает результаты самого крупного в России опыта применения анти-PD-1-препара-тов в пределах одного центра. В табл. 3 мы приводим сравнительную характеристику пациентов, включенных в исследования, а также результаты международных исследований и проведенной нами работы [6–9]. Как можно убедиться, в реальной клинической практике чаще, чем в международных рандомизированных исследованиях, встречаются пациенты со следующими характеристи-
ками: получившие две и более линии предшествующей терапии, имеющие метастатическое поражение головного мозга и ECOG-статус 1–2.
Эффективность ниволумаба во второй и последующих линиях терапии значительно ниже, чем показано в результатах рандомизированных исследований по применению анти-PD-1-препаратов в первой линии терапии. Наибольшую схожесть в характеристиках пациентов наше исследование имеет с исследованием CheckMate 037 [7, 8]. Однако в данном исследовании II фазы не было получено статистически значимых различий в медиане общей выживаемости между группами ниволумаба и химиотерапии (дакарбазин в монотерапии или паклитаксел и карбоплатин).
Согласно полученным нами данным, наибольшую выгоду от назначения ниволумаба получают пациенты со следующими благоприятными прогностическими факторами: ЛДГ ниже ВГН; ECOG-статус 0; суммарный размер таргетных очагов менее 100 мм; отсутствие метастатического поражения печени. Эти данные нашли подтверждение в других международных исследованиях [10]. Назначение ниволумаба во второй и последующих линиях терапии метастатической меланомы должно быть в первую очередь рассмотрено у пациентов с наличием указанных благоприятных прогностических факторов.
Профиль безопасности ниволумаба соответствует ранее приводимым данным международных исследований.
Список литературы Опыт применения ниволумаба в терапии предлеченных пациентов с метастатической меланомой кожи
- Robert C., Thomas L., Bondarenko I., O’Day S., Weber J., Garbe C. et al. Ipilimumab plus dacarbazine for previously untreated metastatic melanoma. N. Engl. J. Med. 2011. Vol. 364 (26). P. 2517-2526. PMID: 1639810. DOI: 10.1056/NEJMoa1104621.
- Mellman I., Coukos G., Dranoff G. Cancer immunotherapy comes of age. Nature. 2011. Vol. 480 (7378). P. 480-489. PMID: 22193102 DOI: 10.1038/nature10673.
- Kaufman H. L., Kirkwood J. M., Hodi F. S., Agarwala S., Amatruda T., Bines S. D. et al. The Society for Immunotherapy of Cancer consensus statement on tumour immunotherapy for the treatment of cutaneous melanoma. Nat. Rev. Clin. Oncol. 2013. Vol. 10 (10). P. 588-598. PMID: 23982524. DOI: 10.1038/nrclinonc. 2013.153.
- Hodi F. S., O’Day S. J., McDermott D. F., Weber R. W., Sosman J. A., Haanen J. B. et al. Improved survival with ipilimumab in patients with metastatic melanoma. N. Engl. J. Med. 2010. Vol. 363 (8). P. 711-723. PMID: 20525992. DOI: 10.1056/NEJMoa1003466.
- Schadendorf D., Hodi F. S., Robert C., Weber J. C., Margolin K., Hamid O. et al. Pooled analysis of long-term survival data from phase II and phase III trials of ipilimumab in unresectable or metastatic melanoma. J. Clin. Oncol. 2015. Vol. 33. P. 1889-1894. PMID: 25667295. DOI: 10.1200/JCO. 2014.56.2736.
- Wolchok J. D., Chiarion-Sileni V., Gonzalez R., Rutkowski P., Grob J. J., Cowey C. L. et al. Overall Survival with Combined Nivolumab and Ipilimumab in Advanced Melanoma. N. Engl. J. Med. 2017. Vol. 377 (14). P. 1345-1356. PMID: 28889792. DOI: 10.1056/NEJMoa1709684.
- Larkin J., Minor D., D’Angelo S., Neyns B., Smylie M., Miller W. H. et al. Overall Survival in Patients With Advanced Melanoma Who Received Nivolumab Versus Investigator’s Choice Chemotherapy in CheckMate 037: A Randomized, Controlled, Open-Label Phase III Trial. J. Clin. Oncol. 2018. Vol. 36 (4). P. 383-390. PMID: 28671856. DOI: 10.1200/JCO. 2016.71.8023.
- Weber J. S, D’Angelo S. P., Minor D., Hodi F. S., Gutzmer R., Neyns B. et al. Nivolumab versus chemotherapy in patients with advanced melanoma who progressed after anti-CTLA-4 treatment (CheckMate 037): a randomised, controlled, open-label, phase 3 trial. Lancet Oncol. 2015. Vol. 16 (4). P. 375-384. PMID: 25795410. DOI: 10.1016/S1470-2045 (15) 70076-8.
- Ribas A., Hamid O., Daud A., Hodi F. S., Wolchok J. D., Kefford R. et al. Association of Pembrolizumab With Tumor Response and Survival Among Patients With Advanced Melanoma. JAMA. 2016. Vol. 315 (15). P. 1600-1609. PMID: 27092830. DOI: 10.1001/jama. 2016.4059.
- Specenier P. Nivolumab in melanoma. Expert Rev. Anticancer Ther. 2016. Vol. 16 (12). P. 1247-1261. PMID: 27776441. DOI: 10.1080/14737140.2016.1249856.


