Опыт применения терагерцевой терапии у больных аденомой простаты в сочетании с хроническим абактериальным простатитом
Автор: Попков В.М., Киричук В.Ф., Лойко В.С., Маслякова Г.Н., Блюмберг Б.И.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Урология
Статья в выпуске: 4 т.10, 2014 года.
Бесплатный доступ
Цель: улучшенؐՠ ՐבÐۑ̑БސҠлечения больных с аденомой простаты (АП) I-II стадии и хроническим абактериальным простатитом (ХПА) (категория III А) с помощью дополнительного воздействия терагерцевой терапии (ТГЧ-терапия) на частотах молекулярного спектра излучения и поглощения оксида азота 150,176-150,664 ГГц. Материал и методы. В работе обобщены результаты наблюдения 75 мужчин (1-я (основная) группа: 25 больных с АП 1-11 стадии и ХПА (категории III А), которым проводилась стандартная медикаментозная терапия в сочетании с ТГЧ-терапией; 2-я группа (сравнения): 25 больных с АП 1-11 стадии и ХПА, которым проводилась стандартная медикаментозная терапия; 3-я группа (контроля): 25 практически здоровых мужчин). Результаты. Сочетание ТГЧ-терапии и стандартного медикаментозного лечения у пациентов с АП и ХПА (категория III А) позволило достичь более выраженных улучшений по системе IPSS и QoL, более быстрого и выраженного обезболивающего эффекта, более значимого уменьшения объема простаты у пациентов в основной группе. После курса ТГЧ-терапии у данной категории пациентов выявлено статистически достоверное увеличение максимальной скорости кровотока в сосудах простаты, более значимое улучшение показателей секрета простаты, установлено улучшение реологических свойств крови. Заключение. ТГЧ-терапия оказывает благоприятное воздействие на клиническое течение АП 1-И стадии и ХПА (категория III А) и является вспомогательным методом лечения данной когорты пациентов.
Аденома простаты, терагерцевая терапия, хронический абактериальный простатит
Короткий адрес: https://sciup.org/14918025
IDR: 14918025
Experience of terahertz therapy in benign prostatic hyperplasia combined with chronic abacterial prostatitis
Objective: to improve the treatment results of patients with benign prostatic hyperplasia (stage l-ll) accompanied with chronic abacterial prostatitis (category III A) by the use of terahertz therapy at frequencies of molecular spectrum of emission and absorption of nitric oxide 150,176-150,664 GHz. Material and methods. Atotal number of 75 patients met the inclusion criteria and were available for analysis. They were divided into three groups: 1st core group — 25 patients with BPH (stage l-ll) accompanied with chronic abacterial prostatitis (category III), which received standard medical therapy in combination with THZ-therapy; second group — 25 patients with BPH (stage l-ll) accompanied with CAP, which received standard medical therapy; third control group — 25 healthy men. Results. The combination of THZ — therapy with standard medical treatment allowed us to achieve marked improvements in the IPSS and QoL system, rapid anesthetic effect, more significant volume reduction of the prostate tissue in the 1st core group. Also THZ-therapy in 1st core group revealed a statistically significant increase of the maximum speed of blood vessels in the prostate tissue, improved a prostate secretion and rheological properties of blood. Conclusion. THZ-therapy as a complementary treatment has a beneficial effect on the clinical course of BPH (stage l-ll) accompanied with CAP (category III).
Текст научной статьи Опыт применения терагерцевой терапии у больных аденомой простаты в сочетании с хроническим абактериальным простатитом
1Введение. Аденомой простаты ( АП) в сочетании с хроническим простатитом (ХП) болеют около 70% мужчин в возрасте 60–80 лет [1]. АП является распространенным, социально значимым заболеванием. Консервативное лечение возможно в начальной стадии заболевания, однако в более поздние стадии единственным выходом является тяжелая травматическая операция, которая в пожилом возрасте пациента не всегда выполнима. Эффективное лечение АП на ранней стадии является актуальной задачей врачей-урологов.
В проблеме АП, а также АП с ХПА практически нет ни одного до конца решенного вопроса, поэтому проблема лечения больных АП не сходит с повестки урологических конференций.
Недостатком современной консервативной терапии является длительное наступление клинического эффекта, а также достаточно быстрое рецидивиро-вание процесса в случае отмены лечения. При медикаментозной терапии АП перечень лекарственных средств насчитывает более десяти групп препаратов [1, 2], что указывает на их недостаточную эффективность.
Доказательством того, что течение ХП имеет непосредственную связь с развитием АП, служат исследования, которые показали, что в 90,9% удаленных аденомотозных узлов имеется воспалительная инфильтрация, по объему она составляет 1/5 часть узлов гиперплазии. Естественно, что наличие воспалительных очагов в узлах значительно ухудшает клинические проявления, а также увеличивает вероятность послеоперационных осложнений [3, 4]. Воспаление играет важную роль в механизме увеличения ПЖ в размерах за счет цитокинов, секретируемых макрофагами, инфильтрирующими ПЖ при ее воспалении, что в свою очередь стимулирует образование HIF-1α и ведет к пролиферации клеток ПЖ и увеличению ее размеров [5].
Кроме того, в одном из звеньев патогенеза АП важную роль играет тканевая гипоксия простаты. Данные Vaupel P. et al. [6] показали, что парциальное давление кислорода в ткани патологичной ПЖ составляет 6 мм рт.ст., тогда как у здоровых пациентов 26 мм рт.ст.
Состояние гипоксии гиперплазированной ПЖ подтверждают данные Vaupel P. et al. [6], которые выявили усиление экспрессии фактора 1α (HIF-1α), относящегося к противовоспалительным цитокинам.
Известно, что дисфункция сосудистого эндотелия, имеющая системный характер, играет ключевую роль в патологическом механизме гипоксии. На фоне эндотелиальной дисфункции нарушаются реологические свойства крови, что проявляется повышением вязкости крови [7].
Многочисленные исследования [8] показали, что электромагнитное излучение терагерцевого диапа-
зона частот 150,176–150,664 ГГц (ТГЧ-облучение) является одним из наиболее действенных физиотерапевтических методов и обладает обезболивающим действием; нормализует реологические свойства крови; являясь антиоксидантом физической природы, вызывает нормализацию тонуса мозговых и периферических сосудов; улучшает микроциркуляцию в поврежденных тканях; снижает импульсную активность и пороги восприятия рецепторов; влияет на функциональные параметры периферических нервов и стимулирует регенеративные процессы в них; повышает биоэлектрическую активность мышечной ткани. Все это может эффективно использоваться при лечении заболеваний урологического профиля.
Кроме того, ТГЧ-терапия не является тепловым методом воздействия, что дает ему преимущество перед УВЧ, микроволновой, ультразвуковой и другими методами физиотерапевтического лечения, при которых происходит тепловое воздействие на простату и может вызываться стимулирование роста АП.
Таким образом, цель исследования : улучшение результатов лечения больных АП I–II стадии в сочетании с ХПА (категория III А) с помощью дополнительного применения ТГЧ-терапии на частотах молекулярного спектра излучения и поглощения оксида азота 150,176–150,664 ГГц.
Материал и методы. В работе обобщены результаты наблюдения за 75 пациентами. Критериями включения явились: диагноз «АП I–II стадии в сочетании с ХПА (категория III А)», наличие умеренно выраженной инфравезикальной обструкции, подписанное информированное согласие на участие в исследовании, абактериальный характер воспаления (микробное число <103 КОЕ/мл).
В исследование не включались пациенты, которые на момент визита: нуждались в оперативном вмешательстве или применении любого другого вида лечения АП (помимо оговоренного в исследовании) с целью предотвращения прогрессирования заболевания и нанесения вреда здоровью пациента; имели диагностированные заболевания МПС: почек, мочевого пузыря, простаты (кроме АП и простатита), уретры и др.; имели выраженные нарушения функции печени и/или почек и/или других жизненно важных органов, сопровождающиеся декомпенсацией их функций; не были способны адекватно отвечать на вопросы исследователя, заполнять необходимые документы; участвовали в исследовании какого-либо другого лекарственного препарата и/или метода лечения; наличие ВИЧ-инфекции, инфекции HBS или HCV; наличие инфекций, передающихся половым путем.
Пациенты были разделены на 3 группы:
1-я (основная) группа: 25 больных с АП I–II стадии и ХПА (категории III А), которым проводилась стандартная медикаментозная терапия в сочетании с ТГЧ-терапией;
2-я группа (сравнения): 25 больных с АП I–II стадии и ХПА, которым проводилась только стандартная медикаментозная терапия;
Показатели системы суммарной оценки симптомов до и после лечения (Х±Δ)
Таблица 1
|
Показатель |
Основная группа |
Группа сравнения |
Через 3 месяца после лечения |
Группа контроля |
|||
|
До лечения |
После лечения |
До лечения |
После лечения |
Основная группа |
Группа сравнения |
||
|
IPSS (балл) (норма 0) |
16±3 |
10±2 р<0,001 |
15±4 |
12±1 р<0,001 |
11±2 р<0,001 |
15±3 р<0,001 |
1 ± 1 |
|
QoL (балл) (норма 0) |
5±1 |
2±1 р<0,001 |
5±1 |
3±1 р<0,001 |
2±1 р<0,001 |
5±1 р<0,001 |
1 ± 1 |
Показатели УЗИ простаты и мочевого пузыря до и после лечения в двух группах (Х±Δ)
Таблица 2
|
Показатель |
Основная группа (n=25) |
Группа сравнения (n=25) |
Группа контроля |
||
|
До лечения |
После лечения |
До лечения |
После лечения |
||
|
Объем простаты |
55±5 |
45±2 р<0,001 |
56±5 |
50±2 р<0,001 |
26±5 |
|
Объем остаточной мочи (мл), норма: следы |
50±4 |
10±4 р<0,001 |
55±3 |
20±10 р<0,001 |
нет |
3-я -группа (контроля): 25 практически здоровых мужчин.
Стандартная консервативная медикаментозная терапия включала в себя антогонисты α1-адренорецепторов (0,4 мг 1 раз в сутки), ингибиторы 5α-редуктазы (0,5 мг 1 раз в сутки), препараты растительного происхождения, ферменто- и витами-нотерпию, антиоксиданты.
ТГЧ-терапию проводили с помощью аппарата «Орбита» ЯКУЛ.941526.001–02 производства ООО «Стрела» ДП ОАО ЦНИИИА, Россия, г. Саратов, по ТУ 9444-001-0756-4993-2008. Регистрационное удостоверение № ФСР 2009/05497. Аппарат «Орбита» действует на частоте 150,176–150,664 ГГц, что соответствует спектральной линии молекулярного спектра излучения и поглощения оксида азота.
В исследовании оценивали данные пальцевого ректального исследования. При выполнении ТРУЗИ простаты определяли объем простаты, исходный объем мочи и количество остаточной мочи, наличие кальцификатов. В дуплексном режиме сканирования анализировали максимальную и среднюю скорость кровотока, а также индексы резистентности при визуализации уретральных и капсулярных артерий. Проводили анализ клинико-лаборторных данных: общего анализа крови, мочи, биохимическго анализа крови, результатов PSA; реологических свойств крови (вязкость цельной крови, вязкость плазмы крови, вязкость сыворотки крови, вязкость взвеси отмытых эритроцитов, индекс агрегации эритроцитов и индекс деформации эритроцитов). Исследование реологических свойств крови проводилось на вискозиметре со свободноплавающим цилиндром АКР-2.
В процессе исследования информация о пациентах вносилась в базу данных и подвергалась статистической обработке. Расчеты производились с использованием пакета прикладных программ Statistica v.6.0 for Windows производства компании «StatSoft», а также приложения Exel Microsoft Office’ 2011. Для всех изучаемых признаков оценивали вид распределения. Исследуемые показатели имели симметричное распределение количественных признаков, соответствующее нормальному распределению. Для оценки значимости различий использовали критерий Стьюдента.
Результаты. Все пациенты до лечения предъявляли жалобы на боли в тазовой области нарушения мочеиспускания. При тестировании по системе IPSS и качества жизни пациентов (QoL) установлено повышение баллов (табл. 1). На фоне проведенного курса лечения в 1-й и 2-й группах пациентов наблюдался положительный эффект, который проявлялся в улучшении субъективных ощущений пациентов: снижение болевого синдрома, улучшение качества мочеиспускания.
После проведенного курса стандартного медикаментозного лечения в сочетании с терагерцевой терапией у пациентов основной группы отмечались более выраженные улучшения субъективных и объективных данных, отображающихся в положительной динамике данных по системе IPSS и QoL пациентов, по-видимому, за счет суммарного эффекта от проведенной терапии.
У пациентов 1-й группы наблюдался более быстрый и выраженный обезболивающий эффект, наступающий после 3–4-й процедуры.
Данные проведенного ТРУЗИ у пациентов обеих групп показали, что объем ПЖ уменьшился в обеих группах: в основной группе на 18%, в группе сравнения на 11 % (табл. 2).
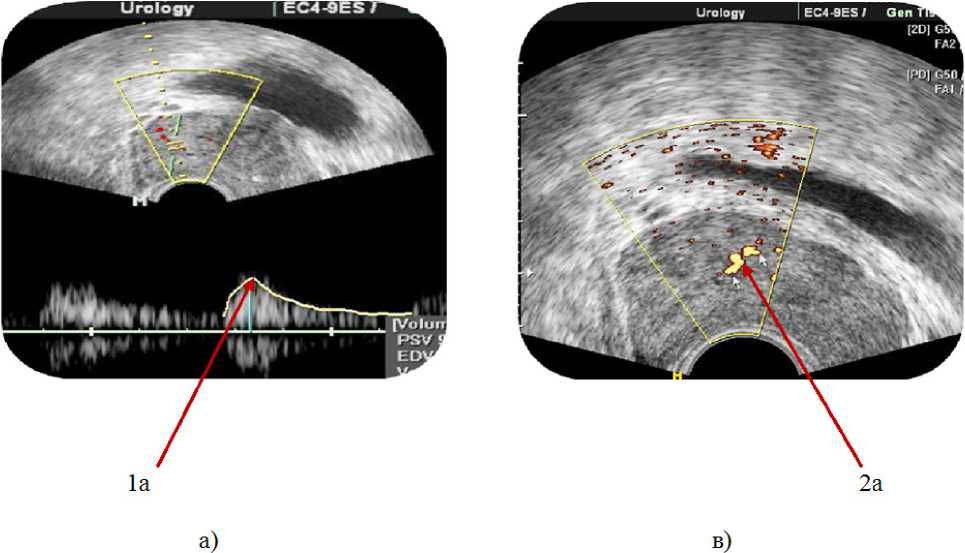
Анализ допплерографии ПЖ выявил статистически достоверное значительное увеличение максимальной скорости кровотока в сосудах ПЖ у пациентов основной группы после проведенного курса ТГЧ-терапии (рис. 1). Так, если до лечения максимальная скорость кровотока (PSV) в сосудах ПЖ составляла 9,15 см/с, то после курса терапии PSV составила 14,91 см/с.
Как видно из рис. 1, максимальная скорость после лечения (1б) стала в 2 раза выше, чем максимальная скорость кровотока до лечения (1а). Наблюдалось увеличение числа функционирующих сосудов (2б) в зоне поражения ткани ПЖ после проведенного курса лечения по сравнению с числом сосудов до лечения (2а).
Динамика лабораторных данных также отражала преимущество дополнительного воздействия ТГЧ-терапии (табл. 3).
Так, в основной группе отмечено улучшение показателей секрета простаты. Количество лейкоцитов в
до лечения
после лечения
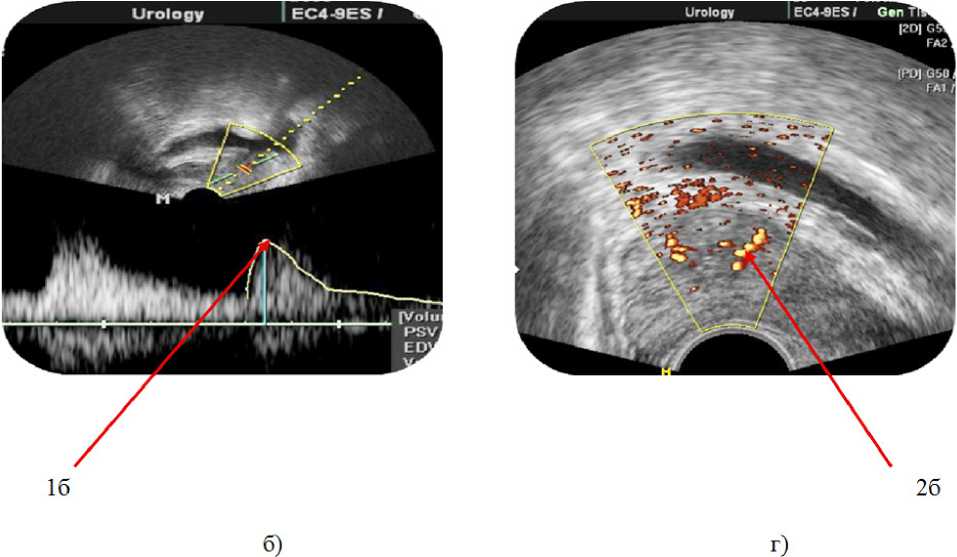
Рис. 1. Допплерограмма ПЖ пациентов основной группы: а) до лечения, б) после лечения, в) состояние кровотока до лечения, г) состояние кровотока после лечения
Показатели микроскопии секрета простаты до и после лечения (Х±Δ)
Таблица 3
|
Показатель |
Основная группа |
Группа сравнения |
Через 3 месяца после лечения |
|||
|
До лечения |
После лечения |
До лечения |
После лечения |
Основная группа |
Группа сравнения |
|
|
Лейкоциты (в поле зрения), норма 0–10 при увеличении 280 |
17±3 |
23±5 р<0,001 |
16±4 |
18±4 р<0,001 |
7±3 р<0,001 |
16±5 р<0,001 |
|
Лецитиновые зерна (норма — более 10 млн/мл) |
7±2 |
15±2 р<0,001 |
8±1 |
11±1 р<0,001 |
15±2 р<0,001 |
8±2 р<0,001 |
|
Макрофаги (в поле зрения), норма — 0 |
ед. в п/зр |
отсутствуют |
ед. в п/зр |
ед. в п/зр |
отсутствуют |
ед. в п/зр |
|
Эпителиоциты (в по-ле зрения), норма — 1–2 в п/з |
3±1 |
1±0 р<0,001 |
3±1 |
2±2 р<0,001 |
1±0 р<0,001 |
3±1 р<0,001 |
|
PSA сыворотки крови (нг/ мл), норма 0–4 |
2,1±1 |
1,0±1 р<0,001 |
2,5±1 |
2,2±1 р<0,001 |
1,2±1 р<0,001 |
2,4±1 р<0,001 |
-
3. Arnoldi EK. Chronic prostatitis: problems, experiences and perspectives. Rostov n/D: Phoenix, 1999; 320 p. Russian (Арнольди Э. К. Хронический простатит: проблемы, опыт, перспективы. Ростов н/Д: Феникс, 1999; 320 с.)
-
4. Alchinbaev MK, Ibraeva AS. The use of morphometry in the morphological diagnosis of chronic inflammation in the nodes of prostatic hyperplasia. In: Modern Problems of Urology: Materials of scientific works of the VI International Congress of Urology. Kharkov, 1998; с. 228–230. Russian (Алчинбаев М. К., Ибраева А. Ш. Использование метода морфометрии в морфологической диагностике хронического воспаления в узлах гиперплазии предстательной железы. В сб.: Современные проблемы урологии: Материалы научных трудов VI международного конгресса урологов. Харьков, 1998; с. 228–230)
-
5. Kim MK, Zhao C, Kim SD, et. al. Relationship of sex hormones and nocturia in lower urinary tract symptoms induced by benign prostatic hyperplasia. Aging Male 2012; 15 (2): 90–95.
-
6. Vaupel P, Kelleher DK. Blood flow and oxygenation status jf prostate cancer. Adv Exp Med Biol 2013; 765: 299–305.
-
7. Kirichuk VF, Glybochko PV, Ponomarev AI. Endothelial dysfunction. Saratov: SSMU, 2008; 111 p. Russian (Киричук В. Ф., Глыбочко П. В., Пономарева А. И. Дисфункция эндотелия. Саратов: Изд-во СГМУ, 2008; 111 с.)
-
8. Kirichuk VF, Antipova ON, Velykanova TS, et. al. Influence of terahertz waves on biological objects. Saratov: SSMU, 2014; 325 p. Russian (Киричук В. Ф., Антипова О. Н., Великанова Т. С. и др. Влияние терагерцевых волн на сложные живые биообъекты. Саратов: Изд-во СГМУ, 2014; 325 с.)
Список литературы Опыт применения терагерцевой терапии у больных аденомой простаты в сочетании с хроническим абактериальным простатитом
- Лопаткин H.A. Доброкачественная гиперплазия предстательной железы. М.: Медицина, 1999; 356 с.
- Блюмберг Б.И., Шатылко Т.В., Долгов А.Б. и др. Современные возможности медикаментозного лечения доброкачественной гиперплазии предстательной железы. Ремедиум Приволжье, Нижний Новгород, май 2013, с. 39
- Арнольди Э.К. Хронический простатит: проблемы, опыт, перспективы. Ростов н/Д: Феникс, 1999; 320 с.
- Алчинбаев M.K., Ибраева A. 111. Использование метода морфометрии в морфологической диагностике хронического воспаления в узлах гиперплазии предстательной железы. В сб.: Современные проблемы урологии: Материалы научных трудов VI международного конгресса урологов. Харьков, 1998; с. 228-230
- Kim МК, Zhao С, Kim SD, et. al. Relationship of sex hormones and nocturia in lower urinary tract symptoms induced by benign prostatic hyperplasia. Aging Male 2012; 15 (2): 90-95
- Vaupel P, Kelleher DK Blood flow and oxygenation status jf prostate cancer. Adv Exp Med Biol 2013; 765: 299-305
- Киричук В.Ф., Глыбочко П.В., Пономарева А.И. Дисфункция эндотелия. Саратов: Изд-во СГМУ, 2008; 111 с.
- Киричук В.Ф., Антипова O.H., Великанова Т.С. и др. Влияние терагерцевых волн на сложные живые биообъекты. Саратов: Изд-во СГМУ, 2014; 325 с.


