Опыт выполнения протезирования митрального клапана в раннем постинфарктном периоде у пациента с инфарктом миокарда с подъемом сегмента ST
Автор: Суспицына И.Н., Сукманова И.А., Ануфриенко Е.В.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические случаи
Статья в выпуске: 2 т.39, 2024 года.
Бесплатный доступ
Острая ишемическая митральная недостаточность (ИМН) является серьезным и жизнеугрожающим осложнением течения острого инфаркта миокарда (ОИМ). Развитие острой митральной недостаточности резко ограничивает возможности консервативной терапии и чаще всего требует проведения экстренного хирургического вмешательства. Однако сроки, выбор тактики оперативного вмешательства у пациентов с ОИМ дискутабельны. Нами представлен клинический пример развития острой митральной недостаточности у пациента 50 лет с нижним инфарктом миокарда (ИМ) при позднем обращении за медицинской помощью. Учитывая неэффективность консервативной тактики ведения и прогрессирование сердечной недостаточности, было принято решение о проведении протезирования митрального клапана (МК) в условиях искусственного кровообращения (ИК) на 12-е сут ИМ с предварительным использованием устройства вспомогательного кровообращения (экстракорпоральной мембранной оксигенации - ЭКМО) в качестве терапии «моста». Представленный нами клинический пример подтверждает, что использование ЭКМО позволяет расширить возможности проведения кардиохирургического лечения в раннем постинфарктном периоде у пациентов с механическими разрывами сердца и снижает риск развития летальных исходов.
Острый инфаркт миокарда, острая сердечная недостаточность, острая митральная недостаточность, устройства вспомогательного кровообращения, экстракорпоральная мембранная оксигенация, постоянная заместительная почечная терапия, искусственное кровообращение
Короткий адрес: https://sciup.org/149145408
IDR: 149145408 | УДК: 616.126.42-77:616.127-005.8-036.82 | DOI: 10.29001/2073-8552-2024-39-2-190-194
Experience in mitral valve replacement in the early post-infarction period in a patient with ST-segment elevation myocardial infarction
Acute ischemic mitral insufficiency is a serious and life-threatening complication of acute myocardial infarction (MI). The development of acute mitral insufficiency (AMI) severely limits the possibilities of conservative therapy and most often requires emergency surgical intervention. However, the timing and choice of surgical intervention in patients with AMI are debatable. We present a clinical case of AMI development in a 50-year-old patient with inferior MI with late medical care. Given the ineffectiveness of conservative treatment and the progress of acute heart failure, it was decided to perform mitral valve replacement under conditions of cardiopulmonary bypass on the 12th day of MI with the preliminary use of a circulatory assist device (ECMO) as a “bridge” therapy. The presented clinical case confirms that the use of auxiliary blood circulation devices allows expanding the possibilities of cardiac surgical treatment in the early post-infarction period in patients with mechanical ruptures of the heart and reduces the risk of fatal outcomes.
Текст научной статьи Опыт выполнения протезирования митрального клапана в раннем постинфарктном периоде у пациента с инфарктом миокарда с подъемом сегмента ST
Суспицына И.Н., Сукманова И.А., Ануфриенко Е.В. Опыт выполнения протезирования митрального клапана в раннем постинфарктном периоде у пациента с инфарктом миокарда с подъемом сегмента ST. Сибирский журнал клинической и экспериментальной медицины. 2024;39(2):190–194.
Острая ишемическая митральная недостаточность (ИМН) на фоне совершенствования высокотехнологичных реперфузионных вмешательств современной кардиологии становится более редким, но тем не менее грозным осложнением острого инфаркта миокарда (ОИМ) [1]. Наиболее частой причиной ИМН становится разрыв митрального подклапанного аппарата. Строение створок митрального клапана (МК), их анатомия и геометрические характеристики определяют более часто развитие острой ИМН в рамках окклюзии правой коронарной артерии (ПКА) или огибающей артерии (ОА) с развитием нижнего или заднего ОИМ с последующим отрывом папиллярных мышц и закономерным развитием тяжелой острой левожелудочковой недостаточности [2, 3].
Острая митральная недостаточность чаще всего вызвана отрывом одновременно нескольких хорд МК и является опасным для жизни состоянием, требующим проведения экстренного хирургического вмешательства [4]. Чаще всего ИМН приводит к развитию нестабильности гемодинамики, отеку легких и связано с худшим прогнозом для пациента даже после реперфузии. Особенно неблагоприятный прогноз характерен для пациентов без своевременного хирургического вмешательства, так как консервативная тактика ведения данной группы пациентов не перспективна [3, 5]. Чем выше степень ИМН у пациента, тем более плохими краткосрочными и долгосрочными результатами характеризуется течение заболевания [6]. При физикальном обследовании пациентов с ИМН выслушивается пансистолический шум с иррадиацией в левую подмышечную линию [2].
Эхокардиография (ЭхоКГ) является золотым стандартом диагностики митральной недостаточности. В настоящее время особую диагностическую ценность имеют современные эхокардиографические методики с 3D и 4D моделированием [2]. Возможности медикаментозной терапии являются крайне ограниченными, однако назначение ингибиторов ангиотензинпревращающего фермента (иАПФ), бета-адреноблокаторов (БАБ), мочегонных, сосудорасширяющих препаратов будет способствовать уменьшению пре- и постнагрузки, тем самым оказывая положительное влияние на степень митральной недостаточности, а также приведет к обратному ремоделированию миокарда.
Задачей медикаментозной терапии, прежде всего, является стабилизация состояния пациента и предоперационная подготовка [3]. Не вызывает сомнений, что своевременное проведение чрескожного коронарного вмешательства (ЧКВ) для пациента с ОИМ будет способствовать уменьшению степени регургитации (только в случае отсутствия у пациента механических осложнений, таких как разрыв папиллярных мышц) [2, 3]. Использование вспомогательных механических технологий приведет к улучшению прогноза и является терапией «моста» перед хирургическим лечением.
Внутриаортальная баллонная контрпульсация (ВАБК) – это надежный метод временной поддержки кровообращения, уменьшающий пост- и преднагрузку, использование которого может ограничивать зону ишемии у пациентов с ИМ [2]. Однако, по литературным данным, применение данного метода ранее ограничивалось пациентами с ИМН без разрыва папиллярных мышц [7].
Экстракорпоральная мембранная оксигенация (ЭКМО) – высокотехнологичный метод, направленный на поддержание насосной функции сердца и газообменной функции легких у пациентов, находящихся в критическом состоянии с острой сердечной (ОСН) или дыхательной недостаточностью. Этот метод является особенно полезным для лиц с ОИМ и сопутствующими механическими осложнениями, когда консервативные методы ведения становятся неэффективными. В таких случаях использование ЭКМО дает возможность выполнить кардиохирургические вмешательства (закрытие механических дефектов, протезирование клапанов) в раннем постинфарктном периоде. В настоящее время существуют как классические хирургические методы протезирования или пластики МК – как в сочетании с аортокоронарным шунтированием (АКШ), так и без АКШ, – так и катетерные технологии: система контурирования МК Carillon, клапаны Fortis, Medtronic, CardiAQ, NaviGate, Tiara, Tendyne и др. [2].
Учитывая техническую сложность катетерных технологий для коррекции патологии МК, они не получили столь широкого распространения [3]. Первые клинические исследования (Everest I) продемонстрировали высокую эффективность и безопасность кететерных технологий (у значительной части (66%) пациентов удалось избежать преждевременной смерти, необходимости в экстренной или плановой операции, клинические улучшения также были отмечены у большинства лиц), однако более поздние исследования (Everest II) показали более хорошие результаты для открытого хирургического оперативного лечения [3]. Согласно литературным данным, уровень госпитальной летальности в группе пациентов с ОИМ и острой митральной недостаточностью составляет 31–69% [3, 8, 9]. Сроки оперативного лечения, согласно клиническим рекомендациям Министерства здравоохранения РФ по ведению пациентов с ОИМ с подъемом сегмента ST (ОИМпST) по ЭКГ (2020), зависят от степени митральной регургитации и состояния пациента, и в большинстве случаев операции проводятся по экстренным показаниям [10].
Факторами, ухудшающими прогноз, являются: пожилой возраст, наличие кардиогенного шока, комор- бидность, большая зона ОИМ, отсрочка оперативного лечения.
Описание клинического случая. Больной П., 50 лет, курит (индекс курильщика – 10 пачка/лет), страдает артериальной гипертензией (АГ) с максимальными подъемами артериального давления (АД) до 150 мм рт. ст., без регулярной гипотензивной терапии. Перенесенные заболевания, травмы, операции, хронические заболевания отрицает. Наследственность по ранним сердечно-сосудистым заболеваниям не отягощена. Ишемический анамнез не отягощен.
Настоящее ухудшение состояния возникло после физической нагрузки, когда впервые в жизни появилась интенсивная давящая боль за грудиной с иррадиацией в плечевые суставы, локти, боль сохранялась в течение суток. На следующий день – аналогичный рецидив вышеописанного болевого синдрома, потливость, чувство страха, нарастающая нехватка воздуха. В итоге пациент вызвал бригаду скорой медицинской помощи через 27 ч после начала заболевания. По ЭКГ скорой медицинской помощи – ритм синусовый, формирование подострой стадии Q нижнего ИМ (рис. 1).

Рис. 1. Электрокардиограмма пациента при поступлении Fig. 1. Patient’s ECG on admission
Пациент был доставлен в ЧКВ-центр согласно локальному приказу о маршрутизации пациентов с острым коронарным синдромом с подъемом сегмента ST (ОКС-пST). Догоспитальная терапия: ацетилсалициловая кислота – 250 мг, клопидогрел – 300 мг, гепарин – 5000 единиц (ЕД) внутривенно. Госпитализирован в Алтайский краевой кардиологический диспансер. Общее состояние пациента при поступлении: тяжелое. По данным объективного осмотра: признаки Killip II (влажные хрипы в нижних отделах легких, сатурация – 85%), аускульта-тивно – грубый систолический шум, частота сердечных сокращений (ЧСС) 130 в мин, АД – 105/60 мм рт. ст. Несмотря на сроки начала заболевания, учитывая осложненное течение ОИМ, пациент транспортирован в рентгеноперационную для выполнения экстренной коронарной ангиографии, по результатам которой вы- явлена субокклюзия ПКА и гемодинамически незначимый стеноз ОА (30–40%). Выполнено стентирование инфарктзависимой артерии (ПКА) двумя стентами с лекарственным покрытием (METAFOR 2,75 × 19 мм; 3,0 × 37 мм) (рис. 2).
Проведена ЭхоКГ, по результатам которой выявлен отрыв хорд передней створки МК (ПСМК) (А2) с выраженной митральной peгуpгитацией (v. Contr. 8 мм), не-большая-умеренная трикуспидальная pегуpгитация, умеренная легочная гипертензия (систолическое давление правого желудочка (ПЖ) – 56 мм рт. ст.), гипокинез базального и среднего сегментов нижней стенки левого желудочка (ЛЖ), фракция выброса (ФВ) ЛЖ – 64%, размер полости левого предсердия – 49 мм, ЛЖ: конечно-диастолический размер – 61 мм, конечно-систолический размер – 35 мм, ударный объем – 136 мл.
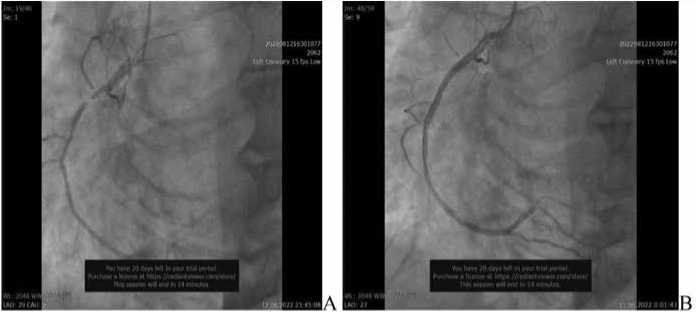
Рис. 2. Данные коронарографии до стентирования (A) и во время завершения чрескожного коронарного вмешательства (B)
Fig. 2. Coronary angiography data before stenting (A) and during completion of percutaneous coronary intervention (B)
По лабораторным данным – повышение уровня тропонина I до 39,3 нг/мл. В отделении реанимации пациент получал ацетилсалициловую кислоту – 100 мг, тикагрелор – по 90 мг × 2 р/д, БАБ и иАПФ – в минимальной дозе, статины, диуретики, ингибиторы протонной помпы. На фоне терапии прогрессировали явления ОСН и дыхательной недостаточности, переведен на неинвазивную вентиляцию легких (НИВЛ), затем – на инвазивную вентиляцию легких (ИВЛ). Учитывая нестабильность гемодинамики, к терапии был добавлен норадреналин. В дальнейшем нарастали признаки ОСН и полиорганной недостаточности. В связи с этим было принято решение о подключении пациента к веноартериальной ЭКМО и постоянной заместительной почечной терапии (ПЗПТ), начата гемосорбция колонкой Jafron HA 330 на 7-й день госпитализации.
Через контур ЭКМО был подключен аппарат ПЗПТ в режиме продленной вено-венозной гемодиафильтрации. На фоне проведения ЭКМО и ПЗПТ отмечалась относительная положительная динамика – снижение дозы норадреналина и параметров ИВЛ. Несмотря на первоначальные положительные результаты, в динамике вновь отмечена дестабилизация гемодинамики пациента, нарастание дозы инотропной поддержки, рецидивирующие неустойчивые пароксизмы фибрилляции предсердий.
Учитывая невозможность достичь компенсации по ОСН на фоне отрыва передней створки МК, несмотря на крайне высокий риск оперативного лечения, кардиокомандой принято решение об оперативном лечении по жизненным показаниям – протезирование МК в условиях искусственного кровообращения (ИК).
На 12-е сут ОИМ выполнено оперативное лечение в объеме протезирования МК клапаном Мединж 2-29. Из особенностей операции отмечалась выраженная диффузная кровоточивость за счет гепаринизации (на фоне продолжающейся ЭКМО), осуществлялась повторная рестернотомия с проведением гемостаза. После оперативного вмешательства была продолжена вено-артериальная ЭКМО, неоднократно проводилась аутореинфузия эритроцитарной массы, коррекция показателей гемостаза, гомеостаза, ПЗПТ с сорбирующими колонками Jafron HA 330.
Пациент был экстубирован на 7-е сут после проведения оперативного лечения, тогда же была завершена ЭКМО, еще через 5 дней было завершена ПЗПТ, функция почек восстановлена, переведен в кардиологическое отделение. Начата активизация пациента с привлечением специалистов лечебной физкультуры. Проведена динамика ЭхоКГ после протезирования: ФВ по Тейхольцу – 57%, систолическое давление в ПЖ – 29 мм рт. ст., протез МК: двухстворчатый. Небольшая-умеренная митральная peгуpгитация.
После оперативного лечения проведена коррекция медикаментозной терапии. На фоне лечения и реабилитации ангинозные боли не рецидивировали, гемодинамика стабилизировалась. Пациент был выписан в удовлетворительном состоянии на 22-е сут после проведения оперативного лечения с рекомендациями для дальнейшего наблюдения на амбулаторном этапе.
Обсуждение
Представлен случай развития ОСН на фоне механических осложнений ИМ (отрыв хорд МК). Консервативные методы ведения ОСН оказались неэффективными, что привело к развитию полиорганной недостаточности, септического процесса и поставило под угрозу жизнь пациента. Оперативное лечение (протезирование МК) в раннем постинфарктном периоде обладает высоким риском неблагоприятных исходов. Однако использование метода вено-артериальной ЭКМО и проведение ПЗПТ обеспечило сохранение жизнеспособности организма пациента, поддержание системной гемодинамики, коррекцию кардиальной дисфункции, нормализацию метаболизма и биохимических показателей, а также предотвратило развитие необратимых органных изменений, что позволило успешно выполнить оперативное вмешательство по жизненным показаниям на 12-е сут ИМ.
Не вызывает сомнений, что эффективность применения ЭКМО во многом зависит от своевременной и адекватной оценки состояния пациента, хорошо скоординированной и компетентной работы анестезиологов, реаниматологов, хирургов, перфузиологов и реабилито-логов.
Заключение
ОСН является основной причиной летальности у пациентов с ИМ. Достаточно частыми осложнениями ИМ являются механические разрывы сердца. Единственной возможностью спасения жизни данной категории пациентов является проведение оперативного лечения (протезирование клапана, закрытие дефектов) в раннем постинфарктном периоде. Оперативное лечение у таких пациентов обладает высоким риском неблагоприятных исходов, учитывая ранний постинфарктный период. Представленный нами клинический пример подтвержда- ет, что использование устройств вспомогательного кровообращения, в частности ЭКМО, позволяет расширить возможности проведения кардиохирургического лечения в раннем постинфарктном периоде у пациентов с механическими разрывами сердца и снижает риск развития летальных исходов.
Список литературы Опыт выполнения протезирования митрального клапана в раннем постинфарктном периоде у пациента с инфарктом миокарда с подъемом сегмента ST
- Hennessey B., Sabatovicz N.Jr., Del Trigo M. Acute ischaemic mitral valve regurgitation. J. Clin. Med. 2022;11(19):5526. DOI: 10.3390/jcm11195526
- Báez-Ferrer N., Izquierdo-Gómez M.M., Marí-López B., Montoto-López J., Duque-Gómez A., García-Niebla J. et al. Clinical manifestations, diagnosis, and treatment of ischemic mitral regurgitation: a review. J. Thorac. Dis. 2018;10(12):6969-6986. DOI: 10.21037/jtd.2018.10.64
- Сапельников О.В., Латыпов Р.С., Акчурин Р.С. Современный подход к лечению ишемической митральной недостаточности. Кардиология и сердечно-сосудистая хирургия. 2015;8(3):64-69. DOI: 10.17116/kardio20158364-69
- Журавлева Л.В., Лопина Н.А., Кузнецов И.В., Лопин Д.А., Крамаренко И.А., Суманова И.А. Острый отрыв хорды задней створки митрального клапана у пациентки пожилого возраста с артериальной гипертензией и ишемической болезнью сердца. Сердце i судини. 2015;(4):16-21.
- Estévez-Loureiro R., Tavares Da Silva M., Baz-Alonso J.A., Caneiro-Queija B., Barreiro-Pérez M., Calvo-Iglesias F. et al. Percutaneous mitral valve repair in patients developing severe mitral regurgitation early after an acute myocardial infarction: A review. Front. Cardiovasc. Med. 2022;9:987122. DOI: 10.3389/fcvm.2022.987122
- Mentias A., Raza M.Q., Barakat A.F., Hill E., Youssef D., Krishnaswamy A. et al. Prognostic significance of ischemic mitral regurgitation on outcomes in acute ST-elevation myocardial infarction managed by primary percutaneous coronary intervention. Am. J. Cardiol. 2017;119(1):20-26. DOI: 10.1016/j.amj-card.2016.09.00
- Otto C., Bonow R.; eds. Valvular heart disease: A Companion to Braunwald's Heart Disease. 4th edition. Saunders Elsevier; 2014:494.
- Акчурин Р.С., Комлев А.Е., Сапельников О.В., Латыпов Р.С. Приобретенные пороки сердца. Хирургическое лечение митральных пороков сердца. В кн.: Руководство по кардиологии; под ред. акад. Е.И. Чазова. Т. 4. Заболевания сердечно-сосудистой системы. М.: Практика; 2014;259-284.
- Корней С.М. Сравнение методов хирургической коррекции функциональной митральной недостаточности ишемического генеза. Сердце. 2011;10:1(57):86-92.
- Министерство здравоохранения Российской Федерации. Острый инфаркт миокарда с подъемом сегмента ST электрокардиограммы. Клинические рекомендации, 2020. URL: https://cr.minzdrav.gov.ru/schema/157_4 (02.05.2023).


