Ортопедический режим после хирургического лечения статических деформаций переднего отдела стоп у пациентов с синдромом диабетической стопы
Автор: Паршиков М.В., Бардюгов П.С.
Журнал: Кафедра травматологии и ортопедии @jkto
Статья в выпуске: 1 (43), 2021 года.
Бесплатный доступ
Обоснование. Сахарный диабет и статические деформации переднего отдела стоп являются распространенными заболеваниями. Их сочетание часто приводит к развитию синдрома диабетической стопы. Хирургическое лечение статических деформаций стоп применяется в лечении проявлений нейропатической формы синдрома диабетической стопы, однако в литературе уделяется мало внимания послеоперационному периоду после данного метода лечения.Цель исследования. Улучшение результатов хирургического лечения пациентов со статическими деформациями переднего отдела стоп и синдромадиабетической стопы за счет подбора рационального ортопедического в послеоперационном периоде.Методы. В период с 2015 по 2020 гг. наблюдались 39 больных с синдромом диабетической стопы и получивших хирургическое лечение статических деформаций переднего отдела стоп. У 33 пациентов имелись нейропатические язвы в зоне повышенного механического воздействия. В остальных 6 случаях в этой области имелись предъязвенные изменения кожного покрова. В послеоперационном периоде применялся определенный режим активизации для пациентов с синдромом диабетической стопы.Результаты. После полученного лечения у всех пациентов наступило заживление нейропатических язв в срок до 3 месяцев (у кого они были).В одном случае отмечалось нагноение послеоперационной раны. Рецидив язвообразования, потребовавший повторного хирургического лечения отмечался в одном случае. Результаты оценивали так же по шкале AOFAS. Согласно которой, в 97 % случаев получены хорошие и удовлетворительные результаты.Выводы. Полученные результаты расцениваются нами как положительные. В значительной степени, как нам представляется, это обусловленопримененным ортопедическим режимом в послеоперационном периоде, который может быть предложен для лечения данной категории больных.
Синдром диабетической стопы, статические деформации переднего отдела стоп, ортопедический режим
Короткий адрес: https://sciup.org/142229996
IDR: 142229996 | УДК: 617.3 | DOI: 10.17238/issn2226-2016.2021.1.34-41
Orthopedic mode after surgical treatment of static deformities of the forefoot in patients with diabetic foot syndrome
Diabetes mellitus and static deformities of the forefoot are common diseases. Their combination often leads to the development of diabetic foot syndrome. Surgical treatment of static foot deformities is used in the treatment of manifestations of the neuropathic form of diabetic foot syndrome; however, little attention is paid in the literature to the postoperative period and the period of rehabilitation after this method of treatment.Purpose of the study. Improving the results of surgical treatment of patients with static deformities of the forefoot and diabetic foot syndrome due to theselection of a rational regimen of the postoperative period.Methods. In the period from 2015 to 2020. observed 39 patients with diabetic foot syndrome and who received surgical treatment for static deformities of the forefoot. 33 patients had neuropathic ulcers in the area of increased mechanical impact. In the remaining 6 cases, there were pre-ulcer changes in the skin in this area. In the postoperative period, specific methods of treatment and activation were used, which are characteristic only for patients with diabetic foot syndrome. Results. After the received treatment, all patients experienced healing of neuropathic ulcers within 3 months (who had them). In one case, postoperative wound suppuration was noted. Relapse of ulceration requiring repeated surgical treatment was noted in one case. The results were also assessed using the AOFAS scale. According to which, in 97% of cases, good and satisfactory results were obtained.Conclusion. The results obtained are regarded by us as positive. To a large extent, in our opinion, this is due to the applied mode of postoperative rehabilitation,which can be proposed for the treatment of this category of patients.
Текст научной статьи Ортопедический режим после хирургического лечения статических деформаций переднего отдела стоп у пациентов с синдромом диабетической стопы
В 2016 г. распространенность синдрома диабетической стопы (СДС) в РФ среди больных сахарным диабетом (СД) составила: СД 1 типа – 4,7%, СД 2 типа – 1,9%. Соотношение различных форм СДС при СД 1 типа: нейропатическая с трофической язвой – 41,6%, нейропатическая (стопа Шарко) – 17,9%, нейроише-мическая – 28,3%, ишемическая – 12,2%; СД 2 типа: 41,6%, 7,4%, 32,4%, 18,5% соответственно [1].
Статические деформации переднего отдела стоп (СДПОС) – одно из самых распространенных заболеваний костно-мышечной системы [2]. Так, согласно некоторым отечественным источникам, заболеваемость вальгусным отклонением первого пальца стопы и поперечным плоскостопием составляет до 70% популяции [3,4].
В современной ортопедии большое распространение получили оперативные методики лечения СДПОС. Это связано с относительно низкой эффективностью коррекции деформаций при помощи консервативного лечения, возможности которого изучались отечественными и зарубежными исследователями на протяжении многих лет в сравнении с хирургическим [5-7].
Однако в иностранных и отечественных публикациях уделено не так много внимания реабилитации пациентов после хирургического лечения СДПОС. Особенно это касается пациентов с СДС. Хирургу-ортопеду сложно ориентироваться на опубликованный опыт коллег, подбирая послеоперационный режим для оперированных пациентов.
Цель исследования
Улучшение результатов лечения пациентов со СДПОС и СДС за счет подбора рационального режима послеоперационного периода.
Задачи
-
1. Сформировать комплекс мероприятий ортопедического режима послеоперационного периода для пациентов с СДС, получивших различное по объёму и характеру хирургическое лечение СДПОС.
-
2. Оценить его эффективность.
Пациенты и методы исследования
В период с 2015 по 2020 гг. в ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Минздрава России и в ГБУЗ МО «Видновская районная клиническая больница» наблюдались 39 больных с СДС и получивших хирургическое лечение СтДПОС. Возраст пациентов колебался от 40 до 75 лет. Из них женщин было 23, мужчин – 16. СД 1 типа диагностирован у 8-и пациентов, СД 2 типа - у 31 пациента.
Средняя длительность заболевания сахарным диабетом пациентов составила 10 [5; 14] лет. Медианный уровень гликированного гемоглобина (HbA1c) составлял 7,1% и не превышал 9,5 %. Уровень глюкозы крови колебался от 3,3 ммоль\л до 17 ммоль\л, при среднем уровне от 6,5 до 10,0 ммоль\л.
Основными жалобами являлись длительное время незаживающие \ рецидивирующие нейропатические язвы (НЯ) переднего отдела стопы, и трудности при подборе обуви. Болевой синдром отмечали всего 11 больных и по шкале ВАШ составил от 5 до 45 мм., что соответствовало слабому болевому синдрому. Индекс массы тела (ИМТ) составил 30,2 [26,5; 36,1] кг/м2. Ожирение (ИМТ более 30 кг/м²) имели 30 пациентов.
У 33 пациентов имелись НЯ в зоне повышенного механического воздействия. В остальных 6 случаях в этой области имелись предъязвенные изменения кожного покрова: участки гиперкератоза, кровоизлияние в дерму. Наличие НЯ у больных отмечалось от 1 месяца до 3 лет. Средняя продолжительность составила 4 месяца.
Для определения характера и степени глубины НЯ у исследуемых больных применяли классификацию Wagner [8] (Таблица 1). Характер язвенных дефектов был следующий: Wagner 1 – в 6 случаях, Wagner 2 у 23 пациентов. Wagner 3 у 4 пациентов: хронический остеомиелит головки плюсневой кости с рентгенологическими проявлениями в виде снижения плотности костной ткани, узурации кортикального слоя кости, кистозная перестройка губчатой костной ткани.
Таблица 1
Классификация язвенных дефектов по Wagner
|
Степень |
Характеристика |
|
0 степень |
кожа не повреждена - |
|
I степень |
поверхностная язва (в пределах эпидермиса, дермы) 6 |
|
II степень |
в пределах клетчатки, сухожилий, связок, мышц 23 |
|
III степень |
абсцесс, остеомиелит, септический артрит 4 |
|
IV степень |
гангрена участка стопы - |
|
V степень |
гангрена всей стопы - |
Для хирургического лечения деформаций стоп использовались следующие технологии: вмешательства на мягких тканях (тенотомии сухожилий сгибателей и разгибателей пальцев) и операции на костной ткани. При операциях на костной ткани применялись хирургические техники, широко распространенные в хирургии деформаций стоп и освещенные в литературе, такие как остеотомии плюсневых костей Weil, Hilal, SCARF, Wilson; остеотомия основной фаланги 1-го пальца – Akin; резекция костно-хрящевого разрастания головки первой плюсневой кости по Шеде. Так же применялась резекция головки плюсневой кости и артродез межфалангового сустава первого пальца.
Резекция головки плюсневой кости применялась в случае полного вывиха пальца или остеомиелита последней. При поперечной распластанности применялись остеотомии II - IV плюсневых костей Weil, Hila. Для коррекции молоткообразной деформации малых пальцев использовалась артропластика проксимального межфалангового сустава (по Hohmann), тенотомии сухожилий сгибателей и разгибателей. Коррекция вальгусного отведения
1–го пальца осуществлялась за счет применения резекции кост-но - хрящевого разрастания головки I – ой плюсневой кости по Шеде в сочетании с остеотомиями I – ой плюсневой кости SCARF или Wilson; остеотомией основной фаланги 1-го пальца Akin. При деформации тейлора - нефиксированная остеотомия Weil \Hilal или резекция головки V-й плюсневой кости. Вальгусная деформация 1–го пальца – артродез межфаланговго сустава. При гиперсводчатом переднем отделе стопы - нефиксируемая остеотомия пятой плюсневой кости Hilal в сочетании с остеотомией первой плюсневой кости Weil (Таблица 2).
Таблица 2
Тип операции в зависимости от характера деформации стопы и локализации язвенного дефекта у пациентов, получавших хирургическое лечение
|
Тип деформации |
Локализация язвы / количество пациентов |
Тип операции / количество пациентов |
|
Поперечное плоскостопие |
подошвенная поверхность в проекции головок средних плюсневых костей / 9 |
разгрузочная нефик-сируемая остеотомия плюсневой кости Weil или Hilal / 4; резекция головки плюсневой кости /5 |
|
Вальгусное отведение первого пальца |
внутренняя поверхность стопы в проекции головки 1 плюсневой кости / 1; боковая поверхность 1 или 2 пальца / 3 |
резекция костнохрящевого разрастания по Шеде / 1; остеотомия проксимальной фаланги по типу «закрытый клин» Akin / 2; остеотомия 1 плюсневой кости Wilson или SCARF в сочетании с Аkin / 1 |
|
Молоткообразная деформация пальцев |
тыльная поверхность пальцев в проекции проксимального межфалангового сустава / 1; проекция бугристости ногтевой фаланги / 5 |
резекционная артропластика проксимального межфалангового сустава по Hohmann с фиксацией спицей в сочетании с подкожной мининвазивной те-нотомией сухожилий сгибателей и разгибателей / 4; изолированная тено-томия сгибателей и разгибателей / 2 |
|
Деформация тейлора |
подошвенная поверхность в проекции головки 5 плюсневой кости / 11 |
резекция головки пятой плюсневой кости / 3; нефикисируемая остеотомия пятой плюсневой кости Weil или Hilal / 8 |
|
Вальгусное отведение ногтевой фаланги первого пальца |
внутренне-подошвенная поверхность первого пальца / 1 |
артродез межфалангового сустава 1 пальца в положении коррекции /1 |
|
Гиперсводчатость переднего отдела стопы |
подошвенная поверхность в проекции головки 1 и 5 плюсневой плюсневой кости / 2 |
нефиксируемая остеотомия пятой плюсневой кости Hilal в сочетании с остеотомией первой плюсневой кости Weil / 2 |
В 6 случаях хирургическое лечение выполнено пациентам без НЯ: изолированная тенотомия сухожилий сгибателей и разгибателей пальцев (n=3), остеотомии первой плюсневой кости SCARF в сочетании с остеотомией основной фаланги 1-го пальца Аkin (n=2), остеотомия V плюсневой кости (n=1).
В большинстве случаев хирургического лечения ( п = 24) доступ осуществлялся из отдельного линейного разреза от 1,0 до 6,0 см. Локализация разреза была в зависимости от типа деформации: по внутренней поверхности стопы для коррекции деформации «первого луча», тыльной поверхности при операциях на II - IV плюсневых костях и наружной поверхности стопы для коррекции деформации V-й плюсневой кости. Операционные раны ушивались наглухо.
В 6 – и случаях, когда хирургический доступ целесообразно было осуществлятьс иссечением язвенного дефекта. Полученная интраоперационная рана ушивалась наглухо или частично. Данная манипуляция проводилась при коррекции молоткообразной деформации по Hohmann (один пациент) и резекции головок плюсневых костей (5 пациентов). Рана ушивалась частично в четырех случаях на фоне хронического остеомиелита головки плюсневой кости. Это позволяло образовавшейся после удаления головки плюсневой кости полости полноценно дренироваться, а ране заживать вторичным натяжением.
Миниинвазивный способ остеотомии плюсневых костей специальной фрезой (буром) применялся в четырех случаях через кожный прокол.
В 5-ти случаях, когда выполнялась коррекция молоткообразной деформации пальцев только на мягких тканях за счет тенотомии, операционных ран как таковых не было – данная манипуляция выполнялась так же через проколы кожи толстой иглой.
Для остеосинтеза костных фрагментов при коррекции Hallux valgus в двух случаях, когда у пациента не было нейропатической язвы на стопе использовали погружные металлофиксаторы (канюлированные винты Герберта).
В 13 – и наблюдениях применяли спицы Киршнера, не погруженные под кожу, которые удалялись через 21 день после операции. В остальных случаях костные фрагменты не фиксировались.
Операции заканчивались наложением асептических повязок: 0,5 % спиртовой раствор Хлоргексидина на операционные раны и 10% раствор Бетадин на язвенные дефекты; приданием возвышенного положения конечности. Дополнительная иммобилизация конечности не проводилась.
Послеоперационный период и реабилитационные мероприятия
В первый день после операции пациентам назначался строгий постельный режим для уменьшения вероятности образования гематомы послеоперационной раны. Сохраняли возвышенное положение оперированной конечности 7-10 дней. При отсутствии язвы проводили антибиотикопрофилактику, которую начинали в день операции и продолжали следующие 5 дней. У пациентов с язвой антибиотикотерапия продолжалась более длительно: до 7–10 дней. Применялись антибактериальные препараты из группы Цефалоспоринов третьего поколения (по 1.0 г два раза в день внуримышечно или внутривенно). При хроническом остеомиелите у 4 пациентов дополнительно назначался Клиндамицин (внутрь по 300 Мг 3 раза в день до снятия швов).
Тактику послеоперационной коррекции уровня сахара крови вырабатывали совместно с эндокринологом. У большинства больных в течение первых 24–48 ч после операции отмечалось повышение уровня сахара крови до 9–17 ммоль/л, что было обусловлено операционной травмой, поэтому схему коррекции уровня глюкозы крови не меняли. В течение 2–3 дней после операции уровень сахара стабилизировался в пределах 3–9 ммоль/л. Хотели бы отметить, что болевой синдром в раннем послеоперационном периоде был слабо выражен (за счет наличия дистальной полинейропатии) и купировался в течение 3–5 дней при приеме НПВП (Кетопрофен 2,0 мл в\м 2-3 раза в день).
Первую перевязку после операции проводили на следующий день с использованием антисептических растворов: 0,5 % спиртовой раствор Хлоргексидина на операционные раны, 10% раствор Бетадин на язвенные дефекты. Предварительно обработав раны раствором Мирамистин 0,01%. Перевязки осуществляли ежедневно или через день (в зависимости от количества раневого отделяемого) до полного заживления раневого дефекта.
После операций на костях, на начальном этапе исследования активизация пациентов осуществлялась на следующий день после операции с нагрузкой в разгрузочном полуботинке по типу Бару-ка (Рис.1). Однако от данной тактики было принято отказаться после получения нагноения п\о гематомы (n=1). В последующем, в первые 14 дней исключалась нагрузка на оперированную конечность. В этот период пациенты перемещались с помощью костылей или на кресле – каталке. Затем плавно возрастающая нагрузка без средств дополнительной опоры была разрешена в разгрузочном полуботинке Барука до 1,5-2–х месяцев после операции.

Рис.1 Разгрузочный полуботинок (ботинок Барука).
У 4-х больных, у которых была резецирована головка плюсневой кости по поводу хронического остеомиелита, фиксации каким – либо имплантом не проводилось. Данным пациентам в послеоперационном периоде осуществлялось тейпирование соответствующего пальца узким бинтом в положении коррекции в течение месяца. Техника бинтования не являлась сложной чтобы пациент мог самостоятельно её выполнять: туры повязки поочерёдно накладываются на каждый палец, отделяя один от другого. Через месяц после операции, пациент переставал использовать бинтование, продолжая носить разгрузочную обувь, корректор деформации пальцев. В качестве корректора деформации пальца использовалось предложенное нами устройство [9] в виде трикотажной мягкой петли фиксированной в плоской подушечке, в которую вставляется палец (Рис. 2).
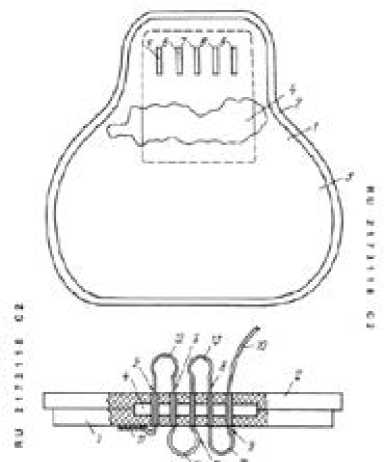
Рис.2 Устройство для коррекции молоткообразной деформации пальцев (Патент RU 217 3118 C2).
По истечению этого срока после операции на костях осуществлялся переход на ортопедическую обувь со специальной стелькой , которые предназначены для пациентов с сахарным диабетом без дополнительных ортопедических приспособлений (Рис .3).

Рис. 3 Внешний вид ортопедической обуви и стельки предназначенных для пациентов с СДС.
У такой обуви есть ряд общих характеристик:
-
1. ригидная негнущаяся подошва с перекатом «rockersole» или «rollersole» ;
-
2. мягкий верх без подноска;
-
3. ширина обуви не менее ширины стопы;
-
4. скошенный передний край каблука (снижает вероятность получения травм и падений);
-
5. достаточная глубина модели для возможности ношения специальной стельки[10-14].
Обработка кожи мест повышенного механического воздействия после заживления ран осуществлялась при помощи кремов с высоким содержанием мочевины.
Иной режим послеоперационной активизации применялся если операция проводилась только на мягких тканях (тено-томии сухожилий сгибателей и разгибателей): полная нагрузка начиналась на следующий день после операции, но в разгрузочном полуботинке по типу Барука. Если больные, перенесшие вмешательство на костях переходили на ортопедическую обувь и стельку через 1,5-2 месяца, то пациенты после коррекции деформации только за счет мягких тканей делали это через 14 дней после операции.
После полного заживления ран пациентам предписывалось использовать крема с высоким уровнем мочевины для ухода за кожей стоп. Аккуратно обрабатывать места особенно толстого кожного покрова удаляя избыток ороговевающего эпителия с помощью близких людей или пользуясь услугами медицинского педикюра. Обрабатывать ногтевые пластины, не обрезая их коротко, но и в то же время, не допуская контакта их с соседними пальцами.
Результаты
Результаты лечения оценивали через 2 месяца (ближайший результат), через 6 месяцев (как среднесрочный результат) и через 3 года как результат отдаленный.
Во всех 33-х случаях, когда проводилось хирургическое лечение у пациента с язвой, удалось достичь её заживления в срок до 6-и месяцев. За счет выполнения предотвращающих появление язвенных дефектов оперативных вмешательств ( п = 6) удалось избежать рецидива язвообразования в течение всего периода наблюдения.
Послеоперационные раны зажили первично, если хирургический доступ осуществлялся, минуя язвенный дефект. Язвенные дефекты в таком случае зажили в течение 2 месяцев у всех пациентов.
У 4 больных, которые были оперированы на фоне хронического инфекционного поражения головки плюсневой кости и которым, последняя была резецирована, послеоперационная рана (сформированная с иссечением имеющегося язвенного дефекта) заживала вторично в течение 3-х месяцев . Рецидива деформации и образования новых нейропатических язв не было в течение всего периода наблюдения.
В одном случае после хирургического лечения наблюдался рецидив язвообразования через 3 года. Данной пациентке выполнена нефиксируемая остеотомия 2-4 плюсневых костей по поводу поперечной распластанности и наличия нейропатической язвы под головками 4 и 3 плюсневых костей. Ещё в одном случае наблюдалось нагноение области операционной раны (после мининвазивной остеотомии плюсневых костей) пациентке с поперечной распластанностью и язвой на подошвенной по- верхности в проекции головок 3-4 плюсневых костей. Данной пациентке произведено дренирование нагноившейся гематомы с вторичным заживлением раны без рецидива язвообразования.
Для скрининга ортопедического статуса стоп у изучаемых пациентов применялась шкала AOFAS, предложенная H. Kitaoka с соавторами [15], которая получила наиболее широкое распространение при оценке ортопедического статуса у больных со статическими деформациями переднего отдела стоп.
В двух случаях отмечалось появление поверхностных язвенных дефектов Wagner I через 1 год и через 8 месяцев. Это сопровождалось нарушением ортопедического режима: пренебрежение ношением ортопедической обуви и стельки. В этих случаях удалось добиться заживления язвенных дефектов и компенсации биомеханических нарушений за счет ношения болуботинка Барука в течение 1 –го месяца с последующим возвратом к предписанному режиму.
Более чем у половины пациентов (n= 19) на разных сроках послеоперационного периода (от 6-и месяцев до 3-х лет) отмечались новые предъязвенные изменения: гиперкератоз кожного покрова, кровоизлияние в дерму в месте повышенного механического воздействия. Данные явления удалось купировать или уменьшить за счет смены стельки в обуви на индивидуальную или новую, полного перехода на ортопедическую диабетическую обувь со стелькой (как для уличного, так и для домашнего использования).
К сроку 2 месяца после операции все оперированные больные, которым выполнялись операции на костях (n=34) имели только «удовлетворительный» балл от 50 до 70. Это обусловлено необходимостью ношения разгрузочного ботинка, сохранением слабого болевого синдрома в области операционного вмешательства. Те больные, которым выполнялись вмешательства только на мягких тканях (n=5), через 2 месяца имели «хороший» балл от 70 до 94.
Через 6 месяцев и 3 года, когда больные стали использовать ортопедическую обувь, при этом отсутствовал болевой синдром и нейропатическая язва, количество баллов согласно шкале AOFAS было от 72 до 92; через 3 года – от 75 до 95. У пациентов, которым выполнялась резекция головки плюсневой кости (n=5), через 6 месяцев балл AOFAS составлял от 50 до 70, через 3 года – от 52 до 72, что соответствует оценке «удовлетворительно», и обусловлено гипермобильностью соответствующего пальца, тыльной его девиацией (Таблица 3, Рис. 4).
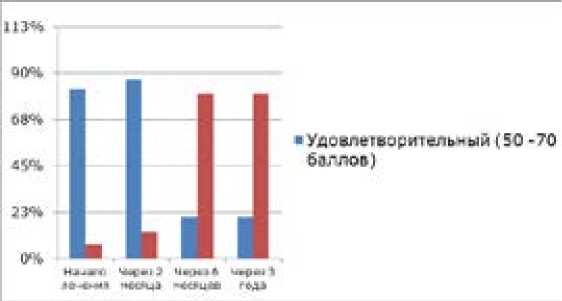
Рис.4 Ортопедический статус согласно шкале AOFAS
Таблица 3Ортопедический статус согласно шкале AOFAS
|
Исходно |
Через 2 месяца |
Через 6 месяцев |
Через 3 года |
p |
|
|
Пациенты, которым выполнялись операции на костях (n=34) |
69 [60; 76] |
58 [52; 65] |
78 [75; 86] |
83 [79; 90] |
p<0.05 |
|
Пациенты, которым выполнялась резекция головки плюсневой кости (n=5) |
64[58;71] |
81 [76; 88] |
59 [53; 65] |
61 [56; 65] |
p<0.05 |
Список литературы Ортопедический режим после хирургического лечения статических деформаций переднего отдела стоп у пациентов с синдромом диабетической стопы
- Г.Р. Галстян, О.К. Викулова*, М.А. Исаков, А.В. Железнякова, А.А. Серков, Д.Н. Егорова, Е.В. Артемова, М.В. Шестакова, И.И. Дедов. ЭПИДЕМИОЛОГИЯ СИНДРОМА ДИАБЕТИЧЕСКОЙ СТОПЫ И АМПУТАЦИЙ НИЖНИХ КОНЕЧНОСТЕЙ В РОССИЙСКОЙ ФЕДЕРАЦИИ ПО ДАННЫМ ФЕДЕРАЛЬНОГО РЕГИСТРА БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ (2013–2016 ГГ.). Сахарный диабет. 2018;21(3):170-177 [GagikR. Galstyan, OlgaK. Vikulova*, MichailA. Isakov, AnnaV. Zheleznyakova, AlexeyA. Serkov, DariaN. Egorova, EkaterinaV. Artemova, MarinaV. Shestakova, IvanI. Dedov. TRENDS IN THE EPIDEMIOLOGY OF DIABETIC FOOT AND LOWER LIMB AMPUTA TIONS IN RUSSIAN FEDERATION ACCORDING TO THE FEDERAL DIABETES REGISTER (2013–2016). Diabetes Mellitus. 2018;21(3):170-177 (In Russ.)] https://doi.org/10.14341/dm9688
- Миронов С.П., Очкуренко А.А., Андреева Т.М. ТРАВМАТИЗМ И ЗАБОЛЕВАЕМОСТЬ КОСТНО-МЫШЕЧНОЙ СИСТЕМЫ В РОССИЙСКОЙ ФЕДЕРАЦИИ. Материалы XI Всероссийского съезда травматологов-ортопедов Том II. 2018. С.53-56. Режим доступа:http://cabinet.ator-rf.ru/materials/index . Ссылка активна на 11.03.2020. [MironovS.P., OchkurenkoA.A., AndreyevaT.M. TRAVMATIZM I ZABOLEVAEMOST KOSTNO-MYShEChNOY SISTEMY V ROSSIYSKOY FEDERATsII. Materialy XI Vserossyskogo syezda travmatologov-ortopedov Tom II. 2018. S.53-56. Available at: http://elibrary.ru/item.asp?id=26636130. Accessed 11.03.2020. (In Russ.)].
- Сорокин Е.П., Карданов А.А., Ласунский С.А. и др. Хирургическое лечение вальгусного отклонения первого пальца стопы и его возможные осложнения (обзор литературы). Травматология и ортопедия России // 2011; 4 (62): 123-130. [SorokinYe.P., KardanovA.A., LasunskyS.A. idr. Khirurgicheskoye lecheniye valgusnogo otkloneniya pervogo paltsa stopy i ego vozmozhnye oslozhneniya (obzor literatury). Travmatologiya i ortopediya Rossii // 2011; 4 (62): 123-130. (In Russ.)].https://doi.org/10.21823/2311-2905-2011--4-123-130
- Ежов М.Ю. Диагностика и лечение вальгусной деформации первого пальца стопы: Дис. ... канд. мед. наук. Нижний Новгород: ФГБУ «Нижегородский НИИТО», 2005. 158. [EzhovM.Yu. Diagnostika i lecheniye valgusnoy deformatsii pervogo paltsa stopy: Dis. ... kand. med. nauk. NizhnyNovgorod: FGBU «Nizhegorodsky NIITO», 2005; 158. (InRuss).]
- Payr E.. Pathologie und Therapie des Hallux valgus. Braunmuller, Wienund Leipzig. 1894.
- Попов А.В., Зоря В.И. Современная система оперативной коррекции поперечно-распластанной стопы с вальгусным отклонением первого пальца // Травматология и ортопедия России.-2000.-2(3).-С.55-59. [PopovA.V., ZoryaV.I. Sovremennayasistemaoperativnoykorrektsiipoperechno-rasplastannoystopysvalgusnymotkloneniyempervogopaltsa. TravmatologiyaiortopediyaRossii. 2000; 2(3): 55-59. (InRuss.)].
- Бобров Д.С., Слиняков Л.Ю., Ригин Н.В. Перегрузочная метатарзалгия: патогенез, биомеханика и хирургическое лечение (аналитический обзор литературы) // Вестник Российской академии медицинских наук. - 2017. - Т. 72. - №1. - C. 53-58.[Bobrov D.S., Slinjakov L.J., Rigin N.V. The Primary Metatarsalgia: Pathogenesis, Biomechanics and Surgical Treatment // Annals of the Russian academy of medical sciences. - 2017. - Vol. 72. - N. 1. - P. 53-58. (In Russ.)]. doi: 10.15690/vramn756
- Wagner F.M. A classification and treatment program of diabetic, neuropathic and disvascular foot problems. In: American Academy of Orthopaedic Surgeons instructional course lectures. St. Luis: Mosby year book. 1979: 143-165. https://doi:10.1177/107110079001100211
- Патент РФ № 97120180/14, 1997.12.03 Корректор пальцев стопы // Патент России № RU 2 173 118 C2 / Паршиков М.В., Сергеева В.В., Попов А.В., Паршиков И.В.
- Nawoczenski D., Birke J., Coleman W.. Effects of rocker sole designs on plantar forefoot pressures. J. Am. Podiatr. Med. Assoc. 1998;(78): 455-460. https://doi.org/10.7547/87507315-78-9-455
- Van Schie, C., Ulbrecht, J. S., Becker, M. B., & Cavanagh, P. R. (2000). Design Criteria for Rigid Rocker Shoes. Foot & Ankle International, 21(10), 833–844. https://doi.org/10.1177/107110070002101007
- Uccioli L. The role of footwear in prevention of diabetic foot problems.The Diabetic Foot. Ed. By A. Veves, J. Giurini, F. LoGerfo. 2nd ed. 2006: 523-543.https://doi.org/10.1007/978-1-59745-075-1
- Tovey F.I. The manufacture of diabetic footwear. DiabetMed. 1984: 69-71.
- Bus S.A. , Ulbrecht J. S., Cavanagh P. R. Pressure relief and load redistribution by custom-made insoles in diabetic patients with neuropathy and foot deformity. Clin. Biomech. 2004; 19(6): 629 – 638.https://doi.org/10.1016/j.clinbiomech.2004.02.010
- Kitaoka, H.B., et al., Clinical rating systems for the anklehindfoot, midfoot, hallux, and lesser toes//Foot Ankle Int, 1994. 15(7): 349-53.
- Fleischli, J. E., Anderson, R. B., & Davis, W. H. Dorsiflexion Metatarsal Osteotomy for Treatment of Recalcitrant Diabetic Neuropathic Ulcers. Foot & Ankle International. 1999; 20(2): 80 - 85. http://dx.doi:10.1177/107110079902000203
- Tamir, E., Vigler, M., Avisar, E., & Finestone, A. S. Percutaneous Tenotomy for the Treatment of Diabetic Toe Ulcers. Foot & Ankle International.2013; 35(1):38-43. https://doi.org/10.1177/1071100713509604
- Mueller MJ, Sinacore DR, Hastings MK, Strube MJ, Johnson JE. Effect of Achilles tendon lengthening on neuropathic plantar ulcers. A randomized clinical trial. J Bone Joint Surg Am. 2003;85-A(8):1436-1445. https://doi.org/10.2106/00004623-200308000-00003
- Kalantar Motamedi A., Ansari M. Comparison of Metatarsal Head Resection Versus Conservative Care in Treatment of Neuropathic Diabetic Foot Ulcers. Journal of Foot and Ankle Surgery. 2017; 56 (3): 428-433. https://doi.org/10.1053/j.jfas.2016.11.019
- Armstrong D.G., Lavery L.A., Vazquez J.R., et al. Clinical efficacy of the first metatarsophalangeal joint arthroplasty as a curative procedure for hallux interphalangeal joint wounds in patients with diabetes. Diabetes Care. 2003; 26: 3284-3287. https://doi.org/10.2337/diacare.26.12.3284
- Biz C, Gastaldo S, Dalmau-Pastor M, Corradin M, Volpin A, Ruggieri P. Minimally invasive distal metatarsal diaphyseal osteotomy (DMDO) for chronic plantar diabetic foot ulcers. Foot Ankle Int. 2018;39:83-92. https://doi.org/10.1177/1071100717735640
- Frykberg Robert G.. The high risk foot in diabetes mellitus. Prophylactic Surgery in the Diabetic Foot. Churchill Livingstone. 1991: 513-541.
- Singh N., Armstrong D.G., Lipsky B.A.. Preventing Foot Ulcers in Patients With Diabetes. JAMA. 2005;293(2):217–228. https://doi:10.1001/jama.293.2.217
- Önder İ. Kılıçoğlu, Mehmet Demirel, Şamil Aktaş. New trends in the orthopaedic management of diabetic foot.EFORT Open Reviews 2018 3:5, 269-277. https://doi: 10.1302/2058-5241.3.170073 25. Armstrong David G., Lawrence A. Lavery, Sharone Stern, Lawrence B. Harkless. Is Prophylactic Diabetic Foot Surgery Dangerous? The Journal of Foot and Ankle Surgery. 1996; 35 (6): 585–589. https://doi:10.1016/s1067- 2516(96)80134-7
- Yammine K., Assi C.. Surgical Offloading Techniques Should be Used More Often and Earlier in Treating Forefoot Diabetic Ulcers: An Evidence-Based Review. The International Journal of Lower Extremity Wounds. 2019; 20: 153473461988836. https://doi.org/10.1177/1534734619888361
- Yammine K, Nahed M, Assi C. Metatarsal Osteotomies for Treating Neuropathic Diabetic Foot Ulcers: A Meta-analysis. Foot & Ankle Specialist. SAGE Publications; 2018 Dec 19;12(6):555–62. http://dx.doi.org/10.1177/1938640018819784
- Bonanno D.R., Gillies E.J. Flexor tenotomy improves healing and prevention of diabetes-related toe ulcers: a systematic review. J Foot Ankle Surg. 2017;56:600-604. https://doi.org/10.1053/j.jfas.2017.02.011
- Botezatu I., Laptoiu D.. Minimally invasive surgery of diabetic foot - review of current techniques. J Med Life. 2016;9(3):249–254.
- Bus SA, Armstrong DG, Gooday C, et al. Guidelines on offloading foot ulcers in persons with diabetes (IWGDF 2019 update).DiabetesMetab Res Rev. 2020;36 (S1):e3274. https://doi.org/10.1002/dmrr.3274


