Особенность экспрессии каспазы-3 в гиппокампе при моделировании острого эпилептического припадка
Автор: Демяшкин Г.А., Шаповалова Е.Ю., Григорян М.С., Зорин И.А.
Журнал: Морфологические ведомости @morpholetter
Рубрика: Краткие сообщения
Статья в выпуске: 2 т.31, 2023 года.
Бесплатный доступ
Эпилепсия является одной из наиболее распространенных неврологических патологий, однако биологический субстрат заболевания до сих пор остается малоизученным. В ряде немногочисленных исследований было показано, что у экспериментальных животных после приступа эпилепсии отмечается повышение уровня некоторых каспаз, но имеющихся данных недостаточно для полного представления о природе каспазного каскада при эпилепсии, и, особенно, его терминальной фазы. Особого интереса заслуживает анализ патоморфологических изменений структур гиппокампа на фоне острого эпилептического припадка в корреляции между нейрональной потерей и терминальной фазой апоптоза или количественная оценка активности каспазы-3. Целью исследования явилась иммуногистохимическая оценка экспрессии каспазы-3 в гиппокампе в экспериментальной модели эпилепсии на лабораторных мышах. Животные были поделены на две группы: животным первой группы (n=28) внутрибрюшинно вводили препарат пентилентетразола однократно в дозе 45 мкг/кг для моделирования острого приступа эпилепсии, который оценивался по модифицированной шкале Расина, вторая группа животных была контрольной (n=20). Животных выводили из эксперимента через 3 часа и последовательно на 1, 3 и 5 сутки от начала введения препарата для динамического исследования изменений гиппокампа. Выведение животных из эксперимента осуществляли путем введения высоких доз анестетика. Фрагменты головного мозга животных исследовали с помощью окраски по Нисслю и оценивали количественные показатели экспрессии каспазы-3 при помощи иммуногистохимического метода в субрегионах СА1, СА3 и зубчатой извилины гиппокампа. Через 24 часа после моделирования острого эпилептического припадка обнаружили признаки гиппокампального склероза (глиоз, потерю нейронов) и увеличение количества нейронов, экспрессирующих каспазу-3 в 2,68 раза по сравнению с контрольной группой. В результате эксперимента выявили, что потеря нейронов гиппокампа субрегиона CA3 ассоциирована с увеличением экспрессии каспазы-3 через 24 часа после моделирования острого генерализованного припадка с помощью инъекции пентилентетразола.
Гиппокамп, эпилепсия, нейроны, каспаза-3, апоптоз
Короткий адрес: https://sciup.org/143180796
IDR: 143180796 | DOI: 10.20340/mv-mn.2023.31(2).801
Features of the caspase-3 expression in the hippocampus at the modelling of the experimental acute epileptic fit
Epilepsy is one of the most common neurological pathologies, but the biological substrate of the disease is still poorly understood. A few studies have shown that in experimental animals after an epileptic fit there is an increase in the level of some caspases, but the available data are not enough to fully understand the nature of the caspase cascade in epilepsy, and especially its terminal phase. Of particular interest is the analysis of morphological changes in the structures of the hippocampus on the background of an acute epileptic fit in the correlation between neuronal loss and the terminal phase of apoptosis or the quantitative assessment of caspase-3 activity. The aim of the study was the immunohistochemical evaluation of caspase-3 expression in the hippocampus in an experimental model of epilepsy in laboratory mice. The animals were divided into two groups, the animals of the first group (n=28) were intraperitoneally injected with pentilenetetrazole once at a dose of 45 μg/kg to simulate an acute epileptic fit, which was assessed by the modified Racine scale, the second group of animals was the control (n=20). Animals were taken out of the experiment after 3 hours and consecutively on days 1, 3, and 5 from the start of the drug administration for a dynamic study of changes in the hippocampus. Animals were withdrawn from the experiment by introducing high doses of anaesthetic. Animal brain fragments were examined by Nissl staining and caspase-3 expression was quantified by immunohistochemistry in the subregions CA1, CA3 and the dentate gyrus of the hippocampus. 24 hours after the modelling of an acute epileptic fit, the preparations showed signs of hippocampal sclerosis (gliosis, loss of neurons) and an increase in the number of neurons expressing caspase-3 by 2.68 times compared to the number of neurons in the preparations of animals in the control group. As a result of the experiment, it was revealed that the loss of neurons in the hippocampus of the CA3 subregion is associated with an increase in the expression of caspase-3 24 hours after the simulation of an acute generalized seizure using an injection of pentilenetetrazole.
Текст краткого сообщения Особенность экспрессии каспазы-3 в гиппокампе при моделировании острого эпилептического припадка
Демяшкин Г.А., Шаповалова Е.Ю., Григорян М.С., Зорин И.А. Особенность экспрессии каспазы-3 в гиппокампе при моделировании острого эпилептического припадка. Морфологические ведомости. 2023;31(2):801. (2).801
Demyashkin GA, Shapovalova EY, Grigoryan MS, Zorin IA. Features of the сaspase-3 expression in the hippocampus at the modelling of the experimental acute epileptic fit. Morfologicheskie Vedomosti – Morphological newsletter. 2023;31(2):801. (2).801
Введение. Эпилепсия является одной из наиболее распространенных неврологических патологий. Несмотря на длительное изучение эпилепсии и эпилептических припадков нейробиологиче-ский субстрат заболевания до сих пор остается малоизученным [1-4]. В настоящее время согласно протоколу Международной лиги по борьбе с эпилепсией (ILAE) склероз гиппокампа (мезиальный височный склероз) характеризуется потерей нейронов и глиозом и в котором выделяют 3 формы: типичная (I тип) и атипичная (II-III типы) [5]. Тем не менее, на сегодня остается неясным, является ли склероз гиппокампа причиной или следствием эпилепсии и эпилептических припадков [1, 6]. Для изучения эпилептогенеза и нейробиологического субстрата широко применяется экспериментальный метод моделирования эпилептических припадков. В большинстве работ отмечалось, что в эксперименте у животных обнаруживаются признаки повреждения гиппокампа, характерные для пациентов с эпилепсией [710]. Однако вопрос о механизмах нейронального повреждения до сих пор остается открытым. В ряде немногочисленных исследований было показано, что у экспериментальных животных после приступа эпилепсии отмечается повышение уровня некоторых каспаз в нейронах [11-12]. Такие данные позволяют предположить, что нарушение местного гомеостаза запускает апоптотический каскад, который приводит к гибели нейронов. Известно, что в головном мозге инициация апоптоза происходит через каспазы-8, -9, -10, которые активируют терминальные каспазы -3, -6, -7 [13-14]. Имеющихся данных недостаточно для полного представления о природе каспазного каскада при эпилепсии, и, особенно, его терминальной фазы. Особого интереса заслуживает анализ патоморфо-логических изменений структур гиппокампа на фоне острого эпилептического припадка в корреляции между нейрональной потерей и терминальной фазой апоптоза и количественная оценка активности каспазы-3 в связи с этим.
Цель исследования - иммуногистохимическая оценка экспрессии каспазы-3 в гиппокампе в экспериментальной модели эпилепсии на лабораторных мышах.
Материалы и методы исследования. Экспериментальное морфологическое исследование проводили в лабораториях Медицинской академии имени С.И. Георгиевского Крымского федерального университета имени В.И. Вернадского (Симферополь) и Институте трансляционной медицины и биотехнологии Первого Московского государственного медицинского университета имени И.М. Сеченова (Москва). В качестве животных моделей использовали самцов половозрелых мышей популяции CBA (весом 30-35 грамм, 12-ти недель жизни, n=30). Все манипуляции осуществляли согласно международным рекомендациям и руководствам по проведению медикобиологических исследований по уходу и использованию лабораторных животных (ILAR, DELS) и Правилам лабораторной практики и приказа Министерства здравоохранения РФ № 199-н от 01.04.2016 «Об утверждении правил лабораторной практики». Животные были поделены на группы: I-я (n=28) - моделирование острого приступа эпилепсии, который оценивался по модифицированной шкале Расина [10]; II-я группа (n=20) - контрольная. Для моделирования острого генерализованного приступа эпилепсии животным вводили эпилептогенный препарат пен-тилентетразол интраперитонеально, однократно, в дозе 45 мкг/ кг. Животных I-й и II-й группы выводили из эксперимента через 3 часа и последовательно на 1, 3 и 5 сутки от начала введения препарата для динамического исследования изменений в гиппокампе. Выведение животных из эксперимента осуществляли путем введения высоких доз анестетика. Для оценки морфологического субстрата эпилепсии при исследовании гиппокампа экспериментальных животных изучали субрегионы СА1, СА3 и область зубчатой извилины. Фрагменты головного мозга фиксировали в 10% нейтральном формалине, забуфе-ренном по Лилли при рН 7,2-7,4, затем заливали в парафин. После депарафинизации и регидратации парафиновых срезов их окрашивали по Нисслю. Иммуногистохимическое исследование проводили по стандартному протоколу в автоматическом режиме в иммуногистостейнере Bond-Max (Leica, Германия). Использовались первичные мышиные моноклональные антитела к Caspase 3 (3CSP03; 0,1 мл) и вторичные – универсальные антитела (HiDef Detection™ HRP Polymer system, Cell Marque, США). Количество иммуно-позитивных клеток подсчитывали в 10 полях зрения препарата гиппокампа при увеличении х400. Для проверки выборки полученных данных на нормальность распределения использовали Критерий Шапиро–Уилка. Для проверки различий значений использовали t-критерий Стьюдента. Статистически значимыми считали результаты при p<0,05.
Результаты исследования и обсуждение. У всех животных I группы отмечали генерализованный эпилептический припадок, который, согласно модифицированной шкале Расина, соответствовал 4 (n=14), 5 (n=11) и 3 (n=3) баллам. Среднее время приступа составило 5,19±0,7 минут. В контрольной группе после интраперитонеальной инъекции физиологического раствора у животных не обнаружили судорожной активности, их поведение оценили на –1 балл по шкале Расина. После развития эпилептического приступа у всех животных не наблюдали признаков нарушения гемодинамики и расстройства поведенческих реакций. При гистологическом исследовании микропрепаратов гиппокампа опытной группы, окрашенных по Нисслю, через 3 часа после интраперитонеальной инъекции пентилентетразола нарушения его гистоархитектоники не обнаружили. Через 24 часа у животных опытной группы визу- ализировали дезинтеграцию темных нейронов с признаками пикноза и трудно различимыми границами между цитоплазмой и ядром (рис. 1). В динамике на 3 и 5 сутки отмечали тенденцию к уменьшению количества патологических нейронов.
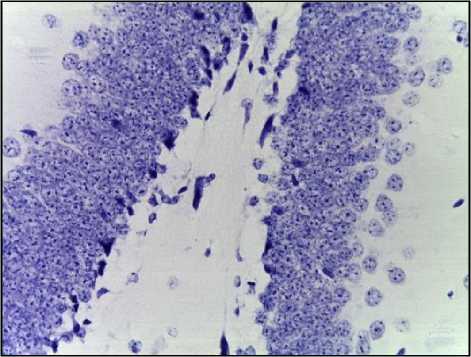
Рис. 1. Микрофото гистологического препарата головного мозга мыши экспериментальной группы. Окр.: по Нисс-лю. Ув.: х200
В контрольной группе наблюдали нормальное гистологическое строение вещества головного мозга и зоны гиппокампа. При исследовании уровня каспазы-3 в субрегионе CA3 через 24 часа после моделирования острого эпилептического припадка также наблюдали увеличение положительно окрашенных пирамидальных нейронов гиппокампа в 2,68 раза (рис. 2) по сравнению с контрольной группой (таблица 1). В других временных точках количество иммунопозитивных клеток статистически значимо не отличалось от контрольных значений.
Таблица 1
Относительное количество нейронов в % экспрессирующих каспазу-3 в субрегионе СА3 гиппокампа мыши при моделировании эпилептического припадка (M ± a)
|
Маркер |
Срок |
Группа I |
Группа II |
p-значение |
|
Каспаза-3 |
3 часа |
7,71 ± 1,12 |
6,80 ± 0,84 |
0,5 |
|
Каспаза-3 |
1 сутки |
21,95 ± 3,03 |
6,60 ± 1,96 |
< 0,01 |
|
Каспаза-3 |
3 сутки |
10,43 ± 1,72 |
7,80 ± 0,92 |
0,2 |
|
Каспаза-3 |
5 сутки |
8,20 ± 2,10 |
7,40 ± 1,14 |
0,39 |
Настоящее исследование посвящено изучению молекулярных механизмов клеточной гибели нейронов гиппокампа при остром генерализованном приступе эпилепсии, вызванного пентилентетразо-лом у мышей линии СВА. Для оценки эффекта острого эпилептического припадка (появление мезиального склероза) мы использовали окраску по Нисслю, позволяющую обнаружить темные нейроны, роль которых в настоящее время до конца не изучена. Раньше предполагалось, что их количество прямо пропорционально степени повреждения головного мозга, однако, на сегодня такая корреляция подвергается сомнению [15–17].
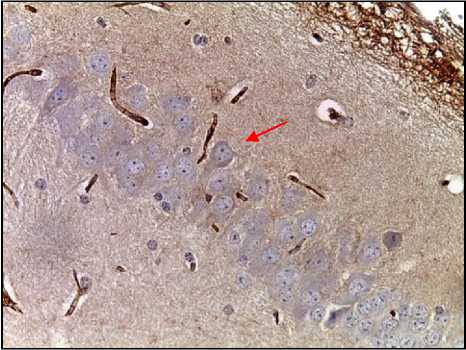
А
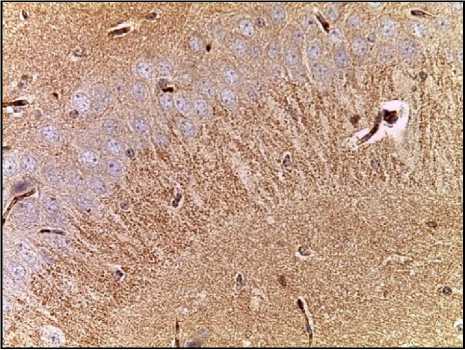
Б
Рис. 2. Микрофото гистологических препаратов головного мозга мыши экспериментальной (А) и контрольной (Б) групп СА3 региона гиппокампа через 24 часа после инъекции. Окр.: иммуногистохимическая с антителами к каспазе-3, докрашивание гематоксилином. Ув.: х400
Иммуногистохимическое исследование уровня активированной каспазы-3 показало, что через 24 часа после введения препарата пентилентетразола наблюдается наибольшее количество нейронов, экспрессирующих каспазу-3. Как известно, каспаза-3 является терминальной сигнальной молекулой в каспазном каскаде, инициирующем апоптоз. Принято считать, что при эпилептических припадках активация каспазы-3 происходит в ответ на повреждение и фрагментацию молекул ДНК в пирамидных нейронах, преимущественно СА1-СА3 региона гиппокампа [18-19]. Более того, существуют исследования, в которых ингибирование каспазы-3 приводило к увеличению количества выживших клеток после генерации эпилептического припадка [20]. Результаты настоящего исследования согласуются с устоявшимися представлениями о роли каспазы-3 в регуляции апоптоза, так как наибольшая экспрессия каспазы-3 ассоциируется с максимальной клеточной гибелью [21]. Особо стоит отметить, что уже на 5-е сутки гистоархитектоника гиппокампа соответствует норме. Та- кое быстрое восстановление не исключает того явления, что каспаза-3 в гиппокампе может регулировать не только терминальную стадию апоптоза, но и участвовать в ремоделировании синапсов и цитоскелета, клеточной дифференцировке и реинтеграции нейритов, необходимых для нейропластичности, как было показано в единичных исследованиях [22].
Заключение. Таким образом, суммируя полученные данные, можно отметить, что однократная инъекция пентилен-тетразола вызывает генерализованный эпилептический припадок, ассоциированный с увеличением экспрессии каспаза-3 при нейрональной гибели. В дальнейшем необходимо продолжить изучение роли каспазы-3 в этом явлении, так как, возможно, она не ограничивается лишь апоптоти-ческим действием. Потеря нейронов гиппокампа субрегиона CA3 ассоциирована с увеличением экспрессии каспазы-3 через 24 часа после моделирования острого генерализованного припадка с помощью инъекции пентилентетразола.
Список литературы Особенность экспрессии каспазы-3 в гиппокампе при моделировании острого эпилептического припадка
- Thom M. Review: Hippocampal sclerosis in epilepsy: a neuropathology review. Neuropathol Appl Neurobiol. 2014;40(5):520-543. DOI: 10.1111/nan.12150
- Chatzikonstantinou A. Epilepsy and the hippocampus. Front Neurol Neurosci. 2014;34:121-142. DOI: 10.1159/000356435
- Wolinski P, Ksiazek-Winiarek D, Glabinski A. Cytokines and Neurodegeneration in Epileptogenesis. Brain Sci. 2022;12(3):380. DOI: 10.3390/brainsci12030380
- Beghi E. The Epidemiology of Epilepsy. NED. 2020;54(2):185-191. DOI: 10.1159/000503831
- Blümcke I, Thom M, Aronica E et al. International consensus classification of hippocampal sclerosis in temporal lobe epilepsy: a Task Force report from the ILAE Commission on Diagnostic Methods. Epilepsia. 2013;54(7):1315-1329. DOI: 10.1111/epi.12220
- Walker MC. Hippocampal Sclerosis: Causes and Prevention. Semin Neurol. 2015;35(3):193-200. DOI: 10.1055/s-0035-1552618
- Kandratavicius L, Balista PA, Lopes-Aguiar C et al. Animal models of epilepsy: use and limitations. Neuropsychiatr Dis Treat. 2014;10:1693-1705. DOI: 10.2147/NDT.S50371
- Löscher W. Animal Models of Seizures and Epilepsy: Past, Present, and Future Role for the Discovery of Antiseizure Drugs. Neurochem Res. 2017;42(7):1873-1888. DOI: 10.1007/s11064-017-2222-z
- Shimada T, Yamagata K. Pentylenetetrazole-Induced Kindling Mouse Model. J Vis Exp. 2018;(136):56573. DOI: 10.3791/56573
- Van Erum J, Van Dam D, De Deyn PP. PTZ-induced seizures in mice require a revised Racine scale. Epilepsy & Behavior. 2019;95:51-55. DOI: 10.1016/j.yebeh.2019.02.029
- Engel T, Henshall DC. Apoptosis, Bcl-2 family proteins and caspases: the ABCs of seizure-damage and epileptogenesis? Int J Physiol Pathophys-iol Pharmacol. 2009;1(2):97-115. PMID: 21383882
- Sun J, Xie C, Liu W et al. The effects of simvastatin on hippocampal caspase-3 and Bcl-2 expression following kainate-induced seizures in rats. International Journal of Molecular Medicine. 2012;30(4):739-746. DOI: 10.3892/ijmm.2012.1076
- Nguyen TTM, Gillet G, Popgeorgiev N. Caspases in the Developing Central Nervous System: Apoptosis and Beyond. Frontiers in Cell and De-velopmental Biology. 2021;9. Accessed January 8, 2023. https://www.frontiersin.org/articles/10.3389/fcell.2021.702404
- Sharangpani A, Takanohashi A, Bell MJ. Caspase Activation in Fetal Rat Brain Following Experimental Intrauterine Inflammation. Brain Res. 2008;1200:138-145. DOI: 10.1016/j.brainres.2008.01.045
- Zimatkin SM, Bon’ EI. Dark Neurons of the Brain. Neurosci Behav Physi. 2018;48(8):908-912. DOI: 10.1007/s11055-018-0648-7
- Ahmadpour S, Behrad A, Vega IF. Dark Neurons: A protective mechanism or a mode of death. Journal of Medical Histology. 2019;3(2):125-131. DOI: 10.21608/jmh.2020.40221.1081
- Ooigawa H, Nawashiro H, Fukui S et al. The fate of Nissl-stained dark neurons following traumatic brain injury in rats: difference between neo-cortex and hippocampus regarding survival rate. Acta Neuropathol. 2006;112(4):471-481. DOI: 10.1007/s00401-006-0108-2
- Liu JP, Chang LR, Gao XL, Wu Y. Different expression of caspase-3 in rat hippocampal subregions during postnatal development. Microsc Res Tech. 2008;71(9):633-638. DOI: 10.1002/jemt.20600
- Basaranlar G, Derin N, Kencebay Manas C et al. The effects of sulfite on cPLA2, caspase-3, oxidative stress and locomotor activity in rats. Food and Chemical Toxicology. 2019;123:453-458. DOI: 10.1016/j.fct.2018.11.021
- Narkilahti S, Nissinen J, Pitkänen A. Administration of caspase 3 inhibitor during and after status epilepticus in rat: effect on neuronal damage and epileptogenesis. Neuropharmacology. 2003;44(8):1068-1088. DOI: 10.1016/s0028-3908(03)00115-1
- Baculis BC, Weiss AC, Pang W et al. Prolonged seizure activity causes caspase dependent cleavage and dysfunction of G-protein activated in-wardly rectifying potassium channels. Sci Rep. 2017;7(1):12313. DOI: 10.1038/s41598-017-12508-y
- Tzeng TT, Tsay HJ, Chang L et al. Caspase 3 involves in neuroplasticity, microglial activation and neurogenesis in the mice hippocampus after intracerebral injection of kainic acid. J Biomed Sci. 2013;20(1):90. DOI: 10.1186/1423-0127-20-90


