Особенность преобразования световой энергии в биологических фотоэлементах
Автор: Буханов Е.Р., Логинов Ю.Ю., Познахарева О.А., Волочаев М.Н., Шабанов В.Ф.
Журнал: Сибирский аэрокосмический журнал @vestnik-sibsau
Рубрика: Технологические процессы и материалы
Статья в выпуске: 1 т.27, 2026 года.
Бесплатный доступ
Исследование направлено на анализ преобразования световой энергии в биологических фотоэлементах, влияния структурных изменений тилакоидных мембран, индуцированных внекорневыми подкормками, на перенос энергии в фотосинтетическом аппарате с использованием методов флуоресцентной спектроскопии, что важно, в частности, для разработки моделей жизнеобеспечения в замкнутых космических системах. Для проведения исследований были сформированы контрольная и опытная группы растений. Структурный анализ проводился с использованием просвечивающей электронной микроскопии (ПЭМ), что позволило получить изображения ультратонких срезов листовой пластинки с последующей количественной оценкой морфометрических параметров гран (стопок тилакоидных мембран) хлоропластов. Обработка микрофотографий и статистический анализ выполнялись с применением программного обеспечения на основе искусственного интеллекта (GRANA). Функциональное состояние фотосистем оценивалось по спектрам флуоресценции хлорофилла, зарегистрированным на спектрофлуориметре в режиме 90-градусной геометрии при возбуждении светом с длиной волны 425 нм. Результаты. Установлено, что применение внекорневой подкормки приводит к статистически значимой структурной перестройке тилакоидных мембран. У опытных образцов зафиксировано уменьшение медианной площади гран на ~ 38 %, а их периметра – на ~ 16 %, что свидетельствует о более плотной и упорядоченной упаковке. Одновременно с этим метод флуоресцентной спектроскопии выявил сужение полуширины пика, соответствующего фотосистеме II, на 1,8 нм (8 %) для обработанных растений. Это изменение указывает на снижение энергетической неоднородности антенных комплексов и повышение эффективности переноса энергии возбуждения. Заключение. На основании комплекса проведенных исследований сделан вывод о том, что основным механизмом воздействия внекорневых подкормок является оптимизация наноструктуры тилакоидных мембран, которая, в рамках концепции фотонных кристаллов, создает более благоприятные условия для преобразования световой энергии. Показано повышение регулярности ультраструктурной организации. Полученные результаты подтверждают перспективность использования флуоресцентной спектроскопии в качестве быстрого неинвазивного метода для диагностики физиологического состояния растений в замкнутых космических системах.
Преобразование солнечной энергии, биологический фотонный кристалл, тилакоидные мембраны, флуоресцентная спектроскопия, просвечивающая электронная микроскопия, фотосинтез, перенос энергии
Короткий адрес: https://sciup.org/148333116
IDR: 148333116 | УДК: 535.37 | DOI: 10.31772/2712-8970-2026-27-1-174-186
Specific features of light energy conversion in biological photo-elements
The study aims to analyze the influence of structural changes in thylakoid membranes, induced by foliar fertilization, on energy transfer in the photosynthetic system using fluorescence spectroscopy methods. Control and experimental plant groups were established for the research. Structural analysis was performed using transmission electron microscopy (TEM), which provided images of ultra-thin leaf sections followed by quantitative assessment of the morphometric parameters of chloroplast grana. Micrograph processing and statistical analysis were carried out using artificial intelligence-based software (GRANA). The functional state of the photosystems was evaluated based on chlorophyll fluorescence spectra were obtained using a spectrofluorometer in a 90-degree geometry mode upon excitation with light at a wavelength of 425 nm. Results. It was found that the application of foliar fertilization leads to a statistically significant structural reorganization of the thylakoid membranes. The experimental samples showed a reduction in the median grana area by ~ 38 % and their perimeter by ~ 16 %, indicating denser and more ordered packing. Simultaneously, fluorescence spectroscopy revealed a narrowing of the peak half-width corresponding to photosystem II by 1.8 nm (8%) in the treated plants. This change indicates a reduction in the energetic heterogeneity of the antenna complexes and an increase in the efficiency of excitation energy transfer. Conclusion. Based on the comprehensive studies, it was concluded that the primary mechanism of action of foliar fertilizers is the optimization of the thylakoid membrane nanostructure, which, within the concept of photonic crystals, creates more favorable conditions for light energy conversion. An increase in the regularity of the ultrastructural organization was demonstrated. The obtained results confirm the potential of using fluorescence spectroscopy as a rapid, non-invasive method for diagnosing the physiological state of plants in closed space systems.
Текст научной статьи Особенность преобразования световой энергии в биологических фотоэлементах
Эффективное преобразование солнечной энергии является одной из фундаментальных задач для обеспечения жизнедеятельности замкнутых космических систем и спутниковых систем связи. С точки зрения энергетики биосферы фотосинтез – это ключевой космический процесс, поскольку только он аккумулирует энергию внешнего источника (солнечного света), обеспечивая тем самым прирост свободной энергии и уменьшение энтропии в системе. Таким образом, он служит основой для существования жизни, генерируя кислород и создавая все необходимые органические вещества.
В последние годы активно ведутся исследования по преобразованию световой энергии в биоэлектричество с использованием фотосинтетических биоэлектрохимических систем [1–3].
Если в фотовольтаике инженеры оптимизируют коэффициент полезного действия (КПД) за счет улучшения морфологии и материалов фотоактивных слоев, то в агрономии аналогичная задача решается путем повышения эффективности работы фотосинтетического аппарата растений. Фотосинтез, по своей сути, представляет собой процесс преобразования световой энергии в химическую, где хлоропласт выполняет функцию высокоорганизованной биологической «солнечной батареи» [4].
В обзорной работе А. Г. Яковлева и В. А. Шувалова [5] сообщается, что физическая стадия фотосинтеза демонстрирует феноменально высокую эффективность преобразования световой энергии. Квантовая эффективность первичного разделения зарядов в реакционных центрах приближается к 100 %, а это значит, что практически каждый поглощённый фотон приводит к переносу одного электрона. Это достигается за счёт исключительно быстрого и направленного многоступенчатого переноса электрона по цепи пигментов (P* → Bₐ → Hₐ → Qₐ), где каждый следующий шаг сопровождается потерей энергии, но увеличением стабильности разделённых зарядов. Высокая скорость прямых реакций, значительно превышающая скорости обратных процессов и потерь энергии, обеспечивается оптимальным пространственным расположением пигментов и влиянием белкового окружения. Такая совершенная организация делает первичный акт фотосинтеза уникальным примером высокоэффективного преобразования энергии в живой природе.
В контексте коммерциализации, где каждый ресурс, включая воду и питательные субстраты, строго лимитирован, особую актуальность приобретают высокоэффективные и ресурсосберегающие агротехнологии. Одной из таких технологий является внекорневая подкормка, позволяющая осуществлять целенаправленную доставку макро- и микроэлементов непосредственно в метаболически активные ткани растения, минуя почвенный путь [6; 7]. Этот подход не только обеспечивает быстрое усвоение питательных веществ, но и минимизирует их неизбежные потери, что делает его экономически и экологически предпочтительным для использования в агропромышленных комплексах.
В данном исследовании мы рассматриваем листовую подкормку не просто как агротехнический приём, а как инструмент целенаправленного «инжиниринга» ультраструктуры хлоропластов. Мы предполагаем, что определенные составы удобрений могут действовать аналогично легирующим добавкам в полупроводниках [8] или оптическим покрытиям в солнечных элементах [9], минимизируя потери энергии на структурных дефектах и повышая эффективность её использования.
Ключевым механизмом, определяющим эффективность данной технологии, является ее влияние на ультраструктурную организацию фотосинтетического аппарата, в частности, тилакоидных мембран хлоропластов. Оптимизация пространственного расположения тилакоидов, выступающих в роли природных оптических преобразователей, напрямую определяет эффективность переноса энергии [10]. Для неинвазивной диагностики функционального состояния фотосистем в настоящем исследовании применяется метод флуоресцентной спектроскопии, позволяющий с высокой точностью отслеживать изменения в первичных процессах фотосинтеза, индуцированные воздействием со структурными перестройками, наблюдаемыми методами электронной микроскопии.
Целью настоящей работы являлось изучение влияния структурных изменений тилакоидных мембран, индуцированных внекорневыми подкормками, на перенос энергии в фотосинтетическом аппарате. Для этого методами просвечивающей электронной микроскопии были исследо- ваны изменения в организации тилакоидных мембран и с помощью флуоресцентной спектроскопии была произведена оценка функционального состояние фотосистем. Установленные корреляции между структурой, спектральными характеристиками и продуктивностью позволяют предложить новый подход к оптимизации «биологических фотоэлементов».
Материалы и методы исследований
Культивирование растений. В настоящее время рапс – одна из ведущих сельскохозяйственных культур в мире, ареал возделывания озимого и ярового рапса необычайно широк и охватывает практически все природно-климатические зоны земледелия. Чрезвычайно разнообразна и область его применения. Семена ярового рапса содержат 40–48 % пищевого масла и 18–22 % кормового белка высокого качества, используются для получения масла, идущего на пищевые и технические цели.
Полевые исследования были организованы на территории опытного хозяйства «Михайловское». Исследования по влиянию внекорневых подкормок производилось на рапсе яровом – сорт «Сибирский». Для проведения сравнительного анализа было выделено два экспериментальных участка. На контрольном участке применялась исключительно базовая химическая обработка, направленная на защиту от сорной растительности и возбудителей заболеваний: без обработки гуминатрином, семена протравлены Табу Нео, 6 л/т; обработка гербицидами в фазе стеблевания (до бутонизации); обработка инсектицидом в фазе начала цветения. На другом, помимо указанных защитных мероприятий, осуществлялось листовое питание растений специализированным составом: протравливание семян Табу Нео, 6 л/т + Гуминатрин, 0,5 л/т; обработка гербицидами в фазе стеблевания (до бутонизации); обработка инсектицидом в фазе начала цветения. В результате урожайность составила 20,8 ц/га для контрольных образцов и 21,9 ц/га для опытных. Сырая масса растений увеличилась с 7,98 до 11,72 г, а масса листьев с 4,6 до 6,30 г. При этом, концентрация фотосинтетических пигментов в листьях уменьшилась с 4,2 до 4,156 мг/г сырой массы.
Электронно-микроскопический анализ. Для исследования ультраструктурных особенностей отбирались флаговые листья растений на стадии колошения. Первичная фиксация образцов проводилась с использованием 2,5 % раствора глутарового альдегида на какодилатном буфере (рН 7,4). Последующая фиксация выполнялась в 1% растворе OsO 4 . Дегидратация проводилась в спиртах возрастающей концентрации и ацетоне с последующей полимеризацией в смоле (EMbed 812 Kit, Merck). Ультратонкие срезы, толщиной 20–30 нм были получены с помощью ультрамикротома Leica EM UC7. Дополнительное контрастирование срезов производилось с помощью уранилацетата и цитрата свинца.
Изображения структуры хлоропластов на ультратонких срезах получали с помощью просвечивающего электронного микроскопа Hitachi HT7700. Анализ проводился при ускоряющем напряжении 90 кВ в режиме светлого поля. Для получения репрезентативных данных о пространственной организации тилакоидных мембран проводилась серийная съемка при различных ориентациях образца.
Флуоресцентная спектроскопия. Регистрация спектров флуоресценции проводилась на спек-трофлуориметре CM-2203 (производитель – ЗАО «Спектроскопия, Оптика и Лазеры – Авангардные разработки» (SOLAR), Республика Беларусь). В качестве источника возбуждения использовалась импульсная ксеноновая лампа FX-4401. Детектирование осуществлялось приемником излучения – ФЭУ R928. Образцы для исследования готовились путем вырезания сегментов листовой пластинки длиной 20–25 мм с последующим креплением на специальном держателе. Измерения проводились в 90-градусной геометрии с углом наклона образца 60° к направлению детектирования.
Возбуждение флуоресценции производилось при длине волны 425 нм (ширина щели 20 нм), регистрация спектров осуществлялась в диапазоне 600–800 нм (ширина щели 5 нм). Сканирование проводилось с шагом 1 нм при максимальной чувствительности детектирующей системы.
Для контрольных и опытных образцов были отобраны по 100 снимков для каждого, где отчетливо наблюдалась хотя бы одна грана. Также проводилось дополнительное контрастирование изображений с помощью программного обеспечения.
Результаты исследований
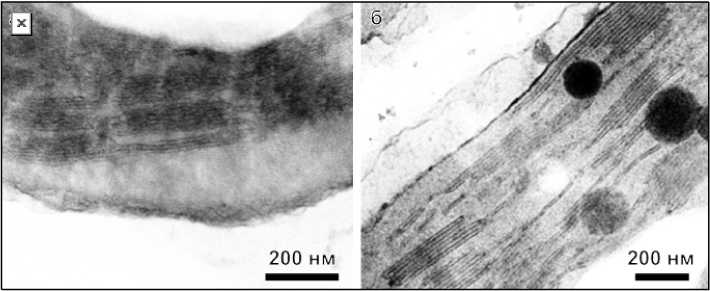
На рис. 1 представлены среднестатистические микрофотографии структуры хлоропластов листьев рапса, полученные с помощью просвечивающей электронной микроскопии для контрольного (рис. 1, а ) и опытного (рис. 1, б ) образцов. Из визуального сравнения рисунков видно, что в первом случае граны имеют более деформированный вид. Это касается как плотности прилегания тилакоидных мембран друг к другу, так и геометрических искажений.
а б
Рис. 1. Снимки структуры хлоропластов листьев рапса, не получавших ( а ) и получавших ( б ) добавку
Fig. 1. Photographs of the chloroplast structure of rapeseed leaves that did not receive ( a ) and received ( б ) the addition
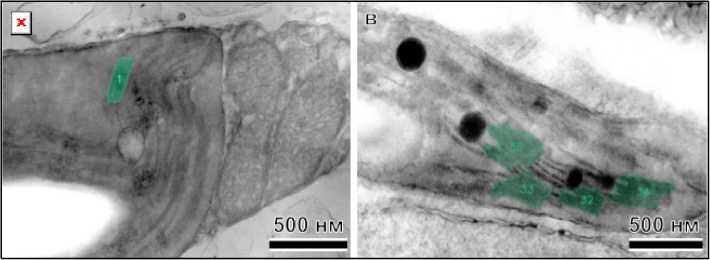
Измерение параметров тилакоидных мембран ручным методом является достаточно сложным и затратным по времени процессом, например, как это было реализовано в работе [10]. Главным плюсом такого подхода является то, что наличие полного набора данных позволяет рассчитывать любые зависимости и корреляции. В 2025 г. в работе [11] был представлен и подробно описан инструмент под названием GRANA для ускорения анализа наноморфологии гран хлоропластов на основе искусственного интеллекта. Этот метод позволяет быстро проводить оценку для сотни снимков структуры, однако его главными недостатками являются достаточно плохое распознавание гран с геометрией отличной от прямой линии и ограниченность в выборе выводимых параметров. Результаты обработки среднестатистических снимков программой GRANA для обоих типов образцов представлены на рис. 2.
Из сравнения изображений между контрольными и опытными образцами наглядно видно, что программа лучше распознает граны во втором случае. При визуальном подсчете всех отчетливо видимых гран на исследуемых снимках и всех, что были выделены с помощью искусственного интеллекта, можно определить первую численную характеристику для сравнения образцов. Предложенная программа автоматического распознавания гран смогла найти 39 % видимых гран для контрольных образцов против 61 % для опытных образцов. Это можно описать тем, что во втором случае граны имеют более типичную форму и более ярко выраженные очертания тилакоидных мембран. К тому же меньший контраст у контрольных образцов может свидетельствовать о недостаточном получении компонентов, необходимых для полноценной жизнедеятельности растений. По результатам сканирования изображений структуры хлоропластов были получены данные, представленные в табл. 1.
а б
а
б
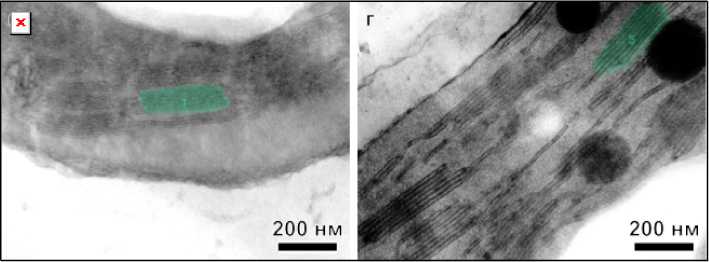
Рис. 2. Снимки структуры хлоропластов листьев рапса после обработки с помощью GRANA, не получавшие ( а , б ) и получавшие добавку ( в , г )
Fig. 2. Images of the chloroplast structure of rapeseed leaves after treatment with GRANA, not treated ( a , б ) and treated with the additive ( в , г )
Результаты анализа изображений структуры хлоропластов для контрольных и опытных образцов
Таблица 1
|
Контроль |
Опыт |
|
|
Область (нм2) |
40622 ± 37344 |
25054 ± 13495 |
|
Периметр (нм) |
980 ± 423 |
824 ± 270 |
|
Диаметр (нм) |
314 ± 77 |
283,89 ± 82,35 |
|
Высота (нм) |
101,63 ± 28,40 |
92,16 ± 30,29 |
|
Количество тилакоидов |
– |
7,50 ± 2,12 |
|
Параметр повторения гран (нм) |
– |
15,01 ± 1,15 |
Представленные в табл. 1 данные показывают медианное значение по каждому параметру, а также стандартное отклонение относительно медианы. Прочерки в последних двух строках для контрольных образцов означают, что программа не смогла определить данные параметры. Из сравнения результатов видно, что характеристики структуры хлоропластов опытных образцов стали значительно меньше (порядка 16 % по ключевым параметрам). Это может быть напрямую связанно с более плотным и прямолинейным упорядочением тилакоидных мембран в гранах. В работах [10; 12; 13] было отмечено, что плотная упаковка гран может способствовать более эффективному переносу электронов между фотосистемами, и как следствие, более эффективному протеканию процесса фотосинтеза. Этот эффект можно описать тем, что фолиарные удобрения благоприятно воздействуют на достижение наиболее эффективного процесса фотосинтеза и могут напрямую влиять на внутреннюю архитектуру листьев.
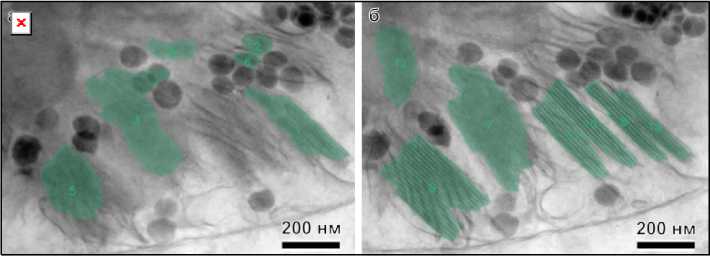
В работах [14; 15] отмечается, что угол наблюдения по отношению к образцу напрямую влияет на результаты структуры. Так, например, при отклонении образца, когда грана не перпендикулярна электронному пучку, конечные размеры и внешний вид тилакоидных мембран могут искажаться. На рис. 3 представлены изображения структуры хлоропласта, полученные с помощью просвечивающей электронной микроскопии после обработки программным обеспечением GRANA. На рис. 3, а образец находился под углом 60о по отношению к электронному пучку, тогда как на рис. 3, б по углом 90о. Из результатов сравнения рисунков видно, что при отклонении образца на 30о от перпендикулярной плоскости падения к гранам происходит размытие гран. Программа, основанная на искусственном интеллекте, частично определила 3 граны, в то время как при ортогональном расположении пучка к гранам отчетливо выделены все граны на изображении.
б
Рис. 3. Снимки структуры хлоропластов листьев высших растений после обработки с помощью GRANA при угле наблюдения к гранам 30о ( а ) и под прямым углом ( б )
-
Fig. 3. Images of the chloroplast structure of higher plant leaves after processing using GRANA at an observation angle of 30° to the grana ( a ) and at a right angle ( б )
По результатам сканирования изображений структуры хлоропластов с рис. 3 были получены данные, представленные в табл. 2. Из результатов сканирования видно, что при искажении гран искусственный интеллект не смог определить и половины параметров, в то время как при оценке снимка под прямым углом к гране программа смогла определить все доступные характеристики.
Таблица 2
Результаты анализа изображений структуры хлоропластов для 30о и прямого угла
|
Параметр |
Прямой угол |
|
Область (нм2) |
130221 ± 101300 |
|
Периметр (нм) |
1928 ± 878 |
|
Диаметр (нм) |
650,99 ± 65,71 |
|
Высота (нм) |
287,23 ± 134,61 |
|
Количество тилакоидов |
11,67 ± 5,07 |
|
Параметр повторения гран (нм) |
24,01 ± 1,02 |
Для оценки эффективности переноса энергии через изменение структуры представляло интерес измерить спектры флуоресценции. Результаты флуориметрии представлены на рис. 4. Из сравнения спектральной ширины пиков флуоресценции на полувысоте, соответствующих фотосистеме II (685 нм), наблюдается заметная разница. Ширина пика для контрольных образцов составляет 24,2 нм. В то же время ширина пика для опытных образцов составила 22,4 нм. Таким образом, разница между спектральной шириной пиков на полувысоте составила 1,8 нм в абсолютных величинах или 8 % в относительных.
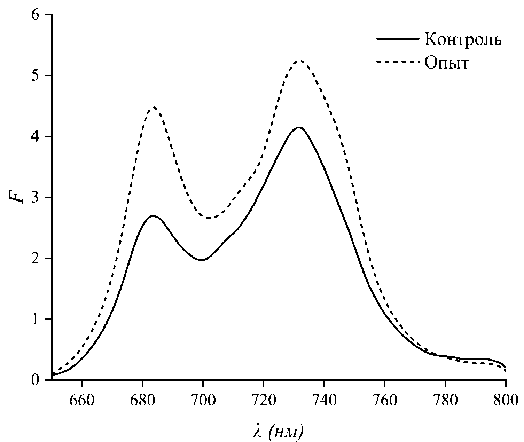
Рис. 4. Спектры флуоресценции листьев рапса, не получавших (контроль) и получавших добавки (опыт)
-
Fig. 4. Fluorescence spectra of rapeseed leaves that did not receive (control) and received additives (experiment)
Обсуждение
Ключевым структурным следствием обработки явилось увеличение упорядоченности тилакоидных мембран в гранах хлоропластов опытного образца. Полученные электронномикроскопические данные указывают на уменьшение средних размеров гран и их более плотную упаковку. Уменьшение геометрических параметров гран и повышение однородности их размерного распределения приводит к снижению степени разупорядоченности системы. Эти структурные изменения должны повлиять на параметры ФС II. Согласно современным представлениям, в листьях растений существует две фотосистемы [16], представляющие собой белковые комплексы, которые содержат множество (антенных) светособирательных пигментов, проводящие компоненты для переноса электронов, а также реакционный центр.
Фотохимический реакционный центр включает молекулы хлорофилла у растений, а также пигменты хлорофилловой природы у водорослей и фотосинтезирующих бактерий, которые окисляются под действием света и являются первичными донорами электронов.
Эти особые пигменты хлорофилловой природы с максимум поглощения у 700 нм вместе со светособирающими антеннами стали называть системой ФС I, а с максимумом поглощения 680 нм называть фотосистемой ФС II.
Исследуемый спектр флуоресценции листа растений представляет собой комбинацию вкладов от двух фотосистем. Принято считать, что при комнатной температуре большая часть этой флуоресценции испускается системой ФС II. Вклад от ФС I при длине волн 683 нм составляет около 5 %, а при длине волны 700–740 нм – 30–35 %. Более того, выяснено [17], что флуоресценция ФС I слабо зависит от состояния реакционного центра.
Что касается спектра флуоресценции ФС II – здесь все проще, поскольку разработана простая техника фракционирования хлоропластов [18]. Экстрагированный ФС II (обычно называют ВВУ грана) считается нативным, поскольку в нем присутствует как реакционный центр, так и комплекс сбора света (LHC-II).
Впервые [19] получен собственный спектр излучения флуоресценции ФС II для нескольких концентраций суспензий изолированных ФС II. В дальнейшем исследованы его зависимости от различных внешних условий, что существенно прояснило многие микропроцессы, протекающие в органеллах зеленых растений. К сожалению, не удалось добиться поглощения СО 2
в количественном отношении с зеленым листом. Поэтому вопрос о величинах оптимальных структурных параметров гран листьев, концентрации пигментов, их пропорции и регулярности ультраструктурной организации хлоропластов при фотосинтезе остается открытым.
Для решения этой задачи нами предложен способ исследования изменений вышеназванных параметров для систем, отличающихся своей эффективностью. Известно, что подкормка листьев растений в ряде случаев позволяет повысить урожайность.
В работе [20] было проведено численное моделирование одномерных фотонных кристаллов с постепенным увеличением разупорядочением толщин слоёв. На рис. 5 изображен фрагмент этих результатов со спектрами пропускания от 0 до 30 % разупорядочения. В работе [20] отмечается, что запрещенная зона сохраняется при случайном отклонении толщин слоёв вплоть до 40 %. Однако не было подмечено, что полоса отражения способна смещаться в длинноволновую область совместно с уменьшением степени разупорядочения слоёв. На рис. 5 проведена пунктирная линия, соответствующая спектральному положения максимума коротковолновой полосы отражения при отсутствии искажений в слоях. По мере увеличения степени упорядочения видно, что максимум данной полосы смещается в сторону меньших частот или же длинноволновую область. Данный эффект находит согласование с результатами, представленными на рис. 4. На спектрах флуоресценции, в случае более упорядоченной структуры, отчетливо наблюдается дополнительное плечо в длинноволновой области.
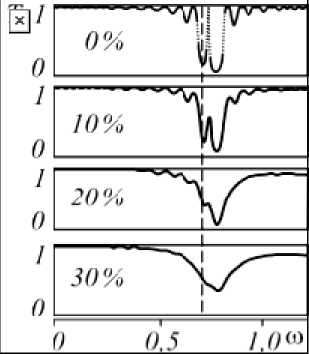
Рис. 5. Усредненные спектры пропускания ФК-решетки с варьируемой толщиной слоёв в зависимости от максимальной амплитуды случайных отклонений линейных размеров от первоначально заданных [20]
-
Fig. 5. Averaged transmission spectra of a PC grating with variable layer thickness depending on the maximum amplitude of random deviations of linear dimensions from the initially specified ones [20]
Сравнительный анализ контрольного и опытного образцов выявил статистически значимые изменения как на ультраструктурном, так и на оптическом уровне, что позволяет говорить о прямом воздействии применяемых агрохимикатов на фотосинтетический метаболизм. Как следствие, в такой структуре ожидается увеличение плотности фотонных состояний на краях стоп-зоны, что теоретически предсказывает более эффективное удержание и преобразование световой энергии [21].
Объединение двух ключевых наблюдений – увеличения структурного порядка тилакоидов и снижения энергетической неоднородности, регистрируемой по флуоресценции – позволяет построить непротиворечивую причинно-следственную связь. Внесение некорневых подкормок, содержащих макро- и микроэлементы, а также, вероятно, поверхностно-активные вещества, инициирует перестройку ультраструктуры хлоропластов. Эта перестройка выражается в опти- мизации пространственной организации тилакоидных мембран, что, в свою очередь, создает более благоприятные условия для миграции энергии возбуждения. Уменьшение структурного разупорядочения напрямую снижает потери энергии на рассеяние, что и проявляется в виде сужения пика флуоресценции ФСII.
Таким образом, основным механизмом, лежащим в основе наблюдаемого эффекта, является повышение эффективности первичных стадий фотосинтеза за счет оптимизации световой стадии. Более эффективный перенос энергии в антенном комплексе ФС II приводит к увеличению вероятности попадания кванта света в реакционный центр. Это создает предпосылки для повышения эффективности всех последующих этапов фотосинтетического электронного транспорта, синтеза АТФ и НАДФH, что в конечном итоге и должно обуславливать увеличение биохимической продуктивности растения, выраженной в росте урожайности, как это было показано в аналогичных работах [7].
Заключение
-
1. Методом просвечивающей электронной микроскопии установлено, что применение некорневых подкормок приводит к уменьшению размеров гран опытных образцов по сравнению с контрольными. Это связано с упорядочением тилакоидных мембран опытных образцов.
-
2. Обнаружено сужение полуширины пика флуоресценции фотосистемы II в опытном образце по сравнению с контрольным, что свидетельствует о повышении эффективности миграции энергии возбуждения.
-
3. Показано, что более плотная упаковка гран в хлоропластах способствует увеличению эффективности переноса энергии возбуждения между фотосистемами.
Полученные результаты не только вносят вклад в фундаментальное понимание механизмов воздействия агрохимикатов на фотосинтетический аппарат, но и имеют практическую значимость. Метод флуоресцентной спектроскопии подтверждает свою эффективность в качестве быстрого и неинвазивного инструмента для диагностики функционального состояния растений и прогнозирования эффективности применяемых технологий, в том числе, в замкнутых космических системах.
Acknowledgment. The work was carried out within the framework of the scientific topic of the state assignment of the FRC SB RAS.


