Особенности анестезиологического обеспечения и послеоперационного мониторинга у животных с брахицефальным синдромом
Автор: Прусакова В.А.
Журнал: Научный журнал молодых ученых @young-scientists-journal
Рубрика: Сельскохозяйственные науки
Статья в выпуске: 4 (44), 2025 года.
Бесплатный доступ
Брахицефальный синдром (БС) представляет значительную проблему в ветеринарной практике в связи с популярностью пород-брахицефалов. Анестезиологический риск у таких животных многократно повышен из-за анатомических особенностей верхних дыхательных путей, склонности к гипоксии и риска развития жизнеугрожающих осложнений в интра- и послеоперационном периоде.
Брахицефальный синдром, анестезия, послеоперационный мониторинг, интубация, оксигенотерапия, собаки, кошки, дыхательная недостаточность, периоперационные риски
Короткий адрес: https://sciup.org/147252254
IDR: 147252254 | УДК: 619:616-089.5:616.21-008.46
Features of anesthetic management and postoperative monitoring in animals with brachycephalic syndrome
Brachycephalic syndrome (BS) is a significant problem in veterinary practice due to the popularity of brachycephalic breeds. The anesthetic risk in such animals is significantly increased due to the anatomical features of the upper respiratory tract, the tendency to hypoxia, and the risk of developing life-threatening complications during the intra- and postoperative periods. The purpose of this article is to describe and justify a comprehensive approach to anesthetic support and postoperative monitoring in animals with brachycephalic syndrome using clinical cases as examples.
Текст научной статьи Особенности анестезиологического обеспечения и послеоперационного мониторинга у животных с брахицефальным синдромом
Введение. Рост популярности брахицефальных пород собак и кошек закономерно приводит к увеличению количества хирургических вмешательств у данной группы пациентов. Анестезиологическое обеспечение таких животных сопряжено с повышенным риском в связи с их специфической анатомией: обструкцией верхних дыхательных путей, склонностью к ларингоспазму, хронической гипоксией и высоким потенциалом развития жизнеугрожающих осложнений в послеоперационном периоде. Критически важными становятся не только техника проведения наркоза, но и протоколы продленного мониторинга в процессе восстановления. Теоретической и практической основой исследования послужили данные, полученные в условиях ветеринарного центра «Свой доктор г. Орел», при хирургической коррекции проявлений брахицефального синдрома у собак и кошек.
Цель исследований. Описать и обосновать комплексный подход к анестезиологическому обеспечению и послеоперационному мониторингу животных с брахицефальным синдромом на примере клинических случаев/
Материалы и методы. Клиническое исследование животных производили последовательно по общепринятой в ветеринарной практике методике, которая включала в себя регистрацию поступившего на прием животного, сбор анамнеза, проведение общего и специального обследования. Для уточнения диагноза использовали визуальный и инструментальный осмотр, рентгенологический метод. Среди собак наиболее часто встречались такие патологии, как: стеноз ноздрей, гиперплазия небной занавески и коллапс трахеи; у кошек был диагностирован стеноз ноздрей, и лишь у одного из пациентов в ходе инструментального обследования и визуального осмотра было выявлено удлиненное мягкое небо.
Для диагностики вышеперечисленных патологий использовали следующие методы:
-
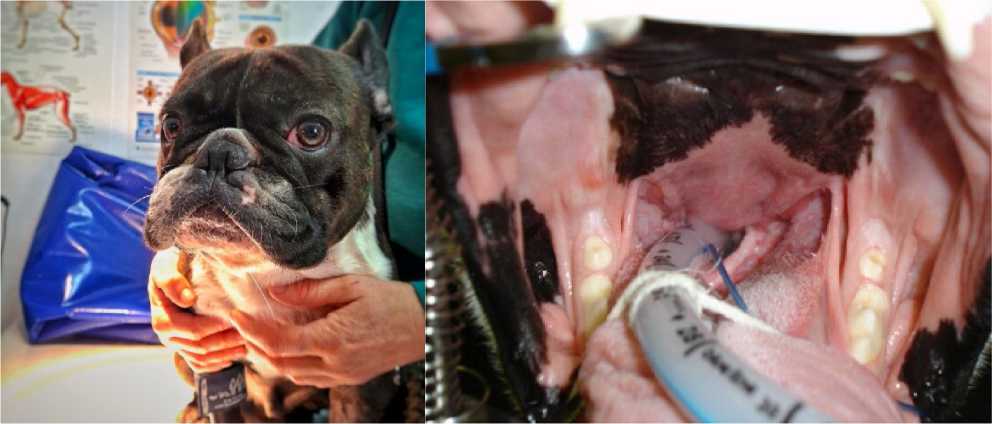
1. Визуальный осмотр пациентов – позволил выявить патологии верхних дыхательных путей (стеноз ноздрей (рис. 1), гиперплазию небной занавески (рис. 2)).
-
2. Инструментальный метод обследования с использованием стетоскопа – позволил выявить дыхательные шумы, определить их местоположение, оценить тоны сердца, шумы сердечные, нарушения ритма (табл. 1).
-
3. Ультразвуковое исследование (УЗИ-аппарат Chison, Mindray) – позволило выявить сердечные патологии, исключить отек легких.
-
4. Рентгенография – для оценки верхних и нижних дыхательных путей, и других сопутствующих патологий – позволила выявить коллапс трахеи, увеличенный индекс сердца.
Рисунок 1 – Стеноз ноздрей у собаки Рисунок 2 – Гиперплазия небной занавески
Таблица 1 – Средние показатели инструментальных методов исследования
|
Анамнез |
ЧСС уд/мин |
ЧДД дв/мин |
УЗИ |
Рентген |
|
|
Собаки |
Стеноз ноздрей, гиперплазия небной занавески |
80-95 |
27-30 |
Нет отека легких |
Увеличенный индекс сердца, коллапс трахеи |
|
Кошки |
Стеноз ноздрей |
115-128 |
16-22 |
Нет отека легких |
Патологий не выявлено |
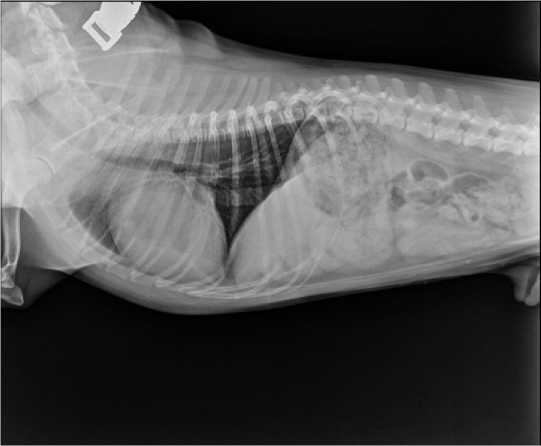
Рисунок 3 – Увеличенный индекс сердца у мопса
Всем животным с диагностированным брахицефальным синдромом за семь дней до планируемого хирургического вмешательства назначался пероральный препарат Мекситар в дозе 5 мг/кг массы тела дважды в день. Целью назначения являлась медикаментозная коррекция потенциальной сердечно-сосудистой и дыхательной недостаточности, а также профилактика наркозных и постнаркозных осложнений на фоне хронической гипоксии, ассоциированной с брахицефалическим синдромом.
Всем животным в качестве премедикации внутримышечно вводился препарат Дексодия 0,5 мг/мл (действующее вещество – дексмедетомидин) в дозировке, соответствующей инструкции производителя. Выбор данного а2-агониста был обусловлен его выраженным седативным и анальгезирующим эффектом, что позволяло достичь необходимого уровня премедикации: снижения тревожности и двигательной активности пациента, минимизации стрессовой реакции и обеспечения предварительного обезболивания перед индукцией в наркоз. После наступления умеренной седации проводилось предварительное инструментальное обследование верхних дыхательных путей для визуальной оценки степени их обструкции. У некоторых пациентов была подтверждена гиперплазия мягкого неба, проявляющаяся в его удлинении (выходе за пределы надгортанника) и утолщении, что визуализировалось как обтурация просвета гортани. Дополнительно отмечались цианоз слизистых оболочек и отек тканей гортани, обусловленные хронической дыхательной недостаточностью.
С целью обеспечения проходимости дыхательных путей на весь период хирургического вмешательства и для профилактики аспирации всем животным была проведена эндотрахеальная интубация. У собак применялись эндотрахеальные трубки диаметром 5.0-7.0 мм (I.D./O.D.), у кошек – трубки большого объема с низким давлением манжеты размером 3.5-4.0 мм. Подбор размера осуществлялся индивидуально с учетом анатомических особенностей и данных о возможной гипоплазии трахеи.
Индукция в наркоз осуществлялась препаратом Золетил (комплекс на основе золетилама и тилетамина) внутривенно в расчетной дозе 7.5 мг/кг. Данный препарат был выбран благодаря быстрому и предсказуемому действию, что является критически важным для минимизации периода неуправляемой проходимости дыхательных путей у брахицефальных пациентов.
На протяжении всего периода хирургического вмешательства и выхода из наркоза осуществлялся непрерывный мониторинг ключевых физиологических параметров с использованием многопараметрического монитора пациента Mindray (рис. 4). Данный подход является обязательным стандартом при проведении анестезии у брахицефальных животных в связи с высоким риском развития у них перфузионно-гипоксических осложнений и нестабильности гемодинамики. Мониторинг включал в себя: электрокардиографию (ЭКГ) для контроля сердечного ритма и раннего выявления аритмий: измерение частоты сердечных сокращений (ЧСС) и частоты пульса (ЧП); пульсоксиметрию (SpO 2 ) для неинвазивной оценки степени насыщения гемоглобина артериальной крови кислородом, что является критически важным параметром для своевременного выявления гипоксемии; капнографию – измерение содержания углекислого газа (CO 2 ) в конце выдоха (EtCO 2 ), позволяющее контролировать адекватность вентиляции легких и корректировать параметры ИВЛ при необходимости; измерение частоты дыхания (ЧДД), неинвазивное измерение артериального давления (НИАД) для оценки системной гемодинамики; мониторинг температуры тела для профилактики интра- и послеоперационной гипотермии (рис.5). Непрерывная визуализация динамики жизненно важных показателей на экране монитора позволяла в реальном времени оценивать глубину анестезии, оперативно корректировать дозировку анестезиологических препаратов и незамедлительно реагировать на любые отклонения параметров от нормы (тахипноэ, брадикардия, десатурация, гипотония), тем самым повышая безопасность проведения процедуры у животных с клиническими проявлениями брахицефального синдрома.
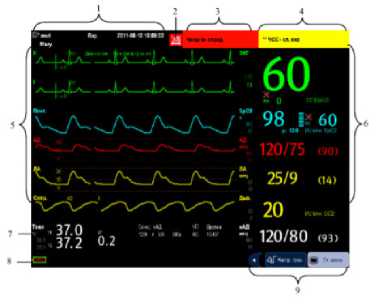
Рисунок 4 – Монитор пациента фирмы Mindray
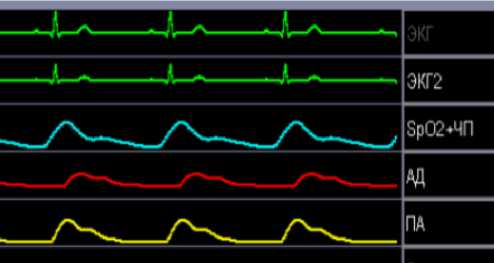
Рисунок 5 – Основные показатели монитора пациента
После завершения хирургического вмешательства и прекращения подачи анестезиологических препаратов пациент переводился в отделение интенсивной терапии, где осуществлялось его постоянное наблюдение до полного восстановления сознания и самостоятельного поддержания проходимости дыхательных путей. В раннем послеоперационном периоде проводился мониторинг следующих ключевых параметров с интервалом 15-30 минут: частота сердечных сокращений и качество пульса, частота дыхательных движений и характер дыхания, степень насыщения крови кислородом с помощью пульсоксиметра, мониторинг цвета видимых слизистых оболочек, время капиллярного наполнения и измерение температуры тела с периодичность в каждые 30 минут для контроля и профилактики послеоперационной гипотермии. После полного пробуждения животного, восстановления глотательного рефлекса и способности самостоятельно поддерживать адекватную дыхательную функцию осуществлялось удаление внутривенного катетера. Парентеральное питание не проводилось в связи с быстрым восстановлением перистальтики и отсутствием показаний.
Сразу после перевода животного в послеоперационную палату была назначена оксигенотерапия путем подачи увлажненного кислорода с концентрацией 40-60% через кислородную камеру в течение не менее 1 часа. Данная мера была направлена на коррекцию потенциальной гипоксемии, неизбежно возникающей на фоне остаточного действия анестетиков, угнетения дыхательного центра и отека тканей верхних дыхательных путей после экстубации.
При проведении хирургической коррекции гиперплазии небной занавески для санации ротоглотки и профилактики аспирации проводилось осторожное промывание полости рта и глотки физиологическим раствором с целью удаления остаточных кровяных сгустков, слюны и частиц иссеченных тканей. Дополнительно выполнялась аускультация и перкуссия трахеи и легочных полей для раннего выявления возможных осложнений (ателектазы, аспирация).
Медикаментозная поддержка в раннем послеоперационном периоде включала в себя использование следующих препаратов:
-
1. Эмидонол 5% (этилметилгидроксипиридина сукцинат): вводился подкожно однократно в дозе 0,1 мл/кг. Применение антигипоксанта было направлено на улучшение оксигенации тканей и профилактику реперфузионных повреждений после искусственной вентиляции легких и потенциальных эпизодов интраоперационной гипоксии.
-
2. Фуросемид 5%: вводился внутримышечно однократно в дозе 0.5-1 мл/10 кг (что эквивалентно 2.5-5 мг/кг). Петлевой диуретик применялся с целью купирования и профилактики отека слизистых оболочек верхних и нижних дыхательных путей, развивающегося вследствие травматизации тканей во время операции и на фоне повышенного венозного давления.
-
3. Мекситар (мексидол, этилметилгидроксипиридина сукцинат): назначался перорально в дозе 5 мг/кг дважды в сутки в течение следующих пяти дней после операции. Продленный курс антигипоксанта и мембраностабилизатора был показан для коррекции метаболических нарушений, улучшения реологических свойств крови и профилактики сердечно-сосудистых и бронхолегочных осложнений в период реабилитации.
При необходимости снятие швов (например, при проведении ринопластики) производили на десятый день после операции с предварительным проведением полного визуального и инструментального осмотра животного.
Результаты и обсуждение. Разработанный протокол позволил минимизировать периоперационные риски. Ключевыми факторами успеха стали: тщательная предоперационная оценка проходимости дыхательных путей, быстрая и уверенная интубация, плавный выход из наркоза с продленной оксигенотерапией и интенсивный послеоперационный мониторинг в течение первых 24 часов. Осложнений, связанных непосредственно с анестезией, зафиксировано не было.
Вывод. Анестезия животных с брахицефальным синдромом требует специализированного подхода, основанного на понимании их уникальной анатомии и физиологии. Обязательными условиями являются премедикация седативными анальгетиками, обеспечение проходимости дыхательных путей с помощью интубации, готовность к быстрому реагированию на обструкцию, а также продленный послеоперационный мониторинг и поддержка. Применение описанного алгоритма действий позволяет безопасно проводить хирургические вмешательства у данной группы пациентов и снижает риск осложнений и летальных исходов.


