Особенности биохимической адаптации сосудистых растений верховых болот в условиях Среднего Приобья
Автор: Иванова Н.А., Юмагулова Э.Р.
Журнал: Вестник Нижневартовского государственного университета @vestnik-nvsu
Рубрика: Биология и экология
Статья в выпуске: 4, 2009 года.
Бесплатный доступ
Изучены особенности биохимической композиции листьев сосудистых растений верховых болот и их жизненных форм. Показано, что наблюдается видовая специфичность в накоплении углерода, азота, растворимых и структурных сахаров, органических форм азота. Жизненные формы растений также отличались по химическому составу листьев. Отношение количества углерода к азоту достоверно отличалось у растений разных жизненных форм и видов.
Короткий адрес: https://sciup.org/14116545
IDR: 14116545
Текст научной статьи Особенности биохимической адаптации сосудистых растений верховых болот в условиях Среднего Приобья
Характерной чертой Западно-Сибирской равнины является чрезвычайно высокая заболоченность, достигающая 30—75% от всей площади, большая часть болот приходится на долю сфагновых [2, 12].
Болота — неотъемлемая часть ландшафта таежной зоны Западно-Сибирской равнины. Они играют большую роль в природе, имеют научное, хозяйственное и экологическое значение. Болота, в том числе и верховые, — уникальные экосистемы биосферы постоянного стока атмосферного углерода, накапливаемого в виде торфа, обладающие одним из главных углеродных пулов в биосфере [3, 5, 9, 12].
В настоящее время накоплен большой экспериментальный материал по особенностям функционирования растительных сообществ болот [1, 2, 7, 11, 23, 25, 26, 27].
Рост и развитие растений верховых болот, формирование их эколого-физиологических, биохимических особенностей происходит в неблагоприятных условиях обитания: обилие влаги, ее застойность или слабая проточность, недостаток кислорода в почве (1%), низкая теплопроводность, бедность торфа элементами минерального питания, повышенная кислотность, постоянное нарастание сфагновой дернины и торфа [4, 23, 25].
Важное место в системе адаптации растений к совокупности действующих факторов, в том числе стрессовых, принадлежит биохимическим механизмам адаптации [8, 10, 21, 28].
Биохимический механизм адаптации — это особенность метаболизма растений, которая снижает вероятность повреждения растений в условиях произрастания и обеспечивает оптимальную жизнеспособность, создание высокой биологической продуктивности и воспроизведение потомства.
Растения с разными биохимическими типами адаптации имеют разный химический состав: содержание липидов, лигнина, органических азотсодержащих компонентов, целлюлозы, гемицеллюлозы, неструктурных углеводов, органических кислот и минеральных веществ.
Большое значение в адаптации к факторам внешней среды у растений имеет соотношение в листьях количества углерода и азота, которое характеризует направленность синтеза углеводных и азотсодержащих органических соединений [8, 21, 30].
Биохимическая направленность синтеза отдельных органических соединений определяется генотипической особенностью организма и его фенотипической изменчивостью.
Для сосудистых растений верховых болот биохимические механизмы адаптации к факторам внешней среды практически не изучены.
Объекты и методы исследований. Исследования проводили в 2001—2006 гг., в период активной вегетации болотных растений на территории Нижневартовского района (конец июня, июль), в 20 км от п.Высокого. Описание сообщества верхового болота сделано по стандартной методике [17, 24]. Все определения вели в солнечную погоду. Средняя температура воздуха составляла 26—28 ºС, почвы на глубине 30 см — 12—14 ºС; рН болотной воды — 3,7.
Сообщество верхового болота представлено сосново-кустарничково-сфагновой ассоциацией. Рельеф выположенный, грядово-мочажинный. Почвы торфяно-глеевые, с торфяным слоем до 1—2 м.
Объектами исследования были следующие сосудистые растения верхового болота: подбел восколистный ( Аndromeda polifolia L.), мирт болотный ( Chamaedaphne calyculata (L.) Moench), клюква болотная ( Oxycoccus palustris Pers.), багульник болотный ( Ledum palu-stre L.), голубика ( Vaccinium uliginоsum L.), береза карликовая ( Betula nana L.), пушица влагалищная ( Eriophorum vaginatum L.), осока шаровидная ( Сarex globularis L.), осока пузырчатая ( Сarex vesicaria L.), морошка ( Rubus chamaemorus L.), сосна обыкновенная ( Pinus sylvestris L.) и сосна сибирская ( Pinus sibirica Rupr. Mayer), — которые относятся к разным жизненным формам: вечнозеленым кустарничкам брусничного типа, вечнозеленым кустарничкам эрикоидного типа, летнезеленым листопадным кустарничкам, травам с длинными узкими складчатыми или свернутыми листьями, травам с широкими толстыми жестковатыми листьями и деревьям.
Листья кустарничков для исследования отбирали со среднего яруса, деревьев — из средней части кроны с южной стороны. В среднем возраст деревьев составлял 17—20 лет. Возраст деревьев определяли на основе анатомических и морфологических признаков по методикам А.А.Корчагина [19].
Для биохимического анализа брали листья, завершившие свой рост. Среднюю пробу листьев с 10—15 растений фиксировали при 125 ºС и досушивали при 75 ºС в термостате.
Содержание общего азота определяли методом Къельдаля [13]. Навеска сухого вещества составляла 0,3 г. Серную кислоту (плотностью 1,84 г/мл) добавляли из расчета 3 мл на 0,1 г сухого материала.
Для расчета общего азота в растительном материале использовали формулу:
Х = 0,28∙V∙(Y1T1 – Y2T2)/(A∙P), где Х — содержание азота в сухом веществе, мг/г; Y1 — количество 0,02 н. серной кислоты, помещенной в приемную колбу, мл; Y2 — количество 0,02 н. гидроксида натрия, израсходованного на титрование, мл; T1, T2, — поправочные коэффициенты к титру кислоты и щелочи соответственно; 0,28 — количество азота (мг), которое связывается в виде сульфата аммония 1 мл 0,02 н. серной кислотой; А — объем исследуемого раствора, взятого для отгонки, мл; Р — навеска растительного материала, взятого для сжигания, г; V — объем раствора в мерной колбе (после озоления), мл [13].
Нитратный азот определяли в водном экстракте (30 мин на водяной бане) с добавлением 5% раствора салициловой кислоты в Н 2 SO 4 и 4% NaOH , на приборе КФК-2 (Россия) [13].
Растворимые сахара экстрагировали из растительного материала 80% этанолом двукратно при 40 ºС. После центрифугирования раствор использовали для определения суммы растворимых сахаров (фруктозы, сахарозы и глюкозы), остаток подвергали кислотному гидролизу (3% соляной кислотой) для отделения неструктурных полисахаридов. Количественное определение растворимых сахаров и неструктурных полисахаридов проводили методами тонкослойной хроматографии и колориметрическим методом с антроном КФК-2 (Россия) [29].
Массу золы определяли после сжигания навески растительного материала в муфельной печи при 550 ºС в течение 8 часов.
Зольные элементы определяли атомно-адсорбционным методом анализа [14]. Пробо-подготовку для проведения анализа осуществляли по стандартной методике. Образцы растительной массы фиксировали при 125 ºС, досушивали до воздушно-сухого состояния (температура 75 ºС) и измельчали. Сухие, измельченные образцы отбирали методом средней пробы до веса 0,01 г, и сжигали в муфельной печи при температуре 400—500 ºС в течение 90 мин. После сжигания тигли с золой охлаждали и взвешивали. К полученным образцам приливали 4 мл азотной кислоты (2 моль/л) и 2 мл соляной кислоты (1:1) и проводили разложение в автоклаве XF100, используя микроволновую печь Multiave 3000 фирмы Anton Paar. Разложение вели, изменяя мощность разложения от 800 Ватт в течение 5 мин до 1000 Ватт в течение 15 мин, на завершающей стадии 60 Ватт в течение 20 мин. Мощность контролировали с помощью ИК датчика ротора. Полученные в результате разложения пробы исследовали на приборе Aanalist 700 фирмы Perkin Elmer.
Градуировку прибора проводили в соответствии с рекомендациями, изложенными в МИ 2345-95 «ГСИ. Характеристики градуировочных средств измерений состава и свойств веществ и материалов. Методы выполнения измерений с использованием стандартных образцов». Содержание элементов в представленных образцах рассчитывали по следующей формуле:
С = S × Vpr / Mnav, где S — показания прибора; Mnav — навеска пробы исследуемого образца, г; Vpr — объем анализируемого раствора, мл.
Углерод определяли сжиганием проб растительного материала в струе кислорода в трубчатой печи при температуре 850 ºС и улавливанием продуктов их сгорания, в которых измеряли выделившийся СО 2 по его поглощению гидроксидом калия [22].
Статистическая обработка данных проведена с использованием пакета прикладных программ Statistica 11.5; Excel 2005 из пакета Microsoft Office XP. Для оценки различий между разными группами видов использовали критерии Стьюдента и Манна-Уитни [15].
Результаты исследований. Соотношение синтеза азотсодержащих продуктов и углеводов является одним из факторов, регулирующих рост растений [18]. Изменения в содержании углеводных и белковых продуктов у растений в разных экологических условиях и у разных систематических групп показаны на большом экспериментальном материале [6, 20, 21].
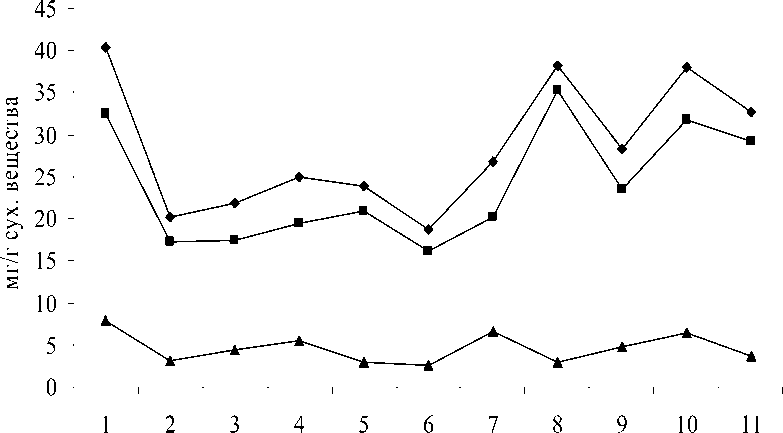
Концентрация азота в листьях болотных растений изменялась от 18,7 мг/г у пушицы влагалищной до 40,37 мг/г у сосны сибирской, и у большинства видов составляла 22—33 мг/г (рис. 1). Содержание неорганической формы азота в виде иона NO 3- (нитратный азот) в листьях растений менялось от 2,57 мг/г у пушицы влагалищной до 7,87 мг/г у сосны сибирской. У 64% видов растений содержание NO 3- в листьях составляло от 2,89 до 5,5 мг/г. Накопление органического азота варьировало от 16,13 мг/г у пушицы влагалищной до 35,24 мг/г у березы карликовой и в среднем в 5 раз превышало содержание неорганической формы азота (нитратного азота).
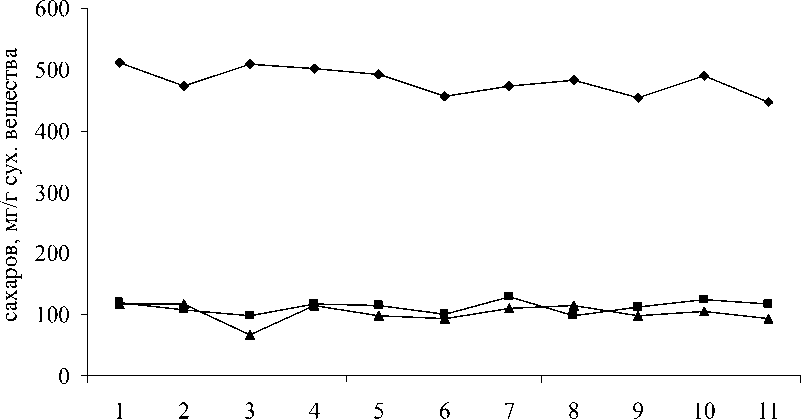
Содержание углерода изменялось от 446,77 мг/г (морошка приземистая) до 510,37 мг/г (сосна сибирская), т.е. всего в 1,1 раза в пределах всей изученной группы растений верхового болота (рис. 2).
—♦— общий азот —■— органический азот —нитратный азот
виды растений
Рис. 1. Особенности содержания различных форм азота в листьях растений верхового болота:
1 — сосна сибирская, 2 — сосна обыкновенная, 3 — мирт болотный, 4 — клюква болотная,
5 — подбел многолистный, 6 — пушица влагалищная, 7 — осока шаровидная, 8 — береза карликовая, 9 — голубика, 10 — багульник болотный, 11 — морошка приземистая
♦ углерод —■— неструк. полисахариды ▲ растворимые сахара
виды растений
Рис. 2. Особенности содержания углерода и различных форм сахаров в листьях растений верхового болота:
1 — сосна сибирская, 2 — сосна обыкновенная, 3 — мирт болотный, 4 — клюква болотная, 5 — подбел многолистный, 6 — пушица влагалищная, 7 — осока шаровидная, 8 — береза карликовая, 9 — голубика, 10 — багульник болотный, 11 — морошка приземистая
Минимальное содержание растворимых сахаров обнаружено у мирта болотного (66,53 мг/г), максимальное — у деревьев сосны сибирской (117,67 мг/г) и сосны обыкновенной (117 мг/г). Минимум неструктурных полисахаридов мы наблюдали у березы карликовой (98,1 мг/г), максимум — у осоки шаровидной (129,13 мг/г). До 55% изученных видов растений содержали от 92,8 до 109,13 мг/г, большинство видов (64%) — от 108 до 120 мг/г.
Общее содержание азота и углерода в листьях растений варьировало значительно больше, чем содержание углеводов.
Достоверные различия по содержанию общего азота, углерода, неструктурных полисахаридов и растворимых сахаров отмечены: у багульника болотного с клюквой болотной, пушицей влагалищной, миртом и сосной обыкновенной (р<0,05; р<0,01; р<0,001); у березы карликовой с сосной сибирской, осокой шаровидной, сосной обыкновенной (р<0,01; р<0,001); у мирта болотного с сосной обыкновенной, морошкой приземистой, осокой шаровидной (р<0,001); у пушицы влагалищной с осокой шаровидной, сосной сибирской (р<0,01; р<0,001).
Содержание зольных элементов в листьях растений было невелико и варьировало от 1,29% у сосны обыкновенной до 7,29% у осоки шаровидной.
У большинства видов по данному показателю отмечены достоверные различия (р<0,05; р<0,001).
Известно, что листья растений в среднем содержат от 3 до 15% золы [21]. На основе этого мы делаем заключение о низком содержании зольных элементов в листьях болотных растений, что, вероятно, связано с бедностью торфа элементами минерального питания (табл. 1).
Таблица 1
Зольность листьев растений верховых болот (%)
|
А |
К. |
С.о. |
М.б. |
К.б. |
П.м. |
П.в. |
О.ш. |
О.п. |
Б.н. |
Г. |
Б.б. |
М.п. |
|||||
|
2,29 |
1,29 |
3,29 |
3,29 |
3,29 |
3,29 |
7,29 |
5,29 |
3,29 |
3,29 |
3,29 |
5,29 |
||||||
|
Б |
ВКБ |
ВКЭ |
ЛЗК |
Т.уз. |
Т.ш. |
Дер. |
|||||||||||
|
2,29 |
1,29 |
3,29 |
3,29 |
3,29 |
3,29 |
||||||||||||
А — зольность листьев разных видов растений: С.с. — сосна сибирская, С.о. — Сосна обыкновенная, М.б. — мирт болотный, К.б. — клюква болотная, П.м. — подбел многолистный, П.в. — пушица влагалищная, О.ш. — осока шаровидная, О.п. — осока пузырчатая, Б.н. — береза карликовая, Г. — голубика, Б.б. — багульник болотный, М.п. — морошка приземистая
Б — зольность листьев растений разных жизненных форм: ВКБ — вечнозеленые кустарнички брусничного типа; ВКЭ — вечнозеленые кустарнички эрикоидного типа; ЛЗК — летнезеленые листопадные кустарнички; Т.уз. — травы с узкими свернутыми или складчатыми листьями; Т.ш. — травы с широкими толстыми жестковатыми листьями; Дер. — деревья.
Из изученных видов самую высокую концентрацию зольных элементов имели осоки заячья и пузырчатая.
Количество отдельных микроэлементов в листьях варьировало в широких пределах — от 8,67 мг/кг (свинец) в листьях мирта болотного до 8959 мг/кг (железо) в листьях осоки шаровидной. У всех видов растений отмечено высокое содержание ионов железа (Fe 3+ ); его содержание составило у сосны обыкновенной до 8959 мг/кг, у осоки шаровидной — 7578 мг/кг.
Листья растений верховых болот характеризуются высоким накоплением марганца и железа. Содержание марганца варьировало от 179 у сосны обыкновенной до 244 мг/кг у сосны сибирской. Количество железа составляло от 7578 мг/кг до 8958,71 мг/кг, его содержание мало изменялось у отдельных видов. Это обусловлено, вероятно, высоким природным содержанием вышеуказанных элементов в болотной воде и торфе, являющихся питательным субстратом для растений.
Растения разных жизненных форм также имели различия по химическим показателям (табл. 2).
Таблица 2
Биохимический и микроэлементный состав листьев растений разных ЖФ
|
Показатель |
ВКБ |
ВКЭ |
ЛЗК |
Т.уз. |
Т.ш. |
Дер. |
|
Общий азот, мг/г |
23,56±5,35 |
38,1±7,88 |
33,17±10,32 |
22,77±5,21 |
32,77±0,63 |
30,28±10,4 8 |
|
Нитратный азот, мг/г |
4,3±1,31 |
6,37±2,61 |
3,81±1,19 |
4,56±2,78 |
3,63±0,77 |
5,48±2,48 |
|
Органический азот, мг/г |
19,26±5,21 |
31,73±7,45 |
29,36±10,44 |
18,21±2,82 |
29,13±0,68 |
24,87±7,93 |
|
Углерод, мг/г |
502,02±10,4 |
489,57±7,37 |
467,37±19,5 |
465,67±10,2 |
446,77±11,6 |
491,43±20 |
|
С/N |
22,86±6,17 |
13,48±3,17 |
16,26±6,69 |
21,52±4,85 |
13,63±0,6 |
18,02±5,59 |
|
Неструк. полисахариды, мг/г |
110,28±12,5 |
123,93±3,33 |
105,25±8,58 |
115,12±17,1 |
117,57±11,4 |
113,88±6,12 |
|
Растворимые сахара, мг/г |
93,24±22,78 |
105,77±6,89 |
105,95±10,2 |
100,97±9,33 |
93±18,28 |
117,33±0,65 |
|
Mn — марганец, мг/кг |
215,9±18,23 |
218,71±29,7 |
228,71±9,14 |
206,86±22,1 |
199,29±0,95 |
211,5±33,75 |
|
Fe — железо, мг/кг |
8303,57±41 6 |
8421,71±50 1 |
8130±648,5 8 |
8728,71±37 9 |
7897,71±35 6 |
7786,5±216 |
|
Pb — свинец, мг/кг |
11,14±2,37 |
12±2 |
14,71±1,68 |
12,36±2,68 |
14±1,63 |
11,89±2,13 |
|
Ni — никель, мг/кг |
27,24±1,79 |
27±2,16 |
24,14±3,44 |
25,36±3,15 |
24±3,56 |
27±1,41 |
|
Zn — цинк, мг/кг |
46,9±10,66 |
48,71±3,2 |
35,79±7,8 |
42,71±1,38 |
53,71±5,47 |
51,5±8,91 |
|
Cr — хром, мг/кг |
50,67±3,75 |
51,29±6,52 |
57,14±1,75 |
55,86±4,8 |
52±2,16 |
53±5,36 |
Примечание : ВКБ — вечнозеленые кустарнички брусничного типа, ВКЭ — вечнозеленые кустарнички эрикоидного типа; ЛЗК — летнезеленые листопадные кустарнички; Т.уз. — травы с узкими свернутыми или складчатыми листьями; Т.ш. — травы с широкими толстыми жестковатыми листьями; Дер. — деревья.
Высокие показатели содержания общего азота — 38,1 мг/г, углерода — 489,57 мг/г, неструктурных полисахаридов — 123,93 мг/г и растворимых сахаров — 105,77 мг/г отмечены у вечнозеленых кустарничков эрикоидного типа. Вечнозеленые кустарнички брусничного типа имели низкие показатели общего азота — 23,56 мг/г, неструктурных полисахаридов — 110,28 мг/г и растворимых сахаров — 93,24 мг/г, но высокое содержание углерода — 502,02 мг/г.
Травы с узкими свернутыми и складчатыми листьями отличались низкими значениями общего азота — 22,77 мг/г, углерода — 465,67 мг/г, неструктурных полисахаридов — 115,12 мг/г и высоким содержанием растворимых сахаров — 100,97 мг/г.
Летнезеленые листопадные кустарнички имели высокие значения общего азота — 33,17 мг/г, растворимых сахаров — 105,95 мг/г и низкие показатели углерода — 468 мг/г, неструктурных полисахаридов — 105,25 мг/г.
У трав с широкими толстыми жестковатыми листьями высокое содержание общего азота — 32,77 мг/г и неструктурных полисахаридов — 117,57 мг/г; невысокие показатели углерода — 446,77 мг/г и растворимых сахаров — 93 мг/г.
У деревьев высокие показатели общего азота — 30,28 мг/г, углерода — 491,43 мг/г, растворимых сахаров — 117,33 мг/г и невысокие значения неструктурных полисахаридов — 113,88 мг/г.
По зольности показатели у разных жизненных форм варьировали от 1,79% до 5,29% (табл. 2). У 67% изученных групп жизненных форм растений зольность не превышала 3,29%.
Для растений разных жизненных форм так же, как и для отдельных видов, наблюдалось повышенное содержание железа и марганца среди зольных элементов (табл. 2).
По содержанию микроэлементов достоверных различий не отмечено только у вечнозеленых кустарничков эрикоидного типа с вечнозелеными кустарничками брусничного типа и травами с широкими толстыми жестковатыми листьями.
Список литературы Особенности биохимической адаптации сосудистых растений верховых болот в условиях Среднего Приобья
- Богдановская-Гиенэф И.Д. Закономерности формирования сфагновых болот верхового типа. Л., 1969.
- Валеева Э.И., Моковченко Д.В. Роль водно-болотных угодий в устойчивом развитии севера Западной Сибири. Тюмень, 2001.
- Вомперский С.Э. Биосферное значение болот в углеродном цикле//Природа. 1994. № 7. С. 44-50.
- Денисенков В.П. Основы болотоведения. СПб., 2000.
- Ефремова Т.Т., Ефремов С.П., Мелентьева Н.В. Запасы и содержание соединений углерода в болотных экосистемах России//Почвоведение. 1997. № 12. С. 1470-1477.
- Ефремов С.П., Ефремова Т.Т., Мелентьева Н.В. Запасы соединений углерода в экосистемах болот//Углерод в экосистемах лесов и болот России/Под. ред. В.А.Алексеева и Р.А.Бердси. Красноярск, 1994. С. 128-139.
- Журавлева Е.Н., Ипатов В.С. Взаимоотношения видов растений в заболоченных сосновых лесах северо-запада России//Ботанический журнал. 2005. Т. 90. № 5. С. 702-712.
- Иванов Л.А. Морфологические и биохимические особенности бореальной зоны с разными типами адаптивных стратегий: Автореф. дис. … канд. биол. наук. Томск, 2001.
- Инишева Л.И., Головацкая Е.А. Элементы углеродного баланса олиготрофных болот//Экология. 2002. № 4. С. 261-266.
- Куриленко В.В., Осмоловская Н.Г. Эколого-биогеохимическая роль макрофитов в водных экосистемах урбанизированных территорий (на примере малых водоемов Санкт-Петербурга)//Экология. 2006. № 3. С. 163-167.
- Лапшина Е.Д. Флора болот юго-востока Западной Сибири. Томск, 2003.
- Лисс О.Л. Болотные системы Западной Сибири и их природоохранное значение. Тула, 2001.
- Медведев С.С. Практикум по минеральному питанию и водному обмену растений: Учеб. пособие. СПб., 1996.
- Методика выполнения изменений массовой доли нефтепродуктов в почвах и донных отложениях методом ИК-спектрометрии ПДН Ф 16.1:2.2.22-98. М., 1998.
- Наследов А.Д. Компьютерный анализ данных в психологии и социальных науках. СПб., 2005.
- Нифонтова М.Г., Маковский В.И. Содержание радионуклидов в торфяной залежи низинных болот//Экология. 1995. № 6. С. 448-454.
- Нешатаев Ю.Н. Методы анализа геоботанических материалов. Л., 1987.
- Полевой В.В. Физиология растений. М., 1989.
- Полевая геоботаника/Под ред. Е.М.Лавренко, А.А.Корчагина. М.; Л., 1960. Т. 2.
- Пьянков В.И., Иванов Л.А. Структура биомассы у растений бореальной зоны с разными типами экологических стратегий//Экология. 2000. № 1. С. 3-10.
- Пьянков В.И., Иванов Л.А., Ламберс Х. Характеристика химического состава листьев растений бореальной зоны с разными типами экологических стратегий//Экология. 2001. № 4. С. 243-251.
- Посыпайко В.И. Химические методы анализа: Учеб. пособие. 2-е изд., перераб. М., 1989.
- Пьявченко Н.И. Об изучении болотных биогеоценозов//Основные принципы изучения болотных биогеоценозов. Л., 1972. С. 5-14.
- Раменский Л.Г. Избранные работы. М., 1971.
- Смагин В.А., Боч М.С. Флора и растительность болот европейского севера России (в пределах таежной зоны)//Ботанический журнал. 2001. Т. 86. № 6. С. 40-55.
- Смагин В.А. О сукцессиях при образовании и развитии болот на месте малых озер (Ленинградская область)//Ботанический журнал. 2003. Т. 88. № 1. С. 76-87.
- Телицын В.Л. Болота Восточного Зауралья: геоэкологические основы оптимизации природопользования. Новосибирск, 2002.
- Усманов И.Ю., Раманкулова З.Ф., Кулагин А.Ю. Экологическая физиология растений: Учебник. М., 2001.
- Филиппович Ю.Б. Практикум по общей биохимии. М., 1982.
- Grime J.P., Hodson J.G., Hunt R. Comparative plant ecology: a functional approach to common British species. L., 1988.


