Особенности деструкции дизельного топлива штаммом Rhodococcus sp. NDT23 в условиях повышенной солености
Автор: Назаров А.В., Пьянкова А.А., Корсакова Е.С.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 3, 2023 года.
Бесплатный доступ
Исследован процесс биодеструкции дизельного топлива (ДТ) в условиях повышенной солености среды с помощью галотолерантного штамма Rhodococcus sp. NDT23, выделенного из загрязненного ДТ образца почвы, отобранной на расстоянии 3 м от солеотвала предприятия ПАО «Уралкалий» (г. Соликамск, Пермский край, Россия). На основе анализа гена 16S рРНК показано, что штамм NDT23 филогенетически близок Rhodococcus fascians DSM 20669T и Rhodococcus cercidiphylli YIM 65003T (сходство 100%). Установлено наличие у штамма NDT23 гена алкан-1-монооксигеназы (alkB), имеющего наибольшее сходство (99.10-100%) с alkB-генами родококков, выделенных из почвы и тканей растений. Выявлено положительное влияние NaCl в концентрации 50 г/л на биодеструкцию длинноцепочечных (С14-С20) углеводородов в составе ДТ, обусловленное увеличением гидрофобности клеточной стенки родококков.
Дизельное топливо, деструкция, rhodococcus, хлорид натрия, засоление
Короткий адрес: https://sciup.org/147241924
IDR: 147241924 | УДК: 579.26: | DOI: 10.17072/1994-9952-2023-3-242-249
Peculiarities of diesel fuel degradation by strain Rhodococcus sp. NDT23 under high salinity conditions
Degradation of diesel fuel by the halotolerant strain Rhodococcus sp. NDT23 under increased salinity conditions was studied. The strain NDT23 was isolated from diesel-contaminated soil sample which collected at a distance of 3 m from the salt dump of the plant of PJSC Uralkali (Solikamsk, Perm region, Russia). On the basis of 16S rRNA gene analysis it was shown that the strain NDT23 is phylogenetically close to Rhodococcus fascians DSM 20669T and Rhodococcus cercidiphylli YIM 65003T (100% similarity). The presence of alkane-1-monooxygenase (alkB) gene in the strain NDT23 was found to have the highest similarity (99.10-100%) with alkB genes of Rhodococcus strains isolated from soil and plant tissues. The ability of the strain NDT23 to degrade diesel fuel (DF) in the medium without salt and at concentrations up to 100 g/L NaCl was detected. A positive effect of NaCl at a concentration of 50 g/L on the degradation of DT by the studied strain was revealed. Moreover, the presence of NaCl in the medium improved the biodegradation of long-chain hydrocarbons (C14-C20) by the strain NDT23 to a greater extent than short-chain hydrocarbons (C9-C13). It is shown that such an increase in the degradation activity of the strain NDT23 is due to an increase in the hydrophobicity of their cell walls in the presence of NaCl in the medium.
Текст научной статьи Особенности деструкции дизельного топлива штаммом Rhodococcus sp. NDT23 в условиях повышенной солености
В настоящее время нефтепродукты являются наиболее распространенными и опасными загрязнителями окружающей среды. Одним из перспективных биотехнологических направлений очистки окружающей среды от органических загрязнителей является биодеструкция с помощью микроорганизмов [Abatenh et al., 2017; Xu et al., 2018; Tarfeen et al., 2022]. Для разработки методов очистки загрязненных природных объектов большое значение имеют исследования деструкции нефтепродуктов микроорганизмами. В ряде случаев эффективность данного метода ограничивается экстремальными условиями среды, в частности высоким засолением [Abed, Al-Kharusi, Al-Hinai, 2015; Edbeib, Wahab, Huyop, 2016; Khalid et al., 2021]. Актинобактерии рода Rhodococcus характеризуются способностью к биодеградации самых разнообразных углеводородов, а также устойчивостью к экстремальным условиям среды, что обусловливает их потенциал в использовании в качестве биопрепаратов для очистки загрязненной среды от нефтепродуктов [Brzeszcz, Kaszycki, 2018]. Особенностью нефтепродуктов как загрязнителей является сложный состав. Так, в дизельном топливе (ДТ) обнаружены тысячи соединений с числом атомов углерода от 8–12 до 25–27, преимущественно – насыщенные углеводороды. Влияние засоления на биодеградацию ДТ, в том числе отдельных углеводородных фракций представителями рода Rhodococcus изучено недостаточно [Brzeszcz, Kaszycki, 2018].
Цель работы – исследование особенностей деструкции дизельного топлива галотолерантным штаммом Rhodococcus sp. NDT23 в условиях повышенной солености.
Материалы и методы
В качестве объекта исследования использовали штамм Rhodococcus sp. NDT23 из коллекции лаборатории микробиологии техногенных экосистем «ИЭГМ УрО РАН», выделенный из загрязненной ДТ дерново-подзолистой почвы с техногенным хлоридно-сульфатным натриево-кальциевым засолением. Образец почвы был отобран на расстоянии 3 м от солеотвала (г. Соликамск, Пермский край, Россия). Координаты участка отбора проб: широта 59°38′00.1′′, долгота 056°45′13.2′′. Концентрация ДТ в почве составляла 5.7%, pH – 7.6, содержание водорастворимых солей – 1.3%.
Для культивирования бактерий использовали минеральную среду Раймонда (МСР) следующего состава (г/л): NH 4 NO 3 - 2.0, MgSO 4 х 7H 2 O - 0.2, K 2 HPO 4 - 2.0, Na 2 HPO 4 - 3.0, CaCh х 6H 2 O - 0.01, Na 2 CO 3 - 0.1, дополненную 1% раствором MnSO4 х 2H 2 O - 2 мл/л и 1% раствором FeSO 4 х 7H 2 O - 1 мл/л среды [Raymond, 1961]. Для приготовления богатой среды Раймонда (БСР) в МСР добавляли 5 г/л триптона («VWR Life Science Amresco», США) и 2.5 г/л дрожжевого экстракта («Biospringer», Франция) в качестве ростовых субстратов. Для приготовления плотной среды вносили агар («Helicon», Россия) до конечной концентрации 15 г/л.
Морфологические и физиологические признаки бактерий определяли при выращивании на агаризо-ванной БСР с добавлением 30 г/л NaCl. Культивирование проводили в термостате при температуре 28°С. Характеристики роста штамма при разных значениях pH определяли при концентрации 30 г/л NaCl в буферных системах, приготовленных на основе БСР. Штаммы культивировали на агаризованной среде БСР при рН 5.0, 6.0, 7.0, 8.0, 9.0, 10.0. Для оценки роста при разных температурах штамм культивировали в диапазоне температур от 4 до 40 °С. Рост учитывали на седьмой день культивирования. [Методы …, 1983].
Рост бактерий на МСР с ДТ оценивали при культивировании в жидких средах без добавления NaCl и с содержанием 30, 50, 70, 100 г/л NaCl. ДТ вносили в МСР до конечной концентрации 1 г/л. Инокулятом служила культура, выращенная при 28°С на агаризованной БСР с 30 г/л NaCl. Биомассу бактерий ресус-пендировали в МСР, содержащей 30 г/л NaCl. Полученную суспензию бактериальных клеток (ОП 600 =1.0) добавляли в 100 мл среды в количестве 1% об./об.
Для оценки роста штамма на БСР без добавления NaCl и с содержанием 30, 50, 70, 100 г/л NaCl инокулят культуры готовили как описано выше.
Культивирование штамма осуществляли в колбах объемом 250 мл на термостатируемом шейкере Environmental Shaker Incubator ES-20/60 («BioSan», Латвия) при температуре 28°С и скорости вращения
140 об/мин. Рост бактериальных клеток оценивали при определении оптической плотности культуральной жидкости (ОП 600 ) на спектрофотометре UV-Visible BioSpec-mini («Shimadzu», Япония) при длине волны 600 нм в кювете с длиной оптического пути 1 см. Удельную скорость роста (μ, ч-1) рассчитывали по стандартной формуле
μ = (lnB2 – lnB1)/(t2 – t1), где В1 и В2 – оптические плотности культуры в моменты времени t1 и t2, соответственно [Нетрусов, 2005].
Через 14 сут. культивирования бактерий в МСР измеряли остаточную концентрацию ДТ в среде в хлороформенных экстрактах на газовом хроматографе Agilent 7890B («Agilent», США) с трехквадрупольным масс-спектрометром Agilent 7010B («Agilent», США) и кварцевой колонкой RESTEK RTx-5MS («Restek » , США). В качестве газа-носителя использовали гелий, скорость потока составляла 1 мл/мин, температура испарителя 260°С. Программирование подъема температуры от 130°С (3-минутная экспозиция), нагрев до 280°С со скоростью 10°С/мин. Анализ хроматограмм проводили с помощью программы MSD Productivity ChemStation («Agilent » , США). Содержание углеводородов оценивали по площадям пиков в сравнении с площадью пиков контрольного образца ДТ, а также хлороформенных растворов индивидуальных углеводородов.
Гидрофобность клеточной поверхности (Н, %) определяли с использованием МATH-теста [Rosenberg, 1984; Maneerat, Dikit, 2007].
Для амплификации гена alkB, кодирующего алкан-1-монооксигеназу, использовали вырожденные праймеры TS2S и Deg1RE [Smits et al., 1999]. В качестве положительного контроля использовали ДНК штамма Rhodococcus wratislaviensis КТ112-7, в геноме которого содержится alkB (GenBank CP072193). Амплификацию осуществляли на приборе C1000 TouchTM Thermal Cycler («Bio-Rad Laboratories», США) согласно условиям [Smits et al., 1999]. Определение нуклеотидной последовательности гена alkB проводили с использованием набора реактивов Big Dye Terminator Cycle Sequencing Kit v. 3.1 («Applied Biosystems», США) на автоматическом секвенаторе Genetic Analyser 3500XL («Applied Biosystems», США) согласно рекомендациям производителя. Анализ нуклеотидной последовательности осуществляли с применением программ Sequence Scanner v 2.0 и MEGA 6.0 . Поиск гомологичных последовательностей проводили в международной базе данных GenBank .
Статистическую обработку данных проводили с помощью программы Statistica 6.0.
Результаты и их обсуждение
Штамм NDT23 при культивировании на агаризованной БСР формировал округлые колонии оранжевого цвета диаметром 2–4 мм с ровным краем, гладкой поверхностью, выпуклым профилем, блестящей поверхностью, однородной структурой и мягкой консистенцией. Клетки штамма грамположительные, каталазо-положительные, оксидазо-отрицательные, имеют цикл развития «палочки-кокки». Исследуемый штамм рос при температуре 4–37°С, pH 5.0–9.0. На основе анализа фрагмента гена 16S рРНК (937 п.н.) установлено, что штамм NDT23 проявлял сходство на уровне 100% со штаммами Rhodococcus fascians DSM 20669T и Rhodococcus cercidiphylli YIM 65003T. Нуклеотидная последовательность гена 16S рРНК штамма NDT23 депонирована в базе данных GenBank под номером ON527782.
Как видно из данных, приведенных в табл. 1, штамм NDT23 способен к росту в жидкой МСР с ДТ в качестве единственного источника углерода и энергии.
Таблица 1
Параметры роста клеток Rhodococcus sp. NDT23 в БСР и МСР с дизельным топливом при различных концентрациях хлорида натрия
[Growth parameters of the Rhodococcus sp. strain NDT23 in NRM and MRM with diesel fuel at different concentrations of sodium chloride]
|
Параметры роста |
Рост штамма в БСР |
Рост штамма в МСР с ДТ (1 г/л) |
||||||
|
Концентрация NaCl, г/л |
||||||||
|
0 |
30 |
50 |
70 |
0 |
30 |
50 |
70 |
|
|
Удельная скорость роста (ч-1) |
0.052 ±0.002 |
0.058 ±0.003 |
0.047 ±0.002 |
0.019 ±0.002 |
0.030 ±0.004 |
0.017 ±0.003 |
0.007 ±0.002 |
0.003 ±0.001 |
|
Максимальное значение ОП 600 |
2.03 |
2.1 |
2.17 |
2.04 |
0.98 |
1.08 |
0.92 |
0.69 |
|
Лаг-фаза роста (ч) |
48 |
48 |
72 |
100 |
46 |
46 |
96 |
263 |
Амплификация гена алкан-1-монооксигеназы (alkB), ключевого фермента аэробной деградации н-алканов (компонентов ДТ), с использованием вырожденных праймеров TS2S и Deg1RE [Smits et al., 1999] приводила к наработке ПЦР-продукта ожидаемого размера (около 550 п.н.). Сравнительный анализ последовательности гена alkB штамма Rhodococcus sp. NDT23 с гомологичными последовательностями из базы данных GenBank показал наибольшее (99.10–100%) сходство с alkB-генами штаммов рода Rhodococcus, выделенных из почвы и тканей растений (рис. 1).
NDT23
Rhodococcusjascians 2D82 (AKP07081)
— Rhodococcus sp.Mt6 (QIM55905)
Rhodococcus sp.PBTS2 (AMY23505)
некупьтивируемый клон P29-3O_C1.1 l_HRB0-5m-200S (CCO96087)
__I Rhodococcusfascians JCM 10002т (AHA51157)
65 Rhodococcusfascians DISS (AMY52517)
----------------некупьтивируемый клон 13232191491 (AGQ21093)
Rhodococcusjasciarcs A25f (QII07998)
I— Rhodococcus sp. B7740 (AJW40969)
Rhodococcus sp. 3.3-VPr (AEH76915)
--------------------------------------Rhodococcus sp. 11/16a (ABD36389)
86 ' Rhodococcus cercidiphyihDSM 45141T (AIA96567)
0.01
Рис. 1. Положение alkB -гена Rhodococcus sp. NDT23 на филогенетическом дереве, построенном на основании сравнительного анализа транслированных аминокислотных последовательностей alkB -генов с использованием метода «neighbor-joining». Эволюционные расстояния рассчитаны с использованием метода «p-distance».
Цифрами показана статистическая достоверность порядка ветвления, установленная с помощью «bootstrap»-анализа 1 000 альтернативных деревьев (приведены значения выше 50%). Масштаб соответствует 1 аминокислотной замене на каждые 100 аминокислот. В скобках указаны номера в базе данных GenBank
[The position of the alkB gene of Rhodococcus sp. NDT23 on a phylogenetic tree constructed based on a comparative analysis of the translated amino acid sequences of the alkB genes using the “neighbor-joining” method. The evolutionary distances were computed using the “p-distance” method.
The numbers show the statistical significance of the branching order, established using a “bootstrap” test of 1000 alternative trees (values above 50% are given). The scale corresponds to 1 amino acid substitution for every 100 amino acids. Numbers in the GenBank database are given in parentheses]
Штамм NDT23 при культивировании в БСР и МСР способен расти как без NaCl, так и при концентрации соли до 70 г/л (рис. 2A, B). Наибольший рост культуры отмечен в БСР и МСР с ДТ без добавления хлорида натрия и при 30 г/л NaCl. Дальнейшее увеличение концентрации NaCl в обеих средах приводило к замедлению роста культуры. Однако в случае использования среды БСР повышение солености оказывало меньшее негативное воздействие на рост бактериальных клеток, чем в МСР с ДТ (см. табл. 1). Так, если при концентрации NaCl 70 г/л в БСР удельная скорость роста снижалась в 2.7 раза, максимальная ОП 600 не изменялась, лаг-фаза роста увеличивалась в 2.1 раза относительно роста штамма в БСР без NaCl, то при росте штамма NDT23 в среде МСР с ДТ при содержании NaCl 70 г/л удельная скорость роста уменьшалась в 10.0 раз, максимальная ОП 600 – в 1.4 раза, а продолжительность лаг-фазы роста культуры увеличивалась в 5.7 раза.
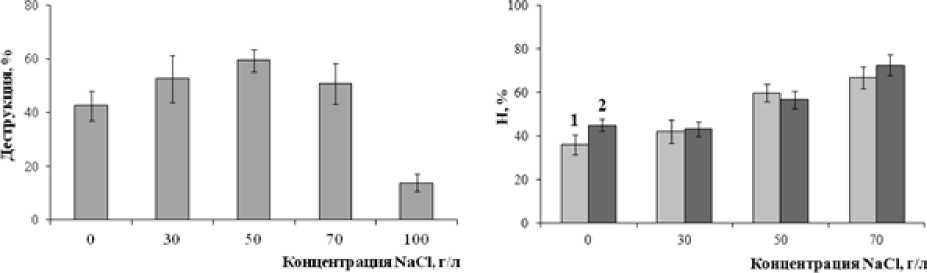
При культивировании Rhodococcus sp. NDT23 на среде с добавлением 30 и 70 г/л NaCl отличия в скорости деструкции ДТ в сравнении с вариантом опыта без добавления NaCl, не обнаружены, в то же время в присутствии 50 г/л NaCl в среде убыль углеводородов ДТ увеличивалась в 1.4 раза (рис. 3A). Наименьший (в 3.1 раза ниже в сравнении с культивированием штамма NDT23 в среде без NaCl) уровень утилизации углеводородов ДТ выявлен при содержании NaCl в среде 100 г/л, при этом рост бактериальной культуры не обнаруживался (рис. 2B).
Положительное влияние в среде NaCl в количестве 50 г/л на деструкцию ДТ проявлялось вследствие увеличения уровня разложения длинноцепочечных (С 14 –С 20 ) углеводородов, содержание которых в среде снижалось в 1.2–2.5 раза относительно контрольного варианта без добавления NaCl (табл. 2). В то же время положительный эффект повышенной солености среды на биодеградацию короткоцепочечных (С 9 – С 13 ) углеводородов не выявлен (табл. 2). Ранее [de Carvalho, 2012] при исследовании деструкции индивидуальных насыщенных (C 12 –C 16 ) углеводородов клетками Rhodococcus erythropolis было показано положительное воздействие NaCl в концентрациях до 5% на биодеградацию длинноцепочечных (C 12 –C 16 ) н -алканов при отсутствии аналогичного влияния NaCl в данных концентрациях на биодеструкцию короткоцепочечных (C 6 –C 11 ) н -алканов. Выявленную закономерность авторы связывали с повышением гидрофобности поверхности бактериальных клеток.
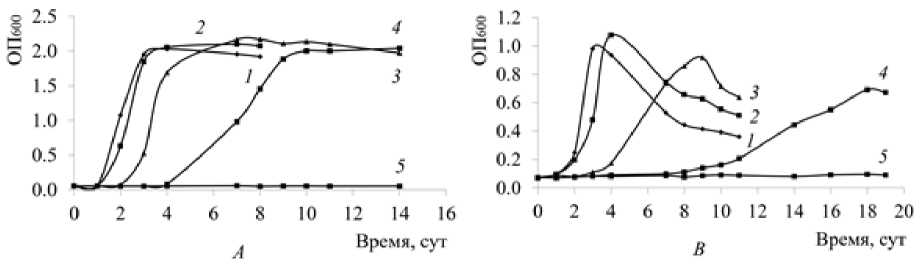
Рис. 2. Рост клеток Rhodococcus sp. NDT23 в питательной среде БСР ( А ) и МСР ( В ) с дизельным топливом (1 г/л) при различных концентрациях NaCl (г/л):
1 – 0; 2 – 30; 3 – 50; 4 – 70; 5 – 100
[Growth of the Rhodococcus sp. strain. NDT23 in NRM ( A ) and MRM ( B ) with diesel fuel (1 g/L) at different NaCl concentrations (g/L):
1 – 0; 2 – 30; 3 – 50; 4 – 70; 5 – 100]
Таблица 2
Остаточное содержание (% от начальной концентрации) углеводородов ДТ после 14 сут. роста клеток Rhodococcus sp. NDT23
[Residual content (% of the initial concentration) of DF hydrocarbons after 14 days of cultivation of the Rhodo-coccus sp. strain NDT23]
|
Концентрация NaCl в среде, г/л |
Количество атомов углерода в углеводороде |
|||||
|
9 |
10 |
11 |
12 |
13 |
14 |
|
|
0 |
13.0±4.5 |
17.1±4.7 |
32.3±3.0 |
38.8±3.3 |
65.2±5.9 |
75.4±4.9 |
|
30 |
10.3±1.8 |
17.4±4.6 |
33.5±3.0 |
41.8±2.1 |
54.8±5.1 |
70.5±5.4 |
|
50 |
14.5±2.2 |
20.4±2.3 |
33.4±4.6 |
31.4±4.4 |
52.8±6.5 |
65.5±5.9 |
|
70 |
11.4±2.6 |
26.0±3.1 |
16.7±3.9 |
66.6±3.3 |
61.0±4.9 |
63.1±4.6 |
|
100 |
63.7±8.1 |
59.1±5.2 |
80.1±8.7 |
93.6±11.6 |
94.7±16.3 |
95.1±10.2 |
|
Концентрация |
Количество атомов углерода в углеводороде |
|||||
|
NaCl в среде, г/л |
15 |
16 |
17 |
18 |
19 |
20 |
|
0 |
76.7±5.8 |
80.1±6.9 |
108.7±8.6 |
101.5±8.6 |
106.9±12.6 |
93.2±7.8 |
|
30 |
56.8±3.6 |
67.9±9.8 |
63.2±6.7 |
60.7±8.2 |
58.3±9.2 |
64.5±11.5 |
|
50 |
42.8±5.2 |
43.8±4.2 |
44.5±4.1 |
43.6±5.3 |
43.2±3.2 |
41.6±3.2 |
|
70 |
57.7±7.0 |
57.3±4.2 |
67.4±5.0 |
67.9±6.6 |
52.8±4.9 |
42.1±6.9 |
|
100 |
98.0±9.4 |
94.0±9.5 |
98.5±8.2 |
97.3±7.2 |
94.9±9.8 |
91.6±5.3 |
Как видно из рис. 3В, с повышением концентрации NaCl в средах БСР и МСР, содержащих ДТ, происходило увеличение гидрофобности поверхности клеток Rhodococcus sp. NDT23. Так, гидрофобность бактериальных клеток при культивировании в среде БСР, содержащей 50 и 70 г/л NaCl, увеличивалась в 1.7 и 1.9 раза в сравнении с таковой клеток, выращенных без добавления NaCl. Аналогичное повышение (в 1.3 и 1.6 раза) гидрофобности клеток Rhodococcus sp. NDT23 отмечено при культивировании их в среде МСР, содержащей 50 и 70 г/л NaCl, соответственно.
Согласно немногочисленным литературным данным, бактерии характеризуются различными изменениями степени гидрофобности клеточной поверхности под действием засоления. Снижение гидрофобности клеток в условиях засоления выявлено у Halomonas elongata [Hart, Vreeland, 1988], Erythrobacter sp . [Longang, Buck, Kirkwood, 2016], Exiguobacterium sp. [Cao et al., 2020], а увеличение – у представителей рода Rhodococcus [Рубцова, Куюкина, Ившина, 2012; Longang, Buck, Kirkwood, 2016] и у почвенных ак-тиномицетов [Zahir et al., 2016]. При этом гидрофобность клеточной поверхности галотолерантных штаммов родококков возрастала с увеличением концентрации NaCl в среде, тогда как гидрофобность клеток Rhodococcus spp., не устойчивых к повышенной солености среды, снижалась или не изменялась [Рубцова, Куюкина, Ившина, 2012].
Известно, что степень гидрофобности клеточной стенки играет важную роль в адсорбции микроорганизмами углеводородов и их поглощении, поэтому рост в присутствии углеводородных субстратов сопровождается повышением гидрофобности клеток у многих актинобактерий, в том числе представителей Dietzia и Rhodococcus [Bredholt et al., 2002; de Carvalho et al., 2007; Hvidstena et al., 2015]. В нашем случае, увеличение гидрофобности клеточной поверхности Rhodococcus sp. NDT23 при концентрации 50 г/л NaCl в среде (рис. 3А) способствовало повышению скорости биодеградации длинноцепочечных алканов
(C 14 –C 20 ) в составе ДТ, которые имеют большую гидрофобность, чем короткоцепочечные углеводороды (С 9 –С 13 ) (табл. 2).
-
4 В
Рис. 3. Влияние различных концентраций NaCl на деструкцию ДТ ( А ) и гидрофобность клеточной поверхности (H, %) Rhodococcus sp. NDT23 ( В ) при росте на среде БСР (1) и МСР (2) с добавлением ДТ (1 г/л) через 14 сут. культивирования
[The influence of different concentrations of NaCl on the destruction of DF ( A ) and cell surface hydrophobicity (H, %) of Rhodococcus sp. NDT23 ( B ) on NRM (1) and MRM (2) with diesel fuel (1 g/L) after 14 days of cultivation ]
Уменьшение скорости биодеструкции ДТ при дальнейшем повышении содержания NaCl в среде до 70 и 100 г/л, очевидно, обусловлено снижением скорости роста и накопления биомассы Rhodococcus sp. NDT23 (рис. 2В). Таким образом, в нашей работе показано, что повышенная соленость среды влияет на процесс деструкции родококками углеводородов (C 9 –C 20 ) в составе ДТ аналогично биодеградации индивидуальных углеводородов (C 6 –C 16 ) клетками R. erythropolis [de Carvalho, 2012]. Подтверждено предположение о положительном влиянии солености среды на биодеструкцию углеводородов вследствие повышения гидрофобности клеточной поверхности Rhodococcus [de Carvalho, 2012]. Противоположная ситуация отмечена в работе [Cao et al., 2020], в которой при увеличении солености среды происходило снижение гидрофобности клеточной поверхности Exiguobacterium sp. N4–1P, что приводило к уменьшению скорости бактериальной деструкции длинноцепочечных алканов, однако, при этом повышалась степень деградация более водорастворимого нафталина.
Заключение
Таким образом, исследованный нами штамм Rhodococcus sp. NDT23 способен к эффективному росту на среде с ДТ в присутствии NaCl до 70 г/л и деградации углеводородов ДТ при концентрациях NaCl до 100 г/л. Показано, что с увеличением концентрации NaCl в среде возрастает гидрофобность клеточной поверхности штамма NDT23, что, в свою очередь, приводит к увеличению деструкции ДТ при содержании в среде NaCl в количестве 50 г/л. При этом наличие NaCl в среде в большей степени увеличивало разложение штаммом Rhodococcus sp. NDT23 длинноцепочечных углеводородов (С 14 –С 20 ), чем короткоцепочечных (С 9 –С 13 ). Штамм Rhodococcus sp. NDT23 может быть использован для разработки биотехнологических методов очистки засоленных экосистем, загрязненных ДТ.
Список литературы Особенности деструкции дизельного топлива штаммом Rhodococcus sp. NDT23 в условиях повышенной солености
- Методы общей бактериологии: пер. с англ. / под ред. Ф. Герхардта с соавт. М.: Мир, 1983. Т. 1–3.
- Нетрусов А.И. Практикум по микробиологии. М.: Академия, 2005. 608 с.
- Рубцова Е.В., Куюкина М.С., Ившина И.Б. Влияние условий культивирования на адгезивную активность родококков к н-гексадекану // Прикладная биохимия и микробиология. 2012. Т. 48, № 5. С. 501‒509.
- Abatenh E. et al. Application of microorganisms in bioremediation-review // J. Env. Microbiol. 2017. Vol. 1(1). P. 2–9.
- Abed R.M.M., Al-Kharusi S., Al-Hinai M. Effect of biostimulation, temperature and salinity on respiration activities and bacterial community composition in an oil polluted desert soil // Int. Biodeter. Biodegr. 2015. Vol. 98. P. 43–52.
- Bredholt H. et al. Hydrophobicity development, alkane oxidation, and crude-oil emulsification in a Rhodo-coccus species // Can. J. Microbiol. 2002. Vol. 48(2). P. 295–304.
- Brzeszcz J., Kaszycki P. Aerobic bacteria degrading both n-alkanes and aromatic hydrocarbons: an under-valued strategy for metabolic diversity and flexibility // Biodegrad. 2018. Vol. 29(4). P. 359–407.
- Cao Y. et al. Microbial eco-physiological strategies for salinity-mediated crude oil biodegradation // Sci. Total. Environ. 2020. Vol. 727. P. 1–7.
- de Carvalho C.C.C.R. Adaptation of Rhodococcus erythropolis cells for growth and bioremediation under extreme conditions // Res. Microbiol. 2012. Vol. 163. P. 125–136.
- de Carvalho C.C.C.R. et al. Adaptation of Rhodococcus erythropolis cells to high concentrations of tolu-ene // Appl. Microbiol. Biotechnol. 2007. Vol. 76. P. 1423–1430.
- Edbeib M.F., Wahab R.A., Huyop F. Halophiles: biology, adaptation, and their role in decontamination of hypersaline environments // World J. Microbiol. Biotechnol. 2016. Vol. 32(8). P. 1–23.
- Gharibzahedi S.M.T., Razavi S.H., Mousavi M. Potential applications and emerging trends of species of the genus Dietzia: a review // Ann. Microbiol. 2014. Vol. 64. P. 421–429.
- Hart D.J., Vreeland R.H. Changes in the hydrophobic-hydrophilic cell surface character of Halomonas elongata in response to NaCl // J. Bacteriol. 1988. Vol. 170. P. 132–135.
- Hvidsten I. et al. Fatty acids in bacterium Dietzia sp: grown on simple and complex hydrocarbons deter-mined as FAME by GC-MS // Chem. Phys. Lipids. 2015. Vol. 190. P. 15–26.
- Khalid F.E. et al. Bioremediation of diesel contaminated marine water by bacteria: a review and biblio-metric analysis // J. Mar. Sci. Eng. 2021. Vol. 9(2). P. 1–19.
- Longang A., Buck C., Kirkwood K.M. Halotolerance and effect of salt on hydrophobicity in hydrocar-bon-degrading bacteria // Environ. Technol. 2016. Vol. 37(9). P. 1133–1140.
- Maneerat S., Dikit P. Characterization of cell-associated bioemulsifier from Myroides sp. SM1, a marine bacterium // Songklanakarin J. Sci. Technol. 2007. Vol. 29(3). P. 769–779.
- Rosenberg M. Bacterial adherence to hydrocarbons: a useful technique for studying cell surface hydro-phobicity // FEMS Microbiol. Lett. 1984. Vol. 22. P. 289–295.
- Smits T.H.M. et al. Molecular screening for alkane hydroxylase genes in gram-negative and gram-positive strains // Environmental Microbiology. 1999. Vol. 1(4). P. 307–317.
- Tarfeen N. et al. Microbial remediation: a promising tool for reclamation of contaminated sites with spe-cial emphasis on heavy metal and pesticide pollution: a review // Proces. 2022. Vol. 10. P. 1–27.
- Xu X. et al. Petroleum hydrocarbon-degrading bacteria for the remediation of oil pollution under aerobic conditions: a perspective analysis // Front. Microbiol. 2018. Vol. 9. P. 1–11.
- Zahir H. et al. Effect of salinity on the adhesive power actinomycetes in soil // J. Mater. Environ Sci. 2016. Vol. 7(9). P. 3327–3333.


