Особенности диагностики рака простаты по биопсийному материалу
Автор: Федорина Т.А., Полетаева С.В.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Макро- и микроморфология
Статья в выпуске: 4 т.9, 2013 года.
Бесплатный доступ
Цель, изучить особенности диагностики рака простаты по биоптатам. Материал и методы. Исследован гистологический материал от 700 пациентов, в том числе от 580 пациентов после радикальной простатэктомии. Всем пациентам до лечения выполнялась биопсия из 12 точек под контролем ТРУЗИ. Проведено гистологическое, морфометрическое, иммуногистохимическое (Р1Ы4-коктейль, рецепторы к андрогену) исследование би-опсийного и операционного материала. Результаты. В 3% имелось завышение, а в 26% — занижение суммы Глисона по биоптатам. В большинстве случаев занижение суммы Глисона связано с низким содержанием опухолевых элементов в биоптатах, мультицентрическим ростом, гетерогенностью строения опухоли. Заключение. Важная задача патолога: выявление даже минимального числа неопластических желез в биоптатах, так как в группе пациентов с аденокарциномой, занимавшей менее 5% площади единичного столбика, часто обнаруживался рак объемом более 1 см3 в операционном материале.
Атипическая аденоматозная гиперплазия, радикальная простатэктомия, рак простаты, трепанбиопсия
Короткий адрес: https://sciup.org/14917810
IDR: 14917810
Текст научной статьи Особенности диагностики рака простаты по биопсийному материалу
-
1В ведение . Рак простаты (РП) является одним из наиболее часто встречающихся злокачественных новообразований у мужчин, занимая второе место в структуре смертности от рака и составляя 12 % от всех злокачественных новообразований у мужчин. Учитывая, что частота РП неуклонно растет, актуальность диагностики ранних, локализованных форм не вызывает сомнений. Гистологическое исследование материала, полученного в результате мультифокальной биопсии, является ответственным этапом диагностики РП [1, 2]. Малые размеры биоптатов и ограниченные по размерам участки патологически измененной ткани создают большие трудности для морфологической верификации заболевания. [3]. Атипическая мелкоацинарная пролиферация представляет собой группу гиперпластических, атрофических и пренео-пластических морфологических изменений, включая атипическую аденоматозную пролиферацию, по клиническому значению приравненную к простатической интраэпителиальной неоплазии высокой степени (ПИН3) [4]. Сходство гистоархитектоники с мелкоацинарной аденокарциномой требует применения дополнительных методов морфологического исследования для верификации диагноза и своевременного назначения адекватного лечения [5]. Дифференциальная диагностика ПИН высокой степени должна проводиться с встречающимися в гистологическом материале участками нормальных анатомических структур (семенные пузырьки, железы центральной зоны простаты), реактивными воспалительными, метапластическими, гиперпластическими изменениями и раком [6].
От 1,5 до 5,3% всех биоптатов простаты содержат единичные очаги из мелких ацинарных структур, вызывающих подозрение на рак, но не достигающих диагностического «порога». Эти очаги атипической мелкоацинарной пролиферации (АМАП) при дальнейшем исследовании в 43% оказываются участками аденокарциномы (по данным результатов 16 исследований) [7].
Основные причины применения этого термина, согласно исследованиям Bostwick и Meiers [8], следующие: чрезвычайно малое количество неопластических желез, противоречивые гистологические или иммуногистохимические данные, а также недостоверная морфологическая картина, например, вследствие артефактов изготовления препарата, ПИН высокой степени, реактивных изменений эпителия воспалительного характера, повреждения ткани.
Иммуногистохимическое окрашивание с помощью PIN4-коктейля в ряде случаев позволяет точно установить характер процесса, что позволяет избежать повторной биопсии. Однако часто требуется применение специальных методик изучения биопта-та. Одна из них включает гистологическое и иммуногистохимическое исследование 12 интервальных срезов биоптата с очагом АМАП. При этом 6 срезов окрашены гематоксилином и эозином, остальные 6 — иммуногистохимически. Еще один метод включает исследование повторного среза. При исполь зовании первой методики, согласно исследованиям
Hameed и Humphrey, вероятность потери интересующего очага 8%, при второй — 50% [9].
Размер небольшого единичного очага аденокарциномы, выявленного только в одном столбике, следует точно обозначать, поскольку это может служить показанием для проведения дополнительных диагностических мероприятий перед назначением лечения. По результатам некоторых исследований, выявление в одном столбике карциномы менее 5% площади биоптата с суммой баллов по Глисону 5–6 во многих случаях связано с клинически незначимой опухолью и с высокой вероятностью спонтанной регрессии рака [10, 11].
Цель исследования : оценить роль морфологического исследования в диагностике ранних латентных форм РП.
Материал и методы. Исследован гистологический материал от 530 пациентов: только биопсийный материал от 60; биопсийный и операционный материал от 470 пациентов онкоурологического отделения ГБУЗ «СОКОД», которым была выполнена радикальная простатэктомия, за период 2009–2012 гг. Трансректальная мультифокальная биопсия выполнялась с помощью системы Fast Gun 18G под контролем УЗИ на GE Logic 7, из 12 точек. При исследовании операционного материала применяли стандартную методику обработки макропрепарата с маркировкой поверхности двумя адгезивными красителями для выявления истинного позитивного хирургического края и исключения артефакта нарезки. Отдельно исследовали семенные пузырьки, апикальную, базальную и среднюю часть железы.
Гистологическое исследование проводилось на парафиновых срезах толщиной 5 мкм, окрашенных гематоксилином и эозином. Определяли гистологический тип опухоли, степень злокачественности по системе Глисона, состояние края резекции. Для установления патологоанатомической стадии оценивали экстрапростатическое распространение. Объем рака в материале определяли с помощью компьютерной планиметрии. При исследовании биоптатов от 70 пациентов для подтверждения злокачественного характера ацинарной пролиферации проводили ИГХ-исследование с PIN-4-коктейлем. Последний представляет собой смесь антител к маркеру онкогенеза и антигенам, отражающим состояние базальной мембраны и базального слоя клеток. PIN4-коктейль включает протеин p504S (альфа-метилацил-коА-ра-цемаза), представляющий собой пероксисомный и митохондриальный фермент, синтезирующийся в раковых клетках простаты, а также антитела к p63 для оценки наличия базальных клеток и антитела к высокомолекулярным цитокератинам (клон 34βЕ12) для визуализации базальной мембраны. Использовали антитела BioGenex. Микрофотографирование проводили с помощью камеры «Leica DFC 420 C» и обрабатывали с помощью пакета компьютерного анализа изображения Leica Qwin Standart V.3.1.0. Статистическую обработку данных проводили с помощью пакета Statistica 7.0.
Результаты. В группе 120 пациентов, которым по результатам исследования биоптатов простаты потребовалось проведение иммуногистохимического исследования, средний возраст пациентов составил 67 лет (от 47 до 84 лет). Средний объем простаты по данным ультразвукового исследования составил 45,5 см³. Средний уровень ПСА — 11,3 нг\мл. В заключениях УЗИ превалировали доброкачественная гиперплазия простаты (ДГПЖ) и хронический про- статит (97), в 14 наблюдениях выявлены изменения, требующие дифференциальной диагностики между раком и хроническим простатитом, в 9 — подозрение на рак.
После иммуногистохимического исследования мелкоацинарная аденокарцинома выявлена в 48 наблюдениях, в 25 — очаги атипической аденоматозной гиперплазии, в том числе в 14 — в сочетании с участками ПИН-3 криброзного и микропапиллярного строения, в 38 — атрофические изменения желез. В 9 наблюдениях изготовление дополнительных срезов биоптата из парафинового блока не привело к увеличению количества неопластических желез, оставаясь на уровне 5 и менее. При этом сделать достоверное заключение о злокачественном новообразовании было невозможно.
Средний возраст пациентов в группе с выявленными атрофическими изменениями составил 64,7 года, в группе с атипической аденоматозной гиперплазией и ПИН-3–66,4 года, в группе с аденокарциномой — 69,9 года. Между тремя группами пациентов (с атрофическими изменениями, с очагами атипической аденоматозной гиперплазии и аденокарциномой) не выявлено статистически значимого отличия по уровню ПСА (средние показатели соот- ветственно 11,41, 10,53 и 12,24 нг\мл.) При сравнении трех групп критерий Крускала — Уоллиса составил 0,705 (p>0,05). Средний объем железы в группе пациентов с ПИН-3 и атипической аденоматозной гиперплазией составил 60,2 см³, тогда как в группах с аденокарциномой и атрофическими изменениями — 32 и 37 см³ соответственно. Критерий Крускала — Уоллиса 1,509, при попарном сопоставлении групп (1-й и 2-й, 1-й и 3-й, 2-й и 3-й) значения критерия Данна составили 1,073, 0,270 и 1,058, статистически достоверного различия не выявлено (p>0,05).
Обсуждение. Под термин АМАП попадают две разные категории наблюдений: во-первых, случаи с сомнительными признаками цитологической атипии и инвазии (рис. 1) при достаточном количестве желез (12 и более); во-вторых, наблюдения с чрезвычайно малым количеством желез (менее 5–7) с признаками атипии и инвазии (рис. 2). В таком случае увеличение количества желез в повторных срезах позволяет решить диагностическую проблему. По нашим данным, количество наблюдений, относящихся ко второй категории, составило 13 (11% от всех АМАП и 27% от пациентов, у которых после ИГХ подтверждена аденокарцинома).
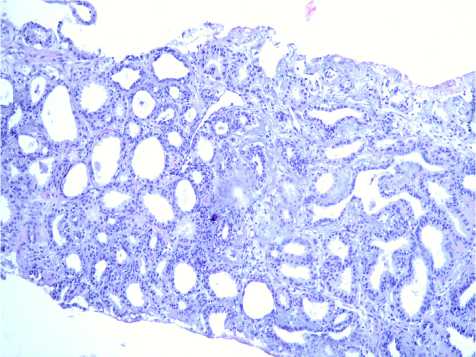
А
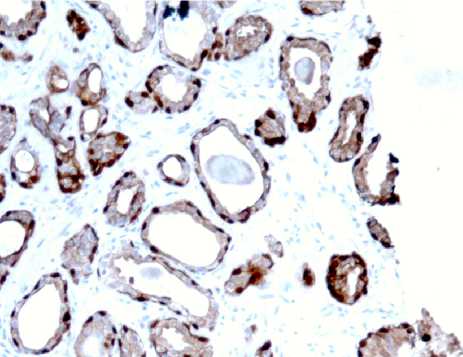
Б
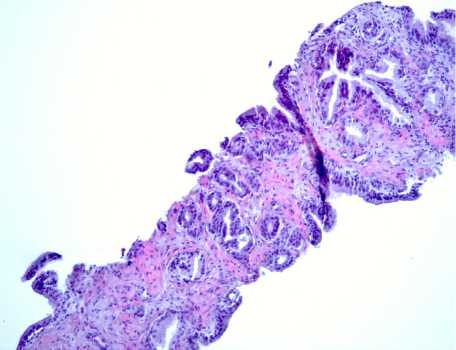
А
Рис. 2. А: очаг АМАП. Окрашивание: гематоксилин и эозин. х100. Б: то же наблюдение. Аденокарцинома. Окрашивание: гематоксилин и ИГХ окрашивание PIN-4 коктейль. х200
Рис. 1. А: очаг АМАП. Окрашивание: гематоксилин и эозин. х200. Б: то же наблюдение. Атрофия желез. Окрашивание: гематоксилин и ИГХ окрашивание PIN-4 коктейль. х200
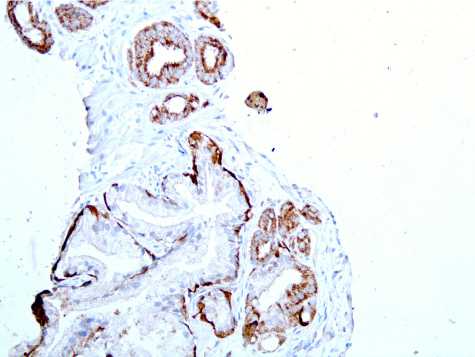
Б
|
Сумма Gleason |
Объем опухоли в биоптатах, количество столбиков \ общий % поражения (n=470) |
Всего |
|||
|
1\< 5% (n=41) |
2\<20% (n=93) |
>3/<60% (n=310) |
>3/ >60% (n= 136) |
||
|
5–6 |
27 |
43 |
218 |
28 |
316 |
|
7 |
10 |
40 |
76 |
60 |
186 |
|
8–10 |
4 |
10 |
16 |
48 |
78 |
В группе пациентов, которым была выполнена радикальная простатэктомия, средний возраст пациентов составил 65 лет (от 49 до 75 лет). При исследовании операционного материала у 316 (54,5%) диагностирован РП G1–2 (сумма Глисона 4–6). Cумма Глисона 7 и 8–10 встретились соответственно в 186 (32%) и 78 (13,5%) наблюдениях.
При сопоставлении степени злокачественности в биопсийном и операционном материале все наблюдения разделили на 3 группы: 1) в 412 наблюдениях (71 %) степень злокачественности не изменилась при полном совпадении суммы Глисона или при изменении ее на 1 балл; 2) в 17 случаях (3%) выявлено завышение степени злокачественности по Глисону; 3) в 151 наблюдениях (26%) имелось занижение суммы Глисона по биоптатам.
При ретроспективном изучении биоптатов 168 пациентов (2-й и 3-й группы) выявлено, что основной причиной (в 126 случаях) завышения или занижения суммы Глисона является гетерогенность структуры РП. В 38 случаях, наряду с разной степенью анаплазии, имелись включения редких вариантов строения ацинарной аденокарциномы (псевдогиперпласти-ческий, атрофический, ксантомоподобный, а также слизеобразующий и перстневидно-клеточный), в 13 случаях выявлен ацинарно-протоковый тип. В 42 случаях в биопсийный материал попали участки и доминантного (большего по размерам, с более высокой степенью злокачественности) узла, и дополнительных, чаще располагающихся в транзиторной зоне, с более низкой степенью злокачественности. Это привело к разной сумме Глисона в разных столбиках, а в 14 случаях в биоптаты попала только ткань дополнительных узлов, что привело к занижению степени злокачественности. В 29 биоптатах встречались кри-брозные структуры, для правильной трактовки которых (ПИН-3, 3 или 4 — градация по Глисону) требовалось иммуногистохимическое исследование. В 11 случаях оценка степени злокачественности опухоли была затруднена из-за выраженного муцинозного компонента.
Среди пролеченных хирургическим методом пациентов с аденокарциномой, определявшейся в единичном столбике с долей поражения менее 5%, оказалось 41 (7%). По результатам исследования удаленной простаты объем рака менее 0,5 см³ выявлен лишь в 7 наблюдениях (17%), от 0,5 до 1 см3 — в 22 наблюдениях (54%). У 9 (23%) объем рака составил более 1, но менее 2 см³, находился в интервале от 2 до 5 см3 у 3 (7%). По степени злокачественности наблюдения распределились следующим образом (таблица).
Объем РП в биоптатах и итоговая сумма Глисона в операционном материале
Заключение. Точная дооперационная оценка степени злокачественности РП по биоптатам часто затруднена. Чаще встречается занижение суммы
Глисона по биоптатам (26%). В большинстве случаев занижение суммы Глисона связано с низким содержанием опухолевых элементов в биоптатах, муль-тицентрическим ростом, гетерогенностью строения опухоли.
Использование иммуногистохимического метода повышает специфичность диагностики и вероятность выявления аденокарциномы при исследовании биоптатов с мелкоацинарными структурами с вариабельными проявлениями цитологической ати-пии и сомнительными признаками инвазии.
Дополнительные методы исследования не всегда позволяют поставить диагноз аденокарциномы, если количество неопластических желез менее 5. Эта группа пациентов нуждается в повторной биопсии.
Выявление в одном столбике карциномы менее 5% площади биоптата с суммой баллов по Глисону 5-6 не всегда (лишь в 17%) связано с клинически незначимой опухолью, что может затруднять выбор тактики лечения у данной группы пациентов.
Список литературы Особенности диагностики рака простаты по биопсийному материалу
- Epstein J.I., Yang X.J. Finding of atypical glands suspicious for cancer//Epstein J.I., Yang X.J., eds. Prostate Biopsy Interpretation. Chicago: Lippincott Williams & Wilkins, 2002. P. 177-184
- Fadare O., Wang S., Mariappan M.R. Practice patterns of clinicians following isolated diagnoses of atypical small acinar proliferation on prostate biopsy specimens//Arch. Pathol. Lab. Med. 2004. № 128. P. 557-560
- Atypical prostatic glandular proliferation on needle biopsy: diagnostic implications, use of immunohistochemistry, and clinical significance/H. Samaratunga, R.A. Gardiner, J. Yaxley [et al.]//Anal. Quant. Cytol. Histol. 2006. № 28. P. 104-110
- Prognostic significance of high grade prostatic intraepithelial neoplasia and atypical small acinar proliferation in the contemporary era/С. К. Moore, S. Karikehalli, T. Nazeer [et al.]//J. Urol. 2005. № 173. P. 70-72
- Predictors of prostate cancer after initial diagnosis of atypical small acinar proliferation at 10 to 12 core biopsies/V. Scattoni, M. Roscigno, M. Freschi [et al.]//Urology. 2005. №66. P. 1043-1047
- Significance of atypical and suspicious small acinar proliferation, and high grade prostatic intraepithelial neoplasia on prostate biopsy: implication for cancer detection and biopsy strategy/C.R. Girasole, M.S. Cookson, M. J Putzi [et al.]//J. Urol. 2006. № 175. P. 929-933
- Humphrey P. A. Focal glandular atypia//Prostate Pathology. Chicago, IL: ASCP Press, 2003. P. 218-225
- Bostwick D.G., Meiers I. Neoplasma of the prostate//Bostwick D.G., Cheng L, eds. Urologic Surgical Pathology. 2nd ed. Philadelphia, PA: Mosby Elsevier, 2008. P. 462-468
- Hameed O., Humphrey P. A. Immunohistochemica I evaluation of prostate needle biopsies using saved interval sections vs new recut sections vs new recut sections from the block: a prospective comparison//Am.J. Clin. Pathol. 2009. № 131. P. 683-688
- Immediate radical prostatectomy in patients with atypical small acinar proliferation: overtreatment?/M. Brausi, G. Castagnetti, A. Dotti [et al.]//J. Urol. 2004. № 172. P. 906-908
- Маслякова Г. Н., Воронина Е.С., Фомкин Р. Н. Морфологические методы исследования в диагностике рака предстательной железы//Фундаментальные исследования. 2012. №12. С. 426-430.


