Особенности хирургической тактики при лечении псевдокисты поджелудочной железы, осложненной кровотечением из ветви левой желудочной артерии
Автор: Стойко Ю.М., Ветшев П.С., Левчук А.Л., Максименков А.В., Масленников М.А., Игнатьев Т.И.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 2 т.17, 2022 года.
Бесплатный доступ
Клиническое наблюдение успешного хирургического и эндоваскулярного лечения пациента с кровотечением в псевдокисту поджелудочной железы.
Псевдокиста поджелудочной железы, кровотечение, хирургический и эндоваскулярный гемостаз
Короткий адрес: https://sciup.org/140294379
IDR: 140294379 | DOI: 10.25881/20728255_2022_17_2_114
Peculiarities of surgical tactics in treatment of hemorrhage complications post necrosis cysts in pancreas from branch of left gastral arteria
Clinical case of successful surgical and endovascular treatment in patient with bleeding in post necrosis pancreatic cyst.
Текст научной статьи Особенности хирургической тактики при лечении псевдокисты поджелудочной железы, осложненной кровотечением из ветви левой желудочной артерии
Keyword: рost necrosis pancreatic cyst, bleeding, surgical and endovascular hemostasis.
Актуальность
Хирургические вмешательства на поджелудочной железе (ПЖ) остаются одними из наиболее сложных в абдоминальной хирургии. Высокий риск развития осложнений обусловлен, с одной стороны, топографо-анатомическими взаимоотношениями этой области (соприкосновение ПЖ с крупными ветвями чревного ствола и мезентерико-порталь-ным сегментом вен), с другой — высокой ферментативной активностью и, связанной с этим, опасностью возникновения аррозивных кровотечений [1]. Эти же факторы создают высокую вероятность развития кровотечений при формировании ложных (постнекротических) кист ПЖ [2]. Геморрагические осложнения при постнекротических кистах (ПК) ПЖ. встречаются относительно редко (от 0,04 до 7,5%) [1]. Однако, они представляют актуальную проблему панкреатологии в связи с трудностями своевременной диагностики их геморрагических осложнений и высокой летальностью — до 90%, при отсутствии своевременного лечения. При выполнении хирургического гемостаза уровень летальности составляет 17–20% [3–6]. Частота кровотечений в полость кисты ПЖ достигает 13,7–37% [1]. Рентгенэн-доваскулярные технологии находят все более широкое применением в хирургической панкреатологии, однако, несмотря на всю свою эффективность и привлекательность, миниинвазивные технологии (МИТ) не являются панацеей и не способны во всех клинических ситуациях обеспечить надежный гемостаз [1; 7; 8].
По эндоскопической картин фибро-гастродуоденоскопии и ЭндоУЗИ часто не удается точно установить источник кровотечения, даже при прорыве кисты в просвет желудочно-кишечного тракта с развитием клинической картины тяжелого геморрагического шока [5; 7].
При выполнении открытых хирургических вмешательств по поводу ПК ПЖ часто отсутствует четкая визуализация значимых источников кровотечения, что не обеспечивает надежность гемостаза [5]. Открытые хирургические вмешательства при развитии кровотечения являются весьма травматичными, сопровождаются высоким риском послеоперационных осложнений, достигающих 50%, даже в специализированных учреждениях [1; 9]. Развитие и широкое применение миниинвазивных эндоваскулярных методов диагностики источника кровотечения с внедрением различных методик выполнения гемостаза (эндоваскулярная эмболизация) в хирургической панкреатологии, имеют важное клиническое значение, и позволяют сократить число послеоперационных осложнений, летальность и сроки реабилитации пациентов в условиях стационара [6]. Однако, ранняя и успешная диагностика и устранение источника кровотечения возможна только при наличии специалистов и технических возможностей проведения экстренной ангиографии и селективного эндоваскулярного гемостаза [8]. Кровотечение из ПК ПЖ часто рецидивирует, что вынуждает прибегать к выполнению срочного хирургического вмешательства, направленного на остановку кровотечения с резекцией кисты или участка ПЖ [1; 4]. Основной механизм развития геморрагических осложнений ПК — ферментативная аррозия стенки сосуда, проходящего в капсуле кисты ПЖ [1; 9].
Целью нашего клинического наблюдения явилась демонстрация трудностей диагностики и лечения кровотечения в полость кисты ПЖ, которые, не смотря на широкие возможности современных лечебно-диагностических миниинвазив-ных методов, потребовали прибегнуть для достижения гемостаза к традиционным хирургическим методам, путем выполнения открытой лапаротомии.
Пациент А., 58 лет, поступил в НМХЦ им. Пирогова 16.11.2018 г. с жалобами на интенсивные боли в левых отделах живота, общую слабость. Из анамнеза выяснено, что в течение 10 дней отмечает боли в эпигастральной области и левом подреберье. Гемодинамически был стабилен: АД 130 / 80 мм рт. ст., пульс 88 в минуту. УЗИ при поступлении: общий желч-

Стойко Ю.М., Ветшев П.С., Левчук А.Л. и др.
ОСОБЕННОСТИ ХИРУРГИЧЕСКОЙ ТАКТИКИ ПРИ ЛЕЧЕНИИ ПСЕВДОКИСТЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ, ОСЛОЖНЕННОЙ КРОВОТЕЧЕНИЕМ ИЗ ВЕТВИ ЛЕВОЙ ЖЕЛУДОЧНОЙ АРТЕРИИ ный проток не расширен, до 3 мм; поджелудочная железа: в проекции головки ПЖ овальное жидкостное образование с неровными четкими контурами, размерами 7,1х4,0 см. Эхо-структура образования неоднородная за счет гиперэхогенного включения размерами 3,3х1,5 см. Тело ПЖ — 1,0 см, хвост — 1,8 см. Их эхо-структура диффузно неоднородная, эхогенность повышена. В проекции головки и хвоста ПЖ определяются множественные округлые гипоэхогенные образования с ровными, четкими контурами, размерами от 1,9х1,3 см до 2,8х2,0 см. Лабораторные данные: липаза 240 ед/л, амилаза 140 ед/л., умеренный лейкоцитоз: 11,2х109/л, с нейтрофильным сдвигом: 9,2х109/л (82,4%), гемоглобин 141 г/л, эритроциты 4,5х 1012/л. Диагностирован: Хронический панкреатит в стадии обострения с формированием ПК в области головки и тела ПЖ. По данным мульти-спиральной компьютерной томографии (МСКТ) с контрастированием (Рис. 1) и ультразвуковой диагностики (УЗИ): в сальниковой сумке и парапанкреатиче-ской клетчатке значимых жидкостных скоплений не было выявлено. Определялся реактивный выпот однородного характера вокруг селезенки до 150 мл. В парапанкреатической клетчатке имеются множественные кистозные образования, размерами от 7х10 мм до 43х45 мм. Наибольшее кистозное образование расположено на границе тела и головки ПЖ, предлежащее к задней стенке желудка. В содержимом кисты выявлены участки повышенной плотности (кровоизлияние). Клетчатка малого сальника была местами инфильтрирована. На ЭГДС диагностирован поверхностный гастрит, дуоденогастральный рефлюкс, недостаточность кардии.
Лечение пациента А. начато в отделении реанимации: антисекреторная терапия — инфузия октреотида, ингибиторов протонной помпы — омепразол, растворов кристаллоидов — до 1500 мл в сутки, проводилась эпидуральная анальгезия наропином. На 3 сутки от момента госпитализации у больного появились признаки гнойно-септических осложнений: лейкоцитоз с нейтрофильным сдвигом до 14,8 х 109/л., концентрация прокальцитонина в крови увеличилась до 0,407 нг/мл.
УЗИ от 18.11.2018 г.: в левом поддиафрагмальном пространстве выявлено скопление жидкости однородного характера, объемом до 60 мл с гиперэ-хогенноым осадком. Под УЗ-наведени-ем выполнена пункция отграниченного
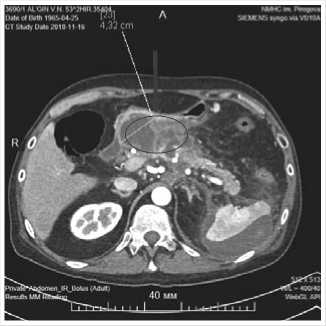
Рис. 1. МСКТ брюшной полости с контрастированием пациента А.: ПК тела ПЖ (указана стрелкой) от 17.11.2018 г.
скопления жидкости поддиафрагмального пространства слева. При аспирации получена мутная бурая жидкость в объеме 60 мл (активность амилазы в содержимом кисты 17136 ед/л.). При контрастной фистлографии диагностировано округлое образование объемом до 100 мл, с четкими, ровными контурами, не связанное с протоковой системой ПЖ, окружающими органами и сосудистыми структурами. 20.11.2018 г. пациент А. переведен в хирургическое отделение. Продолжена плановая консервативная терапия. 22.11.2018 г. выполнена контрольная фистулография, при которой определялась округлая полость до 16 мл в левом поддиафрагмальном пространстве. По УЗИ в левом поддиафрагмальном пространстве сохранилось наличие свободной жидкости объемом до 44 мл и 11 мл в полости малого таза. 23.11.2018 г. отмечено ухудшение общего состояния пациента: появилась резкая слабость, головокружение, с развитием гипотонии (АД 80/40 мм рт. ст.). В клинических анализах крови отмечено снижение гемоглобина до 83 г/л, эритроцитов — 2,8 1012/л. Заподозрено кровотечение в полость ПК ПЖ. Пациент переведен в реанимационное отделение, установлен назогастральный зонд, промыт желудок. Выполнена ЭГДС: в просвете желудка до 50 мл промывных вод с примесью темной крови и сгустков. Слизистая желудка ярко-розовая, гладкая, блестящая; рельеф желудочных полей подчеркнут. В своде и теле желудка единичные острые эрозии до 2–3 мм. Эндоскопическая картина состоявшегося желудочного кровотечения из эрозий желудка.
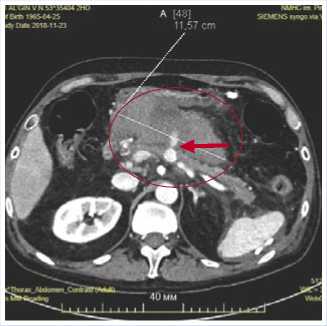
Рис. 2. МСКТ брюшной полости с контрастированием пациента А.: кровотечение в полость кисты ПЖ с прорывом в брюшную полость (указано стрелкой) от 23.11.2018 г.
На экстренной МСКТ с в/в контрастированием от 23.11.2018 г.: в сальниковой сумке, кпереди от ПЖ, определяется содержимое, плотностью до 55–65 HU, объемом до 150 см3. При этом на расстоянии 20 мм от чревного ствола выявлена экстравазация контрастного препарата, с поступлением его в сальниковую сумку. На границе тела и хвоста поджелудочной железы отмечалось поступление контрастного препарата в ПК. Содержимое ПК ПЖ, расположенной в области кардиальной части желудка, стало неоднородным с повышенной плотностью за счет состоявшегося кровотечения в её полость. Размер ПК увеличился до 39 х 46 мм, в её просвете определяются кровяные сгустки (Рис. 2).
В экстренном порядке пациент А. прооперирован 23.11.2018 г. Выполнена лапаротомия, при ревизии в брюшной полости до 1500 мл сгустков и жидкой крови. Установлен источник кровотечения: в дне кисты тела и хвоста ПЖ, по ее верхнему краю, активное кровотечение из аррозии стенки селезеночной артерии (Рис. 3). Выполнена спленэктомия с перевязкой селезеночной артерии, остановка кровотечения. Течение послеоперационного периода — без осложнений.
Контрольное МСКТ от 05.12.2018 г.: сохраняется инфильтрация парапанкреа-тической, мезентериальной и забрюшинной клетчатки в области ложа удаленной селезенки. Форма, размеры и денситоме-трические показатели паренхимы ПЖ в пределах возрастной нормы, отчетливо прослеживается её дольчатое строение (Рис. 4). В удовлетворительном состоянии пациент выписан на амбулаторное лечение 10.12.2018 г.

Стойко Ю.М., Ветшев П.С., Левчук А.Л. и др.
ОСОБЕННОСТИ ХИРУРГИЧЕСКОЙ ТАКТИКИ ПРИ ЛЕЧЕНИИ ПСЕВДОКИСТЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ, ОСЛОЖНЕННОЙ КРОВОТЕЧЕНИЕМ ИЗ ВЕТВИ ЛЕВОЙ ЖЕЛУДОЧНОЙ АРТЕРИИ
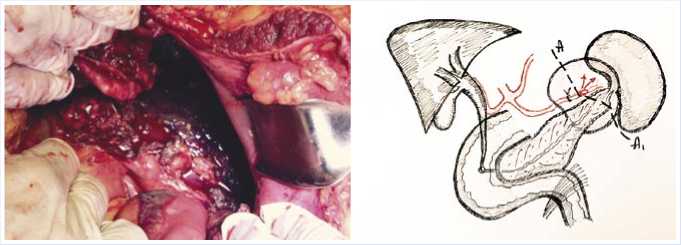
Рис. 3. (Схема к рис.3 справа) Локализация аррозивного кровотечения из селезеночной артерии в кисте хвоста ПЖ пациента А. от 23.11.2018 г. Пунктиром А-AI на схеме указан оперативный доступ к перевязке селезеночной артерии «на протяжении» и спленэктомии.
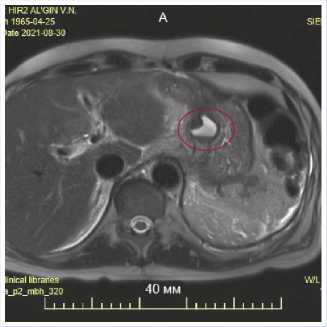
Рис. 6. МРТ брюшной полости пациент А. — обведена ПК ПЖ. 28.08.2021 г.
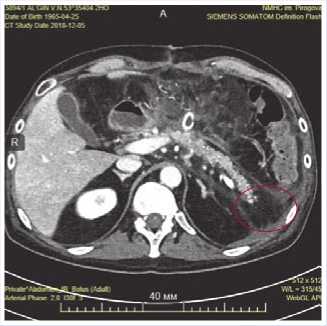
Рис. 4. МСКТ брюшной полости с контрастированием пациента А. Отек и инфильтрация в ложе удаленной селезенки (обведено) от 05.12.2018 г.
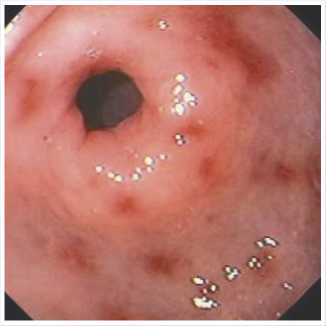
Рис. 5. Эндоскопическая картина эрозивного гастрита пациента А. от 28.08.2021 г.
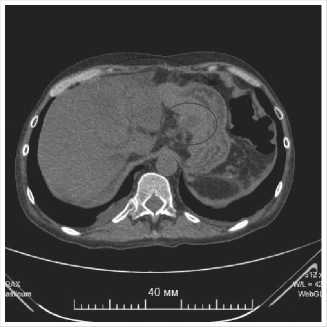
Рис. 7. МСКТ брюшной полости пациента А. ПК ПЖ с распостранением на заднюю стенку желудка (обведена). от 29.08.2021 г.
С июня 2021 г. пациент А. стал отмечать постепенное ухудшение состояния, появление слабости, с эпизодами гипотонии, без признаков желудочно-кишечных кровотечений по результатам анализов крови. Принимал препараты железа (феррум-лек). 28.08.2021 г. в экстренном порядке госпитализирован НМХЦ им. Пирогова с клиникой кровотечения из верхних отделов желудочно-кишечного тракта, проявляющееся рвотой с примесью крови, черным стулом. Артериальное давление 110/70 мм рт. ст., пульс 77 в мин., снижение гемоглобина до 55 г/л. Предварительный диагноз при поступлении: желудочно-кишечное кровотечение. Хроническая железодефицитная анемия тяжелой степени. Хронический рецидивирующий панкреатит с образованием псевдокист в области головки и тела поджелудочной железы (из анамнеза).
Выполнена ЭГДС, при которой диагностировано подслизистое опухолевидное образования желудка с изъязвлением, с признаками состоявшегося кровотечения — «Форрест 2 В». Видимая
слизистая желудка бледная с множественными эрозиями в теле и антральном отделе, размерами 0,1–0,3 см в диаметре. По малой кривизне в верхней трети тела желудка определяется подслизистое образование округлой формы размерами до 1,0 см в диаметре. Слизистая в проекции образования с наличием изъязвления размером 0,3 см в диаметре, дно плоское, черного цвета с налетом фибрина, при отмывании физиологическим раствором сосудов в краях изъязвления не определяется, без признаков активного кровотечения (Рис. 5).
На МРТ и МСКТ от 29.08.2021 г. выявлено кистозное образование в проекции головки и тела ПЖ, с наличием крупной сосудистой ветви в просвете ПК. Размеры кисты по медиальному контуру тела желудка протяженностью до 6 см и 3 см в поперечнике, плотность содержимого кисты 40–60 едН, без значительного накопления контрастного препарата (Рис. 6, 7).
Учитывая данные ЭГДС и МСКТ, анамнез заболевания, и клиническую кар-
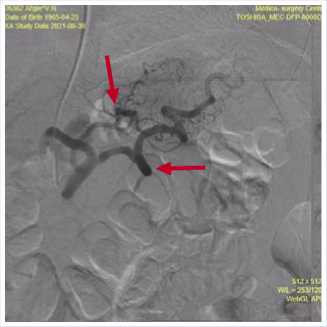
Рис. 8. Ангиограмма пациента А. от 30.08.2021 г. Ветви левой желудочной артерии (отмечены стрелками), на момент исследования без признаков продолжающегося кровотечения.
тину, 30.08.2021 г. Пациенту А. выполнена экстренная ангиография (Рис. 8).
Стойко Ю.М., Ветшев П.С., Левчук А.Л. и др.
ОСОБЕННОСТИ ХИРУРГИЧЕСКОЙ ТАКТИКИ ПРИ ЛЕЧЕНИИ ПСЕВДОКИСТЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ, ОСЛОЖНЕННОЙ КРОВОТЕЧЕНИЕМ ИЗ ВЕТВИ ЛЕВОЙ ЖЕЛУДОЧНОЙ АРТЕРИИ
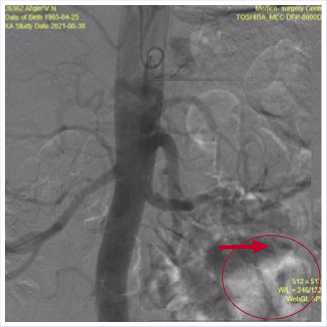
Рис. 9. Ангиограмма пациента А. от 06.09.2021 г.: экстравазация контраста, продолжающееся кровотечение из ветви левой желудочной артерии (источник отмечен стрелкой) в полость ПК (обведена) ПЖ.
В месте отхождения левой желудочной артерии имеется аневризматически расширенная ветвь, идущая по направлению к большой кривизне желудка. Другие ветви абдоминального отдела аорты без патологии. Данных за экстра-вазацию из аневризматически измененного сегмента левой желудочной артерии не получено.
Больному проводилась консервативная противоязвенная, антисекреторная и гемостатическая терапия. 05.09.2021 г. у пациента А., на фоне клинического благополучия, при контрольном анализе крови отмечено значительное снижение гемоглобина до 64 г/л. На ЭГДС: картина протрузии стенки желудка в проксимальной части тела с эрозированием и признаками состоявшегося кровотечения. Учитывая клинико-лабораторные данные, с целью идентификции источника кровотечения, 06.09.2021 г. выполнена повторная ангиография, в результате которой диагностирована массивная экстравазация контрастного препарата в полость ПК тела ПЖ (Рис. 9).
06.09.2021 г. в экстренном порядке выполнена лапаротомия. В свободной брюшной полости наличия крови не выявлено. Из рубцово-спаечного процесса выделена задняя стенка желудка, в её толще вскрыта субсерозная гематома объемом до 150 мл. Из подслизитого слоя выделена ветвь левой желудочной артерии диаметром до 3 мм, с продольным аррозивным дефектом её стенки протяженностью до 4 мм, из которого активно поступет кровь. Выполнена остановка кровотечения с перевязкой проксимального и дистального отделов левой желудочной артерии (Рис. 10).
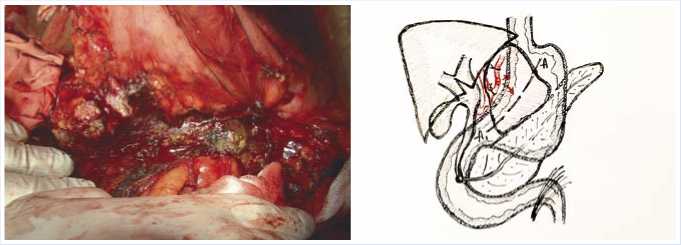
Рис. 10. (Схема к рис.10 справа). Локализация аррозивного кровотечения из левой желудочной артерии в кисту тела ПЖ пациента А. (от 06.09.2021 г.). Пунктиром А-AI (на схеме) указан оперативный доступ вскрытия кисты ПЖ с перевязкой ветви левой желудочной артерии, выполнении гемостаза.
Послеоперационный диагноз: Ложная аневризма левой желудочной артерии, осложненная аррозивным кровотечением в полость ПК ПЖ, с формированием субсерозной гематомы стенки тела желудка. Послеоперационый период без осложнений. Рецидивов желудочных кровотечений не отмечено. 20.09.2021 г. пациент был выписан в удовлетворительном состоянии с уровнем гемоглобина 120 г/л под наблюдение хирурга и гастроэнтеролога.
Заключение
Эндоваскулярные методы лечения геморрагических осложнений ПК ПЖ, путем эмболизации источника кровотечения из висцеральных сосудистых ветвей аорты, могут использоваться в комплексном лечении для выполнения гемостаза. Однако, несмотря на мини-инвазивность и малую травматичность, они имеют ряд ограничений.К ним относятся: параметрический фактор, когда дефект сосудистой стенки, при возникновении дегенерационных ПК ПЖ, может формироваться в течение длительного времени. При этом диаметр сосудистой фистулы обычно превосходит диаметр эмболизируемого сосуда, что затрудняет возможность фиксировать в кровоточащем сосуде вводимых окклюзионных материалов с целью гемостаза. Они током крови вымываются в полость ПК. Важное значение имеет фактор анастомозирования артериальной ветви, т.е. стенки полости ПК ПЖ могут иметь несколько источников кровоснабжения (ветви желудочных, желудочно-сальниковых, панкреатодуоденельных артерий, селезеночной артерий), что создает сложность и бесперспективность селективной эмболизации кровоточащего сосуда; с другой стороны, попытка одномоментной эмболизации всех питающих сосудов, в случае своей эффективности, может привести к острому ишемическому повреждению кровоснабжаемых органов панкреатогастродуоденальной зоны. При этом, успешно выполненный гемостаз, методом эндоваскулярной эмболизации сосудистой мальформации на фоне хронического воспалительного процесса, не исключает развитие фактора реваскуляризации места дефекта сосудистой стенки, с возможным развитием рецидива кровотечения в полость ПК ПЖ.
Таким образом, эндоваскулярный метод часто выступает в качестве дополнительного, этапного, а не окончательного метода остановки кровотечений из ПК ПЖ. При отсутствии эффекта надежного эндоваскулярного гемостаза или невозможности его выполнения по техническим причинам, необходима срочная традиционная операция с резекцией ПК, или участка ПЖ, несущего аррозивный источник кровотечения.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
СТЕНТИРОВАНИЕ ПОДКЛЮЧИНОЙ АРТЕРИИ КАК МЕТОД ЭНДОВАСКУЛЯРНОЙ РЕДУКЦИИ КОНКУРЕНТНОГО КРОВОТОКА
(In Russ).]
Список литературы Особенности хирургической тактики при лечении псевдокисты поджелудочной железы, осложненной кровотечением из ветви левой желудочной артерии
- Ревишвили А.Ш., Кригер А.Г., Горин Д.С. и др. Эндоваскулярные вмешательства в хирургии поджелудочной железы // Хирургия. - 2018. - №4. - С.4-10.
- Абдулаев М.А. и др. Аррозивные кровотечения при псевдокистах поджелудочной железы // Вестник СПбГУ. - 2012. - Сер.11. - Вып.1. - С.133-139.
- Полянцев А.А. и др. Кисты поджелудочной железы как источник желудочно-кишечного кровотечения // Хирургия. - 2011. - №1. - С.49-51.
- Артемьева Н.Н. и др. Геморрагические осложнения псевдокист поджелудочной железы // Анналы хирургической гепатологии. - 1998. - Т.3. - №1. - С.35-40.
- Бороденко А.И. Желудочно-кишечное кровотечение при цистогастральном свище // Пробл. персп. соврем. науки. - 2009. - Т.2. - №1. - С.14-16.
- Malleo G., Vollmer CM Jr. Postpancreatectomy Complications and Management. Surg Clin North Am. 2016; 96(6): 1313-1336.
- Гольцов В.Р., Савелло В.Е., Деменко А.Е. Лечение больных с геморрагическими осложнениями псевдокист поджелудочной железы // Анналы хирургической гепатологии. - 2017. - Т.22. - №2. - С.12-19.
- Кочмашев И.В., Прудков М.И., Мансуров Ю.В. Рентгенваскулярные вмешательства при панкреатогенных кровотечениях // Анналы хирургической гепатологии. - 2017. - Т.22. - №2. - С.30-35.
- Коваленко З.А. Муцинозная цистаженома поджелудочной железы, осложненная кишечным кровотечением // Хирургия. - 2021. - №11. - С.93-96.


